环己烷萃取-微波消解-原子荧光光谱法测定白米中硒含量的方法研究
2022-10-10卢鑫,张琳
卢 鑫,张 琳
(济源职业技术学院 医学护理学院,河南 济源 459000)
硒作为人体健康所必需的微量元素之一,直接作用于机体的代谢过程,而有机硒如硒代半胱氨酸、硒代蛋氨酸等还具有抗肿瘤、提高机体免疫力等生理活性,因此硒也被誉为生命的“火种”。宋婵娟在文章中提出膳食中补充富硒酵母,可使癌症发病率和死亡率下降50%左右[1]。目前,全球有40多个国家或地区处于低硒或缺硒状态[2],因此,近年来富硒稻米、富硒核桃、富硒小麦、富硒苹果等食品的研制开发[3-5],使硒元素日益成为人们和社会关注的热点。
食物补硒是当前最便利、也是最被广泛推崇的方法,但食物中硒分为无机硒和有机硒两类。无机硒如硒酸盐、亚硒酸盐、挥发态的甲基硒和硒化氢等毒性大、生物利用率低;有机硒如硒蛋白、硒代蛋氨酸等多为硒与不同氨基酸结合的大分子氨基酸或是硒代氨基酸的衍生物,由此形成的有机态的硒化物,不仅毒性小,而且生物利用率高,更为重要的是安全性高[6-7]。当前市面上的富硒食品涉及种类多,包括蔬菜、水果和保健食品等,但因其存在的价态和形态不同,不同类富硒食品中具有的生物活性也相差较大。随着我国人民生活水平不断提高,市场上富硒食品越来越多,为了让消费者真正享受富硒食品的保健效果,对食品中硒含量及硒形态的分析显得尤为重要。
目前,测定硒含量多用仪器分析的方法,主要有原子荧光光谱法、比色法和原子吸收法,近年来电感耦合等离子体质谱法、高效液相色谱法等也用于硒含量的测定[8-10]。其中,氢化物-原子荧光光谱法具有灵敏度高、线性范围广、重现性好的优点,并且试剂毒性小、实用性强,开始被广泛使用。
为探索研究运用原子荧光光谱法对当地所产的富硒白米进行检测,试验将采用正交试验对仪器检测条件进行优化,对样品的提取分离条件、前处理方法进行研究,最终建立测定白米中硒种类和含量的方法,从而实现对当地产白米中无机硒和有机硒含量的快速测定。
一、试验材料与方法
(一)试剂与材料
富硒白米取自济源五龙口镇西正村富硒米,其他材料为:硝酸(优级纯,国药集团化学试剂有限公司)、盐酸(优级纯,国药集团化学试剂有限公司)、高氯酸(优级纯,国药集团化学试剂有限公司)、过氧化氢(优级纯,国药集团化学试剂有限公司)、氢氧化钠(优级纯,国药集团化学试剂有限公司)、甲苯(优级纯,国药集团化学试剂有限公司)、环己烷(优级纯,国药集团化学试剂有限公司)、硼氢化钾(分析纯,洛阳昊华化学试剂有限公司)、铁氰化钾(分析纯,洛阳昊华化学试剂有限公司);Se标准溶液(1000 μg/mL,国家有色金属及电子材料分析测试中心)、高纯氩气,试验用水为实验室自制超纯水。
(二)主要仪器
试验采用的仪器主要为:RGF-6300原子荧光光度计(北京博晖创新光电技术股份有限公司)、MD6C-6H型微波消解仪(维克特锐(北京)科技有限公司)、赶酸仪(北京东航科仪有限公司)、FA2204B万分之一天平(上海精密仪器仪表有限公司)、电热恒温水浴锅、超声波清洗器、粉碎机、电热板。
(三)正交试验用溶液配制
准确移取10.00 mL质量浓度为1000 μg/mL的硒标准溶液,用超纯水定容100 mL,摇匀,即得100 μg/mL溶液;移取该溶液5 mL,用超纯水定容至100 mL,即为5 μg/mL标准溶液。
(四)标准溶液系列的配制
准确移取10.00 mL质量浓度为1000 μg/mL的硒标准溶液,用超纯水定容100 mL,摇匀,即得100 μg/mL溶液;从中分别移取100 μg/mL标准溶液1 mL,2 mL、4 mL、8 mL、10 mL至100 mL容量瓶中,采用体积分数为5%的盐酸溶液定容,稀释后溶液质量浓度分别为1 μg/mL、2 μg/mL、4 μg/mL、8 μg/mL、10 μg/mL,依次做好标签标记后待用。
(五)样品处理
将富硒大米在超纯水中清洗后,放置于65 ℃的烘箱中烘干,冷却至室温后用粉碎机进行粉碎,过筛(20目筛),将过筛后的样品置于干燥的塑料瓶中备用。
1.消解样品
湿法消解:精确称取上述制备好的样品0.8 mg置于250 mL锥形瓶中,加入硝酸-高氯酸(体积比为4∶1)的混合溶液,瓶口处放置一弯颈小漏斗,进行冷消化过夜,24 h后置于电加热板上加热消化,若过程中酸液减少,可进行适量补加,再对其加热至冒白烟,浓缩至小体积,至不可蒸干为止,取下冷却后加入5 mL摩尔浓度为 6 mol/L的盐酸溶液,再置于电加热板上加热至白烟冒出,至溶液呈现清亮无色状态,取出冷却后转移至25 mL比色管,加入1.5 mL铁氰化钾溶液,用水定容至25 mL,混匀备用,用于检测总硒含量。同时,同样方法和步骤进行空白试验。
微波消解:精确称取 0.8 mg 样品于消解管中,依次加水30 mL,过氧化氢2 mL、硝酸8 mL,振摇混合均匀后,于微波消解仪中按设定程序(见表1)进行消解,微波消解结束冷却后转入锥形瓶中,再进行加热赶酸,至不可蒸干为止,冷却后加6 mol/L的盐酸溶液5 mL,沸水浴15 min后至溶液呈现清亮无色状态,并同时伴有白烟,冷却至室温后引流转移至25 mL比色管,再加入1.5 mL铁氰化钾溶液混匀,加水定容至25 mL,摇匀备用,用于检测总硒含量。同时,做空白试验。
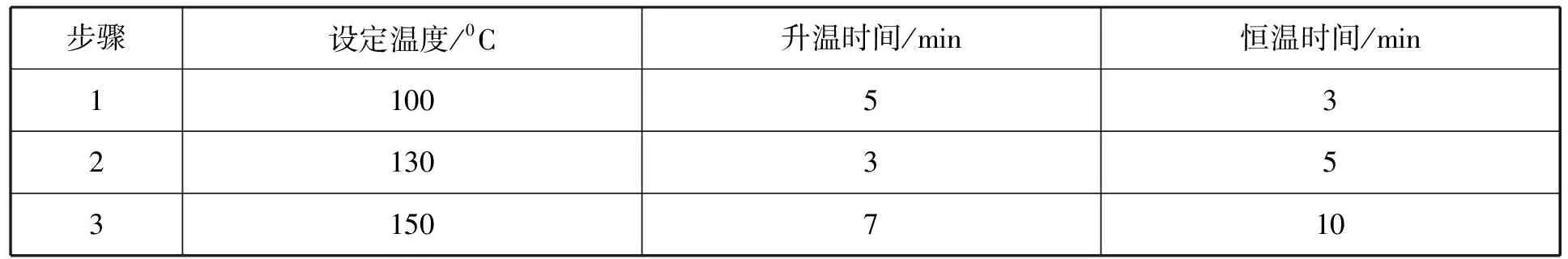
表1 微波消解仪设置条件
2.无机硒萃取
称取0.8 mg样品,加超纯水30 mL摇匀,水浴超声浸提25 min后,再进行85 ℃的水浴10 min,适时补加水,冷却后,用1.25 mol/L的NaOH溶液,将pH值调至为7.0~7.5,之后过滤。将滤液置于分液漏斗中,加入环己烷,振荡萃取,将水相按照表1微波消解处理、备用,用于检测无机硒含量。
(六)样品上机检测和计算公式
检测前先开机通入氩气,设定好各项参数后预热 30 min,用体积分数为 5%盐酸作载流,8%的硼氢化钾溶液和质量浓度为5 g/L的NaOH溶液做还原剂测定。计算公式:X=(C-C0)×V/m。
式中:X—样品中硒的质量比(μg/g);C—样品消化液测定的浓度(μg/mL);C0—样品空白消化液测定浓度(μg/mL);m—样品称量质量(g);V—样品预处理后定容的总体积(mL)。根据差减法算出有机硒质量比,即有机硒=总硒-无机硒。
二、结果与讨论
(一)仪器检测条件优化
使用正交试验设计选择仪器条件,分别定义A为光电倍增管的负高压,包含 280、290、300三个水平;定义B为灯电流,包含60、70、80三个水平,定义 C 为载气流量,包含 300、400、500三个水平,定义 D 为屏蔽气流量,包含 900、1000、1100三个水平,建立4因素3水平的 L9(34)正交试验设计表,用5 μg/L硒标准溶液试验,结果见表2。
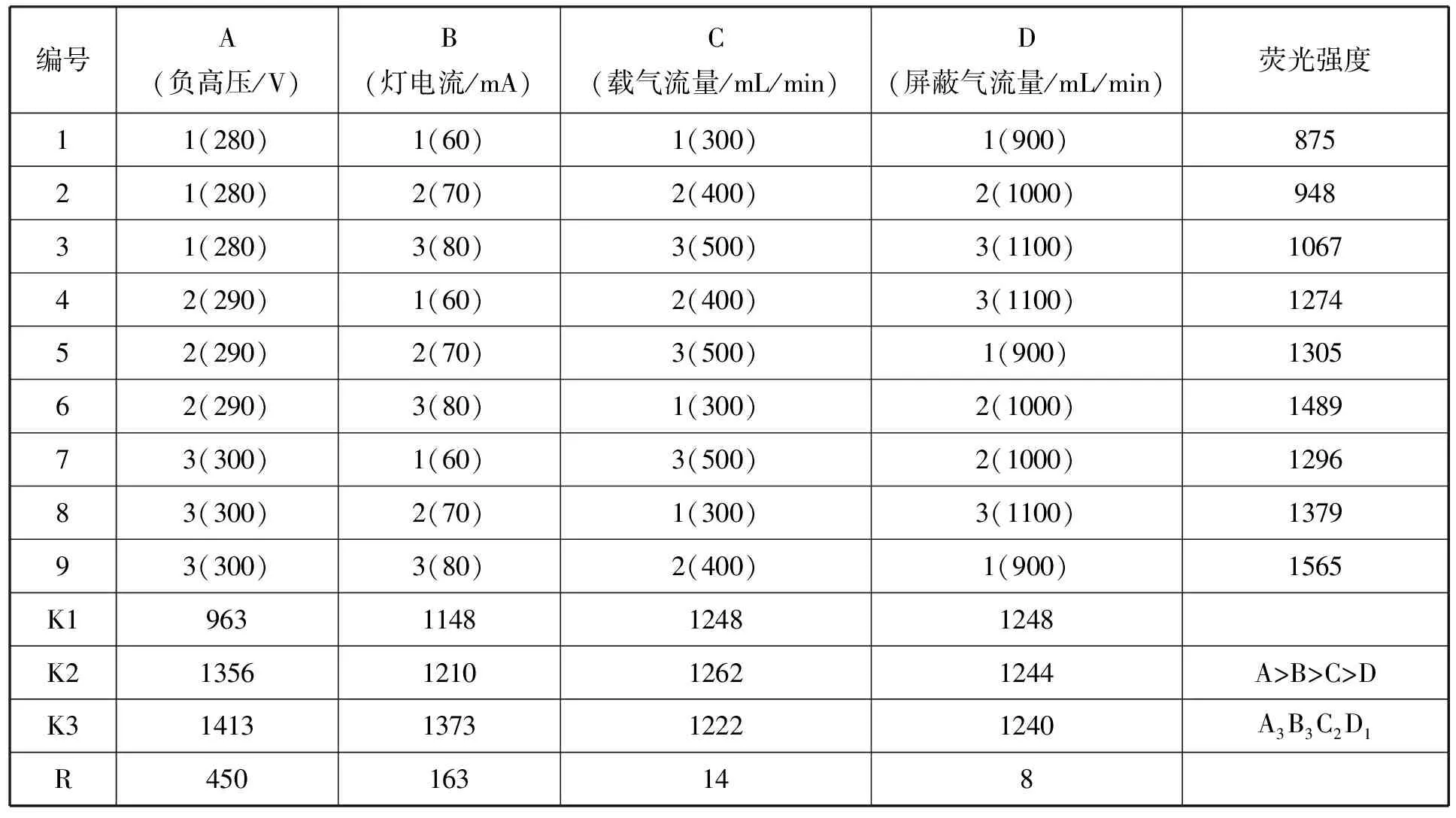
表2 L9(34)仪器检测条件正交表试验方案及结果
由表2可知,影响测定结果中荧光强度的因素由大到小顺序为负高压>灯电流>载气流量>屏蔽气流量。最优条件为A3B3C2D1,结合前期试验结果最终选择测试硒元素的最优条件为:负高压300 V、灯电流80 mA、原子化炉高度8 mm、原子化温度200 ℃、载气流量400 mL/min、屏蔽气流速900 mL/min、延时时间1.0 s、读数时间10 s。在此条件下进行标准曲线的建立和样品测试。
(二)样品前处理的优化
1.消解方法的比较
在上述最优工艺条件下,探讨了湿法消解和微波消解的优劣,结果见表3。由表3可见,3次平行测定中,微波消解比湿法消解测定的结果高且重现性好,湿法消解中料液比对消解有影响,在一定的硝酸-高氯酸混合溶液范围内料液比的影响不大,说明湿法消解会对消解的完全程度有影响;微波消解采用了密闭溶样罐及微波加热的方式,有利于试样的消化,且硒损失较少,结果更准确,故样品测定采取微波消解方式。
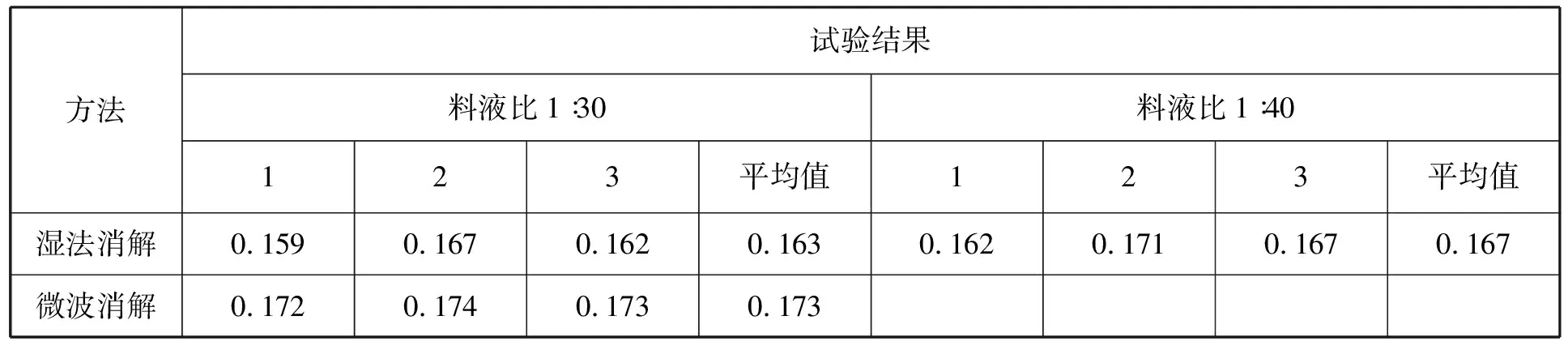
表3 湿法消解和微波消解试验结果 μg
2.环己烷萃取次数的优化
大米中有机硒多是与蛋白质结合的不溶性大分子化合物,而少量没有与蛋白质结合的有机小分子硒化合物,如各种硒代氨基酸可以溶解在水中,其在有机溶剂甲苯、乙醇和环己烷中有较高的溶解度,因此水相中的小分子有机硒可以用有机溶剂分离。本试验采用对环境毒性小,安全性高且易挥发的环己烷进行萃取分离。在最优工艺条件下,探讨不同萃取次数对无机硒测定的影响。4份平行样品过滤后,把滤液分别置于4个分液漏斗中,加入10 mL环己烷,振荡萃取,分别重复萃取1次、2次、3次和4次。试验结果如图1所示,萃取次数越多,水相中无机硒质量比越低,说明有机硒在环己烷试剂中有较大的溶解度,萃取2次后,无机硒含量变化不明显,因此确定萃取次数为2次。
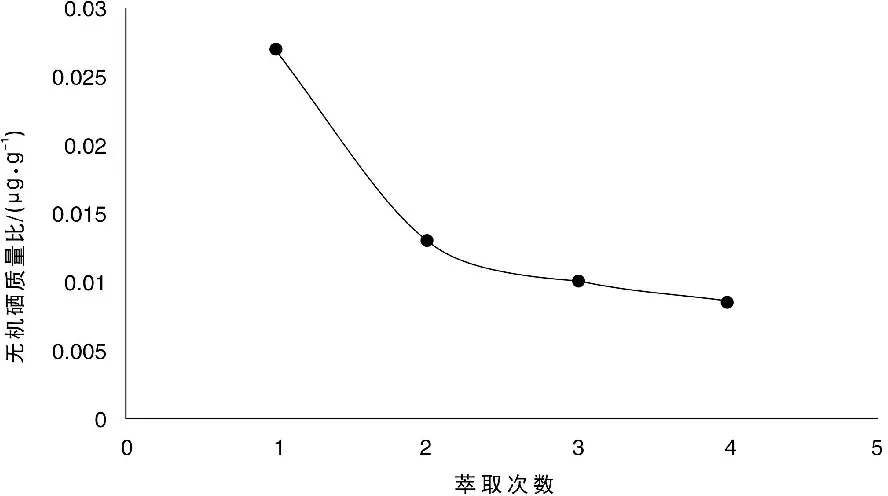
图1 萃取次数对无机硒含量的影响
萃取剂环己烷不同用量对无机硒测定的影响如图2所示。4份平行样品过滤后,将滤液置于4个分液漏斗中,分别加入5 mL、8 mL、10 mL、15 mL环己烷,震荡萃取,各萃取2次。由图2可见,随着萃取剂用量的增加,滤液中无机硒含量降低,当萃取剂用量为10 mL时,无机硒含量最低,继续增加萃取剂用量,无机硒含量不再变化。
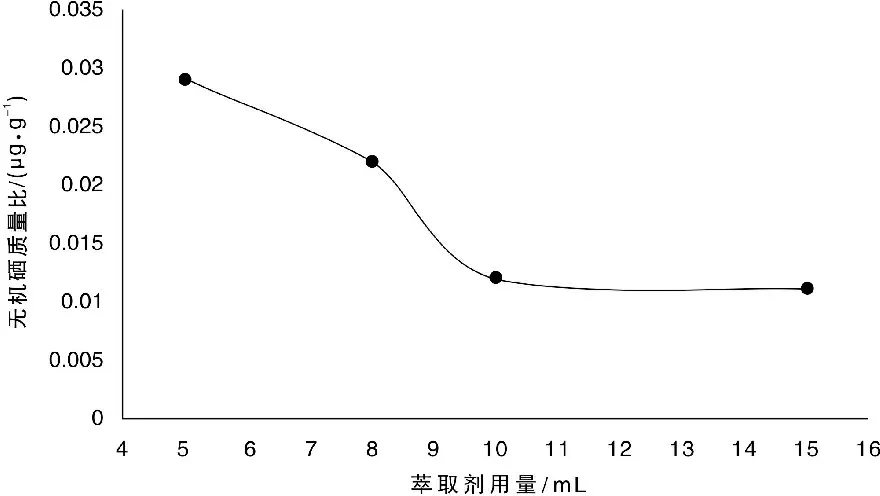
图2 萃取剂用量对无机硒含量的影响
3.氢化物发生条件的选择
(1)盐酸体积分数的选择。载流中的盐酸和还原剂反应产生氢气,使仪器产生氢火焰,盐酸体积分数过低会使与硼氢化钾的反应不完全,不能产生足够的氢气和氢化物,过高体积分数的盐酸会对设备有腐蚀作用。对 5 μg/L硒标准溶液进行测定,分别研究了不同的盐酸体积分数(2.5%~17%)作为载流对荧光强度的影响,结果如图3所示。
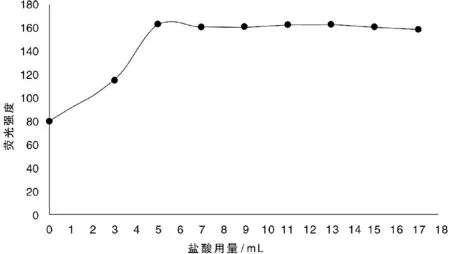
图3 盐酸用量对荧光值的影响
由图3可见,当盐酸的体积分数由0到5%增加时,荧光强度也随之增加,盐酸体积分数在5%~15%时,荧光强度基本趋于稳定且较高,同时考虑到盐酸用量过高会对仪器管路造成影响。因此,本试验采用体积分数为5%的盐酸作为载流液。
(2)硼氢化钾质量浓度的选择。硼氢化钾作为四价硒的还原剂,将四价硒还原成硒化氢后进行原子化,因此,硒的还原程度受硼氢化钾的浓度影响。本试验采用5 μg/L硒标准溶液进行测定,分别研究了5、10、15、20、25、30、35 g/L的KBH4溶液作为还原剂对荧光强度的影响,结果如图4所示。
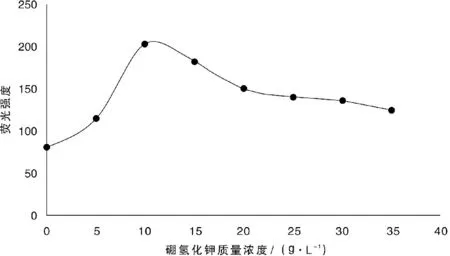
图4 硼氢化钾质量浓度对荧光值的影响
由图4可知,随着KBH4溶液质量浓度增大,荧光强度也随之增加,但当KBH4溶液的质量浓度过高时,荧光强度反而降低,这是因为氢气量太大从而稀释硒原子蒸气造成的,因此,KBH4溶液的最佳质量浓度为10 g/L。
(三)标准曲线、检出限和加标回收结果
1.标准曲线与检出限
为了研究硒含量与荧光强度的关系,以测得的荧光强度为纵坐标、配制的标准溶液浓度为横坐标,得到标准曲线,结果如图5所示。
由图5可见,硒标准溶液质量浓度在0~10 μg/mL时线性关系良好,标准曲线的线性回归方程为y=213.5x-35.6。连续测定11次空白试剂,得到的检出限(3倍标准差/标准曲线的斜率)为0.0072 μg/g。用8 μg/mL的标准浓度测定8次,得到相对标准偏差(RSD)为2.38%。
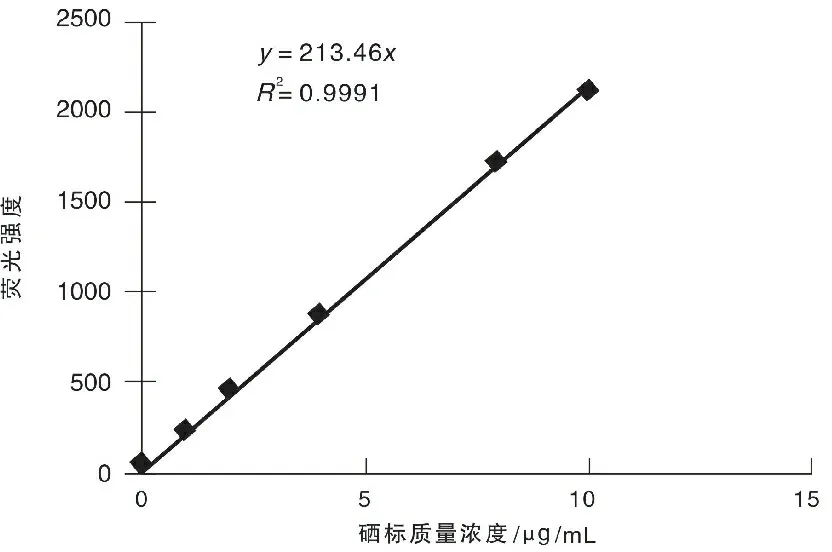
图5 硒标准曲线
2.加标回收结果
通过加标回收试验探究方法的准确度。取样品按照上述微波消解方法测总硒加标试验(n=5)。按照图2中试验过程采用 10 mL萃取剂环己烷萃取2次测无机硒加标试验(n=5)进行加标回收试验,结果见表4。
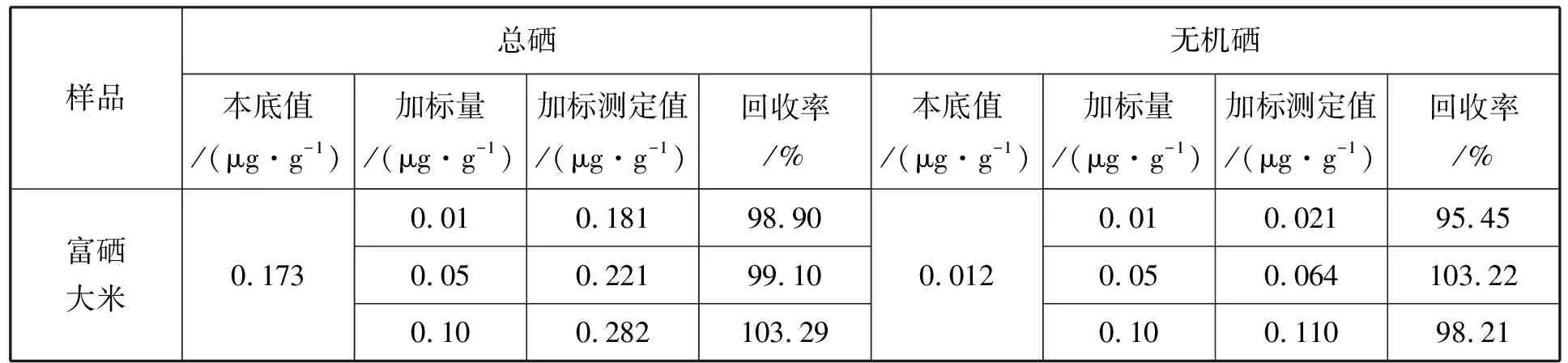
表4 样品总硒和无机硒加标回收试验结果(n=5)
结果表明,总硒加标回收率为98.9%~103.29%,无机硒加标回收率为95.45%~103.22%。有机硒质量比为0.161 μg/g,有机硒含量达93%。
三、结论
(1)通过正交试验,原子荧光的最佳检测条件为负高压300 V、灯电流80 mA、原子化炉高度8 mm、原子化温度200 ℃、载气流量400 mL/min、屏蔽气流速900 mL/min、延时时间1.0 s、读数时间10 s。
(2)在最佳检测条件下,确定环己烷作为萃取剂,萃取2次,每次10 mL,工作曲线在0~10 μg/mL范围内线性良好,检测限0.0072 μg/mL。
(3)本试验建立的测定富硒大米中硒含量的检测方法,不仅灵敏度高、重现性好,而且操作简单、快捷,所有仪器装置也是常见的实验室配备,为进一步推广到富硒大米生产厂家及其他富硒食品检测单位提供了重要路径。
