铁(Ⅱ)配位聚合物电致变色材料研究进展
2022-09-16刘海涛武志荣
束 敏 刘海涛 彭 胜 武志荣 张 蕤 李 峰 刘 建*,
(1南京林业大学化学工程学院,江苏省林业生物资源高效利用协同创新中心,南京 210037)(2潍坊科技大学,山东半岛卤水资源高值化利用绿色化工程技术研发中心,潍坊 262700)
0 引 言
刺激响应型分子材料在高新技术领域具有广泛应用前景,是智能材料领域研究热点之一。电致变色材料是一种能够在外界电压作用下产生可逆的光谱吸收或透射变化,从而产生可逆的颜色变化的一种新型智能材料[1-3]。电致变色材料具有低压驱动、颜色变化可逆和变色持久等优点,在智能窗、低能耗显示器、电子纸、汽车防眩目后视镜以及军事伪装等诸多领域具有广泛应用[4-7]。迄今为止,电致变色材料主要包括过渡金属氧化物[8-11]、过渡金属配位聚合物[12-15]、紫罗精[16-19]、有机共轭聚合物等[20-23],其变色过程主要基于离子脱嵌和氧化还原2种工作机制。
过渡金属配位聚合物兼具无机材料和有机材料的优点,很容易通过配体的分子裁剪、金属离子以及配位方式的变化来调控材料的光电性质[24-29]。基于变价过渡金属的配位聚合物,具有良好的氧化还原性质和丰富的电子跃迁[30-32],是一类性能优异的电致变色材料,具有高的光学对比度、快速的响应时间、多重颜色变化等优点[33-35],受到广泛关注。如 Fe2+[36-38]、Ru2+[39-41]、Os2+[42-44]、Co2+[45-47]和 Cu2+[48-50]等常用来与联吡啶类配体构建配位聚合物,应用于电致变色领域。其中Fe2+来源广泛、价格低廉,易与吡啶类多齿配体形成稳定的配位聚合物,且表现出优异的氧化还原性质。因此,铁配位聚合物类电致变色材料的分子构建和性能调控一直是该领域的研究热点之一,取得了系列进展。本文综述了铁配位聚合物类电致变色材料的研究进展,着重从有机配体的臂形、种类和间隔基团等方面进行系统阐述,并展望了铁配位聚合物类电致变色材料开发的发展趋势,以及亟须解决的问题和途径。
1 电致变色原理及性能参数
1.1 铁配位聚合物的电致变色原理
金属配位聚合物的光谱吸收性质取决于金属离子的种类、配体分子结构及其电荷/能量转移特性。金属配位聚合物中的电子跃迁可源于金属-配体电荷转移(MLCT)或配体-金属电荷转移(LMCT)。在多金属配位聚合物中,还可以观察到金属-金属电荷转移(MMCT)带。对于含有一个以上配体分子的配合物,在吸收光谱中可能出现配体-配体电荷转移(LLCT)带[51-52]。对于变价金属配位聚合物而言,在外界电压作用下,中心金属离子发生氧化还原反应,导致其MLCT跃迁发生变化,从而引起光谱吸收性质的变化[53-55]。二价铁吡啶类配位聚合物通常具有很强的MLCT跃迁,且跃迁能量较低,在可见光区域580 nm附近具有很强的吸收带。在施加外界电压下,中心金属离子被氧化,形成三价铁配位聚合物,可见光区域特征MLCT吸收带消失,颜色发生明显的变化。由于铁配位聚合物具有良好的氧化还原可逆性和循环稳定性,且氧化还原响应速率较快,表现出优异的电致变色性能。
1.2 电致变色性能参数
1.2.1 光学对比度
光学对比度(ΔT)是指在特定波长下电致变色材料着色态和褪色态透过率变化百分比,是表征电致变色性能重要参数之一[56-57]。通常在选择电致变色材料呈现最大光学对比度所对应的波长后,采用紫外可见分光光度计和电化学工作站测试记录后,计算电致变色材料的ΔT。
1.2.2 响应时间和循环稳定性
电致变色响应时间是指材料从一个颜色状态切换到另一个状态所需的时间,包括着色响应时间(tc)和褪色响应时间(tb)。如图1所示,褪色态到着色态所需时间为tc,由着色态切换到褪色态所需时间为tb。通常以透过率变化达到最大值的95%所需时间来计算得到响应时间[58-59]。一般通过电化学工作站和紫外可见分光光度计联用,采用多电位阶跃方法测试。循环稳定性也是衡量电致变色材料或器件性能的一个重要指标,对材料和器件的实际应用有着重要的意义。一般通过连续施加和切换变色电压,观察各项性能参数随着循环次数的变化,性能参数变化越小,表明材料或器件循环稳定性越好。

图1 电致变色响应时间示意图Fig.1 Schematic diagram of electrochromic response time
1.2.3 着色效率
着色效率(CE)是指在特定波长下电致变色材料光学性质变化与单位电荷的比值,表征材料在单位电荷下颜色改变的能力,根据Beer-Lambert定律[60],CE值可以通过公式1计算得到:

其中,ΔOD为光学密度的变化值,Q为单位面积注入和抽出电荷量,Tb为褪色态透过率,Tc为着色态透过率。
2 铁配位聚合物电致变色材料
2.1 单臂有机配体
Boom等[61]通过改变吡啶的数量和吡啶-联吡啶之间的键序(H2C—CH2、HC=CH、C≡C)合成了4种铁多吡啶基配合物1~4(图2a),然后使用浸涂工艺生成4种分子组装体MA1~MA4。4种配合物分别具有以下颜色:紫色(MA1)、蓝灰色(MA2)、粉红色(MA3)和灰色(MA4)。配合物MA1和MA2(X=HC=CH)形成的分子组装体比配合物MA3或MA4(X=H2C—CH2或X=C≡C)形成的分子组装体具有更高的对比度。配合物在λ=535~591 nm处表现出MLCT带。在λ=575 nm处,测得MA1的ΔT为41%,CE为955 cm2·C-1;在λ=591 nm处,测得MA2的ΔT为 31%,CE 为 1 488 cm2·C-1,此外 MA2在经历过1.12×105次氧化还原循环后,仍然具有良好的电化学稳定性。他们还将MA1和MA2制成固态器件,对MA1和MA2分别施加-2.7~2.5 V和-3~3 V的电压,依然可以观察到从有色态到透射态之间的颜色切换(图2b)。

图2 (a)多吡啶配合物1~4的结构;(b)MA1和MA2的固态器件的颜色切换[61]Fig.2 (a)Structures of polypyridyl complexes 1-4;(b)Color switching of solid-state devices of MA1 and MA2[61]
Qiu等[62]在吸电子三联吡啶的4′位引入一个给电子二苯胺(DPA)基团,形成给电子-受体(D-A)结构,与 Fe2+配位形成 Fe(Ⅱ)配合物[Fe(L)2](PF6)2(图3)。引入DPA基团可以作为电聚合位点,经过自由基聚合反应,形成具有高导电性和良好光学性质的π-共轭苯胺基聚合物。将其通过电化学聚合的方法沉积在ITO导电玻璃上得到紫色聚合物薄膜,施加电压后实现从紫色到淡黄色的颜色变化。该电致变色材料在579 nm处测得的ΔT为20.3%,CE为164 cm2·C-1,tc为1.1 s,tb为 2.2 s。

图3 配体L和配合物[Fe(L)2](PF6)2的结构[62]Fig.3 Structures of ligand L and complex[Fe(L)](PF)[62]262
Liu等[63]将具有聚合活性的三苯胺(TPA)基团引入到菲咯啉(Phen)铁配合物中,制备了一种新型Fe(Ⅱ)配合物Fe(TPAPhen)3,进一步采用电化学聚合的方法沉积在ITO导电玻璃上形成聚合物poly-Fe(TPAPhen)3(图4a),并对其电致变色性质进行了研究。poly-Fe(TPAPhen)3薄膜在378 nm处有吸收峰,这主要归属于配体TPAPhen分子内的π-π*跃迁。随着工作电压的逐渐升高,528 nm处的特征吸收峰逐渐升高,电致变色薄膜由橘红色变为黑色,当电压超过1.1 V后,该吸收峰又逐渐降低。相反地,721 nm处的特征吸收峰一直不断增强,电致变色薄膜由黑色逐渐变为深蓝色(图4b)。该电致变色材料在762 nm处表现出高达86%的超高ΔT、971 cm2·C-1的CE和较短的响应时间,具有潜在的应用价值。

图4 (a)poly-Fe(TPAPhen)3的结构示意图;(b)poly-Fe(TPAPhen)3薄膜在不同电压下的吸收光谱图[63]Fig.4 (a)Structure schematic diagram of poly-Fe(TPAPhen)3;(b)Absorption spectra of the poly-Fe(TPAPhen)3 film at different applied potentials[63]
Tao等[64]合成了一类末端含有TPA基团的三联吡啶配体(图5),然后与Fe(Ⅱ)配位,再采用电化学聚合法制备聚合物p-FeL1、p-FeL2和p-FeL3。在0~2 V的电压区间,聚合物薄膜呈现出紫色到蓝色的可逆颜色变化。研究表明,薄膜电致变色记忆能力和稳定性取决于配体的共轭程度。共轭程度高的TPA基配体可以促进分子内电荷转移,从而有效地稳定氧化态的Fe3+,能显著提高电致变色薄膜的记忆能力和稳定性。此外,结构刚性较强的配体的聚合物p-FeL1具有较长的记忆时间(约12 min)和更好的稳定性(氧化还原300次循环后光学密度损失10%),而基于结构相对柔性的配体的p-FeL3表现出较短的记忆时间(约3 min)和较差的循环稳定性(氧化还原300次循环后光学密度损失40%)。

图5 末端含有TPA基团的三联吡啶配体和聚合物p-FeL1、p-FeL2、p-FeL3的结构[64]Fig.5 Structures of terpyridine ligands containing TPA group at the end and polymers p-FeL1,p-FeL2,and p-FeL3[64]
Jones等[65]在三联吡啶配体上引入具有电化学聚合活性的噻吩类取代基,合成了3种新型的Fe(Ⅱ)配合物Fe(L1)2~Fe(L3)2,并通过电化学聚合物制备配位聚合物薄膜,研究了溶剂对电聚合过程的影响,以及BF3·Et2O对电化学聚合的促进作用(图6)。Fe(L1)2在乙腈或BF3·Et2O溶液中均不能电聚合;Fe(L3)2尽管在BF3·Et2O溶剂中可以实现电聚合,可是肉眼几乎看不到沉积在ITO表面的彩色薄膜;配合物Fe(L2)2在无水乙腈溶液中可以电聚合在ITO涂层玻璃表面,且poly-Fe(L2)2电聚合后可以通过肉眼看到沉积在ITO表面上的彩色薄膜。进一步对poly-Fe(L2)2的薄膜展开了电致变色响应特性的研究,该聚合物薄膜可以实现从蓝色到淡黄色的颜色转换,在596 nm处表现出40%的ΔT,3 823 cm2·C-1的CE,经过900圈循环测试,ΔT几乎没有变化。

图6 Fe(L1)2~Fe(L3)2的结构及其电化学聚合过程[65]Fig.6 Structures and electrochemical polymerization of Fe(L1)-Fe(L3)[65]22
2.2 双臂有机配体
Higuchi等[66]将双联吡啶类配体(BP1和BP2)和Fe2+通过液-液界面配位聚合技术制备了2种配位纳米片(CONASHs)NBP1和NBP2(图7)。纳米片薄膜是在CH2Cl2/水的液液界面形成,其中配体在有机相中,金属离子在水相中。2个联吡啶结构单元分别由乙烯基和双(乙烯基)苯间隔基团共轭连接。由于2种配体中的间隔基不同,纳米片的颜色也不相同,NBP1为蓝色,NBP2为洋红色。制备出的多层纳米片溶解度差,可作为自支撑薄膜铺展沉积在任何基板上。将纳米片沉积在ITO玻璃上并进行了电致变色特性的研究。NBP1薄膜可以实现从蓝色到无色的颜色变化,在590 nm处具有62%的ΔT和431 cm2·C-1的高CE以及亚秒级的响应时间;NBP2薄膜可以由洋红色变为黄色,在568 nm处表现出57%的ΔT和382 cm2·C-1的CE以及亚秒级的响应时间。此外,使用该类纳米片薄膜成功制备了固态电致变色器件,在2.5~-2.5 V的电压区间,表现出可逆的电致变色颜色变化,300圈循环后仍表现出很好的稳定性。固态电致变色器件中纳米片薄膜的高稳定性表明了纳米片薄膜可以作为潜在的电致变色材料应用于下一代显示应用。

图7 配体(BP1和BP2)与CONASHs(NBP1和NBP2)的结构[66]Fig.7 Structures of the ligands(BP1 and BP2)and CONASHs(NBP1 and NBP2)[66]
Higuchi等[67]将 4,4-双(2,2∶6,2-三联吡啶基)苯基-三苯胺(LTPA)作为氧化还原活性配体和Fe2+配位,制得配位聚合物polyFe-N(图8)。该聚合物溶液呈红棕色,采用溶液旋涂工艺成膜。施加0.0~1.0 V的电压,聚合物薄膜表现出红棕色到浅绿色的可逆颜色变化。红棕色的薄膜在578 nm处显示出很强的吸收,这归因于MLCT跃迁。通过施加1.0 V的正电压,MLCT特征峰消失了,同时在近红外区域885 nm出现了一个强度几乎相同的宽吸收峰。吸收峰在578 nm下降是因为Fe2+→Fe3+的氧化过程,然而在更高的波长区域出现一个宽带,这是因为TPA基团失去一个电子形成阳离子自由基(TPA+·)。聚合物薄膜在578 nm可见光区的最大ΔT约为52%,在885 nm近红外区的ΔT达到80%。此外,制备了具有该聚合物的固态电致变色器件,通过反复施加0~1.5 V的电压,并在4 000多次循环中在可见光和近红外范围内ΔT几乎不变。双氧化还原金属配位聚合物的设计,从可见光区域到近红外区域的可调节电致变色以及耐用的器件结构,将有助于开发具有可见光到近红外区域可调节遮光功能的下一代节能智能窗。

图8 配体LTPA的结构和相应的Fe(Ⅱ)配位聚合物的形成示意图[67]Fig.8 Structure of ligand LTPAand formation diagram of the corresponding Fe(Ⅱ)coordination polymers[67]
Kurth等[68]将含有二噻吩间隔基的2,6-双(2-吡啶基)嘧啶配体和Fe2+自组装形成配位聚合物(图9a),通过浸涂工艺成膜。对这一薄膜施加0.0~1.6 V的电压,观察到其由绿色到红色的颜色变化。氧化态的薄膜表现出覆盖近红外区域(约1 500 nm)的宽吸收带(图9b),这是由于二噻吩间隔物中的电荷离域引起的LMCT。

图9 (a)含有二噻吩间隔基的2,6-双(2-吡啶基)嘧啶配体的结构及其Fe(Ⅱ)配位聚合物形成示意图;(b)聚合物薄膜的吸收光谱[68]Fig.9 (a)Structure of 2,6-bis(2-pyridyl)pyrimidine ligand containing a di-thiophene spacer and formation diagram of the corresponding Fe(Ⅱ)coordination polymer;(b)Absorption spectra of the coordination polymer film[68]
Higuchi等[69]将2种不同的氧化还原活性金属离子Fe(Ⅱ)和Os(Ⅱ)与三联吡啶单元交替配位形成双金属配位聚合物,并结合阴离子的调控制备了多色显示电致变色器件。异金属会在电压变化时引起多种颜色的变化,而阴离子将有助于调节配位聚合物在不同溶剂中的溶解度。合成了4种具有不同阴离子(BF4-、Cl-、PF6-和OAc-)的双金属配位聚合物(HBPs)。其中,只有HBP-OAc(图10)可以通过喷涂法制备电致变色薄膜。随着施加的电压不断增大(0.0~0.7 V),由于Os(Ⅱ)离子的氧化,薄膜的颜色由紫色变为淡紫色,在496和674 nm处Os(Ⅱ)的MLCT峰消失。当电压继续升高到1.0 V时,Fe(Ⅱ)离子被氧化,薄膜颜色由淡紫色变为黄绿色,在575 nm处Fe(Ⅱ)的MLCT峰消失,同时在405和522 nm处出现2个新的吸收峰。在λ=575 nm处测得薄膜的ΔT为52%(ΔT1),在λ=496 nm(Os(Ⅱ)的MLCT 的高强度峰)测得薄膜的ΔT为45%(ΔT2)。这项工作代表了一种新的分子设计策略,即可以通过在一个聚合物链中引入2种不同的氧化还原活性金属离子用于开发电压可调的多色电致变色器件,还可以通过对阴离子调控来实现可溶液加工的双金属配位聚合物电致变色器件的制备。

图10 HBP-OAc的结构[69]Fig.10 Structure of HBP-OAc[69]
Higuchi等[70]将 Fe(Ⅱ)和 Ru(Ⅱ)离子与双(三联吡啶)苯依次配位,通过改变Fe(Ⅱ)和Ru(Ⅱ)的物质的量之比,合成了一系列Fe/Ru基双金属超分子聚合物,当Fe(Ⅱ)和Ru(Ⅱ)的物质的量之比为0.5∶0.5时,形成高聚物FeL1Ru-2(图11)。所制得配位聚合物可以通过喷涂法成膜。基于2种金属离子的氧化还原电位不同,聚合物在不同的施加电位下,Fe(Ⅱ)先氧化变色,Ru(Ⅱ)再氧化变色,聚合物表现出从紫色变为橙色再变为浅绿色的多色显示电致变色行为。基于Fe(Ⅱ)和Ru(Ⅱ)离子的MLCT效应,光谱分别在508和585 nm处显示了2个特征MLCT吸收峰。由于Fe2+→Fe3+的氧化过程,585 nm处的吸收峰在0.7 V处开始降低,在0.8 V时Fe2+几乎完全被氧化,一些Ru2+开始被氧化,Fe2+在585 nm处的MLCT吸收峰在0.9 V时消失,但Ru(Ⅱ)离子的MLCT吸收仍然存在,直到1.2 V才消失。FeL1Ru-2在508 nm处的ΔT为68%,CE 为 242.1 cm2·C-1;在 585 nm 处的 ΔT为37%,CE为 188.2 cm2·C-1。

图11 FeL1Ru-2的结构[70]Fig.11 Structure of FeL1Ru-2[70]
Higuchi等[71]将Cu(Ⅰ)和Fe(Ⅱ)盐与含有菲咯啉和三联吡啶结构单元的不对称配体合成了一种新的混金属配位聚合物polyCuFe(图12)。该配位聚合物可以采用溶液旋涂工艺成膜,并与凝胶电解质组装成固态器件,施加0~2.2 V的电压,显示出从紫色到蓝色再到无色的颜色变化。

图12 polyCuFe的结构[71]Fig.12 Structure of polyCuFe[71]
Higuchi等[72]将Fe(Ⅱ)离子与顺式或反式有机Pt(Ⅱ)配体1∶1配位,成功地制备了交替引入Pt(Ⅱ)和Fe(Ⅱ)离子的异金属配位聚合物:cis-polyPtFe和transpolyPtFe(图13)。cis-polyPtFe表现出更好的结晶度和低离子电导率,而trans-polyPtFe表现出较高离子电导率的非晶态性质。在0或3 V的电压下,由于Fe(Ⅱ)/(Ⅲ)的氧化还原作用,2种聚合物都表现出了紫色和黄色之间的可逆电致变色。与cis-polyPtFe相比,trans-polyPtFe具有更好的电致变色稳定性和响应时间。在580 nm处测得cis-polyPtFe的tc为2.17 s,tb为4.23 s;在580 nm处测得trans-polyPtFe的tc为1.08 s,tb为0.93 s。

图13 trans-polyPtFe和cis-polyPtFe的结构[72]Fig.13 Structures of trans-polyPtFe and cis-polyPtFe[72]
Kurth等[73]合成了含有吡啶连接体的双三联吡啶配体,然后与Fe2+配位形成2种Fe(Ⅱ)配位聚合物(图14),采用浸涂工艺成膜。研究表明吡啶连接体的引入提高了电致变色开关的稳定性和可逆性。在λ=596 nm处,测得其中一种聚合物薄膜的ΔT为73%,CE为620 cm2·C-1。在λ=594 nm处,测得另外一种聚合物薄膜的ΔT为76%,CE为720 cm2·C-1。这2种薄膜在1 000次循环后ΔT略有下降。

图14 含有吡啶连接体的双三联吡啶配体的结构和相应的Fe(Ⅱ)配位聚合物的形成示意图[73]Fig.14 Structures of bis-terpyridine ligands with pyridine linkers and formation diagram of the corresponding Fe(Ⅱ)coordination polymers[73]
Kurth等[74]使用Fe(Ⅱ)和配体L1~L5自组装合成了铁配位聚合物 Poly-FeL1~Poly-FeL5(图15a),它们具有不同的取代基和不同数量的间隔基。该类聚合物因三联吡啶外围的取代基的不同或间隔基数量的不同表现出不同的颜色(图15b)。配体三联吡啶基团上的取代基对这些配位聚合物的电致变色性能有很大影响,而间隔基的长度对其影响较小。含给电子基团甲氧基的配位聚合物(Poly-FeL3和Poly-FeL4)具有快速的响应速率、良好的可逆性、高的稳定性和良好的光存储性能。

图15 (a)配体L1~L5与配位聚合物Poly-FeL1~Poly-FeL5的结构;(b)Poly-FeL1~Poly-FeL5溶液的颜色(从左到右)[74]Fig.15 (a)Structures of ligands L1-L5and coordination polymers Poly-FeL1-Poly-FeL5;(b)Colors of Poly-FeL1-Poly-FeL5 solutions(from left to right)[74]
Schott等[75]在2个三联吡啶基团之间引入不同数量的亚苯基作为间隔基共轭连接(配体tpy-tpy、tpy-ph-tpy、tpy-ph2-tpy),合成了一系列新型Fe(Ⅱ)配位聚合物(图16a),研究了间隔基的长度对这种薄膜的光学和电致变色性质的影响。聚合物通过浸涂工艺成膜,施加较低电压下Fe-MEPE(MEPE=metallosupramolecular polymer)薄膜可以在还原态和氧化态之间可逆切换。FeL0-MEPE在正电压下可由蓝色变为无色,在负电压下可进一步变为灰色;FeL1-MEPE在正电压下可由蓝紫色变为无色,在负电压下可进一步变为绿色;FeL2-MEPE在正电压下可由蓝紫色变为黄色,在负电压下可进一步变为绿色(图16b)。Fe-MEPEs的循环稳定性在超过10 000次循环中得到了证实,表明该类材料在智能窗户和智能标签方面非常有前景。

图16 (a)配体tpy-tpy、tpy-ph-tpy、tpy-ph2-tpy的结构和相应的Fe-MEPE;(b)FeL0-MEPE、FeL1-MEPE、FeL2-MEPE薄膜在不同电压下的颜色[75]Fig.16 (a)Structures of ligands tpy-tpy,tpy-ph-tpy,tpy-ph2-tpy,and corresponding Fe-MEPE;(b)Colors of FeL0-MEPE,FeL1-MEPE,and FeL2-MEPE films at different voltage[75]
Liu等[76]将2个三联吡啶基团用非共轭烷基链连接,合成了3种新型Fe(Ⅱ)配位聚合物FeL1~FeL3(图17a),采用溶液旋涂法成膜。施加电压后FeL1~FeL3薄膜均能实现从紫色到浅黄色的颜色转变。通过改变烷基链连接体的长度,可以调节Fe(Ⅱ)配位聚合物薄膜的形貌和疏水性。由于FeL2中非共轭烷基链连接体的长度比FeL1更长,相同条件下FeL2具有比FeL1更优越的电致变色性能,包括更短的开关时间、更低的操作电位、更高的ΔT和显色效率。FeL2能表现出高达76%的ΔT。此外FeL3因为含有更长的烷基链,具有更好的疏水性(图17b),可以在环保型水系电解质中实现电致变色的可逆切换。

图17 (a)非共轭烷基链连接的双三联吡啶配体的结构和相应的Fe(Ⅱ)配位聚合物的形成示意图;(b)FeL1、FeL2和FeL3粉末样品的水溶性测试[76]Fig.17 (a)Structures of non-conjugated alkyl chain-linked bisterpyridine ligands and formation diagram of the corresponding Fe(Ⅱ)coordination polymers;(b)Water solubility test for powder samples of FeL1,FeL2,and FeL3[76]
Park等[77]合成了含铁酞菁的金属铁配位聚合物Pc-Fe-polymer(图18a),将聚合物通过喷涂方式成膜,并研究了其在溶液和固体器件中的电致变色行为,均表现出从蓝色到透明绿色的颜色转变。铁酞菁(FePc-TP)间隔基的存在使聚合物在670~700 nm处存在较强吸收,此外聚合物的MLCT特征吸收峰在578 nm附近。因此,Pc-Fe-polymer覆盖了广泛的可见光和近红外区域。Pc-Fe-polymer在溶液和固态器件中都表现出超过1 000次的开关稳定性。将Pc-Fe-polymer应用于塑料基板上的柔性电致变色器件上,柔性器件在平、弯2种状态下均表现出可逆的颜色转变(图18b),证明了配位聚合物用于柔性显示的可行性。

图18 (a)Pc-Fe-polymer的结构;(b)弯曲状态下含有Pc-Fe-polymer的柔性电致器件的颜色切换[77]Fig.18 (a)Structure of Pc-Fe-polymer;(b)Color switching of the flexible electrochromic device containing Pc-Fe-polymer in a bent state[77]
Higuchi等[78]使用含有三联吡啶和菲咯啉部分的不对称双位配体(L)一步合成了三维超支化Fe(Ⅱ)基金属超分子聚合物polyFe-3D(图19)。旋涂聚合物薄膜显示出红色和淡绿色之间的可逆颜色变化,在λmax=573 nm处测出具有70%的ΔT和689 cm2·C-1的高CE。聚合物薄膜在超过1 000次循环测试中表现出高稳定性。同时还制造了一种含polyFe-3D的固态简单器件,该器件在超过1 000次循环测试中仍保持良好的稳定性。

图19 不对称配体(L)的结构式和polyFe-3D结构示意图[78]Fig.19 Structural formula of asymmetric ligand(L)and schematic diagram of polyFe-3D structure[78]
2.3 三臂有机配体
Higuchi等[79]将Fe(Ⅱ)离子和由菲咯啉基团组成的三重双齿配体L3phn通过液-液界面配位聚合技术,成功制备了纳米片薄膜Fe-L3phn(图20)。施加电压后,沉积在ITO上的纳米片薄膜可以显示出从红色到无色的颜色切换,在λmax=518 nm处测得ΔT为55%,tb和tc分别为3.3和2.9 s,该薄膜的CE为230 cm2·C-1。此外,利用该纳米片薄膜制备了固态电致变色器件,令人惊讶的是,该固态器件至少在15 000个电致变色开关周期内具有高度耐用性,这显示出纳米片薄膜作为高耐久性电致变色材料在未来显示应用中的巨大潜力。

图20 通过三重配体(L3phn)与Fe(Ⅱ)配位制备纳米片的合成方案以及在液-液界面形成的纳米片[79]Fig.20 Synthetic scheme for the preparation of the nanosheets by the complexation of the tritopic ligands(L3phn)with Fe(Ⅱ)and picture of the nanosheets formed at the liquid-liquid interface[79]
Nishihara等[80]将三联吡啶配体(1)分别与Fe2+和Co2+通过液-液界配位聚合技术制成了纳米片薄膜1-Fe、1-Co(图21)。1-Fe薄膜可以实现深紫色到浅黄色的可逆颜色变化,并且在800个循环内是稳定的。1-Co薄膜可以呈现橙色到紫色的可逆颜色变化。将1-Fe和1-Co杂化成一个双电致变色的固态器件,将一个沉积在ITO玻璃上的1-Fe薄膜修饰为“0”的形状作为工作电极,将另一个沉积在ITO玻璃上的1-Co薄膜修饰为“1”的形状作为对电极。在施加特定电压后,双电致变色的固态器件交替显示“1”和“0”。

图21 配体1、纳米片1-Fe和1-Co的结构[80]Fig.21 Structures of ligand 1,nanosheet 1-Fe,and 1-Co[80]
Higuchi等[81]将Fe(Ⅱ)盐与不同比例的双(三联吡啶)和三(三联吡啶)配体(图22a)逐步配位,合成了一系列具有三维结构的Fe(Ⅱ)金属配位聚合物(FeL1x%L2y%)。基于MLCT吸收,所有三维聚合物薄膜都呈现蓝色。三维聚合物薄膜的多孔结构有助于氧化还原过程中离子的顺利转移和改善电致变色性能。其中FeL185%L215%(图22b)薄膜表现出最好的电致变色性能,tc为 0.19 s,tb为 0.36 s,ΔT为50.7%,CE为 383.4 cm2·C-1。

图22 (a)双(三联吡啶)和三(三联吡啶)配体的结构;(b)FeL185%L215%的预期结构和AFM图像[81]Fig.22 (a)Structures of bis(terpyridine)and tris(terpyridine)ligands;(b)Anticipated structure and AFM image of FeL1L2[81]85%15%
Zhang等[82]将星形配体三(4-(4′-2,2′∶6′,2″-三联吡啶)-苯基)胺(TPA-TPY)和Fe2+通过液-液界面配位聚合技术制备了不同厚度的纳米片薄膜Fe-TPATPY(图23),研究表明电致变色的响应时间不受纳米片厚度的影响,而CE随着纳米片薄膜厚度的增加而增加。纳米片薄膜在0 V下的中性状态下呈现紫红色,在580 nm处存在Fe(Ⅱ)-三联吡啶基团的MLCT吸收峰。当施加电压逐渐增大到1.4 V时,Fe2+在纳米片膜中发生氧化,在580 nm处的MLCT吸收峰强度下降甚至消失,同时在421 nm处有新的吸收峰强度逐渐上升,纳米片薄膜颜色由紫红色变为橙黄色。进一步将纳米片薄膜上的施加电位从1.4 V提高到1.6 V,TPA部分发生氧化,在780 nm处出现了一个新的吸收峰,纳米片薄膜颜色从橙黄色又变为绿色。该纳米片薄膜经过500次循环后ΔT几乎不变,具有出色的稳定性。这项工作表明,作为纳米片的二维聚合物金属配合物也能够实现多色显示电致变色。
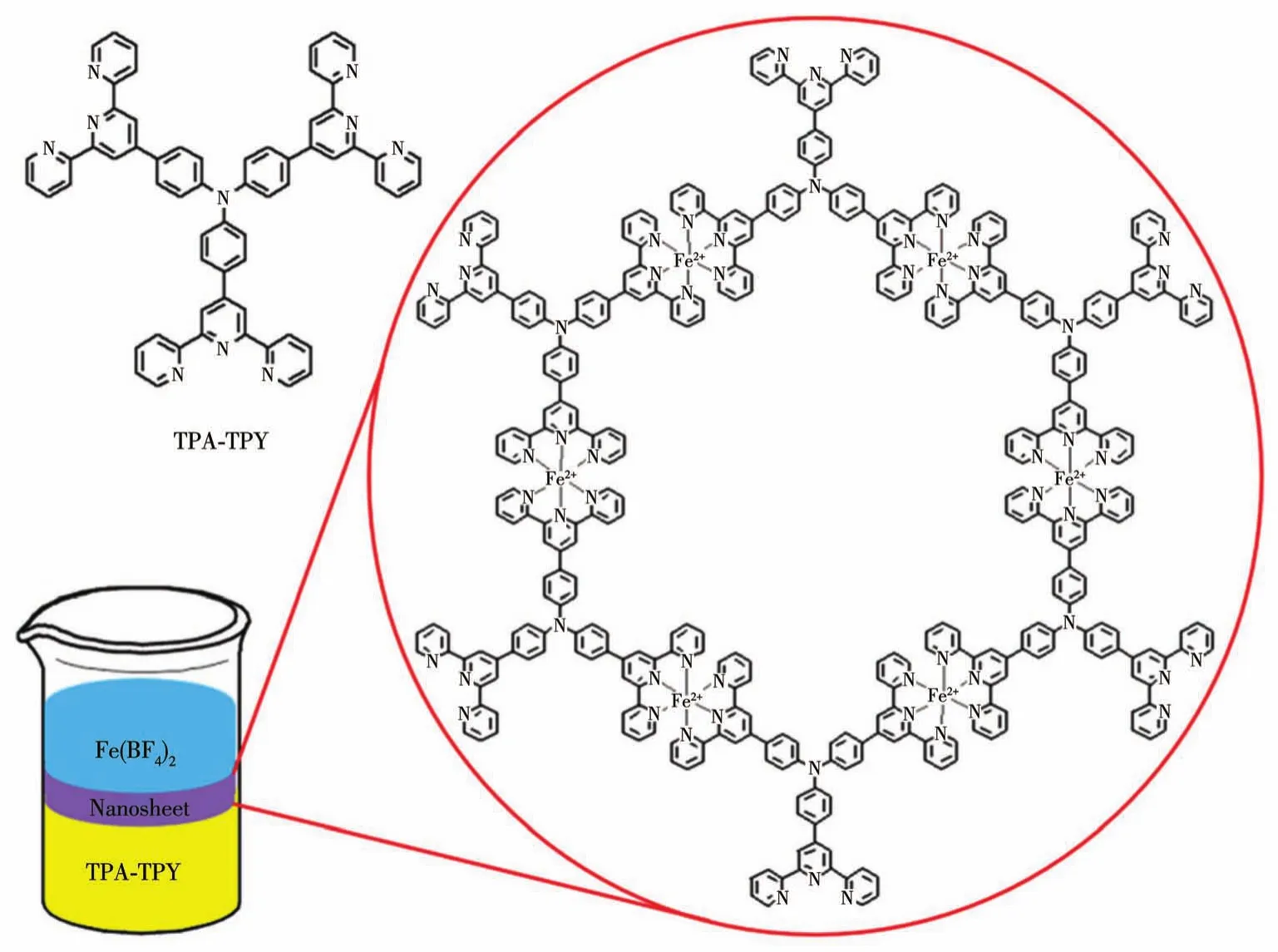
图23 配体TPA-TPY的化学结构及三联吡啶-Fe(Ⅱ)纳米片的液-液界面自组装方法和化学结构[82]Fig.23 Structure of ligand TPA-TPY,the liquid-liquid interface self-assembly method and the structure of the terpyridine-Fe(Ⅱ)nanosheet[82]
Chakraborty等[83]将具有非共轭三联吡啶基的柔性三臂配体3tpy与Fe2+通过液-液界面配位聚合技术制备纳米片薄膜3tpy-Fe(图24)。基于该纳米片薄膜的固态器件在3~-2 V的电压区间表现出粉红色到无色的转变,具有53.1%的高ΔT,470.16 cm2·C-1的高CE,超过1 000次的高循环稳定性。此外,非共轭且柔性的3tpy配体的存在限制了电子在膜内的转移/跃迁,从而降低了膜在开路条件下透射率衰减能力,在25 min时还能保留50%的无色状态。而在类似条件下,具有共轭三联吡啶的3tpyC-Fe仅在20 min内就显示出95%的显色状态。

图24 配体3tpy和纳米片3tpy-Fe的结构[83]Fig.24 Structures of ligand 3tpy and nanosheet 3tpy-Fe[83]
Wong等[84]基于水溶液中的Fe(Ⅱ)金属离子和有机溶剂中的TPA取代的烷基三联吡啶的星形配体TBT,通过液-液界面自组装方法制备了一种新型金属超分子膜(图25)。由于存在柔性烷基臂,所获得的薄膜表现出优异的柔韧性,并且可以紧密黏附在ITO玻璃表面。光谱电化学实验表明,薄膜可以显示出从紫色到黄绿色的颜色变化。TBT-Fe薄膜在570 nm处的ΔT约为20%,CE约为172.82 cm2·C-1,tc约为14.3 s,tb约为7.3 s,TBT-Fe薄膜的响应时间较长是由于烷基链的引入破坏了配体结构的共轭程度,从而降低了TBT-Fe薄膜的电荷传输能力。
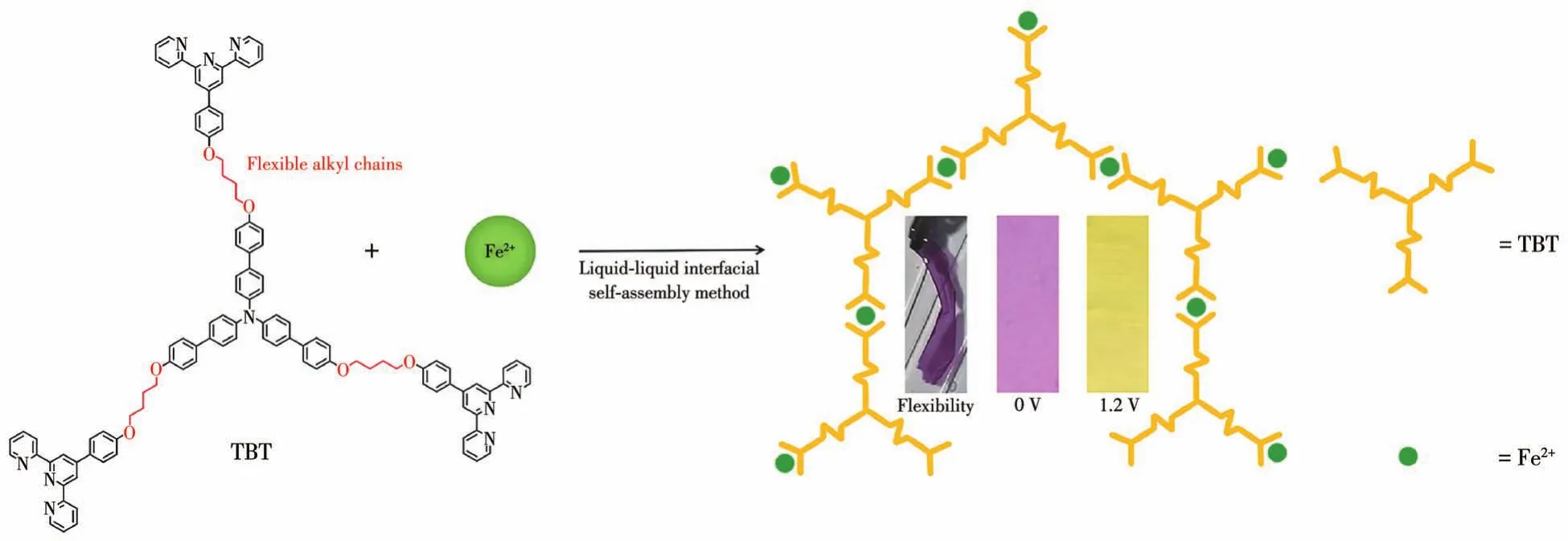
图25 配体TBT的结构和相应的Fe(Ⅱ)配位聚合物的形成示意图[84]Fig.25 Structure of ligand TBT and formation diagram of the corresponding Fe(Ⅱ)coordination polymer[84]
Park等[85]合成了一个轴向取代聚异丁烯(PIB)的三吡啶功能化亚酞菁,并制备了一种新的Fe(Ⅱ)金属配位聚合物poly-subPc-Fe(图26a)。PIB的存在使得该聚合物可以溶解在DMF中,可以通过溶液旋涂成膜。施加0.0~1.6 V的电压,该聚合物薄膜表现出从蓝色到透射态的转变(图26b),且漂白态具有91.8%的高透光率。该聚合物薄膜的稳定性在长达1 000次循环中表现非常好,且具有325.3 cm2·C-1的高显色效率。高分子共轭亚酞菁间隔基通过使电荷离域而提高聚合物薄膜的稳定性。亚酞菁加入到配位聚合物中将引起人们对开发新型电致变色材料的强烈兴趣。

图26 (a)poly-subPc-Fe的结构示意图;(b)poly-subPc-Fe在中性和氧化状态下的颜色转换[85]Fig.26 (a)Structure schematic diagram of poly-subPc-Fe;(b)Color switching of poly-subPc-Fe at neutral and oxidized states[85]
3 总结和展望
配体分子结构设计方面的研究促进了铁配位聚合物电致变色材料及器件的快速发展,已取得了系列进展。这类材料表现出较大的光学对比度(高达76%)、较快的响应速率(响应时间为亚秒级别)和较高的着色效率(高达3 823 cm2·C-1)。这些优越的电致变色性能表明铁金属配位聚合物电致变色材料很有应用前景。此外,基于铁配位聚合物薄膜自组装调控可以提升材料及器件的循环稳定性,为器件的实际应用提出了新的制备途径。多氧化还原活性中心的引入可以丰富铁配位聚合物电致变色材料的变色行为,拓宽了应用领域。为了进一步提升基于铁配位聚合物的电致变色器件性能,一方面需要从分子设计,尤其从配体分子设计来调控配位聚合物分子聚集体的微观结构,以提升材料的氧化还原性质和循环稳定性。可以探索四臂配体乃至多臂配体的铁配位聚合物,研究它们的电致变色性能,并且还可以与电化学储能研究联系起来。另一方面需要匹配固态电解质来获得优异的器件性能,以满足实际应用。此外,实现电致变色器件的柔性化、微型化、可拉伸和图案化也是铁配位聚合物电致变色材料研究的发展趋势。
