面向双碳战略的CO2转化和利用研究进展概述
2022-08-28吴爱青
吴爱青
(山东省济宁市任城区委党校 山东济宁 272000)
我国近期提出了于2060 年实现碳中和的目标,为确保充足的能源供给和减少碳排放,发展CO2综合利用技术具有重要的实际意义。CO2广泛存在于自然界中,是一种潜在的资源,尽管随着工业革命,CO2饱受诟病。但是CO2同时也是一种优质的原料。CO2是一种主要的长寿命温室气体,大约占到所有温室气体的26%。
自从18 世纪下半叶起源于英国的工业革命开始以来,人类生产经营活动对化石燃料的使用量不断增加,以致大气中的CO2分子浓度快速升高。持续上升的CO2浓度使地球上的温室效应异常加重,全球气候总体上来看有持续变暖的趋势,人类活动对自然界气象变化的影响很快超过了火山喷发和太阳活动等自然现象所带来的影响。
近年来,由于人类对不可再生资源的大规模开采和使用,大气中的CO2分子浓度不断增加。根据世界气象组织于2020 年初发布的最新温室气体公报,CO2的含量已经从工业化前的280 ppm 上升到2019 年底的411 ppm,増加了约47%。
不仅如此,根据美国国家海洋与大气管理局公布的最新年度温室气体指数,从20 世纪70 年代末到2019 年,全球大气中CO2分子的浓度平均每年增加1.83 ppm,而在21 世纪20 年代的这10 年里,大气中CO2分子的浓度更是以每年2.3 ppm 的速度增长。也就是说,不仅大气中CO2的浓度没有下降的趋势,CO2浓度的増速也没有放缓的迹象。如果维持目前的排放量,统计工作者预计到2030 年全球CO2排放量仍然不会达到峰值,有继续增加的可能[1]。
大气中不断上升的CO2浓度将引发严峻的环境问题[2]。CO2浓度攀升,最直接的影响是温室效应加重,很多极端气象灾害,如飓风、洪涝和干旱等发生的频率更快,使地表下垫面遭到破坏。生态系统对此变化发生响应,会缩短水循环周期,从而加剧洪涝、干早等灾害。在这种情况下,生态系统很难自然适应或演变,从而减少了原生态系统中的生物多样性。不仅如此,随着温室效应的逐步加重,全球温度攀升,使冰川和极地冰块溶解,再加上海水受热之后膨胀,都将造成海平面升高。
为了应对海平面上升可能带来的危害和风险,人们需要建设大量海岸保护工程。而这些工程将破坏先前的海岸带湿地与沿岸沼泽地区的自然演化,使海洋和生态系统不断退化,从而使自然灾害造成的损失更大。因此降低大气中CO2的浓度,从而缓解温室效应和由此带来的其他环境问题已经成为人类面临的共同任务。
为了减少大气中CO2分子的浓度,并进一步有效解决目前的资源紧缺问题,科研工作者从多种角度尝试将CO2转化为更具工业利用价值的含碳产物[3]。由于CO2分子中碳氧双键的键长短、键能大,因而其化学性质非常稳定。直接将CO2分子进行活化非常困难,往往需要很高的压强或温度。为了使化学反应在相对温和的环境中进行,也为了减小反应所需的外加能量,活化反应需要借助特定的媒介,也就是催化剂,来降低催化反应需用的活化能,从而提高活化过程的速率。根据催化反应原理的不同和催化反应条件的不同,常用的CO2转化方法可以进行如下分类:光合作用[4]、酶促反应[5]、催化重整[6]、光催化反应[7]和电催化反应[8]等。光合作用和酶促反应主要是利用生物体内和生物体外的蛋白质酶在相对温和的环境中催化CO2转化为有机物;催化重整主要是利用CH4热解反应器和CO2消碳反应器在催化剂的作用下将CO2转化为合成气;矿化作用主要是通过地表岩石中的空隙来储存CO2,使CO2在地中经过漫长的物理化学过程形成碳酸盐矿物,从而固定CO2光催化转化CO2主要是利用半导体催化剂在光照下产生的高能量的激发电子来活化CO2,并通过加氢步骤使CO2还原为低价态的碳氢化合物:电催化转化CO2主要是在外加电压的作用下,使电子通过催化剂注入CO2分子中,并在水溶液中质子的作用下,不断加氢最终转变成更具工业价值的碳氢产物。
该文将对CO2的转化与利用展开详细论述。
2 CO2化学利用基础
CO2化学利用主要是利用其化学性质,通过化学、光学、电学、热催化作用,主要将其转化成化学物质、燃料、建筑材料、聚合物以及新型材料,真正地实现了碳资源的循环使用,具体见图1。然而中心碳原子处于最高氧化态,其自由能很小,是一个热力学高度稳定的化合物,所以如何开发高效的催化体系,实现CO2催化转化,需要深入探索与研究,而顺利实现化学转化这一过程中的关键问题是如何将中心碳原子活化。
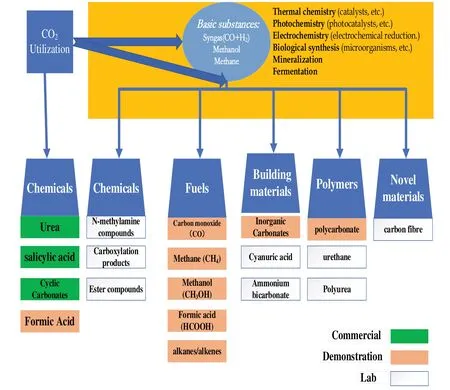
图1 二氧化碳的化学利用技术
2.1 CO2活化与转化的理论基础
为了实现CO2的化学利用,首先要对CO2的结构和活化方式有充分的认识。CO2具有2 个SP 杂化轨道,每个杂化轨道各含有1/2S 和1/2P 轨道,轨道夹角180°。
CO2成键类型(2σg)²(2σu)²(1σg)²(1σu)²(1πu)4(1πg)4(2πu)0,其 中,(1σg)²(1σu)²(1πu)4为成键轨道,(2σg)²(2σu)²(1πg)4为非键轨道,所以CO2分子有2 个σ 键,2个π 键。CO2中的碳原子为缺电子中心,其可以作为一个亲电体,并与亲核试剂或者带电子基团发生反应。
2.2 CO2的活化
CO2中的C 是最高氧化态,整个分子处于最低能量态,化学性质稳定,常见的性质具体见表1,其叙述的都是一种惰性分子。因此,要使CO2活化,需要克服热力学壁垒,通常需要利用催化剂、高温、高压等条件以达到克服热力学壁垒的要求。而最常使用的方法包括电催化/光化学活化/胺活化/Lewis 酸碱对(frustrated Lewis pairs,FLPs)活化/氮杂卡宾(Nheterocyclic carbenes,NHCs)活化以及过渡金属活化等方法。其中,电催化及光化学活化是最为主要的方法。

表1 CO2的化学性质
接下来将对上述方法一一进行总结和评述,具体叙述如下。
2.2.1 电催化
电化学还原CO2是近年来研究的热点,也就是利用电催化的手段将CO2还原生成高附加的化学品(例如甲醇、CO 等),这个技术可以实现将CO2转化为易于存储和运输的稳定的化学能,这个过程可以定义为CO2还原的异相催化反应,其主要在电解池中进行,发生在催化材料的阴极材料表面。对温度要求低(不需要高温,往往室温条件下即可发生反应)。CO2附着在电解池的阴极上,通过捕获电子使自身活化,从而形成还原产物。
这个技术最核心的问题就是开发催化剂用来修饰电极以提高反应速率从而促使转化效率提高。纳米金属材料是一种较好的电催化剂,因其有较高的催化表面积,含有大量的边缘以及低配位位点,同时具有不同的催化行为,因此TiO2等纳米材料受到广泛的关注。
运用电化学合金化/脱合金,并结合酸处理的方法制备出纳米多孔结构金(NP Au)的电催化剂,用于将CO2电化学还原为CO。金属金经过处理得到的纳米多孔结构材料具有电流密度大、产率高和稳定性好等优良特点,有利于电化学还原过程的进行。然而,贵金属的高成本和低丰度制约了其在实际工作中的大规模应用,因此需要选择储量高并且具有高效催化作用的电催化剂来弥补这个问题。
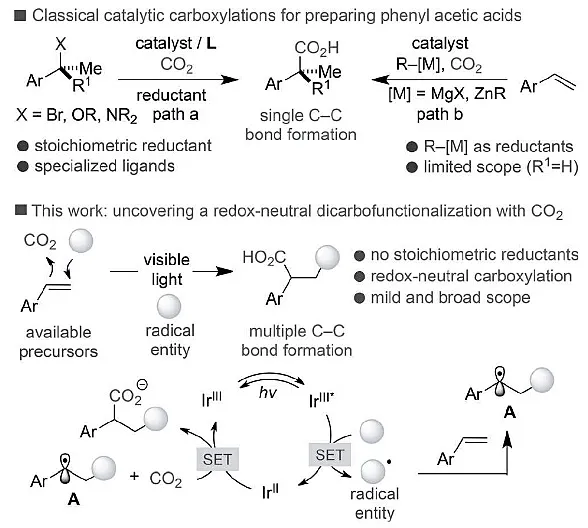
图5 二氧化碳转化为羧酸衍生物的机理
近年来,随着对于纳米技术在非贵金属催化剂的制备中得到更好的应用,其逐渐展现出在CO2还原方面可以媲美贵金属的优异性能,该技术将可能是未来的研究方向[9]。
同时,文中显示的图2 为电化学CO2还原的反应装置示意图。
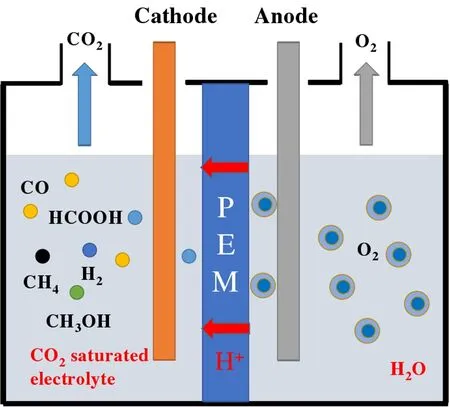
图2 电化学CO2还原的反应装置示意图
2.2.2 光化学活化
因其类似于自然界中的光合作用,所以光化学还原CO2的反应,一般被认为是一种人工的光合作用。光化学催化还原CO2是氧化还原耦合的过程,入射光的能量必须等于或者大于催化剂的带隙,以达到在光照的情况下催化剂被激发,光生电子由价带激发到导带。由于光生电子具有很强的还原能力,催化剂表面吸附的CO2能够用来还原。光催化过程为:光吸收产生电子空穴对、光生载流子分离并转移到光催化剂表面、CO2吸附以及表面氧化还原反应、产物解析。
光催化剂是光催化还原中重要的物质,它在很大程度上决定着CO2的转化效率。目前,一半导体材料为主的催化体系是主要的研究方向,其中TiO2具有无毒、稳定性好、耐光腐蚀和催化性能好的特点,是目前应用比较广泛的光催化材料。然而TiO2因其材料的禁带宽度较大,只能在紫外线辐射下才能被激活,所以光能利用率低,导致CO2的转化率较低,因此许多学者为了提高其转化效率从而开始对TiO2材料进行改性[10]。其中有些方法较为有效,例如:将蔗糖水热聚合得到的碳球(CSs)固定在TiO2表面形成交联碳材料,使其光响应区域得到明显扩增,从而提高了TiO2的可见光吸收效率,增大了CO2转化率。
其中,文中显示的图3 是光催化还原CO2原理图。

图3 光催化还原CO2原理图
3 技术与实践
现如今,随着CO2转化方法及相关技术的发展与精进,CO2被利用于催化转化制备能源产品,催化转化制备化学品,催化转化制备高分子材料,以及矿化制备无机材料,实际生产产物及过程包括其主要转换方式。
CO2的化学转化方式具体情况见图4。
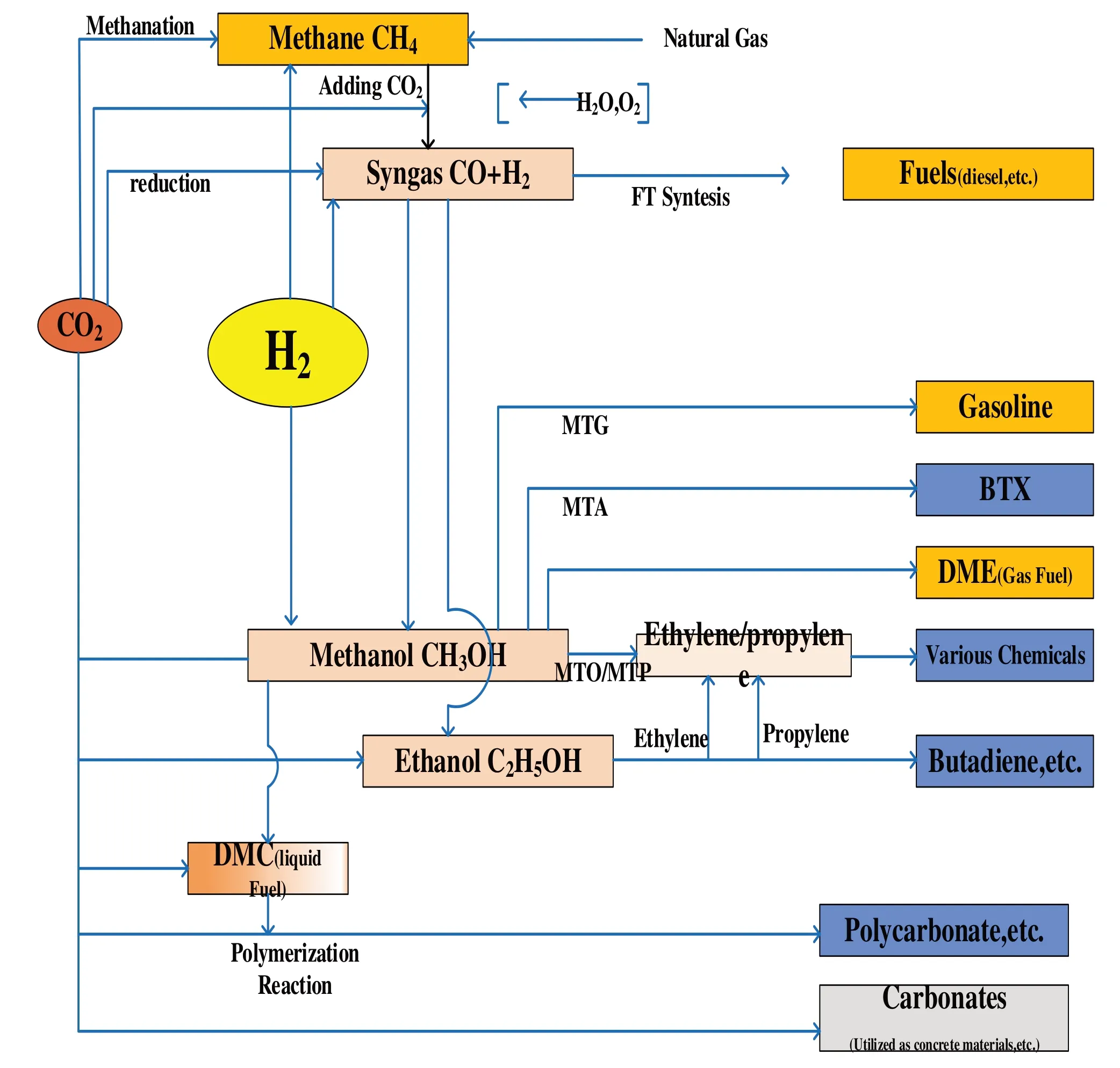
图4 CO2的化学转化方式
3.1 目前主要应用
3.1.1 合成尿素
目前,工业上用液相NH3和CO2反应合成尿素,属于有气相存在的液相反应。反应被认为分两步进行,具体如下。

氨基甲酸铵的生成(液体)是一个体积缩小的、可逆的、反应速率较快的强放热反应,在较短的时间内就可达到化学平衡,并且达到平衡后CO2转化为氨基甲酸铵的百分数很高。
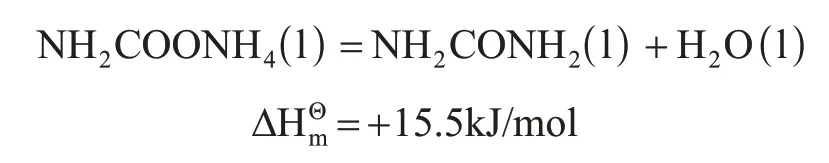
3.1.2 环状碳酸酯
环状碳酸酯是一种应用十分广泛的化合物,广泛应用于混合物的萃取分离、有机合成等领域。利用环氧化物和CO2为原料来合成环状碳酸酯是目前已经工业化的技术,该反应进行的关键在于通过加入催化剂对CO2和环氧化物进行活化,从而使反应顺利进行。
3.2 处于示范应用或者实验室研究阶段
3.2.1 CO2催化转化制备能源产品
(1)CO。
CO 是一种重要的气体工业原料,由CO 出发可以制备几乎所有的液体燃料或基础化学品。将CO2转化为CO 是CO2高值利用的重要途径,从节约资源和能源的角度考虑,是生产CO 的绿色途径。其反应方程式如下。
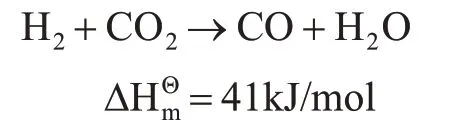
这是一个吸热反应过程,需要较高的反应温度。目前,催化剂普遍存在稳定性较差的问题。例如:Cu 催化剂在高温下易烧结,氧化失活,工业应用中易发生硫中毒;Al/Zn 催化剂易高温还原失活;Pt/Ce催化剂易积炭失活。因此,研究开发高活性和高稳定性的RWGS 反应催化剂,以高效快速制备CO,是实现RWGS 反应过程制备CO 的关键。
(2)CH4。
CH4是最简单的有机化合物,也是重要的基础化工原料。其化学反应方程式如下。
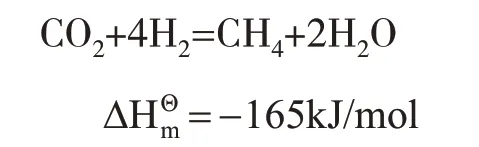
(3)甲醇。
甲醇不仅是一种重要的、需求巨大的有机化工原料,也是一种理想的清洁能源,在农业、畜牧业、石油化工、燃料电池和发电等领域均具有广泛的应用。

要实现CO2的活化和转化需要使用高效催化剂来降低CO2反应的活化能垒。目前,常见的CO2加氢制甲醇催化剂主要包括铜基催化剂、贵金属负载型催化剂及其他类型催化剂。
(4)甲酸。
CO2加氢合成甲酸也是重要的反应,这个反应可以充分利用物质,甲酸也是一个非常理想的化工原料。然而,当前CO2还原制甲酸仍面临着诸多挑战,包括反应动力学迟缓、甲酸选择性较低等。因此,开发经济、稳定、高选择性的电催化材料是实现电化学CO2还原制甲酸技术大规模应用的关键所在。

3.2.2 二氧化碳催化转化制备化学品
(1)酯类化合物。
DMC 是近年来受到国内外广泛关注的环保型绿色化工产品。

(2)N-甲胺化合物。
二甲基甲酰胺既是一种用途极广的化工原料,也是一种用途很广的优良溶剂。由二甲胺和CO2/H2反应合成DMF,是一条合成DMF 的绿色途径,具有重要的实用价值。
(3)羧化产品。
以CO2为原料用于C-C 键形成反应,得到具有重要生物活性的羧酸衍生物。
4 结语
我国于近期提出了2060 年实现碳中和的目标,碳减排和碳中和已成为国家长期战略。低碳发展也是我国实现生态文明重大战略的重要组成。低碳发展目前最艰巨的任务就是减少CO2的排放。CO2作为目前最主要的温室气体,如何将CO2转化为便于存储的化学能,是当前国际前沿课题。为此,该文通过对CO2化学利用基础以及CO2活化与转化的理论基础的综述,总结了CO2的活化方式,重点分析了电催化及光化学活化的CO2转化方式。并根据其活化方式概括其现有应用以及未来的可能应用。
