伏立康唑治疗AIDS合并马尔尼菲篮状菌病患者疗效与剂量的相关性及安全性
2022-07-11李金卓严汝庆李晓云刘燕飞
李金卓 严汝庆 李晓云 刘燕飞
[摘要]目的分析伏立康唑治疗艾滋病(AIDS)合并马尔尼菲篮状菌(TM)病患者疗效与剂量的相关性及安全性。方法选择贺州市人民医院2019年1月至2020年3月收治的50例AIDS合并TM病患者作为研究对象,采用随机数字表法将其分成对照组和方案组,每组各25例,对照组采用负荷剂量伏立康唑治疗,方案组先采用负荷剂量伏立康唑治疗,而后采血监测伏立康唑的血药浓度,并根据检测结果调整伏立康唑的剂量,比较两组患者治疗期间的不良事件发生率、治疗总有效率、平均住院时间及平均住院费用。结果方案组患者治疗期间不良事件发生率显著低于对照组,治疗总有效率显著高于对照组,平均住院时间显著短于对照组,差异均有统计学意义(P<0.05);方案组患者平均住院费用略高于对照组,但差异无统计学意义(P>0.05)。结论伏立康唑治疗AIDS合并TM病患者的疗效与安全性均较高,且其治疗效果与剂量密切相关,需要临床在治疗过程中对患者行血药浓度监测,并根据监测结果合理调整其用药剂量,以提高患者治疗效果。
[关键词]伏立康唑;艾滋病;马尔尼菲蓝状菌病;剂量;血药浓度
[中图分类号]R512.91;R519
[文献标识码]A
[文章编号]2095-0616(2022)11-0005-05
艾滋病即获得性免疫缺陷综合征(acquired immune deficiency syndrome,AIDS),是一种由人类免疫缺陷病毒(human immunodeficiency virus,HIV)感染所致的恶性传染病,不仅可引发患者出现持续发热、盗汗、虚弱、全身淋巴结肿大等症状,同时还易诱发其出现多种并发症,如皮肤和黏膜损伤、马尔尼菲篮状菌(talaromycesmarneffei,TM)病等,其中以并发TM多见[1]。两者合并存在,不仅会加重患者机体不适症状,同时还可加速AIDS病情發展,从而对患者生命安全构成严重威胁,因此,临床需尽早采取有效方案对患者进行治疗,以便改善其预后[2]。既往,临床多采用两性霉素B对AIDS合并TM病患者进行治疗,虽有一定效果,但易引发患者出现较严重的不良反应,从而导致患者治疗耐受性较低,现代临床多采用伏立康唑(voriconazole)对患者进行治疗,该药物具有良好的治疗效果和安全性,但需要监测血药浓度以指导临床合理调整用药剂量,才能保证治疗效果[3]。基于此,本研究分析伏立康唑治疗AIDS合并TM病患者疗效与剂量的相关性及安全性,现报道如下。
1资料与方法
1.1一般资料
选择贺州市人民医院2019年1月至2020年3月收治的50例AIDS合并TM病患者作为研究对象,纳入标准:1符合《艾滋病和艾滋病病毒感染诊断标准》[4]中关于AIDS合并TM病的诊断标准者;2对本研究目的和方法知情同意者。排除标准:1发生不可耐受的不良事件/严重不良事件而中途终止的患者;2妊娠期和哺乳期女性。采用随机数字表法将其分成对照组和方案组,每组各25例,对照组男女比例为2∶3,年龄27~68岁,平均(45.26±2.15)岁,病程1~4年,平均(2.09±0.47)年;方案组男女比例为11∶14,年龄29~67岁,平均(45.28±2.13)岁,病程1~4年,平均(2.12±0.48)年。
两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。医院医学伦理委员会已批准本研究立项。
1.2方法
对照组采用负荷剂量伏立康唑(湖北午时药业股份有限公司,国药准字H20140139,规格:200mg×6片)治疗,第1个24h,每12小时给药1次,静脉滴注,每次6mg/kg,后维持4mg/kg剂量,每12小时给药1次。体温控制、症状改善后,也可改为口服维持200mg,2次/d。使用伏立康唑共14d,然后改为伊曲康唑(西安杨森制药有限公司,国药准字H20020367,规格:0.1g×14片)200mg,口服,q12h。方案组先采用负荷剂量伏立康唑治疗,而后采血监测伏立康唑的血药浓度,并根据检测结果调整伏立康唑剂量,即第1个24h,每12小时给药1次,静脉滴注,每次6mg/kg,48h达稳态血药浓度后(第3天即第五剂给药前30min)采血监测伏立康唑的血药浓度,并根据检测结果调整伏立康唑的剂量(第一次),每12小时给药1次。若有剂量调整,则再经48h后(第5天即第十剂给药前30min)再次采血监测伏立康唑的血药谷浓度,并根据检测结果调整伏立康唑的剂量(第二次)。体温控制、症状改善后,也可改为口服维持200mg,2次/d。使用伏立康唑共14d,调整伏立康唑剂量,从静脉序贯口服给药时,48h后重新监测伏立康唑谷浓度,必要时再根据检测结果调整伏立康唑的剂量(第三次)。然后改为伊曲康唑200mg,口服,q12h。两组患者均连续治疗4周。
1.3观察指标及评价标准
比较两组患者治疗期间的不良事件发生率、治疗总有效率、平均住院时间、平均住院费用,治疗4周后,根据《艾滋病诊疗指南》[5]中相关标准判定疗效:治疗后,患者感染症状消失,病原学、实验室检查均恢复正常为治愈;治疗后,患者感染症状明显减轻,病原学或实验室检查中一项未恢复正常为显效;治疗后,患者感染症状明显减轻,但病原学或实验室检查均未恢复正常为好转:治疗后,患者感染症状未改善,且病原学或实验室检查均未恢复正常为无效,总有效率=(治愈+显效+好转)例数/总例数×100%。
1.4统计学分析
采用SPSS21.0统计学软件进行数据分析,计量资料用均数±标准差(x±s)表示,组间比较采用t检验;计数资料用[n(%)]表示,组间比较采用χ2检验,以P<0.05为差异有统计学意义。
2结果
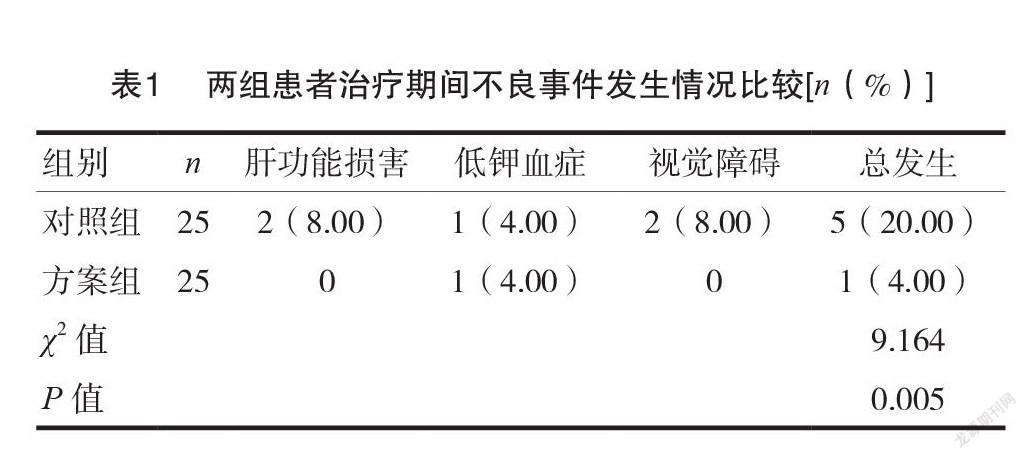
2.1两组患者治疗期间不良事件发生情况比较
方案组患者治疗期间的不良事件发生率显著低于对照组,差异有统计学意义(P<0.05),见表1。
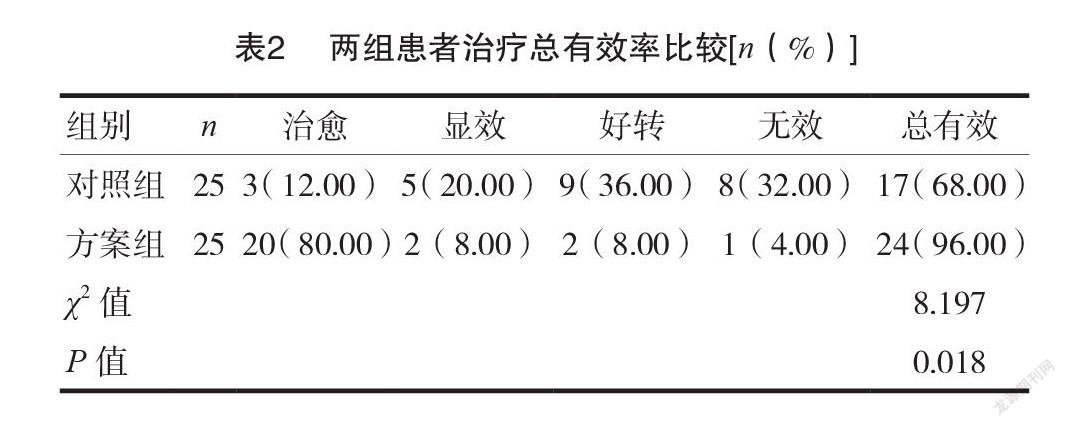
2.2两组患者治疗总有效率比较
方案组患者治疗总有效率显著高于对照组,差异有统计学意义(P<0.05),见表2。
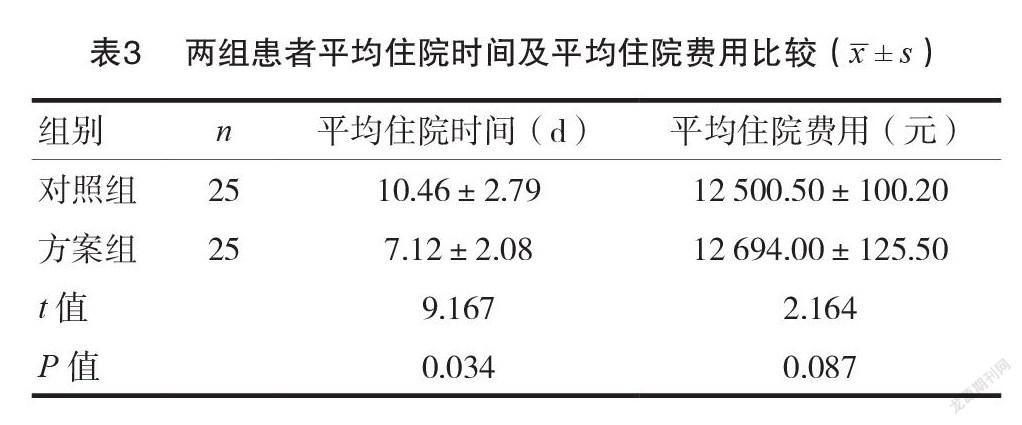
2.3两组患者平均住院时间及平均住院费用比较
方案组患者平均住院时间显著短于对照组,差异有统计学意义(P<0.05);方案组患者平均住院费用略高于对照组,但差异无统计学意义(P>0.05),见表3。
3讨论
AIDS是一种病死率极高的恶性传染病,属于严重威胁全球公共卫生与安全的重大问题。据世界卫生组织报道,到目前为止已造成3500多万人病死[6-7]。截至2017年底,全球有94万人死于艾滋病毒相关病症。全球现存活有3690万HIV/AIDS患者,有2170万例正在接受高效联合抗反转录病毒治疗(highly active anti-retroviral therapy,HAART),俗称“鸡尾酒疗法”,现又称抗反转录病毒治疗[8]。根据我国卫生健康委员会疾病预防控制局权威发布的数据统计,2018年全国法定传染病疫情报告的AIDS患者发病人数为65779人,病死人数为19107人,可见,我国艾滋病流行形势依然严峻[9]。艾滋病不仅会引发患者机体出现多种不适症状,同时还会破坏其机体免疫系统,使其逐渐丧失对各种疾病的抵抗能力而并发各类疾病,TM病便是AIDS患者最常见的并发症之一,TM是条件致病性双相真菌,主要感染免疫缺陷人群,尤其是AIDS患者[10]。AIDS合并TM病不仅可引发患者出现发热、贫血、咳嗽、皮疹、脐凹样皮疹、全身淋巴结肿大及肝脾肿大等症状,随着病情持续进展,还易诱发其出现多器官功能衰竭,最终导致其病死,有相关数据表明,AIDS合并TM病患者的病死率高达33.3%,因此,临床需尽早采取有效方案对患者进行治疗,以改善其预后[11]。
多项权威指南均推荐两性霉素B和伊曲康唑作为治疗TM病的常用药物,伏立康唑亦是治疗方案选择之一,对此,有研究人员采用伏立康唑和两性霉素B对AIDS合并TM病患者进行治疗,结果显示,伏立康唑和两性霉素B治疗AIDS合并TM病的有效率无显著差异,但两性霉素B治疗组临床毒副反应较重且出现了血清肌酐的升高,而伏立康唑组患者肝、肾损害等不良反应较少,说明相比于两性霉素B,伏立康唑治疗安全性更高[12-13]。
从两组病例方案组谷浓度共监测32例次的分布情况分析,血药浓度范围为0.2~13.1μg/ml,其中有效谷浓度(≥1μg/ml)有45例(90.00%),安全谷浓度(≤6.0μg/ml)有39例(78.00%),在有效且安全的谷浓度范围内(1.0~6.0μg/ml)有34例(68.00%),提示谷浓度偏高(7例,21.88%)仍占较高比例。方案组患者临床治疗总有效为24例(96.00%),有7例次血药浓度监测结果超出安全范围。本研究给予相同剂量,在相似的时间点监测其血药浓度,却出现较大的个体差异,提示血药浓度监测的必要性。
本研究结果显示,方案组患者治疗期间不良事件发生率显著低于对照组(P<0.05),其中1例出现不良反应的患者血药浓度监测结果为9.8μg/ml。给予相同的剂量,在相似的时间点监测其血药浓度,却出现较大的个体差异,虽然本研究的样本例数偏少,但仍提示血药浓度监测的必要性。在实际临床应用中,应根据监测的血药浓度调整伏立康唑的给药剂量,使患者的血药浓度达到有效的安全范围。方案组患者治疗总有效率显著高于对照组,平均住院时间显著短于对照组(P<0.05);方案组患者平均住院费用略高于对照组(P>0.05),提示对患者采用伏立康唑治疗,既能提高患者的治疗有效率,还可以降低不良事件发生率,缩短患者住院时间,因而具有良好的经济效益和社会效益。
伏立康唑是一种广谱的第二代三唑类抗真菌药,其作用机制是抑制真菌中由细胞色素P450介导的14α-甾醇去甲基化,从而抑制麦角甾醇的生物合成。临床上主要用于治疗侵袭性曲霉病、对念珠菌属(包括耐氟康唑的克柔念珠菌,光滑念珠菌和白念珠菌耐药株)引起的严重侵袭性感染、足放线菌菌属和镰刀菌属引起的严重感染,对治疗青霉菌属感染亦有效[14-15]。然而,因AIDS合并TM病患者通常同时合用抗逆转录病毒药物、抗结核药物等,使用伏立康唑时可能存在复杂的相互作用,可能会使药物浓度达不到有效治疗范围,从而增加临床合理用药的难度,影响临床治疗效果,甚至是治疗失败。另外,伏立康唑具有较强的靶点亲和力,通过肝脏细胞色素P450同工酶,CYP2C19、CYP2C9和CYP3A4代谢,其代谢具有饱和性[16]。CYP2C19在其代谢中有重要作用,该酶具有基因多态性,所以其药代动力学呈非线性,个体间药代动力学差异较大。暴露药量增加的比例远大于剂量增加的比例,因而个体间用药差异较大。上述酶的抑制剂或诱导剂可能分别增高或降低伏立康唑的血药浓度。研究表明,若给予常规剂量的伏立康唑,仅49%的患者血药浓度达标,达标率低[17]。因此,国内指南推荐:对肝功能不全患者、联合使用影响伏立康唑药代动力学药物的患者、细胞色素P4502C19基因突变的患者、发生不良事件或疗效欠佳的患者、重症真菌感染危及生命的患者应进行伏立康唑血药浓度监测[18]。虽然国外一些指南推荐使用伏立康唑的患者应监测血药浓度以指导其临床用药,但是目前国际上尚无伏立康唑个体化用药指南,仅法国、加拿大、澳大利亚有伏立康唑血药浓度推荐的目标范围,分别为1~4、1.5~5.0、1~6μg/ml,国内外指南推荐的伏立康唑血药浓度目标范围如有效谷浓度、安全谷浓度和推荐范围及采样时间均不一致[19-20]。
本研究中,对两组AIDS合并TM病患者分别按照药品说明书采用负荷剂量伏立康唑治疗(对照组)及先采用负荷剂量伏立康唑治疗,而后采血监测伏立康唑的血药浓度,并根据检测结果调整伏立康唑的剂量(方案组)。结果显示,方案组患者平均住院时间显著短于对照组,治疗期间不良事件发生率均显著低于对照组,方案组患者治疗总有效率显著高于对照组(P<0.05);方案組患者平均住院费用略高于对照组(P>0.05),提示通过监测伏立康唑血药浓度合理调整用药剂量,对提高患者治疗效果具有重要影响。
本研究结果提示伏立康唑治疗AIDS合并TM病患者的疗效与其剂量密切相关,且治疗效果良好、安全性高,但本研究的样本数量较少,可信度存在一定不足,这是本研究的局限之处,在后续研究过程中,将进一步扩大样本量,进行更深入的探究,明确伏立康唑剂量影响其治疗效果的作用机制。
综上所述,伏立康唑治疗AIDS合并TM病患者的疗效与安全性均较高,其治疗效果与剂量密切相关,需要临床在治疗过程中对患者血药浓度进行监测,并根据监测结果合理调整其用药剂量,以提高患者治疗效果。
[参考文献]
[1]张云桂,高丽,李惠琴,等.不同抗真菌药物对艾滋病合并马尔尼菲篮状菌病临床疗效及体外药敏试验结果分析[J].中国皮肤性病学杂志,2020,34(5):555-558.
[2]薛晓拉,高秋洁,陈媛媛,等.2018年郑州市第六人民医院伏立康唑致不良反应分析[J].现代药物与临床,2020,35(3):558-562.
[3]陶然,师金川,郭永征,等.两性霉素B去氧胆酸盐、两性霉素B脂质体和伏立康唑诱导治疗HIV相关性隐球菌脑膜炎的效果比较[J].新发传染病电子杂志,2019,4(2):97-102.
[4]邵一鸣,康来仪,汪宁,等.艾滋病和艾滋病病毒感染诊断标准[J].中国艾滋病性病,2012,18(4):272-275.
[5]中华医学会感染病学会艾滋病学组.艾滋病诊疗指南[J].中华传染病杂志,2006,24(2):133-144.
[6] Costa JDM,Torres TS,Coelho LE,et al.Adherence to antiretroviral therapy for HIV/AIDS in Latin America and the Caribbean:Systematic review and meta-analysis[J].Journal of the International AIDS Society,2018,21(1):25066.
[7]郭剑,高洪艳,王媛.基于组基础模型的全球HIV/AIDS死亡纵向资料分析[J].现代预防医学,2020,47(10):1729-1732.
[8]金颖康,吴上志,辜淑君,等.儿童非人类免疫缺陷病毒感染相关播散性马尔尼菲青霉菌病15例临床回顾分析[J].中国实用儿科杂志,2018,33(9):707-711.
[9]魏金瑛,欧阳沿音,蔡双启,等.伏立康唑治疗播散性马尔尼菲蓝状菌病临床分析[J].中国真菌学杂志,2017,12(2):92-97.
[10]师金川,喻剑华,张忠东,等.艾滋病合并马尔尼菲青霉菌病7例分析[J].浙江预防医学,2016,28(2):178-180.
[11]王星,董明亮.33例艾滋病伴播散性马尔尼菲青霉菌病患者的临床分析及其对抗真菌治疗的影响[J].抗感染药学,2019,16(1):72-75.
[12] Kaneez S.Depression and coping mechanism among HIV/ AIDS patients under anti-retroviral therapy[J].Indian Journal of Social Psychiatry,2019,32(2):149.
[13]張婧,周波,简凤璧,等.人类免疫缺陷病毒感染/获得性免疫缺陷综合征患者门诊药学服务研究进展[J].中国临床药学杂志,2019,28(3):237-240.
[14]倪维,杨柳,刘光忠.中医院艾滋病患者医院感染多重耐药菌监测分析[J].中国医药导报,2018,15(22):143-145,149.
[15]夏华.替诺福韦酯联合拉米夫定治疗获得性免疫缺陷综合征合并乙型肝炎病毒感染的临床效果研究[J].中国医药,2018,13(5):718-720.
[16]樊红丽,高丽,毛小琴,等.云南省艾滋病患者分离新生隐球菌的药物敏感性检测与分析[J].中国感染控制杂志,2019,18(4):340-343.
[17]吴菁,高申苗.伏立康唑血药浓度监测对侵袭性肺部真菌感染患者的影响[J].河南医学研究,2020,29(14):2586-2588.
[18]鲁雁秋,黄晓婕,吴玉珊,等.203例艾滋病合并新型隐球菌性脑膜炎患者预后影响因素研究[J].中华神经医学杂志,2018,17(4):397-401.
[19]李公英.96例肺部真菌感染患者伏立康唑血药浓度监测对临床安全用药的指导意义[J].抗感染药学,2020,17(4):498-501.
[20]江灏,唐敏,李薇,等.1例伏立康唑诱发精神症状的病例分析[J].中国药物应用与监测,2020,17(2):136-138.
(收稿日期:2021-11-23)
