麻竹叶提取物的超声辅助酸水解工艺研究
2022-04-13张芳戴毅李洪庆陶文亮许子竞
张芳,戴毅,李洪庆*,陶文亮,许子竞
(1.贵州民族大学 化学工程学院,贵阳 550025;2.贵州工程应用技术学院 化学工程学院,贵州 毕节 551700)
麻竹(DendrocalamuslatiflorusMunro)是禾本竹亚科牡竹属多年生木本植物[1],主要分布于福建、四川、贵州和云南等地[2]。麻竹应用广泛,竹材可用于建筑、造纸和手工艺术品等[3],竹笋可食用[4],在麻竹的开发利用过程中产生的大量竹叶被当作废弃物丢弃,不仅浪费资源,而且污染环境。有研究发现,麻竹叶中的黄酮类化合物具有抗氧化、消炎和抑菌等作用[5-6],竹叶黄酮类物质作为一种功能性食品[7-8],可作为食品添加剂广泛应用于保鲜剂[9-10]、饲料添加剂[11-12]及调味剂[13-14]等生产中。因此,对麻竹叶中黄酮类化合物进行研究具有重要理论意义。
竹叶中的黄酮类化合物主要以碳苷黄酮为主,其次为氧苷黄酮[15];碳苷黄酮的水溶性较强,且具有较高的稳定性,不易被酸水解,而氧苷黄酮结构不稳定,易被水解[16]。文献调研发现,有关酸水解竹叶黄酮类化合物的研究较少,主要有:张英等[17]发现毛金竹竹叶中碳苷黄酮的键能较强,酸水解条件控制不当会造成含量测定误差;Guo等[18]运用HPLC-光电二极管阵列检测器(DAD)测定筠竹竹叶提取物水解液中的化合物,利用液相色谱-电喷雾离子化-质谱法(LC-ESI-MS)分离鉴定出荭草苷(orientin)、异荭草苷(isoorientin)、牡荆苷(vitexin)和异牡荆苷(isovitexin)等碳苷黄酮。目前,国内外对麻竹叶黄酮类化合物的超声波辅助酸水解工艺研究未见报道。
本文以赤水麻竹叶的提取物为研究对象,考察超声功率、底物浓度、盐酸浓度、时间和温度等因素对4种碳苷黄酮含量的影响,通过响应面法优化超声波辅助酸水解工艺,为进一步开发麻竹叶资源提供了理论依据。
1 材料与方法
1.1 原料及仪器
1.1.1 实验原料
麻竹叶:由贵州赤天化纸业股份有限公司提供,经贵州民族大学生态环境工程学院苏春花副教授鉴定。
1.1.2 实验仪器

1.1.3 实验试剂
荭草苷、异荭草苷、牡荆苷和异牡荆苷标准品:纯度>98%,成都植标化纯生物技术有限公司;盐酸、冰醋酸和甲醇:分析纯,重庆川东化工有限公司;甲醇:色谱纯,安徽天地高纯溶剂有限公司;超纯水:实验室自制。
1.2 实验方法
1.2.1 标准品溶液配制及标准曲线绘制
精密称取适量荭草苷、异荭草苷、牡荆苷和异牡荆苷标准品,用甲醇超声溶解,定容至25 mL容量瓶中,得到单标对照品储备液,见表1。
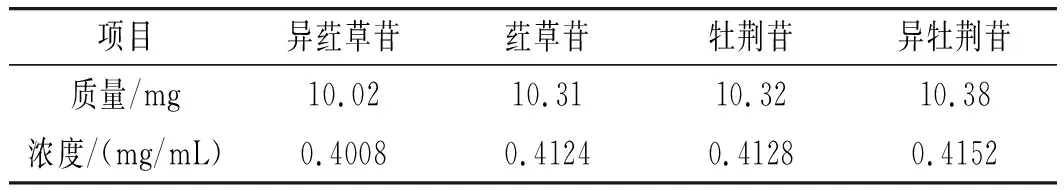
表1 4种碳苷标准品储备液制备Table 1 The preparation of four C-glycoside standard sample stock solution
分别吸取单标储备液,配制成一定浓度的混合对照品标准溶液(见表2),绘制标准曲线。

表2 混合对照品标准溶液浓度Table 2 The concentration of standard solution of mixed reference sample μg/mL
1.2.2 麻竹叶提取物制备
准确称取过60目筛的麻竹叶粉100.0 g于2000 mL烧瓶中,加入1600 mL 80%乙醇,在70 ℃下超声(300 W)回流提取50 min,提取3次,合并提取液,减压浓缩,除醇,冷冻干燥,得麻竹叶提取物。
1.2.3 样品溶液制备
精确称取一定质量的麻竹叶提取物于25 mL容量瓶中,加入甲醇定容,制成一定浓度的麻竹叶提取物样品溶液。从中精密吸取0.5 mL于10 mL水解管中,加入3.5 mL甲醇稀释,摇匀,再加入1 mL一定浓度的盐酸,密封,摇匀,于超声清洗仪中设置一定功率、时间和温度进行水解。超声结束后,冷却至室温,转移到10 mL容量瓶中,用少量甲醇冲洗水解管3次,合并冲洗液与水解液,定容,过0.22 μm滤膜,得样品溶液。
1.2.4 高效液相色谱条件
采用Agilent TC-C18色谱柱(250 mm×4.6 mm,5 μm),流动相为甲醇(A)-0.1%冰醋酸水溶液(B),体积流量1.00 mL/min,柱温30 ℃,检测波长330 nm,进样量10 μL,梯度洗脱条件见表3。

表3 流动相梯度洗脱程序Table 3 The mobile phase gradient elution program
1.2.5 单因素实验
分别考察超声功率(200,250,300,350,400 W)、底物浓度(0.25,0.5,1,1.5,2 mg/mL)、盐酸浓度(0.6,0.8,1.0,1.2,1.4 mol/L)、时间(90,120,150,180,210 min)和温度(55,60,65,70,75 ℃)等因素对4种碳苷黄酮含量的影响。
总含量(%)=异荭草苷含量(%)+荭草苷含量(%)+牡荆苷含量(%)+异牡荆苷含量(%)。
式中:C标为标准品混合液中某种碳苷黄酮浓度,mg/mL;S样为样品溶液中某种碳苷黄酮峰高,mAU;V0为称样后定容体积,mL;V1为取样体积,mL;V2为取样后定容体积,mL;S标为标准品混合液中某种碳苷黄酮峰高,mAU;M为样品称样量,mg。
1.2.6 响应面实验
根据1.2.5中的单因素实验结果,以4种碳苷黄酮的含量为响应值Y,以盐酸浓度(A)、时间(B)和温度(C)为变量,进行响应面实验设计,因子编码及水平见表4。
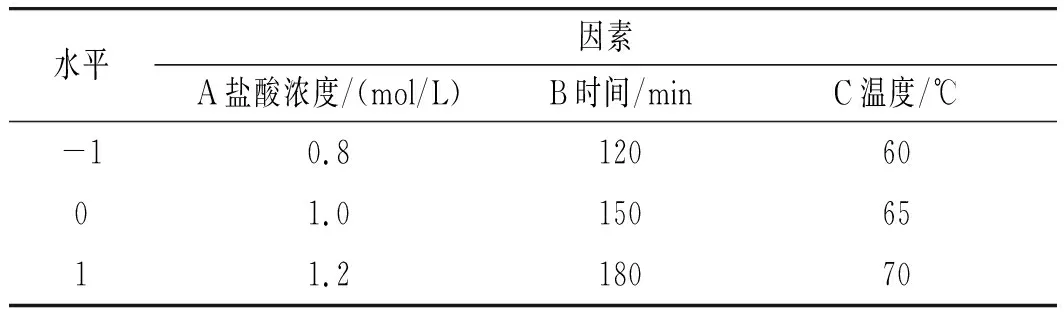
表4 三因素和三水平设计Table 4 Three-factor and three-level design
2 结果与分析
2.1 标准曲线线性关系
由图1可知,在1.2.3液相色谱条件下,异荭草苷、荭草苷、牡荆苷和异牡荆苷的出峰时间依次为29.50,30.75,32.78,36.58 min,具有较好的分离效果。以峰面积为纵坐标、浓度为横坐标,绘制标准曲线,见图2。

图1 标准品色谱图Fig.1 The chromatogram of standard sample
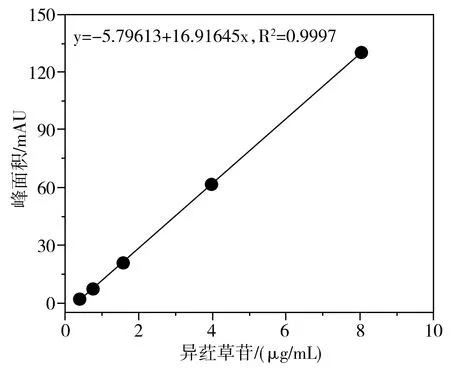
结果表明,相关系数均接近1,可在相应的线性范围内分别对4种碳苷黄酮进行定量测定。
2.2 单因素对麻竹叶提取物4种碳苷黄酮含量的影响
2.2.1 超声功率的影响
由图3可知,超声功率在200~400 W范围内,酸水解对碳苷黄酮含量的影响不明显,但300 W时得率最高。因此,固定超声功率为300 W。
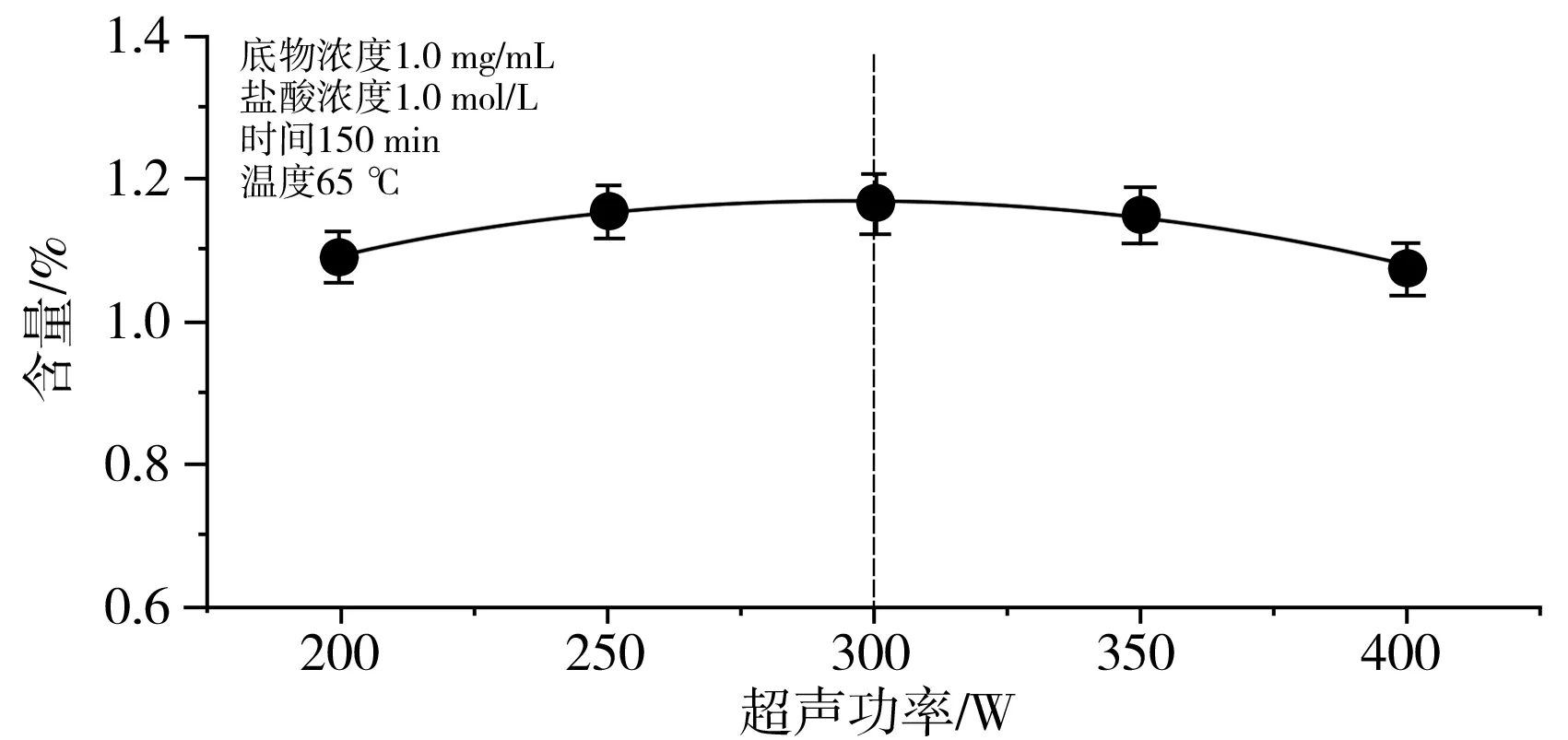
图3 不同超声功率的影响
2.2.2 底物浓度的影响
由图4可知,底物浓度在0.25~2 mg/mL范围内,酸水解对碳苷黄酮含量的影响不明显,但1 mg/mL后得率开始趋于平缓。因此,固定底物浓度为1 mg/mL。

图4 不同底物浓度的影响Fig.4 The effect of different substrate concentration
2.2.3 盐酸浓度的影响
由图5可知,盐酸浓度在0.6~1.0 mol/L的范围内,增加盐酸浓度有利于提高碳苷黄酮含量,其原因可能是在水解过程中,碳苷黄酮的衍生物转化生成4种碳苷黄酮[19]。当盐酸浓度超过1.0 mol/L时,碳苷黄酮含量开始下降,其原因可能是过高的盐酸浓度加剧了黄酮结构的破坏。因此,盐酸浓度选择1.0 mol/L为宜。

图5 不同盐酸浓度的影响Fig.5 The effect of different hydrochloric acid concentration
2.2.4 时间的影响
由图6可知,碳苷黄酮含量随着时间的延长呈先升后降的趋势;时间为150 min时,总含量达到最大值,推测为水解过程基本完成;继续延长时间,可能会更多地破坏黄酮结构。因此,时间选择150 min为宜。

图6 不同时间的影响Fig.6 The effect of different time
2.2.5 温度的影响
由图7可知,碳苷黄酮含量随着温度的升高呈先升后降的趋势;当温度超过65 ℃时,过高的温度有可能会加速黄酮结构的破坏。因此,温度选择65 ℃为宜。
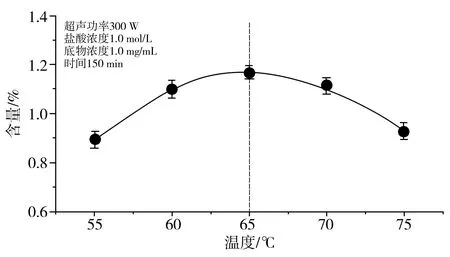
图7 不同温度的影响Fig.7 The effect of different temperatures
2.3 响应面实验优选最优条件
2.3.1 超声波辅助酸水解响应面工艺优化
通过响应面Design-Expert软件进行方差分析,得到以下结果:
将上述实验数据进行多元回归拟合,以麻竹叶提取物4种碳苷黄酮的含量(Y)为评价指标[20],对盐酸浓度(A)、时间(B)和温度(C)进行二次多项式模型方程拟合得到回归模型为:
Y=-11.45985+0.47437A+0.024779B+0.32301C-3.91667×10-3AB+0.03375AC-1.45×10-4BC-1.0575A2-3.86667×10-5B2-2.562×10-3C2。
对该模型进行显著性方差分析,分析结果见表6。

表5 实验设计与结果Table 5 The experimental design and results
由表6可知,该模型中F值为102.34,P值<0.0001,差异极显著;相关系数R2=0.9925,校正系数RAdj2=0.9828,表明实验结果有98.28%以上受到各因素的影响;失拟项的P>0.05,差异不显著,表明该模型可靠。

表6 回归系数的显著性分析Table 6 The significance analysis of regression coefficients
交互项AB、AC和BC的P值均<0.01,说明A、B和C之间交互影响较大,对4种碳苷黄酮含量的影响显著;根据表6中F值推出3个因素的主效关系:温度(C)>盐酸浓度(A)>时间(B)。
对上述回归方程进行求解,得到最优酸水解工艺:盐酸浓度为0.995 mol/L,时间为147.350 min和温度为65.426 ℃,4种碳苷黄酮含量为1.168%。
2.3.2 响应面交互因素
根据盐酸浓度(A)、时间(B)和温度(C)对碳苷黄酮含量的影响,做响应曲面和等高线图[21],见图8。
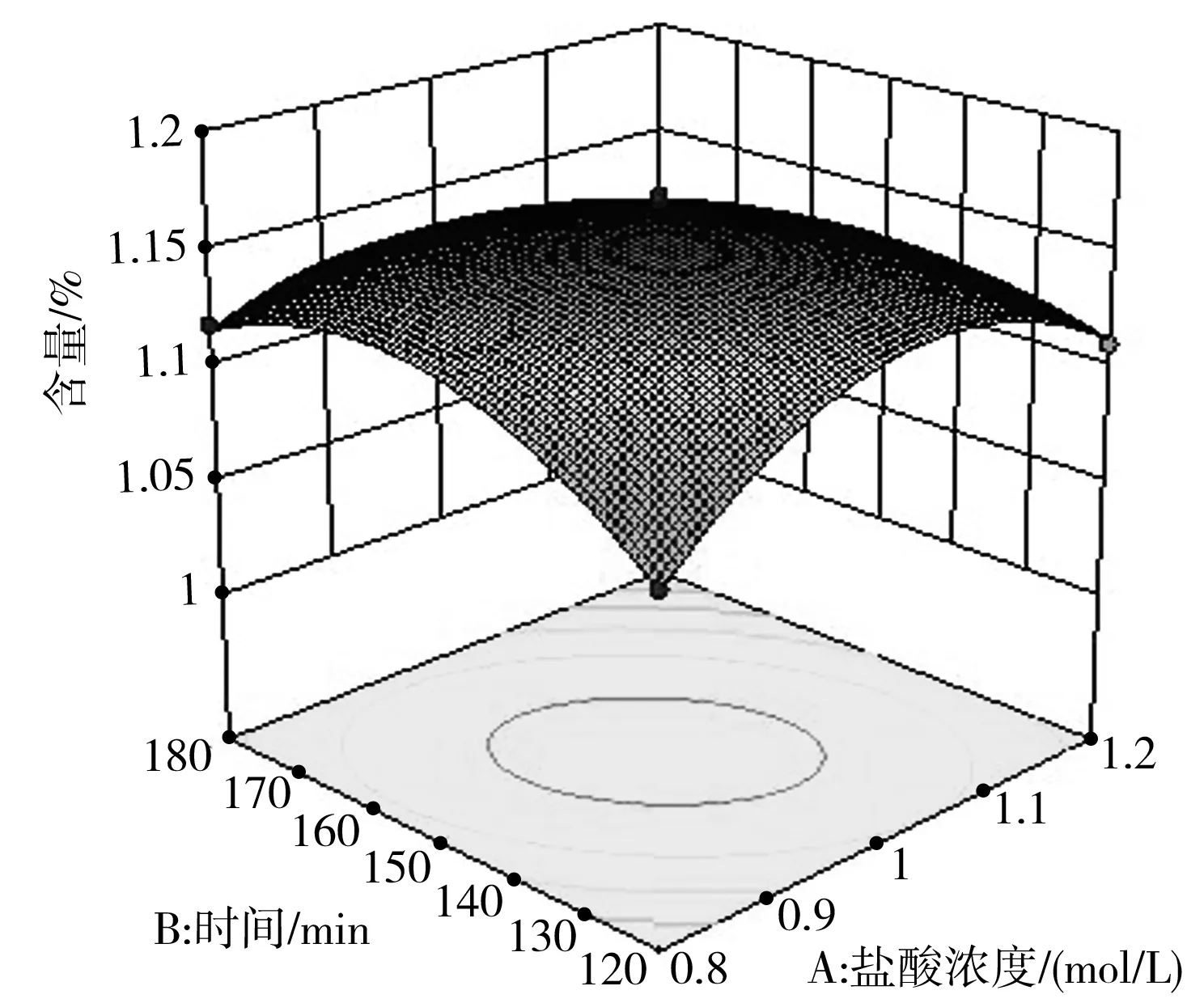
由图8可知,在AB响应面图中,A因素的坡度较陡,对其得率的影响大于B因素[22];同法考察 AC和BC响应面图,确定各因素的影响程度依次为温度(C)>盐酸浓度(A)>时间(B),与方差分析结果一致。本实验中AB、AC和BC的等高线图呈椭圆形,各因素之间的交互作用对酸水解麻竹叶提取物的影响较显著。
2.3.3 工艺验证
结合实际条件,将2.3.1项下优化的超声波辅助酸水解工艺参数调整为:盐酸浓度为1.0 mol/L、温度为65 ℃和时间为147 min。按照1.2.4项色谱条件对酸水解前与酸水解后碳苷黄酮的含量进行测定,结果见表7。

表7 平行实验结果Table 7 The results of parallel experiments %
由表7可知,验证实验得到的4种碳苷黄酮含量为1.157%(n=3,RSD=0.22%),与预测值1.168%的相对误差为0.94%,比酸水解前的4种碳苷黄酮含量高1.384倍,说明该工艺可行。
3 结论
本文在单因素实验基础上,通过固定超声功率(300 W)和底物浓度(1 mg/mL),利用响应面法优化了麻竹叶提取物的超声波辅助酸水解工艺。结果表明,影响因素的主效关系为:温度的影响最大,盐酸浓度次之,时间的影响最小;根据实际情况调整后的工艺为:盐酸浓度为1 mol/L、温度为65 ℃和时间为147 min;在此条件下,得到酸水解后麻竹叶提取物4种碳苷黄酮含量平均值为1.157%,与预测值1.168%的相对误差为0.94%,比酸水解前得率高1.384倍。在食品中添加适量的黄酮化合物可以增加食品的抗脂质氧化性,改善其风味及口感,提高食品性能。因此,深入开展麻竹叶提取物的研究对综合利用麻竹叶黄酮类化合物具有一定的指导和应用价值。
