医疗器械生产企业洁净检测分析
2022-03-30付杉杉江志杰
梁 谋,宣 泽,刘 欢,付杉杉,李 佳,江志杰
(北京市药品检验所·国家药品监督管理局仿制药研究与评价重点实验室·北京市中药成分分析与生物评价重点实验室,北京 102206)
洁净室(区)是对尘粒及微生物含量进行控制的房间(区域),其建筑结构、装备均具有减少污染源介入、产生和滞留的功能[1]。依照法律法规要求,从事医疗器械生产应具有与之相适应的生产场地和环境条件,包括不同功能区总体布局合理,生产环境整洁,厂房与设施满足产品的质量要求,洁净室(区)的洁净度级别设定应充分考虑产品特性、生产工艺和设备条件[2-4]。空气洁净级别不同的洁净室(区)之间的静压差应大于5 Pa,洁净室(区)与室外大气的静压差应大于10 Pa,相同级别洁净室间的压差梯度应合理,特殊生产区域应与相邻区域保持相对负压[5-7]。医疗器械生产企业洁净室(区)的空气净化系统工作状况良好,洁净技术指标符合规定,对于保证产品质量,避免污染环境和物料,以及保护生产工作人员安全具有重要意义。本研究中分析了北京市药品检验所2020年医疗器械生产企业洁净检测数据及检测过程中遇到的问题,为提高检测工作效率及企业生产运营管理提供参考。现报道如下。
1 资料与方法
筛选2020年北京市药品检验所医疗器械生产企业洁净室(区)的洁净级别和面积、温度和相对湿度、换气频率、静压差、沉降菌数、尘埃粒子数等信息。依照《洁净室施工及验收规范》《医药工业洁净室(区)悬浮粒子的测试方法》《医药工业洁净室(区)沉降菌的测试方法》《无菌医疗器具生产管理规范》中规定的检测方法和判定标准,分析洁净检测现场发现的问题。
2 结果
2.1 检测总体完成情况
依据相关检测方法对洁净室进行洁净检测[8],2020年共完成医疗器械生产企业洁净检测71家,包括洁净区249个,洁净室2 384间,检测面积41 269 m2。其中,十万级洁净室1 215间,检测面积25 284.1 m2;万级洁净室1 169间,检测面积15 984.9 m2,其中包括阳性室56间,微生物限度室59间,无菌室47间。
2.2 温度和相对湿度
根据相关要求,十万级和万级洁净室(区)的温度在无特殊要求时应保持在18~28℃,相对湿度保持在45%~65%。71家医疗器械生产企业有十万级和万级洁净室共2 267间(不包括对温度和相对湿度有特殊要求的117间),温度和相对湿度检测结果符合要求。其中,洁净室温度主要分布在20~24℃(64.71%),相对湿度主要分布在45%~50%(64.93%)。详见表1。
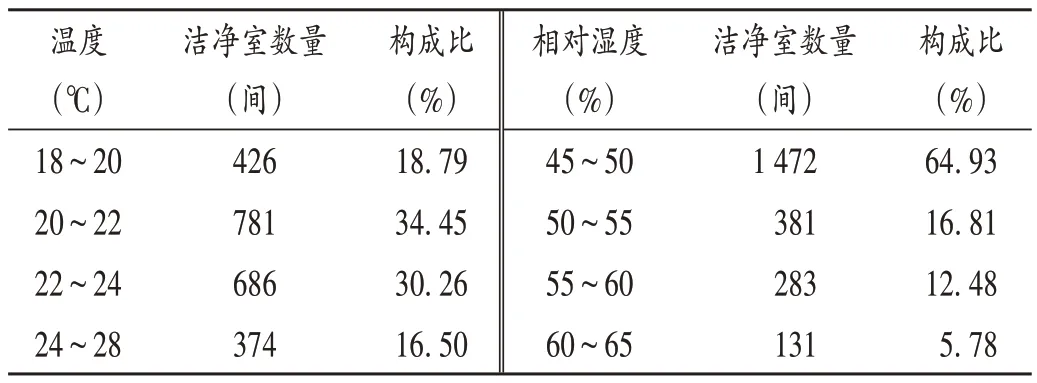
表1 洁净室温度和相对湿度检测结果(n=2 267)Tab.1 Test results of temperature and relative humidity in clean rooms(n=2 267)
2.3 换气频率
根据相关标准要求,十万级和万级洁净室(区)对换气频率的要求分别为每小时不少于15次和20次。结果各洁净室换气频率均符合规定,其中十万级洁净室换气频率以每小时15~20次最多(41.23%),万级洁净室换气频率以每小时21~30次最多(49.36%)。详见表2。检测中发现少量洁净室换气频率较高(>60次/小时),因洁净室面积小、送风量较大,换气次数较多的洁净室主要包括一更间、二更间、缓冲间、洁具间等。换气次数较多的直接影响是洁净室环境噪音增大,生产运营成本增加。
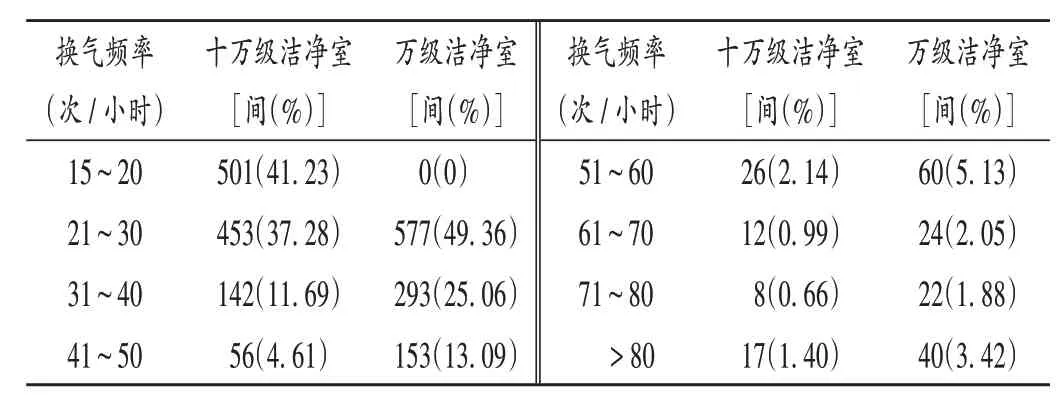
表2 洁净室换气频率检测结果Tab.2 Test results of ventilation frequency in clean rooms
2.4 静压差
根据相关要求,不同级别洁净室(区)及洁净室(区)与非洁净室(区)之间的静压差应不小于5 Pa。十万级和万级洁净室静压差符合要求的房间数量分别为201间和179间,其中十万级洁净室的静压差主要维持在11~20 Pa(51.74%),万级洁净室静压差主要维持在11~20 Pa(45.25%)。详见表3。
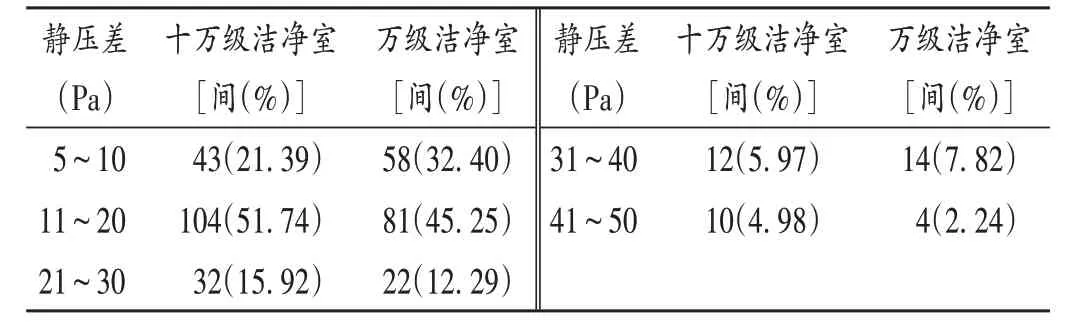
表3 静压差检测结果Tab.3 Test results of static pressure difference
2.5 沉降菌数
沉降菌数为洁净室环境洁净监测的主要指标之一[9],十万级及万级洁净室每皿沉降菌数分别应不超过10个和3个。十万级洁净室中共236间(19.42%)检测出沉降菌,以1个/皿(72间,30.51%)及2个/皿(71间,30.09%)居多;万级洁净室共120间(10.26%)检测出沉降菌,以1个/皿(56间,46.67%)居多。详见表4。
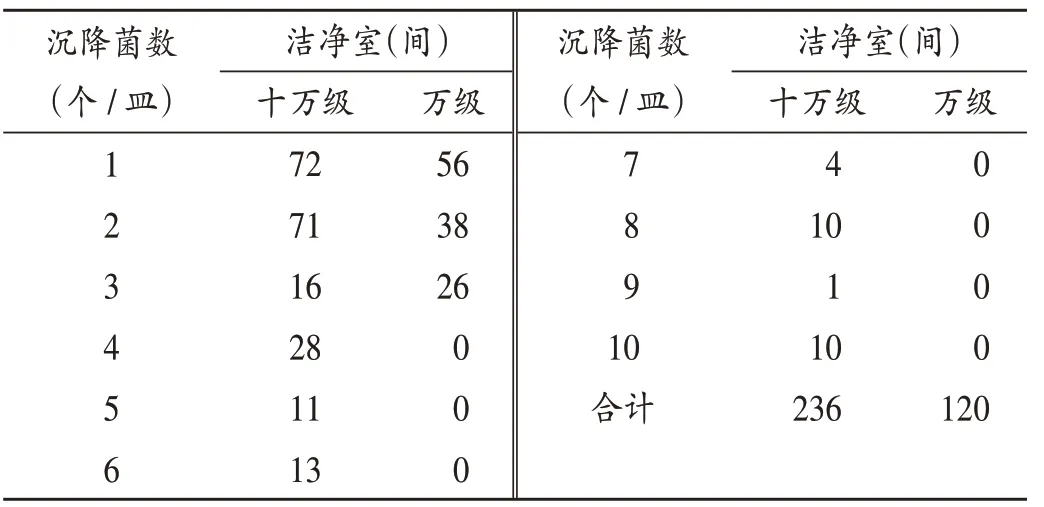
表4 沉降菌检出情况Tab.4 Detection results of sedimentation bacteria
十万级洁净室检测出沉降菌的房间主要包括一更间、二更间、缓冲间、洁净走廊、洁具间、洗衣整衣间,占检测出沉降菌洁净室总数的67.80%;万级洁净室检测出沉降菌的房间主要包括一更间、二更间、缓冲间和洁净走廊,其中,缓冲间占检测出沉降菌房间总数的占比最大(33.33%)。详见表5。
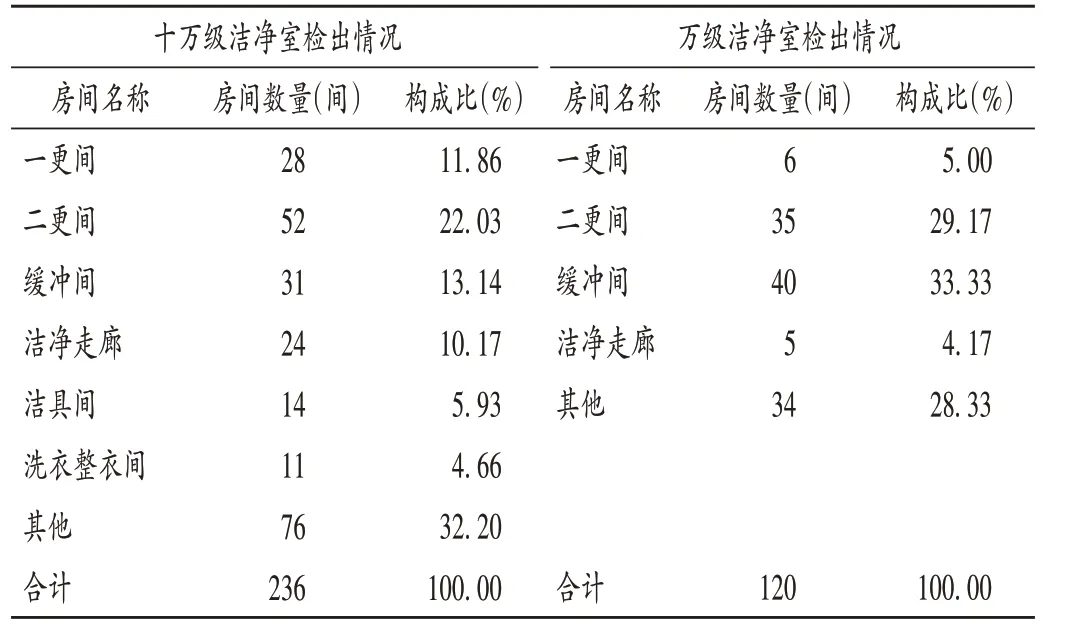
表5 检测出沉降菌洁净室的房间分布情况Tab.5 Room distribution of clean rooms with sedimentation bacteria
2.6 尘埃粒子数
各洁净厂房尘埃粒子数检测结果均符合规定,但个别使用年限较长、硬件环境较差的洁净室尘埃粒子数较高,需引起重视。企业应加强人员培训,保证生产人员净化程序符合规定,适当增加换气频率,强化空气净化硬件系统维修保养,注意洁净室的日常卫生,从而保证尘埃粒子数水平维持在规定范围内。
3 讨论
3.1 现场发现的问题
洁净室设计不合理:71家企业中,1家的洁净室内有承重钢梁,钢梁体积较大,且正对洁净室门口,而洁净室面积较小,且内有实验用操作台和仪器设备,导致进出洁净室不方便,影响实验操作;1家的女闸间和女二更间的门设计较窄,现场测量宽度不足0.6 m,进出时易磕碰到门框;1家的阳性室、无菌室和微生物室面积均仅3.7 m2,根据相关要求,洁净室(区)工作人员人均面积应不少于4 m2。洁净室面积小,给人员进出和日常生产操作及维持内部的洁净环境带来了负面影响;2家阳性室的门向阳性室外打开,这是错误的,为防止污染物扩散,门应向阳性室内打开。
洁净室内实验设备存放位置不合理:有的企业在百级洁净工作台内放置体积较大生产用设备,但洁净工作台的台面面积有限,不便于生产操作,也不易使洁净工作台内部气流保持单向流通。
洁净室维护经验不足:个别企业设备维护人员对洁净室空气净化系统不熟悉,不能及时有效地处理洁净室风量调整及相对湿度调节等一般性问题。
3.2 洁净厂房日常生产和维保建议
对于一更间、二更间和缓冲间等检测出沉降菌概率较高的区域,可适当增加换气次数,或加强对生产人员进出洁净室的程序管理,以此降低对洁净环境的负面影响。目前,一些医疗器械生产企业的部分产品实行订单式生产模式,由于生产期限有严格要求,需短期招聘临时工作人员,更需对人员进出洁净生产区、无菌操作洁净生产区及无菌操作等方面进行培训。对于部分洁净室换气频率较高的情况,应请专业人员对送风系统进行调整,保证洁净室间的压差维持在合理稳定水平[10],在降低洁净室噪音的同时,也可减少生产成本。对于洁净室的不合理设计,应及时调整,有条件的企业可在后续的洁净厂房升级改造过程中进行优化,特别是个别企业的阳性室、微生物室、无菌室面积不足4 m2的,应增加洁净室面积,以满足操作需要[11-13]。
综上所述,洁净区空气净化系统的有效运行是保证洁净度的关键,直接或间接影响医疗器械产品的质量,企业应设置专人专职负责洁净厂房空气净化系统和硬件系统的维护,能及时解决运行管理中的常见问题,提高生产过程中安全风险的处理能力[14-16]。
