狼毒大戟中4种二萜类成分在大鼠肝微粒体中的代谢
2022-03-04马天成马玉坤孙珈张金玲郭丽娜刘琦孙宇
马天成 马玉坤 孙珈 张金玲 郭丽娜 刘琦 孙宇




中圖分类号 R969.1 文献标志码 A 文章编号 1001-0408(2022)04-0465-08
DOI 10.6039/j.issn.1001-0408.2022.04.14
摘 要 目的 研究狼毒大戟中4种二萜类成分在大鼠肝微粒体中的代谢产物并探讨其代谢规律。方法 运用大鼠肝微粒体体外孵育法,将岩大戟内酯A、岩大戟内酯B、17-羟基岩大戟内酯A、17-羟基岩大戟内酯B加至由还原型烟酰胺腺嘌呤二核苷酸磷酸启动的大鼠肝微粒体孵育体系中,于37 ℃条件下孵育30 min,再用乙腈终止反应。以阴性组(先加乙腈再启动孵育30 min)为参考,采用超高效液相色谱-四极杆-飞行时间质谱联用技术,利用Analyst® TF 1.7.1、PeakView®2.2、MetabolitePilot 1.5、MasterView 1.2软件对其质谱裂解规律和代谢产物进行推测与鉴定。结果 4种二萜类成分在二级质谱中均易丢失H2O和CO等中性碎片。岩大戟内酯A和17-羟基岩大戟内酯A在肝微粒中的代谢反应主要为二羟基化、脱氢和一羟基化反应,分别鉴定出6、5个代谢产物。岩大戟内酯B和17-羟基岩大戟内酯B在肝微粒体中的代谢反应主要为一羟基化、水合和同分异构化反应,均鉴定出5个代谢产物。结论 岩大戟内酯A和17-羟基岩大戟内酯A在大鼠肝微粒体中均产生了羟基化及脱氢代谢产物,岩大戟内酯B和17-羟基岩大戟内酯B在大鼠肝微粒体中均产生了羟基化、水合及同分异构化代谢产物。4种二萜类成分的代谢产物均是Ⅰ相代谢产物。
关键词 狼毒大戟;二萜类成分;超高效液相色谱-四极杆-飞行时间质谱联用技术;大鼠肝微粒体;体外代谢
Metabolism of four diterpenoids of Euphorbia fischeriana in liver microsomes of rats
MA Tiancheng1,2,MA Yukun1,SUN Jia1,ZHANG Jinling1,GUO Lina1,LIU Qi1,SUN Yu1(1. Academy of Medical Sciences, Qiqihar Medical University, Heilongjiang Qiqihar 161006, China; 2. College of Traditional Chinese Medicine, Shenyang Pharmaceutical University, Shenyang 110016, China)
ABSTRACT OBJECTIVE To study the metabolites of four diterpenoids of Euphorbia fischeriana in liver microsomes of rats and to investigate its metabolic regularity. METHODS In vitro incubation system of liver microsomes of rats was built. The jolkinolide A, jolkinolide B, 17-hydroxyl jolkinolide A and 17-hydroxyl jolkinolide B were added into incubation system of liver microsomes in rats activated by reduced nicotinamide adenine dinucleotide phosphate, incubated at 37 ℃ for 30 min, and then terminated the reaction with acetonitrile. Taking the negative group (adding acetonitrile firstly and then starting incubation for 30 min) as the reference, the ultra-high performance liquid chromatography-quadrupole time-of-flight mass spectrometry was used; Anaylyst® TF 1.7.1、PeakView® 2.2, MetabolitePilot 1.5 and MasterView 1.2 software were used to speculate and identify the fragmentation law of mass spectrometry and metabolites. RESULTS Four diterpenoids were easy to lose neutral fragments such as H2O and CO in secondary mass spectrometry. Jolkinolide A and 17-hydroxyl jolkinolide A showed similar metabolism pathway, including dihydroxylation, dehydrogenation, and monohydroxylation; six and five metabolites were identified respectively. Jolkinolide B and 17-hydroxyl jolkinolide B showed similar metabolism pathway, including monohydroxylation, hydration and isomerization. Five metabolites were identified. CONCLUSIONS Both jolkinolide A and 17-hydroxyl jolkinolide A produce the metabolites of hydroxylation and dehydrogenation in liver microsomes of rats; both jolkinolide B and 17-hydroxyl jolkinolide B produce the metabolites of hydroxylation, hydration and isomerization in liver microsomes of rats. The metabolites of four diterpenoids are phase Ⅰ metabolites.
KEYWORDS Euphorbia fischeriana; diterpenoids; ultra-high performance liquid chromatography-quadrupole time-of-flight mass spectrometry;liver microsomes in rats; in vitro metabolism
狼毒大戟Euphorbia fischeriana Steud.主要生长于我国内蒙古、东北及河北等地区。其以根入药,味苦、辛,性平,有毒,具有泄水逐饮、破积杀虫的功效,是我国传统中药材[1]。现代药理学研究表明,狼毒大戟具有抗肿瘤、抗细菌、抗真菌、抗病毒、抗癫痫等多种活性[2-3]。狼毒大戟的主要成分包括二萜类、三萜类、香豆素类、酚酸类、甾醇类等,其中二萜类成分为其主要的活性成分[4]。岩大戟内酯A、岩大戟内酯B、17-羟基岩大戟内酯A和17-羟基岩大戟内酯B是狼毒大戟中含量较高且活性较强的二萜类成分[5]。
在早期的药物-药物相互作用研究中,体外肝微粒体孵育体系是探讨药物代谢的重要模型[6]。体外代谢研究可在新药研发早期利用体外代谢参数合理预测候选化合物的体内药动学行为,指导其后期药动学、药效学研究以及安全性评价模型的选择[7]。本研究拟采用大鼠肝微粒体体外孵育法结合超高效液相色谱-四极杆-飞行时间质谱联用技术研究狼毒大戟中岩大戟内酯A、岩大戟内酯B、17-羟基岩大戟内酯A和17-羟基岩大戟内酯B的代谢产物,并对其可能的裂解途径进行推测,探讨其代谢规律,旨在为这4种二萜类活性成分的代谢途径及在体药动学研究奠定基础。
1 材料
1.1 主要仪器
本研究所用主要仪器包括30A型超高效液相色谱仪(日本Shimadzu公司)、Triple TOF 4600型质谱仪(美国AB Sciex公司)、AB135-S型分析天平(瑞士Mettler Toledo公司)、Elix Essential 5 UV型纯水仪(美国Merck Millipore公司)、B8800型超声波清洗器(美国Branson公司)、Centrifuge 5417R型离心机(德国Eppendorf公司)、HYQ-2121A型涡旋混匀器(美国Crystal公司)等。
1.2 主要药品与试剂
岩大戟内酯A、岩大戟内酯B、17-羟基岩大戟内酯A和17-羟基岩大戟内酯B对照品(批号分别为EF-1、EF-2、EF-3、EF-4,经高效液相色谱法检测纯度均大于98%)均由齐齐哈尔医学院医药科学研究院天然药物化学实验中心制备;甲醇(色谱纯)、乙腈(色谱纯)均购自美國Merck公司;甲酸(质谱纯)购自美国Thermo Fisher Scientific公司;还原型烟酰胺腺嘌呤二核苷酸磷酸(reduced nicotinamide adenine dinucleotide phosphate,NADPH)购自大连美仑生物技术有限公司;磷酸二氢钾、磷酸氢二钠、氯化镁均购自天津市科密欧化学试剂有限公司;其余试剂均为分析纯或实验室常用规格,水为纯化水。
1.3 肝微粒体
大鼠肝微粒体(批号M10011,质量浓度20 mg/mL)购自武汉普莱特生物医药技术有限公司。
2 方法与结果
2.1 色谱与质谱条件
2.1.1 色谱条件
以Phenomenex C18(100 mm×2.1 mm,1.7 μm)为色谱柱,以0.1%甲酸溶液(A)-0.1%甲酸乙腈溶液(B)为流动相进行梯度洗脱(0~0.01 min,20%B,0.01~1.00 min,20%B→30%B;1.00~7.00 min,30%B→50%B,7.00~10.00 min,50%B→70%B;10.00~15.00 min,70%B→100%B;15.00~16.00 min,100%B;16.00~16.10 min,100%B→20%B;16.10~18.00 min,20%B);柱温为40 ℃;流速为0.3 mL/min;进样量为2 μL。
2.1.2 质谱条件
离子源为电喷雾离子源;离子喷雾电压为5.5 kV;离子源温度为600 ℃;去簇电压为100 V;碰撞能量为10 eV。雾化气、辅助气和气帘气均为氮气,其压力分别为55、55、35 psi。在正离子模式下进行全扫描,累计时间为250 ms。采用数据依赖采集模式进行分析,即对每个分析物中质谱响应超过100 cps的15个最强碎片离子进行子离子扫描,扫描范围为100~1 200 amu,累计扫描时间为100 ms。碰撞能量差为15 eV,并开启动态背景扣除。采用自动校准系统对质谱和质谱/质谱自动进行调谐和校正。数据获取和处理分析采用Analyst®TF 1.7.1和PeakView®2.2软件,利用MetabolitePilot 1.5和MasterView 1.2软件对代谢产物进行推测与鉴定。
2.2 溶液的配制
2.2.1 磷酸盐缓冲液
精密称取磷酸氢二钠1.496 g,用水定容于50 mL量瓶中;再精密称取磷酸二氢钾1.361 g,用水定容于50 mL量瓶中;将上述配制的磷酸二氢钾溶液逐滴加入到磷酸氢二钠溶液中,直至所得混合溶液的pH为7.4,即得。
2.2.2 氯化镁溶液
精密称取氯化镁0.953 g,用水定容于200 mL量瓶中,得5 mmol/L的氯化镁溶液。
2.2.3 NADPH溶液
精密称取NADPH 10 mg,加水0.6 mL,混匀,得4 mmol/L的NADPH溶液,现用现配。
2.2.4 样品溶液
分别精密称取岩大戟内酯A、岩大戟内酯B、17-羟基岩大戟内酯A和17-羟基岩大戟内酯B对照品适量,加入一定量的二甲基亚砜进行溶解,使上述各成分的质量浓度均为1 mg/mL,即得。
2.3 大鼠肝微粒体体外孵育实验
孵育体系包含pH 7.4的磷酸盐缓冲液100 μL、水49 μL、肝微粒体10 μL、5 mmol/L氯化镁溶液20 μL。本研究设实验组(肝微粒体代谢后组)和阴性组(肝微粒体代谢前组)。两组孵育体系中分别加入1 mg/mL的岩大戟内酯A、岩大戟内酯B、17-羟基岩大戟内酯A、17-羟基岩大戟内酯B樣品溶液各1 μL,在37 ℃下预孵育5 min。然后,实验组加入4 mmol/L的NADPH溶液20 μL启动反应,在37 ℃下继续孵育30 min后,加入冰乙腈600 μL终止反应;阴性组先加入冰乙腈600 μL,再加入4 mmol/L的NADPH溶液20 μL,在37 ℃条件下继续孵育30 min。取各组样品,涡流混匀30 s,以14 000 r/min离心10 min,取上清液于另一EP管中,于37 ℃下以氮气流吹干,残渣加甲醇200 μL复溶,再以14 000 r/min离心10 min,取上清液2 μL按“2.1”项下条件进样分析。
2.4 4种二萜类成分的质谱裂解途径及代谢产物分析
2.4.1 岩大戟内酯A
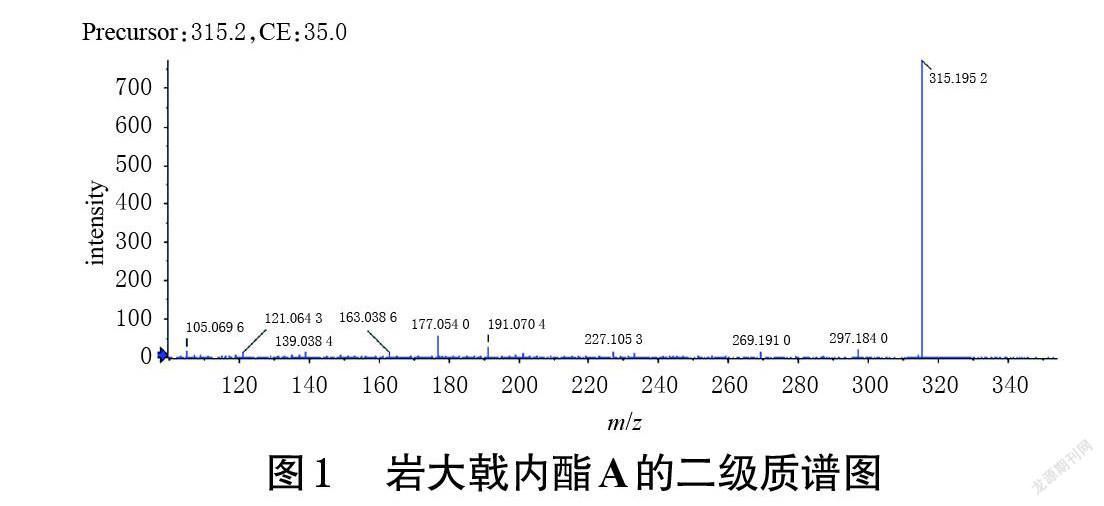
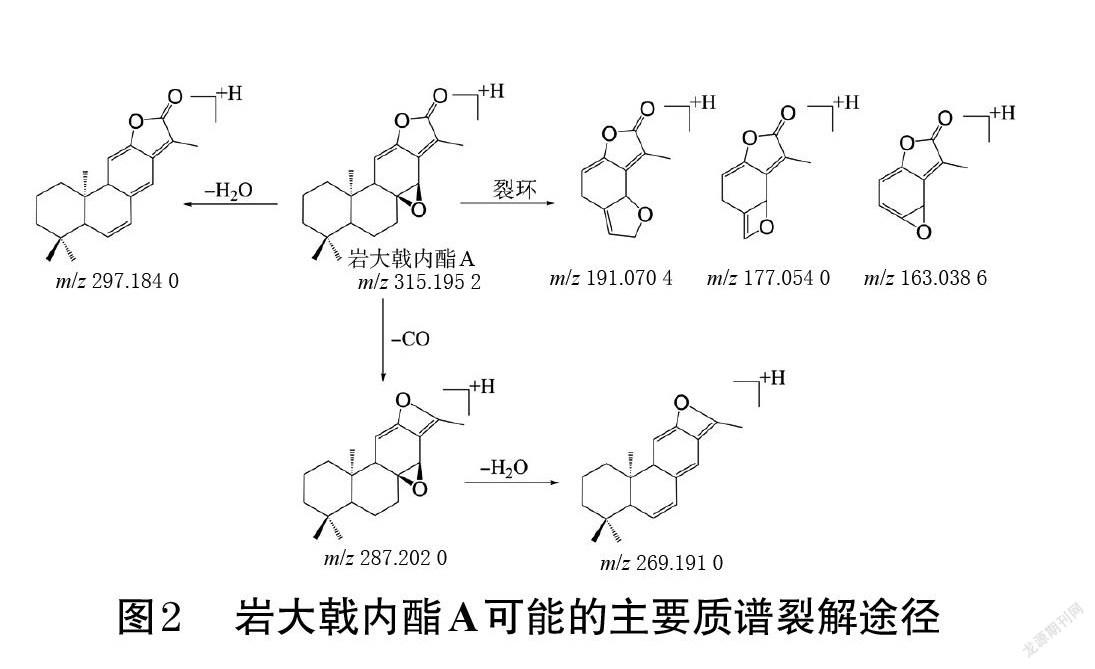
(1)质谱裂解途径:岩大戟内酯A的准分子离子峰的m/z为315.195 2[M+H]+。在其二级质谱图(图1)中,m/z 297.184 0、287.202 0[M+H]+推测是由准分子离子峰分别脱去1分子H2O和1分子CO而得;m/z 287.202 0
[M+H]+继续脱去1分子H2O得到m/z 269.191 0[M+H]+的碎片离子峰;m/z 227.105 3、191.070 4、177.054 0、163.038 6、139.038 4、121.064 3、105.069 6等[M+H]+为岩大戟内酯A裂环后产生的碎片离子峰。岩大戟内酯A可能的主要质谱裂解途径如图2所示。
(2)代谢产物:对实验组和阴性组岩大戟内酯A的提取离子流图(图3)进行比较,根据保留时间(retention time,tR)共鉴定出6个代谢产物(记为M1~M6)。结合其精确分子量和二级质谱信息(表1),参考岩大戟内酯A可能的质谱裂解途径(图2),推测这些化合物是岩大戟内酯A的二羟基化代谢产物、二羟基化+脱氢代谢产物及一羟基化代谢产物。
其中,M1和M2的分子式皆为C20H26O5,tR分别是6.94、7.57 min,准分子离子峰分别为m/z 347.184 0、347.185 7[M+H]+。在M1的二级质谱信息中,主要的碎片离子峰m/z 329.176 4、311.163 9、293.156 0[M+H]+为准分子离子峰依次脱去1分子H2O而得,碎片离子峰m/z 301.176 7、283.165 6[M+H]+分别为m/z 329.176 4、311.163 9[M+H]+进一步脱去1分子CO而得。在M2的二级质谱信息中,主要的碎片离子峰m/z 329.171 9、311.162 8、293.152 1[M+H]+为准分子离子峰依次脱去1分子H2O而得,碎片离子峰m/z 299.165 7、283.153 9[M+H]+分别为329.171 9、311.163 9[M+H]+进一步脱去1分子CH2O和1分子CO而得。与岩大戟内酯A相比,M1和M2的质量数都多了32,推测其可能为岩大戟内酯A的二羟基化代谢产物。
M3、M5和M6的分子式皆为C20H26O4,tR分别是8.80、9.19、11.03 min,准分子离子峰分别为m/z 331.190 9、331.190 8、331.191 1[M+H]+。与岩大戟内酯A相比,质量数都多了16,推测其可能为岩大戟内酯A的一羟基化代谢产物。在二级质谱信息中,M3、M5和M6产生了类似的碎片离子。经过与对照品比对,M6被鉴定为17-羟基岩大戟内酯A,故可确定M6的羟基化位点为C17位。
M4的分子式为C20H24O5,tR为8.96 min,准分子离子峰为m/z 345.169 9[M+H]+。与M1相比,M4的质量数少了2。在M4的二级质谱信息中,主要的碎片离子峰m/z 299.168 9[M+H]+为准分子离子峰脱去1分子H2O和CO而得;m/z 299.168 9[M+H]+再进一步脱水,则可产生m/z 281.143 4[M+H]+的碎片离子峰,推测M4可能为岩大戟内酯A的二羟基化+脱氢代谢产物。
2.4.2 岩大戟内酯B
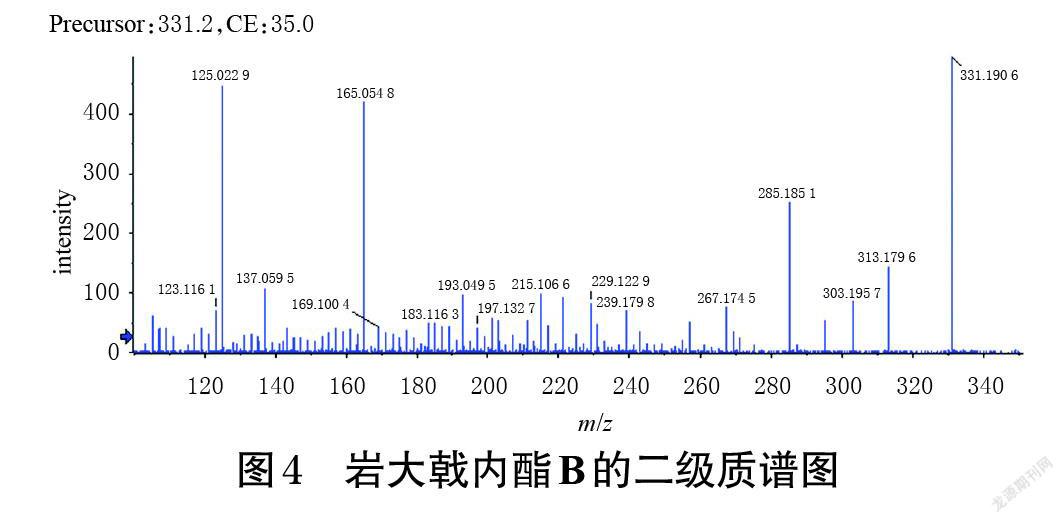
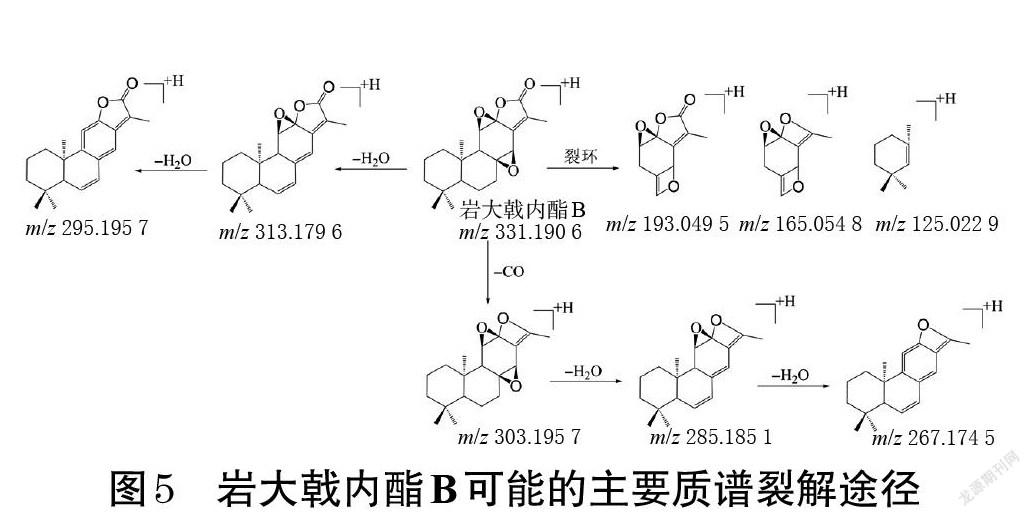
(1)质谱裂解规律:岩大戟内酯B的准分子离子峰为m/z 331.190 6[M+H]+。在其二级质谱图(图4)中,m/z 313.179 6、295.195 7[M+H]+推测是由准分子离子峰依次脱去1分子H2O而得;m/z 303.195 7、285.185 1[M+H]+推测是由准分子离子峰依次脱去1分子CO和1分子H2O而得;此外,岩大戟内酯B还因裂环产生了m/z 193.049 5、183.116 3、165.054 8、137.059 5、125.022 9[M+H]+等一系列碎片离子峰。岩大戟内酯B可能的主要质谱裂解途径如图5所示。
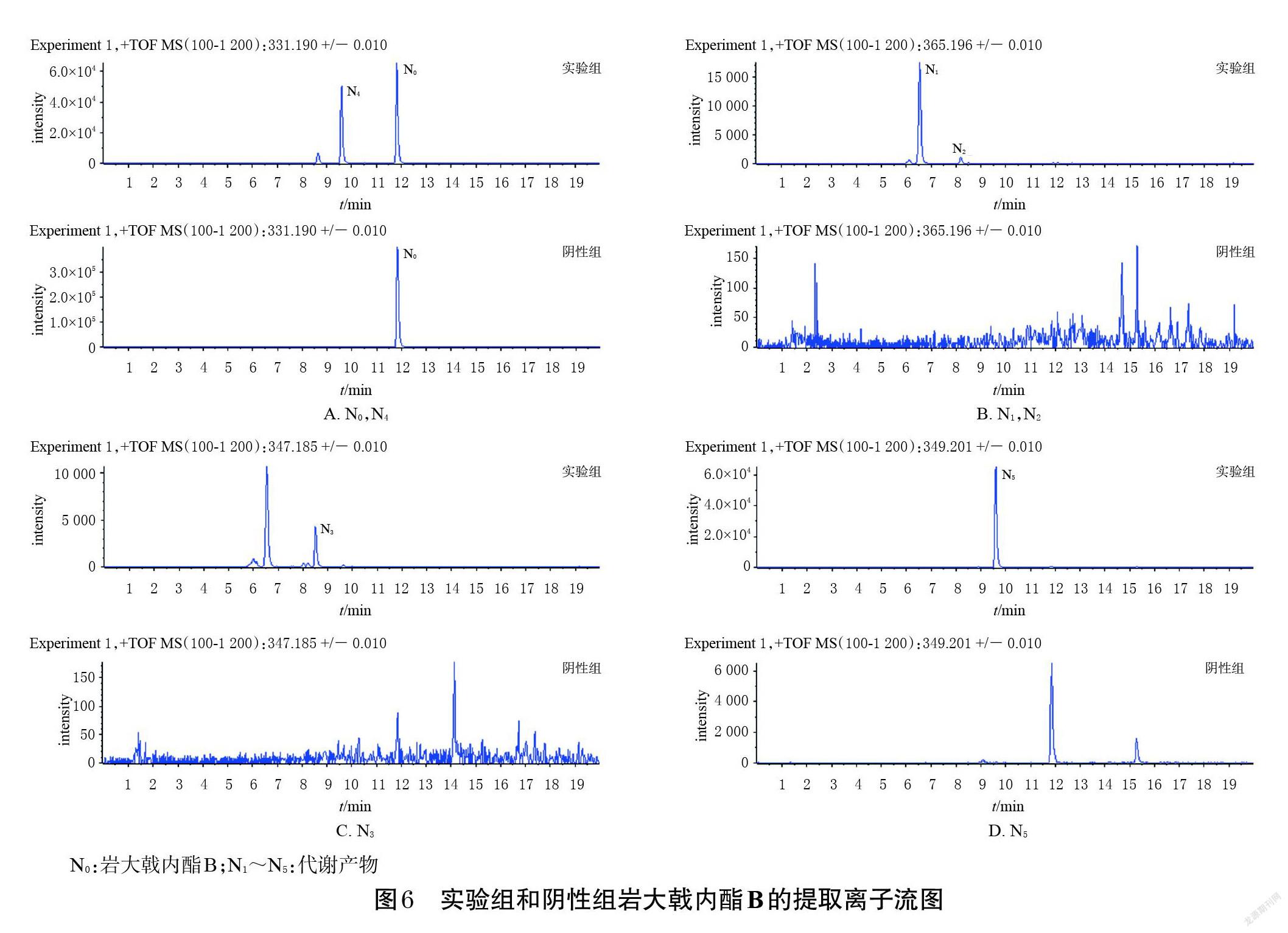
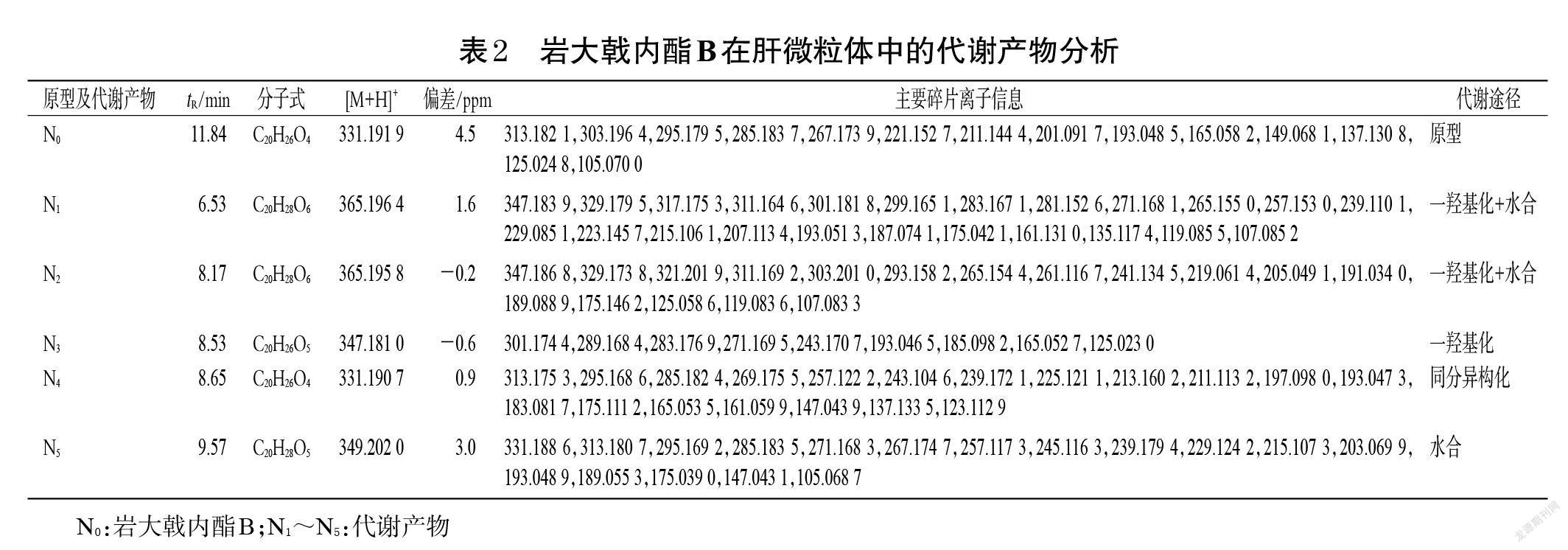
(2)代谢产物:对实验组和阴性组岩大戟内酯B的提取离子流图(图6)进行比较,根据tR共鉴定出5个代谢产物(记为N1~N5)。结合其精确分子量和二级质谱信息(表2),参考岩大戟内酯B可能的质谱裂解途径(图5),推测这些化合物为岩大戟内酯B的一羟基化+水合代谢产物、一羟基化代谢产物、水合代谢产物及同分异构化代谢产物。
N1和N2的分子式皆为C20H28O6,tR分别是6.53、8.17 min,准分子离子峰分别为m/z为365.196 4、365.195 8
[M+H]+。与岩大戟内酯B相比,两者的质量数均多了34,即多了1分子H2O2,因此推测N1、N2为岩大戟内酯B的一羟基化+水合代谢产物。
N3的分子式为C20H26O5,tR为8.53 min,准分子离子峰为m/z 347.181 0[M+H]+。与岩大戟内酯B相比,N3的质量数多了16,因此推测N3为岩大戟内酯B的一羟基化代谢产物。
N4的分子式为C20H26O4,tR为8.65 min,准分子离子峰为m/z 331.190 7[M+H]+。与岩大戟内酯B相比,N4具有相同的分子式,因此推测N4可能为岩大戟内酯B的同分异构化代谢产物。
N5的分子式为C20H28O5,tR为9.57 min,准分子离子峰為m/z 349.202 0[M+H]+。与岩大戟内酯B相比,N5的质量数多了18,即1分子H2O,因此推测N5可能为岩大戟内酯B的水合代谢产物。
2.4.3 17-羟基岩大戟内酯A
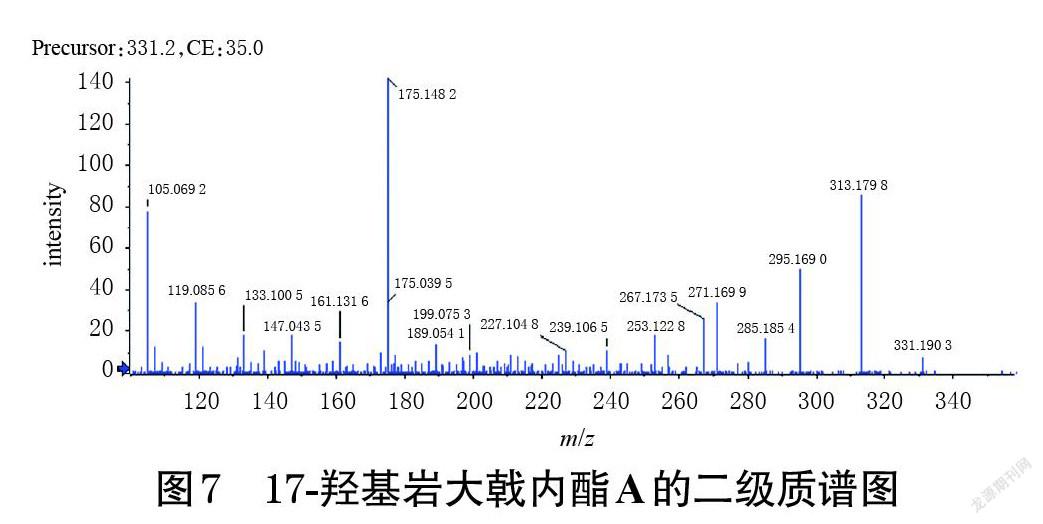
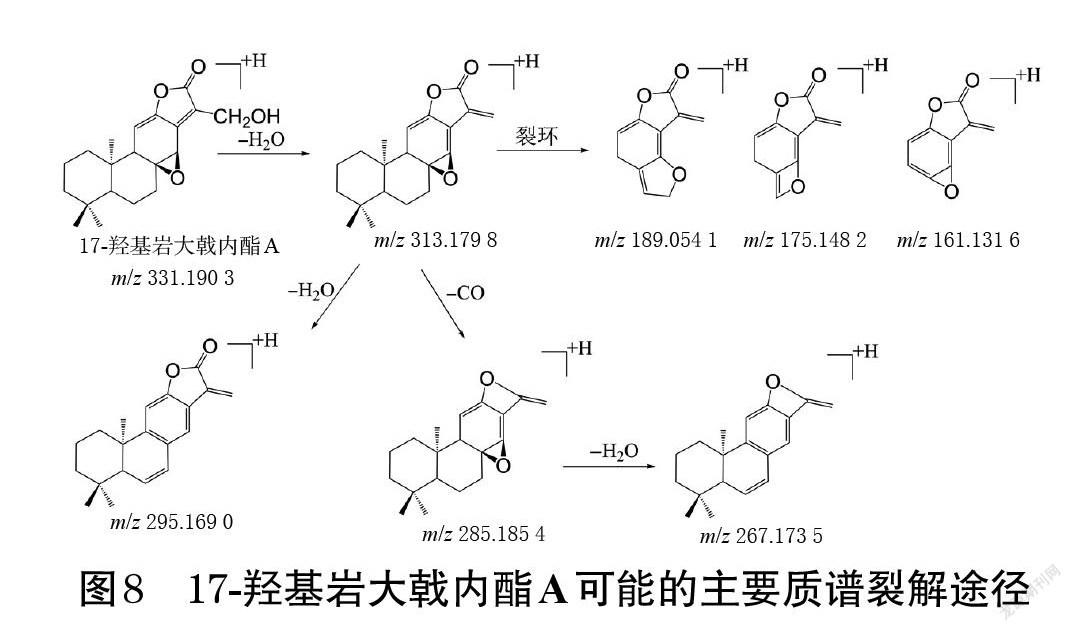
(1)质谱裂解途径:17-羟基岩大戟内酯A的准分子离子峰为m/z 331.190 3[M+H]+。在其二级质谱图(图7)中,m/z 313.179 8、295.169 0[M+H]+推测是由准分子离子峰依次脱去1分子H2O而得;m/z 285.185 4[M+H]+推测是由m/z 313.179 8[M+H]+脱去1分子CO而得;此外,17-羟基岩大戟内酯A还因裂环产生了m/z 239.106 5、227.104 8、199.075 3、189.054 1、175.148 2、161.131 6、147.043 5、133.100 5、119.085 6、105.069 2[M+H]+等一系列碎片离子峰。17-羟基岩大戟内酯A可能的主要质谱裂解途径如图8所示。
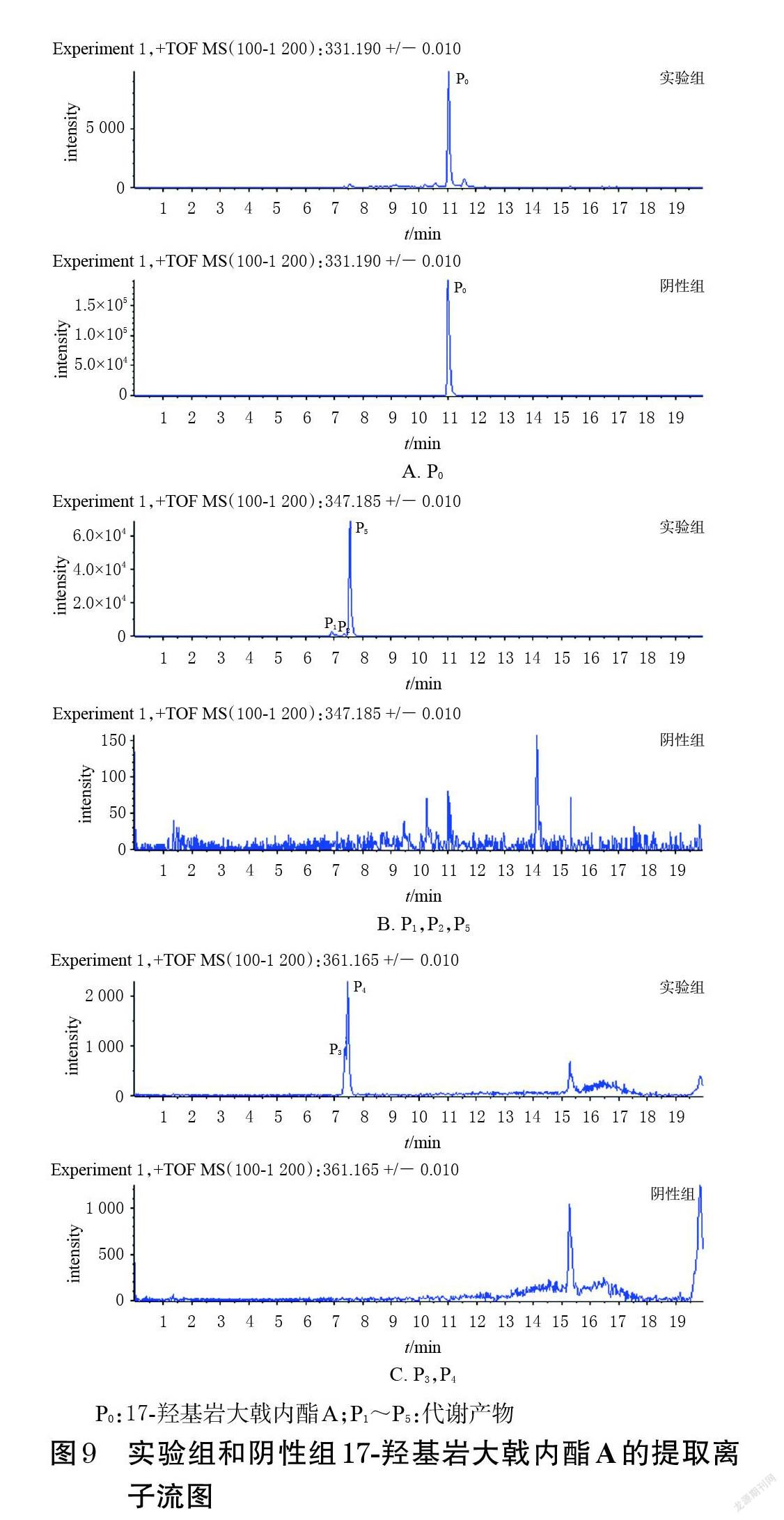
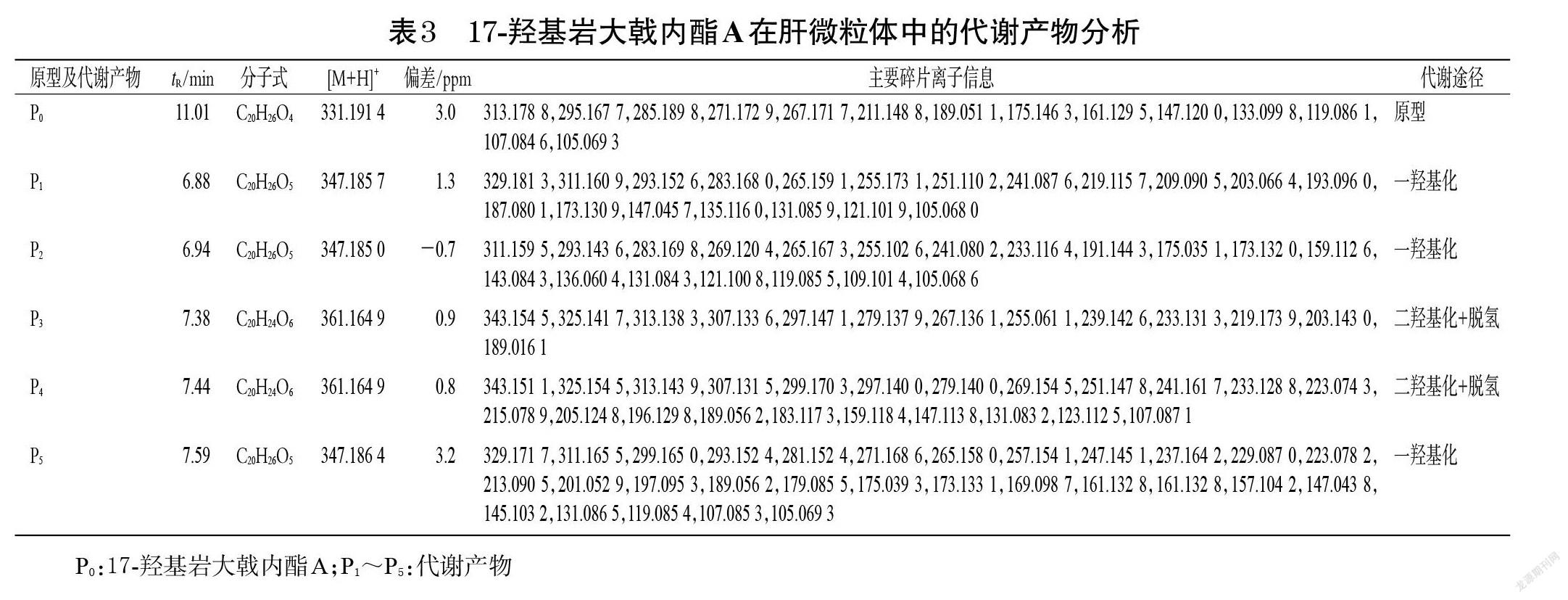
(2)代谢产物:将实验组和阴性组17-羟基岩大戟内酯A的提取离子流图(图9)进行比较,根据tR共鉴定出5个代谢产物(记为P1~P5)。结合其精确分子量和二级质谱信息(表3),参考17-羟基岩大戟内酯A的质谱裂解途径(图8),推测这些化合物可能为17-羟基岩大戟内酯A的一羟基化代谢产物及二羟基化+脱氢代谢产物。
P1、P2、P5的分子式皆为C20H26O5,tR分别为6.88、6.94、7.59 min,准分子离子峰分别为m/z 347.185 7、347.185 0、347.186 4[M+H]+。与17-羟基岩大戟内酯A相比,三者的质量数均多了16,因此推测其可能为17-羟基岩大戟内酯A的一羟基化代谢产物。
P3和P4的分子式皆为C20H24O6,tR分别为7.38、7.44 min,准分子离子峰均为m/z 361.164 9[M+H]+。与17-羟基岩大戟内酯A相比,两者的质量数多了30,即分子式上多了2个O、少了2个H,因此推测其可能为17-羟基岩大戟内酯A的二羟基化+脱氢代谢产物。
2.4.4 17-羟基岩大戟内酯B
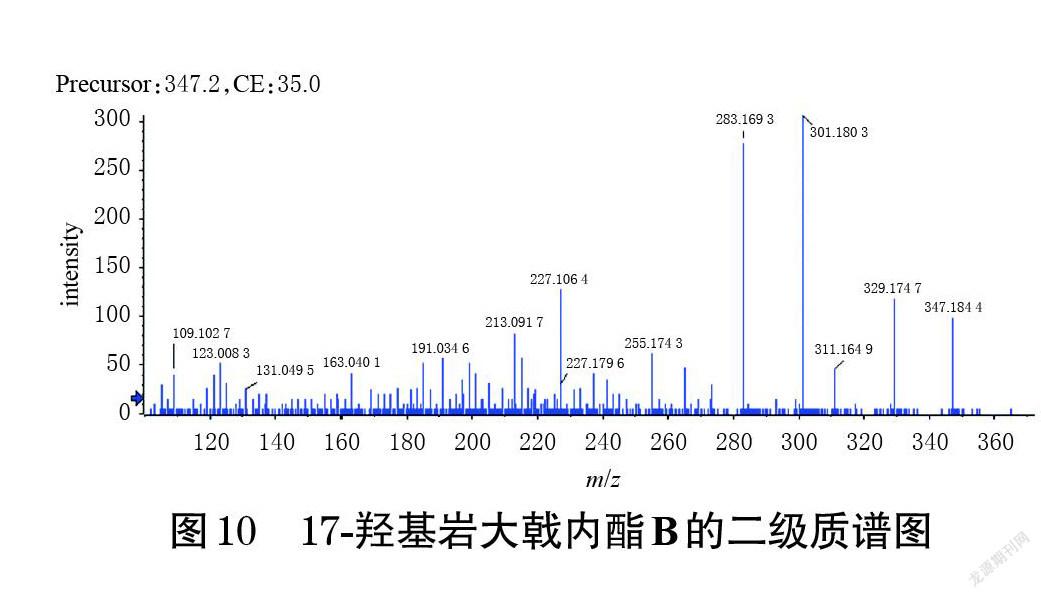
(1)质谱裂解途径:17-羟基岩大戟内酯B的准分子离子峰为m/z 347.186 7[M+H]+。在其二级质谱图(图10)中,m/z 329.174 7、311.164 9[M+H]+推测是由准分子离子峰依次脱去1分子H2O而得;m/z 301.180 3、283.169 3[M+H]+推测是由m/z 329.174 7[M+H]+依次脱去1分子CO和1分子H2O而得;此外,17-羟基岩大戟内酯B还因裂环产生了m/z 227.106 4、213.091 7、191.034 6、163.040 1、131.049 5、123.008 3、109.102 7[M+H]+等一系列碎片离子峰。17-羟基岩大戟内酯B可能的主要质谱裂解途径如图11所示。
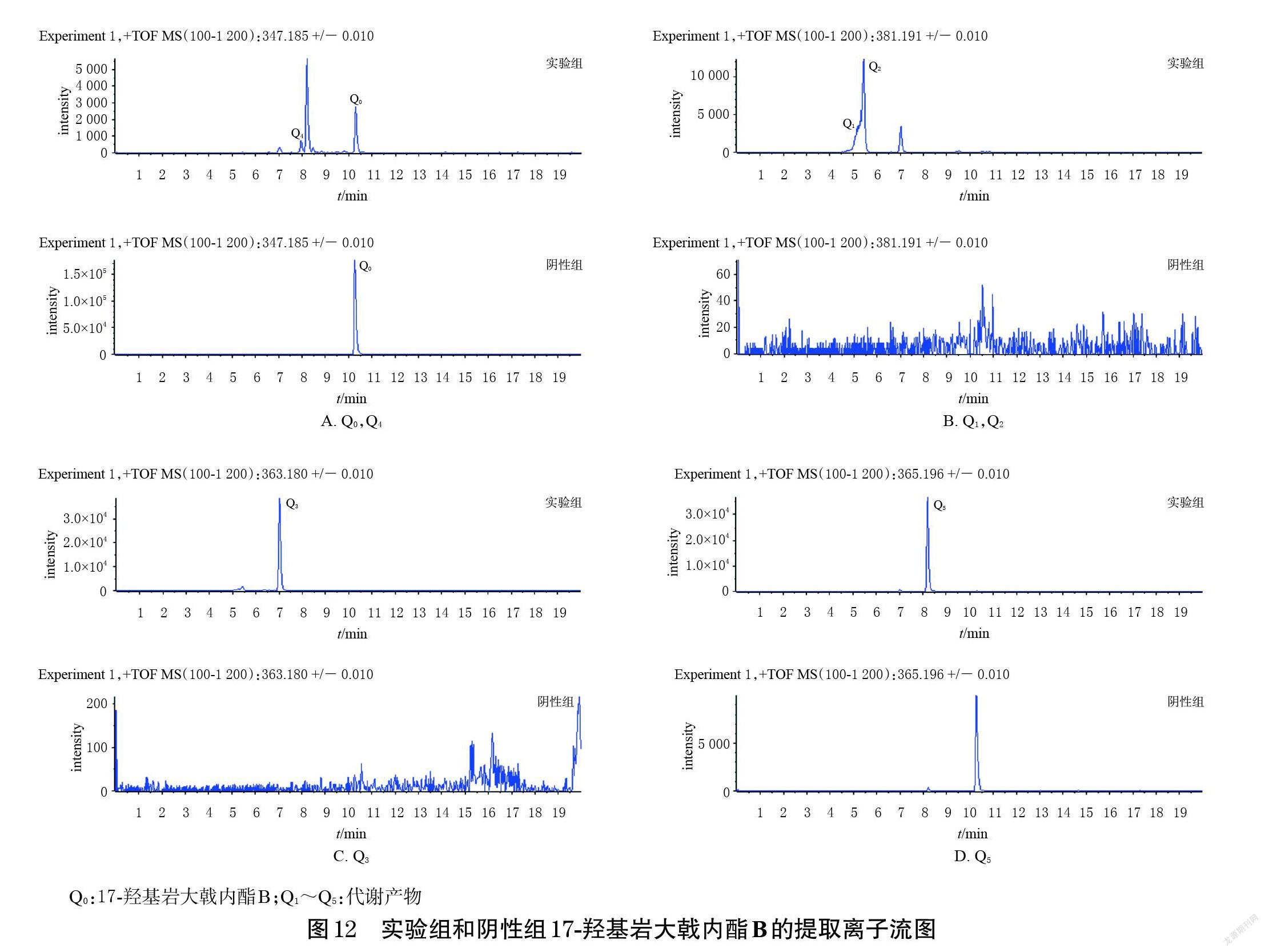
(2)代谢产物:对实验组及阴性组的17-羟基岩大戟内酯B提取离子流图(图12)进行比较,根据tR共鉴定出5个代谢产物(记为Q1~Q5)。结合其精确分子量和二级质谱信息(表4),参考17-羟基岩大戟内酯B可能的质谱裂解途径(图11),推测这些化合物可能为17-羟基岩大戟内酯B的一羟基化+水合代谢产物、一羟基化代谢产物、水合代谢产物及同分异构化代谢产物。
Q1和Q2的分子式皆为C20H28O7,tR分别为5.15、5.43 min,准分子离子峰分别为m/z 381.190 7、391.191 7[M+H]+。与17-羟基岩大戟内酯B相比,两者的质量数多了34,即分子式多了H2O2,因此推测其可能为17-羟基岩大戟内酯B的一羟基化+水合代谢产物。
Q3的分子式为C20H26O6,tR为7.01 min,准分子离子峰为m/z 363.181 6[M+H]+;Q5分子式为C20H28O6,tR为8.18 min,准分子离子峰为m/z 365.196 9[M+H]+。与17-羟基岩大戟内酯B相比,Q3分子式多了O,Q5分子式多了H2O,因此推测Q3可能为17-羟基岩大戟内酯B的一羟基化代谢产物,Q5可能为17-羟基岩大戟内酯B的水合代谢产物。
Q4的分子式为C20H26O5,tR为8.00 min,准分子离子峰为m/z 347.186 2[M+H]+。与17-羟基岩大戟内酯B相比,两者分子量相同,因此推测Q4可能为17-羟基岩大戟内酯B的同分异构化代谢产物。
3 讨论
在预实验中,笔者同时采用了正离子和负离子两种质谱扫描模式对岩大戟内酯A、岩大戟内酯B、17-羟基岩大戟内酯A、17-羟基岩大戟内酯B的肝微粒体代谢产物进行解析,结果显示,正离子扫描模式可获得更多的二级碎片信息,故最终采用正离子模式对代谢产物的结构进行解析。
本研究结果显示,岩大戟内酯A、岩大戟内酯B、17-羟基岩大戟内酯A、17-羟基岩大戟内酯B在正离子检测条件下的二级质谱裂解方式存在共性。经过查阅文献[8-10]和本文结果可知,上述4种二萜类化合物的二级质谱均易丢失H2O和CO等中性碎片,并产生一系列碎片离子。随后,本研究通过解析原型药物及其代谢产物的二级质谱裂解规律、tR、精确分子量等数据发现,岩大戟内酯A和17-羟基岩大戟内酯A在肝微粒中的代谢途径相似,主要为二羟基化、脱氢和一羟基化反应;岩大戟内酯B和17-羟基岩大戟内酯B在肝微粒体中的代谢途径相似,主要为一羟基化、水合及同分异构化反应。通过与对照品比对发现,岩大戟内酯A可在肝微粒体中经一羟基化反应生成17-羟基岩大戟内酯A,进而推断出岩大戟内酯A在肝微粒体中可在C17位发生甲基羟基化。在结构上,与岩大戟内酯A和17-羟基岩大戟内酯A相比,岩大戟内酯B和17-羟基岩大戟内酯B的C11、C12位多了1个三元氧环,由此推测这两个成分可能在肝微粒体中发生C11与C12的氧环开裂,再进一步进行水合反应,然后经羟基脱水生成原型药物的同分异构化代谢产物。岩大戟内酯A、岩大戟内酯B、17-羟基岩大戟内酯A和17-羟基岩大戟内酯B在二级质谱中产生了大量的裂环碎片离子,由于二萜类化合物结构复杂,可能存在多种裂环方式,暂无法对各裂解碎片进行逐一归属。因此,在没有对照品的情况下,较难推测各化合物羟基化代谢产物的羟基结合位点。在今后的研究中,可在大量富集代谢产物后进行分离,得到单体代谢产物,再通过核磁共振等手段对其结构进行鉴定。
通过对比笔者前期对岩大戟内酯B体内代谢的研究结果[9]发现,该成分体内外代谢途径有相似之处,但也存在一定差异。在体内与体外代谢中,岩大戟内酯B均产生了氧化代谢产物,并且推测其C11、C12位的三元氧环在代谢中都发生了开裂现象;不同的是,岩大戟内酯B在体内代谢中产生了脱水代谢产物,而在体外肝微粒体代谢中产生了水合代谢产物。
综上所述,岩大戟内酯A和17-羟基岩大戟内酯A在大鼠肝微粒体中均产生了羟基化及脱氢代谢产物,岩大戟内酯B和17-羟基岩大戟内酯B在大鼠肝微粒体中均产生了羟基化、水合及同分异构化代谢产物。4种二萜类成分在大鼠肝微粒体中的代谢产物均是Ⅰ相代谢产物,未发现Ⅱ相代谢产物。
参考文献
[ 1 ] 谢日晗.狼毒大戟根中二萜类化合物及其抗肿瘤活性研究[D].广州:暨南大学,2020.
[ 2 ] JIAN B Y,ZHANG H,HAN C C,et al. Anti-cancer activities of diterpenoids derived from Euphorbia fischeriana Steud[J]. Molecules,2018,23(2):E387.
[ 3 ] JIAN B Y,ZHANG H,LIU J C. Structural diversity and biological activities of diterpenoids derived from Euphorbia fischeriana Steud[J]. Molecules,2018,23(4):935.
[ 4 ] LI Y N,HE J,ZHANG J,et al. Existing knowledge on Euphorbia fischeriana Steud.(Euphorbiaceae):traditional uses,clinical applications,phytochemistry,pharmacology and toxicology[J]. J Ethnopharmacol,2021,275:114095.
[ 5 ] MA T C,SUN Y,LIU L,et al. Optimization of extraction for diterpenoids from Euphorbia fischeriana Steud using response surface methodology and structure identification by UPLC-Q-TOF-MS[J]. Nat Prod Res,2021,35(14):2458-2462.
[ 6 ] 高路,李葆元,刘佩仪,等.朝藿定B和朝藿定C在人肝微粒体中的体外代谢研究[J].沈阳药科大学学報,2021,38(4):385-394.
[ 7 ] 陈瑞,张丽,蔡进,等.新型胰岛素增敏剂ZG02在大鼠肝微粒体中的代谢稳定性研究[J].中国药房,2018,29(24):3359-3364.
[ 8 ] 赵亮.液质联用在中药狼毒化学成分研究中的应用[D]. 上海:第二军医大学,2007.
[ 9 ] 马天成,孙宇,马玉坤,等. UPLC-Q-TOF/MS法分析岩大戟内酯B在大鼠体内的代谢产物[J].中国药房,2019,30(20):2796-2801.
[10] 夏涛,王昌权,陈浩,等.白及有效成分Militarine在肝微粒体中的体外代谢途径及其酶促动力学特征[J].中国药房,2019,30(10):1316-1320.
(收稿日期:2021-11-12 修回日期:2022-01-20)
(编辑:邹丽娟)
