NGS引导下的奥希替尼耐药肺腺癌1例报道*
2021-11-09何婷婷王玉波
何婷婷,王玉波,付 明
(中国人民解放军陆军特色医学中心呼吸与危重症医学科,重庆 400042)
奥希替尼已在临床广泛应用,为晚期肺腺癌患者带来了较多临床获益,但耐药仍不可避免。其耐药机制仍在探索阶段,下一代测序(next-generation sequencing,NGS)为奥希替尼耐药后患者的个体化治疗提供了更精准的指导。本文报道了1例晚期肺腺癌患者在奥希替尼耐药后经多次动态基因检测,根据不同检测结果,先后采用不同治疗方案取得临床获益的案例。
1 临床资料
患者,男,54岁,因“咳嗽、咳痰、喘累半月”于2015年6月26日到本院就诊。入院前半月患者无明显诱因出现咳嗽、咳白色泡沫痰,伴上坡时喘累。当地医院胸部CT发现右下肺基底段占位,双侧肺门、纵隔及双侧锁骨上窝淋巴结肿大。为求进一步诊治到本院就诊。既往吸烟20余年,1包/天。入院后查体:左锁骨上窝可扪及肿大淋巴结,约1.5 cm×1.5 cm大小,质硬,活动度可,无压痛,余未见异常体征。胸部CT检查示:右下肺片块状致密影(3.0 cm×4.0 cm)。血清癌胚抗原:24.77 μg/L。行CT引导下右下肺经皮肺穿刺活检术,病理诊断:肺浸润性腺癌;左锁骨上淋巴结活检,病理诊断:转移性腺癌。PET-CT提示:(1)右下肺周围型肺癌(SUVmax 17.28,最大直径3.2 cm);(2)左锁骨上窝淋巴结(SUVmax 3.24)、左侧纵隔淋巴结转移(SUVmax 5.85);(3)右侧第4肋骨、腰2/5椎体及坐骨转移(SUVmax 7.11)。最终诊断:右下肺腺癌(T2N3M1 Ⅳ期)、双侧锁骨上窝及纵隔淋巴结转移、多处骨转移。基因检测[扩增阻滞突变系统(ARMS)法,肺组织]提示:EGFR 19 外显子缺失突变(19 exon deletion mutation,19del)。患者于2015年7月开始服用吉非替尼(250 mg/d),治疗1个月后复查胸部CT提示病灶缩小。血清癌胚抗原:14.33 μg/L。吉非替尼最佳疗效为部分缓解(partial response,PR)。患者诉咳嗽、喘累症状均明显缓解。2016年7月患者突发呼吸困难,并迅速加重。当地医院诊断为“Ⅰ型呼吸衰竭”,转至本院呼吸重症监护室(RICU)后行无创呼吸机辅助呼吸。复查胸部CT提示肺部病灶明显增大。血清癌胚抗原升高至38.88 μg/L。抽血行NGS提示:EGFR 19del(丰度:5.24%),EGFR T790M(丰度:6.27%)。患者自购AZD9291(印度版,80 mg/d)治疗,服用第3天自觉呼吸困难症状明显缓解,缺氧症状改善,转出RICU。用药1个月后,复查胸部CT提示肺部病灶明显缩小。口服AZD9291 4个月后复查胸部CT提示病灶明显增大。患者自述无明显不适。再次行血液NGS仍提示:EGFR 19del、EGFR T790M阳性。2016年10月更换为正版奥希替尼(80 mg/d)。服药1个月后复查胸部CT提示右肺病灶明显缩小。癌胚抗原降至14.56 μg/L。2017年4月患者复查胸部CT提示病灶再次增大。血液NGS提示:EGFR 19del(丰度:2.87%),EGFR T790M(丰度:0.22%)、c-MET扩增(Cn=2.33)。血清癌胚抗原升高至21.81 μg/L。遂采用克唑替尼(250 mg/d,2次/天)联合奥希替尼(80 mg/d)治疗。门诊定期复查胸部CT等检查,最佳疗效达PR。2017年10月患者因复查胸部CT再次提示病灶进展。血检NGS提示:EGFR 19del(丰度:2.62%)、EGFR T790M(丰度:3.51%)、EGFR L718Q(丰度:2.83%)、EGFR C797S错义突变(与T790M呈顺式,丰度:0.54%)。行AP26113联合西妥昔单抗治疗1个月后复查胸部CT提示病灶稍缩小(影像学变化见图1);后患者因自身经济原因拒绝继续治疗,自服中药,2个月后病情呈爆发式进展死亡。
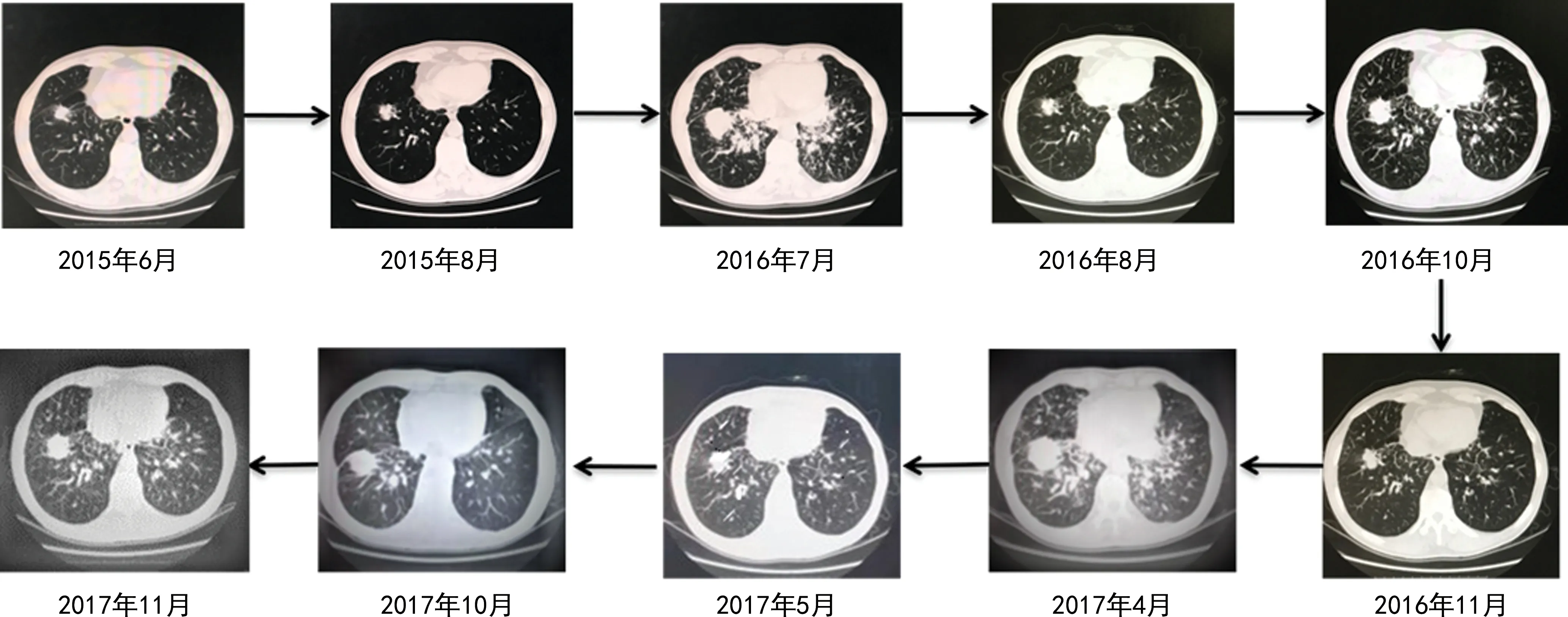
图1 患者胸部CT图像
2 讨 论
第三代表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor,EGFR-TKI)奥希替尼能够克服一、二代EGFR-TKI治疗9~13个月后因EGFR T790M所致的获得性耐药,安全性好[1]。且一线治疗EGFR敏感突变非小细胞肺癌(non-small cell lung cancer,NSCLC)患者的无进展生存期(progression-free survial,PFS)获益更大[2]。但奥希替尼的耐药给临床带来了新挑战,随着对耐药机制的不断探索,多靶点联合治疗应用于临床。
MET扩增是奥希替尼的耐药机制之一,约占耐药机制的15%~19%[3]。克唑替尼通过抑制MET激酶与 ATP的结合及结合之后的自身磷酸化,可克服 MET 扩增导致的获得性耐药[4]。笔者前期研究证实,克唑替尼联合奥希替尼对MET扩增相关奥希替尼耐药的NSCLC患者获益[5-6]。2020年ASCO大会报道了沃利替尼、特泊替尼、卡马替尼3种新型MET抑制剂在MET 14号外显子跳跃突变晚期NSCLC患者中的疗效和安全性,三者客观缓解率(objective response rate,ORR)接近,沃利替尼在疾病控制率(disease control rate,DCR)和PFS方面表现更优,分别达到95.1%、9.7个月[7-9]。TATTON研究中,沃利替尼联合奥希替尼治疗三代EGFR-TKI耐药后出现MET扩增患者的ORR为30%,中位PFS为5.4个月[10]。沃利替尼已向国家药监局提交上市申请,预计今年上市。特泊替尼和卡马替尼已在国外上市。期待后续更多的新药物攻克MET扩增相关EGFR-TKI获得性耐药难题。
EGFR C797S突变是奥希替尼最常见的耐药机制之一,约占奥希替尼二线治疗耐药机制的10%~26%[1]。其表现为3种类型:单纯EGFR C797S突变、EGFR C797S/T790M顺式突变及EGFR C797S/T790M反式突变。其中EGFR C797S/T790M顺式突变最常见,表现为EGFR C797S与T790M同时出现,且位于相同等位基因[11]。布加替尼作为一种新型双靶点ALK-EGFR抑制剂,对EGFR 19del/T790M/C797S 3种突变体细胞有效,与EGFR单抗联用有协同作用[12]。已有文献报道,布加替尼联合西妥昔单抗治疗EGFR C797S/T790M顺式突变相关奥希替尼耐药NSCLC患者取得较化疗更长的PFS[13]。也有个案报道证实了上述结论[14]。
仿制药因其价格低廉,受到部分患者青睐。但其未经过基础试验和临床试验验证其安全性和有效性,且无国内相关行政监管,纯度及疗效并不确切。购买途径及运输方式等也无保障。医务人员应指导患者选择正规、合法、安全的药物,给予精准靶向治疗。
奥希替尼耐药是值得关注的临床问题,其中c-MET扩增、EGFR C797S突变是其常见的耐药机制。靶向治疗患者应进行动态基因检测,了解耐药机制,指导下一步治疗选择。NGS检测可选择液体活检,便于动态了解基因变化。我们可在NGS引导下针对晚期肺腺癌患者不同基因分型开展相应的治疗模式,在精准治疗基础上探索出个体化全程管理方案。
