巧解金属与盐溶液反应的探究题
2021-08-09戴勇
戴勇

在金属活动性顺序表中,除非常活泼的金属外,排在前面的金属一般可以将位于其后的金属从它们的盐溶液中置换出来。本文借用表格法和数轴法讨论金属与盐溶液反应的三种题型,帮助学生更好地掌握这方面的知识,快速、准确地解决问题。
一、一种金属与一种盐溶液的反应
笔者先出示例题:将一定量的铁粉放入硫酸铜溶液中,充分反应后过滤,得到滤渣和滤液。问:滤渣和滤液的成分可能有哪些?
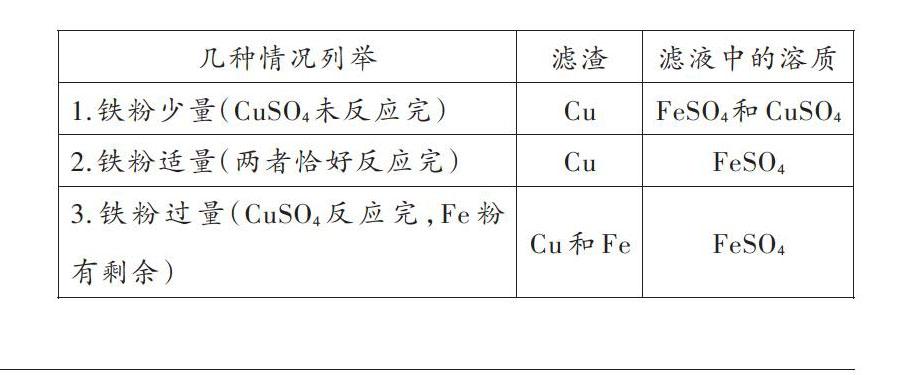
对于这种较为简单的反应,我们从分析铁粉的用量入手,分为三种情况去研究。第一种情况是少量铁粉,未将硫酸铜反应完;第二种情况是铁粉适量,恰好与硫酸铜反应完全;第三种情况是铁粉过量,将硫酸铜反应完全,反应后铁粉有剩余。这种情况采用列表法解答最为直观。先写出发生反应的化学方程式:Fe+CuSO4=Cu+FeSO4。由此得出规律:一种金属与一种盐溶液反应后,滤渣中一定有反应后生成的金属,滤液中一定有反应后生成的可溶性盐。
二、一种金属与多种盐溶液反应
例如:向FeCl2、CuCl2、MgCl2的混合溶液中加入一定量的锌粉,当反应停止后过滤,得到滤液和滤渣。笔者采用表格法进行教学(如上表),分成以下三种情况来说明,清晰易懂。
然后,教师出示以下问题。
(1)滤渣组成可能有哪几种情况:① ;② ;③ ;……
(2)滤液中一定存在的溶质是 ,可能存在的溶质有 。
(3)若锌粉过量,向滤渣中加入稀盐酸溶液后,反应化学方程式为 。
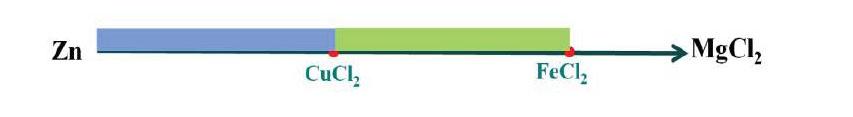
这种较为复杂的题型,教学时可以运用“数轴法”加以分析解决。第一步排序,将题中涉及的几种金属按活动性由强到弱排序为Mg>Zn>Fe>Cu;第二步判断,由金属的活动性判断哪些反应能发生、哪些反应不能发生,能发生的先后顺序是怎样的,活动性最弱的金属的盐先被反应完,再与活动性第二弱的金属的盐反应,以此类推。第三步,画数轴写方程式并分析。先画数轴(如下图),将金属Zn写在最左边,把Zn无法与之反应的MgCl2写在右边箭头的最前端,表示Zn无法触及MgCl2,Zn右边第一点处应当写先与之反应的CuCl2,第二点处才是FeCl2。
这样的两点将数轴分为三个区域,从左向右代表了随着Zn用量的增加反应的进程。这时“两点三区”五种反应情况就十分清晰地展现在我们面前。
第一种情况是Zn量不足,只与部分CuCl2发生了反应,反应后的滤渣中只有Cu,滤液的溶质中有反应生成的ZnCl2和未反应完的CuCl2,还有未反应的FeCl2、MgCl2。第二种情况,Zn的量恰好只与CuCl2反应完,在这个特殊点处,滤渣中只有Cu,滤液中的溶质中有生成的ZnCl2和未反应的FeCl2、MgCl2。第三种情况,Zn的量将CuCl2反应完后,又与部分FeCl2发生了反应,即反应到了第二个区域,此时先后发生了两个反应,因此,反应后的滤渣中有两个反应后分别生成的Cu和Fe,滤液中的溶质有反应生成的ZnCl2、未反应完的FeCl2和未参加反应的MgCl2。第四种情况,Zn的量恰好将CuCl2和FeCl2均反应完,此时反应到了第二个特殊点处,反应后的滤渣中有Cu和Fe,滤液中的溶质有反应生成的ZnCl2和未参加反应的MgCl2。第五种情况,Zn过量,将CuCl2和FeCl2均反应完后尚有剩余,这便到了第三个区域的位置,此时,滤渣中有反应后生成的Cu和Fe,还有未反应完的Zn,滤液中的溶质有反应生成的ZnCl2和未参加反应的MgCl2。
在分析上述五种反应情况的同时,就在对应区域和点位下方将滤液、滤渣成分的化学式记录下来。如下图所示。
教师借助数轴直观呈现反应过程,进而总结规律:一种金属与多种盐溶液反应后,滤渣中一定有已确定发生了的反应所生成的金属,滤液中也一定有已确定发生了的反应所生成的可溶性盐和活动性最强金属的可溶性盐。
三、多种金属与一种盐溶液反应
笔者出示例题:
向硝酸银溶液中加入一定量的铝和铁的混合粉末,充分反应后过滤,得到滤渣和滤液。以下关于滤渣和滤液说法正确的是( )。
①滤渣中加入稀盐酸,一定有气泡产生
②向滤渣中加入稀盐酸可能没有气泡产生
③滤渣中一定含有银可能含有铁
④向滤液中加入稀盐酸,一定有沉淀产生
⑤滤液中不含AgNO3,可能含有Al(NO3)3
A.①③⑤ B.①④ C.②③ D.②④⑤
用數轴法解析此题时,关键是要把AgNO3写在数轴的最左端,数轴上的两点从左向右依次为铝和铁,形成“两点三区”五种情况去分析,对问题逐一查实查否,难题很快就能解决,得出本题选C。
(作者单位:老河口市教研室)
责任编辑 张敏
