光助-电解锰渣/H2O2非均相体系氧化降解双酚S
2021-05-29徐子豪李英杰熊玉路侯智超李金锁田森林
徐子豪,李英杰,熊玉路,侯智超,李金锁,田森林
光助-电解锰渣/H2O2非均相体系氧化降解双酚S
徐子豪,李英杰*,熊玉路,侯智超,李金锁,田森林
(昆明理工大学环境科学与工程学院,云南 昆明 650500)

电解锰渣;双酚S;非均相类光Fenton体系;光降解;•OH;动力学模型
双酚S由于具有良好的热稳定性和光稳定性且与双酚A结构类似,近些年来一直作为双酚A的替代品广泛应用于多种聚合树脂添加剂、染料固色剂、电镀添加剂及染料、药物、农药、助剂等的中间体[1-2].研究发现,双酚S的毒性效应和双酚A类似,可干扰生物内分泌和生殖发育系统[3-4].国内外的研究学者在海洋、湖泊的沉积物以及污水处理厂污水和污泥等水环境介质中均检测出了双酚S,且其具有极高的稳定性,易造成水环境污染进而影响人类身体健康、破坏生态平衡[5-10].
光Fenton法是目前处理环境中有机污染物的一种常见技术[11-12],其原理为通过光诱导产生高氧化活性的•OH氧化降解有机物[13-14].非均相Fenton光催化体系因其反应效率高、不易产生铁泥和催化剂可回收利用而研究较多,光催化剂多为半导体金属氧化物、过渡金属和负载型金属氧化物等[15-16].但是,现有的Fenton光催化剂存在制备较为复杂、成本较高和活性组分流失且造成二次污染等问题,限制了非均相光Fenton技术的进一步应用[17].
电解锰渣是锰矿酸浸后的固体废弃物,我国已堆存的电解锰渣量已超1亿t,电解锰渣因产量大,组分复杂,环境污染问题尤为突出[18].目前对电解锰渣的资源化利用多为制砖、水泥添加剂和回收有价金属等[19-21],但硫含量比较大导致锰渣难以处理,并且剩余废渣较多,很大程度限制了电解锰渣的资源化利用[22].研究报道电解锰渣中含有锰、铁等过渡金属,Mn质量含量大于8%[23];钟超[24]研究发现电解锰渣中部分活性组分对臭氧氧化有催化效果.因此,理论上电解锰渣可以活化H2O2,作为非均相光Fenton体系的催化剂用于有机废水处理,达到以废治废的目的.但是其对有机污染物的降解效能和降解机理需要深入研究.本研究以电解锰渣为催化剂构建光助-电解锰渣/H2O2光Fenton氧化体系,选取双酚S作为模型化合物,探究操作参数对该体系氧化降解的影响,通过响应面法优化影响因素;采用自由基淬灭实验和电子自旋共振光谱研究电解锰渣/H2O2光Fenton氧化体系中自由基的降解机制,同时构建自由基生成速率模型,以预测该体系中有机污染物的降解动力学,并研究了水中常见组分溶解性有机质(DOM)的影响.
1 材料与方法
1.1 实验材料
双酚S、5,5-二甲基-1-吡咯啉-N-氧化物(DMPO)、异丙醇、腐殖酸(含量:质量分数98%,元素组成:C、H、O、N、S,实验中用作DOM类似物)、苯乙酮(分析纯,北京百灵威科技有限公司);甲醇、乙腈(色谱纯,北京百灵威科技有限公司);硝基苯(分析纯,上海阿拉丁生化科技股份有限公司);过氧化氢、硫酸(分析纯,四川西陇科学有限公司);氢氧化钠(分析纯,天津市致远化学试剂有限公司);氯仿(分析纯,重庆川东化工有限公司);无水乙醇、磷酸(分析纯、天津市风船化学试剂科技有限公司);N2、O2、空气(高纯³99.999%;成都金克星气体有限公司);超纯水(18MΩ·cm,天津市兰力科化学电子高科技有限公司生产的超纯水器制备).
电解锰渣是天元锰业电解锰生产过程中用硫酸处理锰矿产生的过滤酸渣,含水量为25%;其中几种质量含量较高的金属中,Mn质量分数为3%,Fe质量分数为1.5%,Mg质量分数为1%,Al质量分数为3.6%,经过烘干研磨后,呈细小颗粒状,用作光催化剂.
1.2 实验方法
电解锰渣和一定浓度的双酚S溶液在25mL石英试管中混合,磁力搅拌,放置于OCRS-PX32T 型光化学反应仪(河南省开封市宏兴仪器厂)进行光降解实验,光源为500W汞灯(配备290nm截止滤光片,>290nm),其中500W汞灯光谱见图1;加入一定量的H2O2,后续试验会加入一定量异丙醇、氯仿等淬灭剂和水环境中溶解性组分.将上述混合溶液用硫酸和氢氧化钠溶液调至所需pH值,在黑暗条件下磁力搅拌10min后,取样作为开始反应的起点.然后放入OCRS-PX32T光化学反应仪中,开启500W汞灯的光源和循环水泵,开始光照,每隔一段时间后取1mL的样品溶液至棕色液相小瓶中,液相小瓶提前加入100μL异丙醇用于终止反应,样品溶液过0.45μm滤头.每组实验重复3次,对比实验设置暗对照.
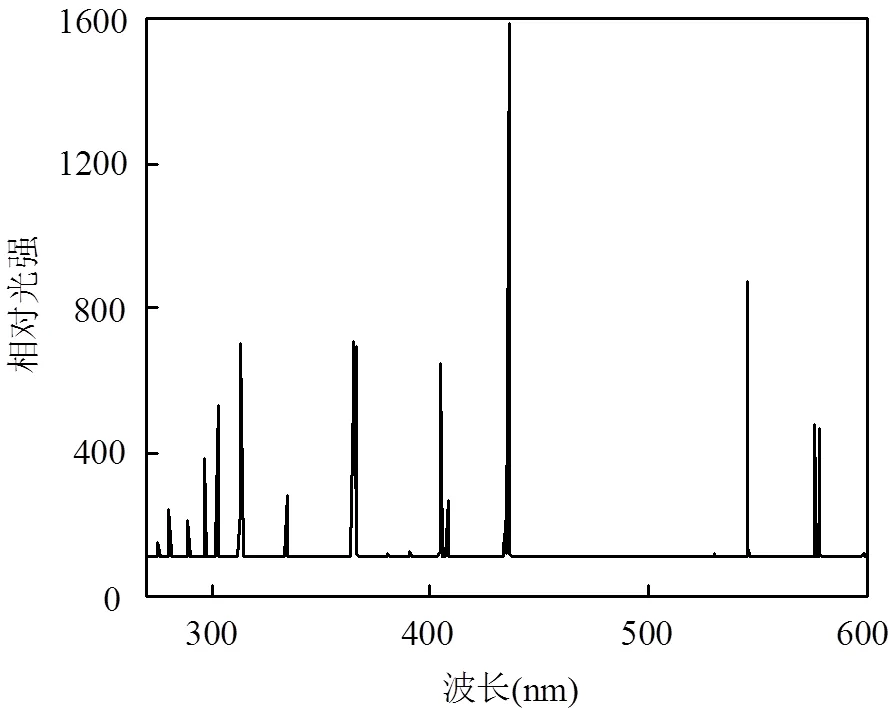
图1 500W汞灯的辐射光谱
为了研究构建的电解锰渣为催化剂的非均相光Fenton体系中双酚S降解的最佳因素,在单因素实验的基础上采用响应面法(RSM)考察双酚S降解因素的影响,响应变量选取初始pH值、电解锰渣投加量、H2O2浓度、双酚S初始浓度4个因素,反应速率为输入变量,并优化选择该体系下的最佳因素.表1为RSM实验设计,并根据Design-Expert8.0.6软件选择做30组中心组合实验.表观降解速率常数(min-1)与上述4种影响因素(1,2,3和4)之间的关系可通过一个完整的二次方程式进行拟合, 如式(1)所示:
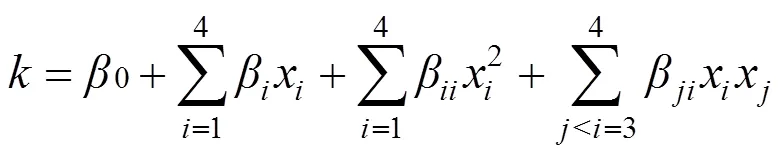
式中:1~4表示pH值、电解锰渣投加量(g/L)、H2O2浓度(mmol/L)、双酚S初始浓度(μmol/L);β是二次方程的拟合系数,包括常数项(0)、一次项系数(1~4)、平方项系数(11~44)以及交叉项系数(12,13,14,23,24,34).
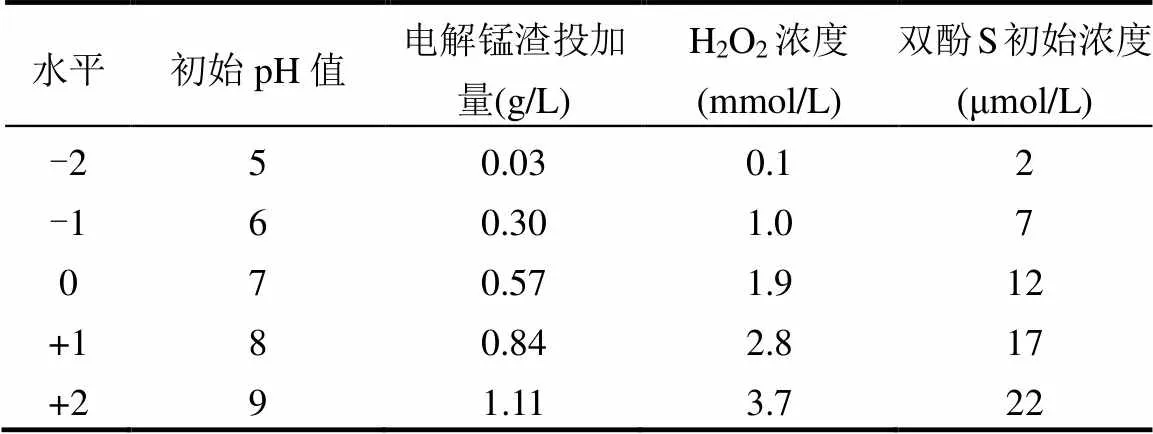
表1 电解锰渣作为光催化剂降解双酚S响应面法试验因素水平
为验证该体系中起氧化降解的活性物质,通过加入•OH淬灭剂异丙醇[25](20mmol/L)、O2•–淬灭剂氯仿(20mmol/L)以及通入N2、O2、空气来探究其生成和影响,并用0~1mmol/L的异丙醇和100μmol/L的硝基苯构建羟基自由基生成速率的模型;最后加入DOM(浓度为0~20mg/L的腐殖酸),模拟在一般水体中有机污染物的降解,构建目标污染物降解的预测模型验证实验值和预测值的差别.
1.3 分析方法
1.3.1 样品分析 液相小瓶中的样品用UltiMate 3000高液相色谱分析仪检测分析目标污染物的浓度,色谱柱型.号为ZORBAX Eclipse XDB-C18 (4.6mm×150mm,5μm),流速为1mL/min,进样量为20μL,检测波长为259nm,流动相为体积50%的甲醇和50%的纯水.
1.3.2 电子自旋共振 将浓度为0.57g/L锰渣溶液与80mmol/L的•OH捕获剂DMPO溶液体积1:1混合均匀,边光照边用EPR光谱仪(Bruker,A300-6/1, Xband)检测信号来响应•OH,电子顺磁共振测量参数为:扫描宽度为100G,微波频率和微波功率分别为9.86GHz和22mW,调制频率和调制幅度分别为100kHz和1.00G,轴的分辨率为1024.
1.3.3 电解锰渣表征 火焰原子吸收: 采用火焰原子吸收的方法测定溶液中Fe和Mn的含量.仪器设定参数:检测波长分别为248.3和279.5nm,狭缝宽度为0.2nm,乙炔流量为1.7L/min,空气流量为7.0L/min,乙炔压力为0.09MPa,空气压力为0.3MPa.配置一系列不同浓度的锰和铁的标准溶液,测定吸光度,在仪器上直接绘制标准工作曲线用于样品测量的计算校正.
X射线荧光光谱分析(XRF):用FL970荧光光谱仪检测电解锰渣中的元素成分含量,样品研磨至200目以下并压至平整,离样品盒底板盖3cm.
X射线衍射分析(XRD):用RIGAKUTTRIII- 18KW转靶X射线多晶衍射仪在10°~80°记录电解锰渣的X射线衍射图,X射线为0.06~20.00nm的电磁波,最小步进为0.0001°,样品过300目筛,水洗至中性.
X射线光电子能谱分析(XPS):用K-Alpha+光电子能谱仪对电解锰渣表面元素进行分析,样品研磨成细粉末,压片后粘到双面胶带上,然后分散到有机溶剂中,形成悬浊液滴到硅片上,预抽、加热脱附进行清洁.检测的能量范围在5~1500eV之间.
BET比表面仪: 用显微研磨技术研究了电解锰渣在-196℃脱氮后的孔结构和BET比表面积.仪器型号:三星II3022分析仪.试验前,样品压成颗粒状并过200目筛,将200mg样品在300℃下煅烧活化4h以脱气.最后由BET方程求出比表面积,用BJH模型计算孔径.
2 结果与讨论
2.1 电解锰渣表征分析
采用XRF、XRD、XPS和BET等分析手段对电解锰渣元素组成、价态和比表面积进行了表征,结果如表2、图2和表3所示.由表2可知,电解锰渣中主要成分有O、Si、S、Ca、K、Al、Mn、Fe.其中O、Si、S、Ca含量比较高,都是矿物类的常规元素,过渡金属元素Mn和Fe的质量分数分别为2.28%和1.49%.XRD分析发现电解锰渣中含有MnO、Mn2O3、FeO、Fe2O3,但衍射峰值相对都较低(图2a),电解锰渣是酸浸渣,不仅含有大量的SiO2,而且钙与硫酸反应会生成大量的硫酸钙,导致部分Mn、Fe等物质的衍射峰被掩盖.

表2 电解锰渣XRF主要成分分析

图2 电解锰渣的表征图谱
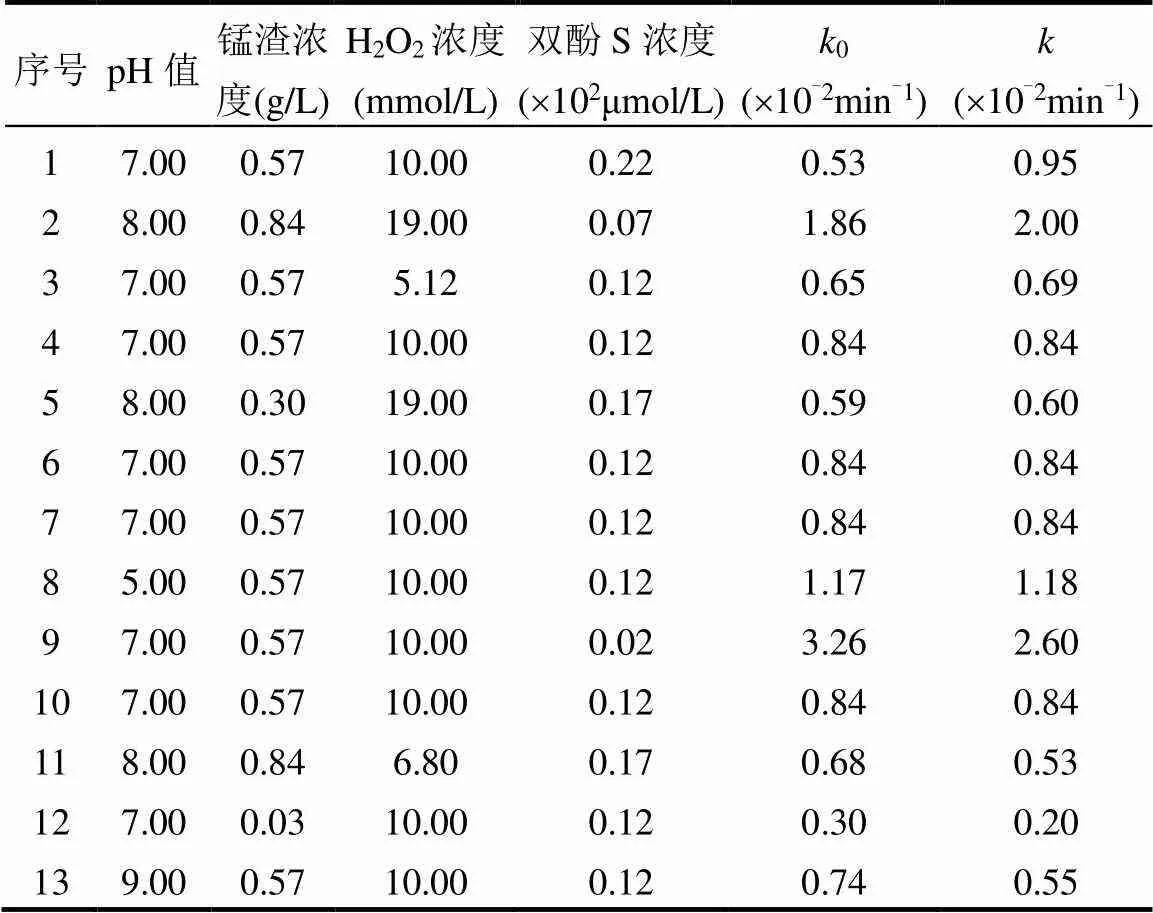
表3 响应面实验设计中双酚S降解的实验条件和动力学参数
通过XPS分析了电解锰渣的表面元素和价态,如图2b~d所示.由图2b可知,电解锰渣表面含有C、O、S、N、Ca、Al、Si、Mn、Mg等元素.图2c和2d的XPS表征结果显示锰渣中的Mn元素存在MnO、Mn2O3两种氧化物形态, Fe元素有FeO和Fe2O3两种化合态,铁和锰有较好的催化活性,铁离子又是光Fenton体系的重要阳离子,因而电解锰渣理论上可具有较好的催化活性.N2吸脱附曲线表征了电解锰渣孔隙率和比表面积.如图2e所示,电解锰渣等温线高压下逐渐弯曲,说明吸附能力比较弱,吸附曲线和脱附曲线不一致,出现迟滞回线,这是介孔固体产生的原因.图2f是电解锰渣的孔径分布图,粒子呈现双峰分布,这是颗粒间距和中空孔结构的结果.计算获得电解锰渣的比表面积、孔隙体积、孔径分别为12.43m2/g、0.06cm3/g和10.38nm.
2.2 双酚S在不同体系中的降解动力学
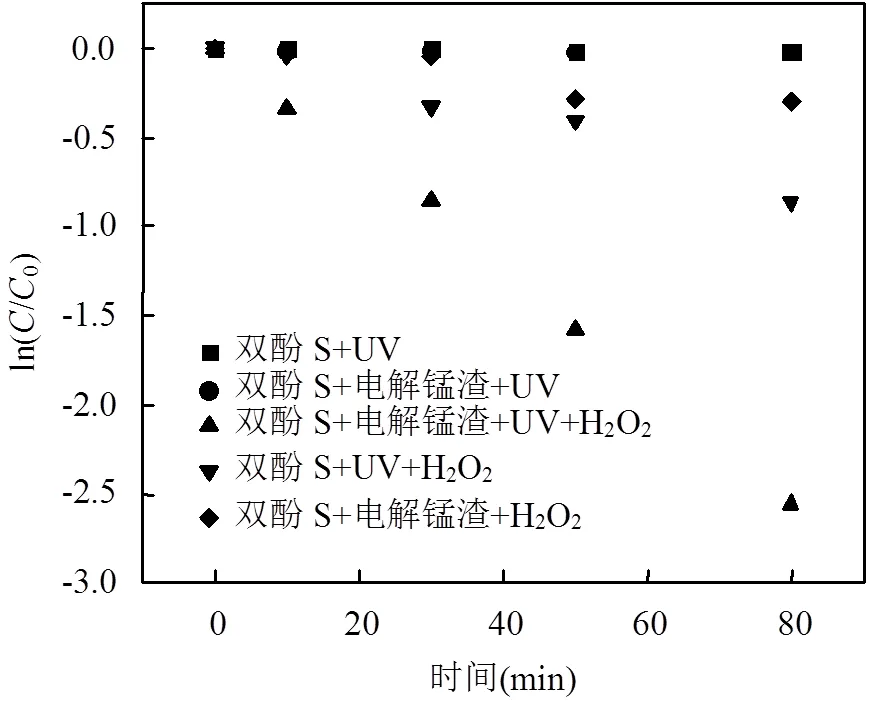
图3 双酚S在不同氧化体系中的降解动力学
[双酚S]=2μmol/L,[电解锰渣]= 0.57g/L,[H2O2]=10mmol/L,pH=7
黑暗条件下,80min反应时间内含有电解锰渣的体系中双酚S的减少量只有5%,说明电解锰渣吸附等行为对双酚S的影响可忽略,这与BET表征结果电解锰渣具有较小的比表面积和孔隙体积一致.由图3可知,在UV照射下,双酚S含量几乎不变,说明双酚S在实验条件下直接光降解可忽略,同时,电解锰渣/UV体系中,双酚S也未有明显渐少;而在UV/H2O2体系中,双酚S降解明显,其降解准一级速率常数为0.0106min-1,且在60min内,双酚S降解了57.9%,这与H2O2光致产生强氧化性的•OH有关;在电解锰渣/UV/H2O2体系中,双酚S的降解更为明显,在反应时间内约有90%的双酚S被氧化降解,其值为0.032min-1,且降解速率远高于UV/H2O2和电解锰渣/H2O2体系中值的加和,说明在上述体系中电解锰渣/UV/H2O2对双酚S具有更好的氧化降解能力.
2.3 初始pH值、电解锰渣投加量、H2O2浓度、双酚S浓度对双酚S降解的影响
为了研究电解锰渣作为光催化剂的非均相光Fenton体系中影响双酚S降解的因素,选取初始pH值、电解锰渣投加量、H2O2浓度、双酚S浓度为目标影响因子,研究其对双酚S降解动力力学的影响.图4a显示了电解锰渣/UV/H2O2体系中双酚S的降解速率随pH值的变化(4~9).值随着pH值的增加逐渐减小,而当pH³6时双酚S的降解速率变化不大.以往研究也发现类Fenton反应体系在酸性条件下具有更强的氧化效果[26].图4b观察到随着电解锰渣投加量的增加,双酚S的降解速率逐渐增加,这与电解锰渣中含有Mn、Fe等活性组分有关.类Fenton体系中H2O2的浓度是影响类Fenton体系氧化效果的重要参数,图4c显示随着H2O2浓度的增加(5.1~ 100.0mmol/L),双酚S降解速率的增加逐渐减小,这是由于过多的H2O2可与•OH反应,导致体系中•OH的稳态浓度降低[27-28].随着双酚S的初始浓度增加,其光解速率也呈现降低的趋势(图4d),说明高浓度目标物浓度不利于其降解.综上,初始pH值、电解锰渣投加量、H2O2浓度和目标物浓度等因素显著影响电解锰渣/UV/H2O2体系的氧化效果.
采用响应面法(RSM)研究了上述影响因素的复合作用对电解锰渣/UV/H2O2体系中双酚S降解动力学的影响.表3显示了操作参数(初始pH值、电解锰渣投加量、H2O2浓度、双酚S浓度)在RSM实验设计条件下双酚S的实际值0和预测值.通过RSM对二次方程式(1)进行统计拟合,可以得到操作参数前面的系数值(表4).从表4可以看出,在< 0.05显著性水平下,一次项pH值、[电解锰渣]、[H2O2]、[双酚S],交叉项[电解锰渣]-[双酚S]和平方项[双酚S]-[双酚S]是影响双酚S降解的显著性因素,[电解锰渣]和[双酚S]-[双酚S]的系数是正值,说明[电解锰渣]和[双酚S]-[双酚S]对双酚S的降解起促进作用;[电解锰渣]-[电解锰渣]的系数是负值,说明两者之间的相互作用对双酚S的降解起抑制作用.虽然交叉项也显著影响双酚S的降解速率,但通过各项系数的平方和的计算,可得一次项对双酚S降解速率的贡献高达80%,说明单因素对双酚S降解的影响占主导地位.利用响应面法得出最佳因素条件为pH=7,电解锰渣投加量为0.57g/L, H2O2浓度=10mmol/L,双酚S初始浓度为2μmol/L.接下来将以此为研究条件,探查电解锰渣/UV/H2O2体系中双酚S的氧化降解机制.

图4 不同因素对双酚S降解动力学的影响

表4 响应面实验中双酚S二次方程式系数评估和假设检验
注:-表示没有该项数值.
2.4 双酚S在电解锰渣/UV/H2O2体系中的降解机制
为研究电解锰渣类光Fenton体系中双酚S的降解过程,通过加入自由基淬灭剂(异丙醇来淬灭•OH;氯仿淬灭O2•–)以及向反应溶液中通入N2和O2来探究自由基的作用.如图5所示,加入异丙醇后双酚S的降解几乎完全被抑制,其降解速率常数只有原来的5%左右,说明在该体系中起主要氧化降解作用的是•OH.以DMPO为•OH捕获剂,采用电子自旋共振技术以验证电解锰渣/UV/H2O2体系中•OH的生成.如图6所示,黑暗条件下,只加入双氧水的体系没有检测到•OH的信号,而电解锰渣类光Fenton反应体系中检测到了1:2:2:1的DMPO-OH加合物的特征峰[29].在0min就产生了•OH,说明电解锰渣在没有光照条件下就催化分解H2O2,在15和30min,峰高显著增加,证明了DMPO-OH浓度增加,在光照条件下,电解锰渣/UV/H2O2体系中的•OH生成量增多,所以得出电解锰渣催化作用和光照对电解锰渣/UV/ H2O2体系中的•OH生成起协同作用.

图5 不同活性物种和通气对双酚S降解的影响
[双酚S]=2μmol/L [H2O2]=10mmol/L,[电解锰渣]= 0.57g/L,[异丙醇]=20mmol/L,[氯仿]=20mmol/L,pH=7
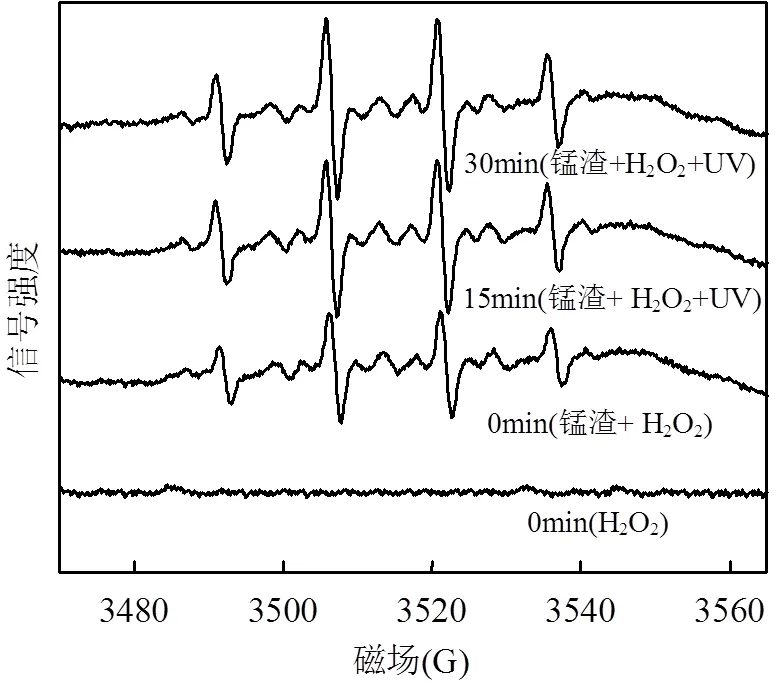
图6 电子自旋共振光谱图
[H2O2]=10mmol/L [电解锰渣]= 0.57g/L,pH=7
加入O2•–淬灭剂氯仿后双酚S的值由0.0254min-1减小为0.0235min-1,约减少了8%,表明O2•–对双酚S的降解也起到一定作用.这是因为O2•–的氧化还原电位1.56V小于•OH的氧化还原电位2.8V,O2•–对双酚S的氧化降解能力弱于•OH.在通入氧气的条件下,双酚S降解的较快,值为原来的1.2倍;而在通氮气除氧气时,双酚S的降解速率显著降低,其值只有原来的64%,表明O2对该非均相光Fenton体系中双酚S的降解有一定的贡献.一方面O2可以接受体系中光诱导产生电子形成O2•–与双酚S直接反应或歧化反应产生•OH.另外,研究发现单羟基化双酚A产品可以在氧气存在下形成过氧自由基,进而产生•OH[30],据此推断双酚S也可以经历类似的反应过程产生•OH,促进其降解.此外,催化活性组分在反应过程中多有金属离子的释放[31],故研究了电解锰渣催化反应过程中Mn、Fe等活性组分的浸出量.由图7a可知,溶液中Mn和Fe的浸出浓度随着pH值的增加逐渐减小,即高pH值条件不利于电解锰渣中金属活性组分的浸出.为此考虑了pH=7条件下Mn和Fe的浸出浓度,通过配制含有Mn和Fe离子的模拟溶液研究金属离子均相光Fenton体系对双酚S降解的影响.由图7b可知,相比于UV/H2O2体系, 6.62mg/L Mn2+和0.36mg/L Fe2+共存条件下,双酚S的降解显著被抑制,其值由0.0106min-1减小到0.0049min-1,表明光助-电解锰渣/ H2O2氧化体系反应浸出的共存活性金属组分不利于双酚S降解,阐明本研究构建的基于电解锰渣的光Fenton体系主要通过界面过程影响双酚S降解.由以上讨论可以推测出电解锰渣作为光催化剂的非均相光Fenton体系中双酚S的降解过程(图8).
电解锰渣/UV/H2O2体系中•OH的产生主要包括以下两方面:①电解锰渣表面的FeO和MnO等活性金属氧化物在光照下受激发产生氧化空穴(h+)和电子(e-),H2O2得到电子或者被h+氧化为•OH,在电解锰渣表面与双酚S反应.②O2得到电子生成超氧自由基(O2•-),可歧化产生•OH与双酚S反应.
•OH的生成速率是类Fenton体系的重要参数,采用硝基苯(NB)和异丙醇(2Pr)作为探针化合物估算出电解锰渣/UV/H2O2体系中的•OH 生成速率f•OH[30].硝基苯与•OH可直接反应生成不同的硝基酚和1,3-二硝基苯.根据以下方程式(2)得出估算•OH形成速率的动力学模型:
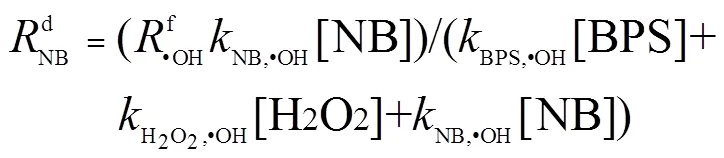
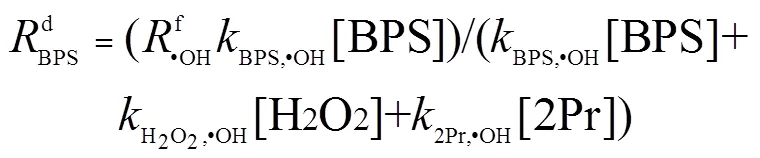
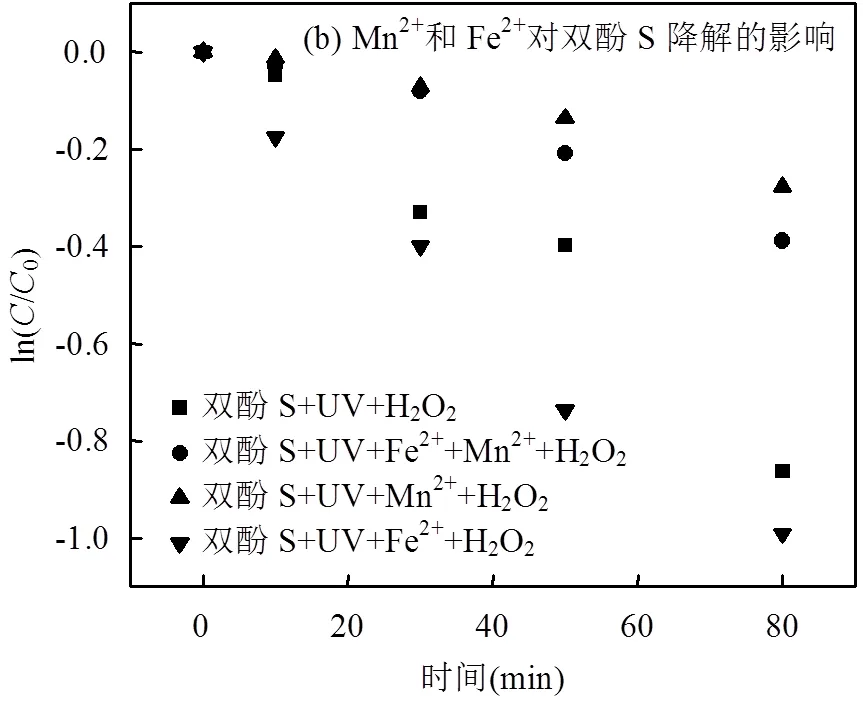
图7 电解锰渣中锰和铁对双酚S降解的影响
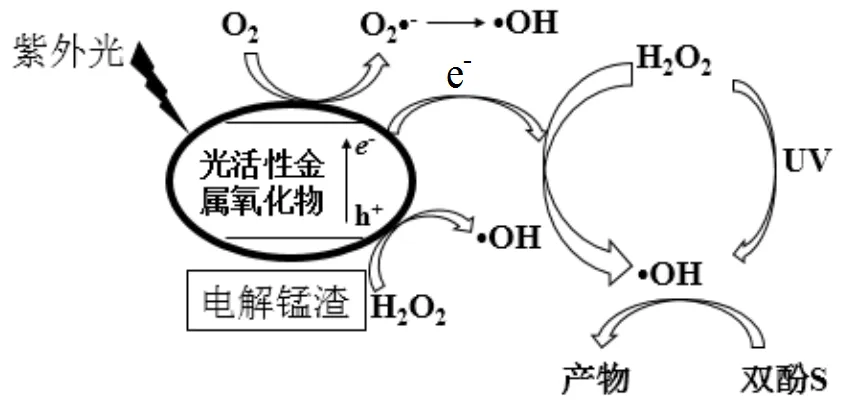
图8 电解锰渣/UV/H2O2体系中•OH产生机制

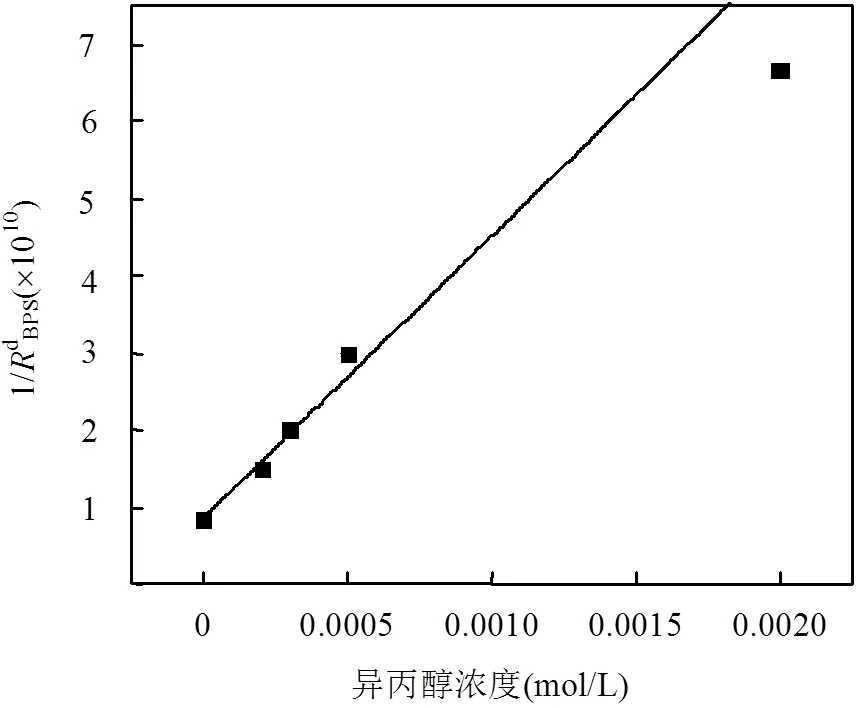
图9 异丙醇体系•OH生成速率拟合
[双酚S]=2μmol/L [H2O2]=10mmol/L,[电解锰渣]= 0.57g/L,[异丙醇,2Pr]=0、100μmol/L、300μmol/L、500μmol/L、2mmol/L,pH=7
2.5 DOM对双酚S在电解锰渣/UV/H2O2体系中降解的影响
DOM普遍存在于自然水体,且也是有机废水中重要的组分,可显著影响类Fenton体系的氧化降解效率[32].为此,研究了DOM对电解锰渣/UV/H2O2体系中双酚S氧化降解的影响.由图10可知,DOM的存在显著抑制双酚S的降解,且随DOM浓度的增加,抑制效应越发明显.以往的研究中发现DOM对光Fenton体系污染物的降解影响包括产生与有污染物反应的激发三重态DOM(3DOM*),淬灭•OH,产生光屏蔽效应等[33].为研究DOM的影响机制,基于•OH稳态近似法构建了可预测DOM存在时双酚S降解的动力学模型,如式(4)所示.

式中:,,分别为双酚S,DOM,OH-与•OH反应的二级反应速率常数,=2.5×104L/ (mg·s)[31],=1.3×1010L/(mol·s)[32],[BPS],[•OH],[DOM],[OH-]代表溶液中双酚S,•OH,DOM,OH-的浓度.电解锰渣/UV/H2O2体系中产生•OH的消耗途径主要包含与双酚S、DOM和OH-的反应.通过式(4)便可预测电解锰渣/UV/H2O2体系中双酚S的降解速率常数,如图10所示.总体上,降解速率的预测值与实际值差别不大,说明DOM影响双酚S的降解主要通过淬灭•OH,且构建的动力学模型可以较好的预测氧化体系中双酚S的降解速率.
[双酚S]=2μmol/L,[H2O2]=10mmol/L,[电解锰渣]= 0.57g/L,pH=7
3 结论
3.1 基于电解锰渣的光Fenton体系氧化降解双酚S是有效可行的,这与H2O2光致产生强氧化性的•OH有关.
3.2 通过电解锰渣的表征发现锰渣是介孔结构,并且含有锰和铁,因此电解锰渣是具有催化活性的.
3.3 双酚S在电解锰渣/UV/H2O2体系中的降解速率与pH值、双酚S初始浓度呈负相关,与电解锰渣投加量、H2O2浓度呈正相关,响应面实验研究发现除了上述单因素外,影响因素间的相互作用[电解锰渣]-[双酚S]和[双酚S]-[双酚S]也影响双酚S的降解(<0.05).
3.4 自由基淬灭实验和电子自旋共振证实了电解锰渣/UV/H2O2体系中起主要作用的活性物种是•OH;通过均相对比实验,发现电解锰渣/UV/H2O2氧化体系反应浸出的共存活性金属组分不利于双酚S降解,主要是非均相的催化作用,同时揭示了锰渣中的活性金属氧化物产生的电子和空穴分解H2O2产生•OH.
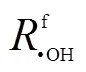
[1] 马海洪,张绍军,石建明.制备双酚S研究的新进展[J]. 化工进展, 2001,20(8):22-26.Ma H H, Zhang S J, Shi J M. New progress in preparation of bisphenol S [J]. Progress in Chemical Industry, 2001,20(8):22-26.
[2] 杨蕴嘉,尹 杰,邵 兵.双酚A替代物-双酚S的研究进展[J]. 首都公共卫生, 2016,10(5):222-225.Yang Y J, Yin J, Shao B. Research progress of bisphenol A substitute bisphenol S [J]. Capital Public Health, 2016,10(5):222-225.
[3] 李晓蒙,张立实,隋海霞,等.双酚S和双酚F的危害识别[J]. 卫生研究, 2018,47(6):149-152.Li X M, Zhang L S, Sui H X, et al. Hazard identification of bisphenol S and bisphenol F [J]. Institute of Health, 2018,47(6):149-152.
[4] Molina-Molina, José-Manuel, Amaya E, et al. In vitro study on the agonistic and antagonistic activities of bisphenol-S and other bisphenol-A congeners and derivatives via nuclear receptors [J]. Toxicology & Applied Pharmacology, 2013,272(1):127-136.
[5] Jin H, Zhu L. Occurrence and partitioning of bisphenol analogues in water and sediment from Liaohe River Basin and Taihu Lake, China [J]. Water Research, 2016,103(15):343-351.
[6] Yamazaki E, Yamashita N, Taniyasu S, et al. Bisphenol A and other bisphenol analogues including BPS and BPF in surface water samples from Japan, China, Korea and India [J]. Ecotoxicology & Environmental Safety, 2015,122(12):565-572.
[7] Wang Q, Chen M, Shan G, et al. Bioaccumulation and biomagnification of emerging bisphenol analogues in aquatic organisms from Taihu Lake, China [J]. ence of the Total Environment, 2017,598:814-820.
[8] Sun Q, Wang Y, Li Y, et al. Fate and mass balance of bisphenol analogues in wastewater treatment plants in Xiamen City, China [J]. Environmental Pollution, 2017,225(6):542.
[9] Song S, Song M, Zeng L, et al. Occurrence and profiles of bisphenol analogues in municipal sewage sludge in China [J]. Environmental Pollution, 2014,186(3):14-19.
[10] Chen D, Kannan K, Tan H, et al. Bisphenol analogues other than BPA: Environmental occurrence, human exposure, and toxicity-A review [J]. Environmental Science & Technology, 2016.
[11] 赵 超,姜利荣,黄应平.Fenton及Photo-Fenton非均相体系降解有机污染物的研究进展[J]. 分析科学学报, 2007,23(3):355-360. Zhao C, Jiang L R, Huang Y P. Research progress on degradation of organic pollutants by Fenton and photo Fenton heterogeneous system [J]. Journal of Analytical Science, 2007,23(3):355-360.
[12] 陈芳艳.光助Fenton法在废水处理中的应用研究进展[J]. 工业用水与废水, 2008,39(3):17-21.Cheng Y F. Research progress of photo assisted Fenton process in wastewater treatment [J]. Industrial Water and Wastewater, 2008,39(3):17-21.
[13] 李国亭,宋海燕,刘秉涛.光催化过程中羟基自由基的产生与效能[J]. 环境工程学报, 2012,6(10):3388-3392. Li G T, Song H Y, Liu B T. Generation and efficiency of hydroxyl radicals in photocatalytic process [J]. Journal of Environmental Engineering, 2012,6(10):3388-3392.
[14] Nosaka Y, Nosaka A. Understanding hydroxyl radical (OH) generation processes in photocatalysis (open access viewpoint) [J]. ACS Energy Letters, 2016,1(2):356-359.
[15] Vione D, Minero C, Maurino V, et al. Degradation of phenol and benzoic acid in the presence of a TiO2-based heterogeneous photocatalyst [J]. Applied Catalysis B Environmental, 2005,58(1/2):79-88.
[16] Kato H, Hori M, Konta R, et al. Construction of Z-scheme type heterogeneous photocatalysis systems for water splitting into H2and O2under visible light irradiation [J]. Chemistry Letters, 2004,33(10): 1348-1349.
[17] Fox M A. Heterogeneous photocatalyst [J]. Chemical Reviews, 1996,93:341-357.
[18] 陈红亮,刘仁龙,李文生,等.电解锰渣的理化特性分析研究[J]. 金属材料与冶金工程, 2014,42(1):3-5. Cheng H L, Liu R L, Li W S, et al. Study on physical and chemical properties of electrolytic manganese slag [J]. Metal Materials and Metallurgical Engineering, 2014,42(1):3-5.
[19] Zhou C B, He J, Meng J L. Advances in comprehensive utilization of electrolytic manganese slag [J]. Research of Environmental Sciences, 2010,23(8):1044-1048.
[20] Li H, Zhang Z, Tang S, et al. Ultrasonically assisted acid extraction of manganese from slag [J]. Ultrasonics Sonochemistry, 2008,15(4): 339-343.
[21] Wang J, Peng B, Chai L, et al. Preparation of electrolytic manganese residue–ground granulated blastfurnace slag cement [J]. Powder Technology, 2013,241:12-18.
[22] 王 智,孙 军,钱觉时.电解锰渣中硫酸盐性质的研究[J]. 材料导报, 2010,(10):61-64. Wang Z, Sun J, Qian J S. Study on the properties of sulfate in electrolytic manganese slag [J]. Materials Guide, 2010,(10):61-64.
[23] 刘胜利.电解金属锰废渣的综合利用[J]. 中国锰业, 1998,16(4):35-36. Liu S L. Comprehensive utilization of electrolytic manganese residue [J]. Manganese industry in China, 1998,16(4):35-36.
[24] 钟 超.催化氧化降解工业废水的催化剂和工程应用研究[D]. 武汉:中南民族大学, 2015. Zhong C. Study on catalysts and engineering application of catalytic oxidation degradation of industrial wastewater [D]. Wuhan: Central South University for Nationalities, 2015.
[25] 戴慧旺,陈建新,苗笑增,等.醇类对UV-Fenton体系羟基自由基淬灭效率的影响[J]. 中国环境科学, 2018,38(1):202-209. Dai H W, Cheng J X, Miao X Z, et al. Effect of alcohols on quenching efficiency of hydroxyl radical in UV Fenton system [J]. China Environmental Science, 2018,38(1):202-209.
[26] Xiao Y, Zhang L, Zhang W, et al. Comparative evaluation of iodoacids removal by UV/persulfate and UV/H2O2processes [J]. Water Research, 2016,102(1):629-639.
[27] Xia M, Long M, Yang Y, et al. A highly active bimetallic oxides catalyst supported on Al-containing MCM-41 for Fenton oxidation of phenol solution [J]. Applied Catalysis B Environmental, 2011,110: 118-125.
[28] 存 洁,田森林,王 倩,等.二茂铁催化光助非均相类Fenton氧化法处理含罗丹明B废水[J]. 中国环境科学, 2013,33(6):1011-1016. Cun J, Tian S L, Wang Q, et al. Treatment of Rhodamine B wastewater by heterogeneous photo-Fenton oxidation catalyzed by ferrocene [J]. China Environmental Science, 2013,33(6):1011-1016.
[29] 刘光虹,王晓旋,胡少刚,等.电子自旋共振仪测定羟基自由基[J]. 高校实验室科学技术, 2019,(1):55-56. Liu G H, Wang X X, Hu S G, et al. Determination of hydroxyl radical by ESR [J]. University Laboratory Science and Technology, 2019, (1):55-56.
[30] Huang W, Brigante M, Wu F, et al. Assessment of the Fe(III)-EDDS complex in fenton-like processes: From the radical formation to the degradation of bisphenol A [J]. Environmental Science & Technology, 2013,47(4):1952-1959.
[31] 董正玉.铁锰双金属催化剂活化过硫酸盐去除水中偶氮染料和双酚A的研究[D]. 厦门:华侨大学, 2019. Dong Z Y. Study on the removal of azo dyes and bisphenol A from water by persulfate activated by Fe Mn bimetallic catalyst [D]. Xiamen: Huaqiao University, 2019.
[32] 李 宁.溶解性有机质对羟基自由基氧化降解有机污染物的影响[D]. 大连:大连理工大学, 2016. Li N. Effect of dissolved organic matter on degradation of organic pollutants by hydroxyl radical oxidation [D]. Dalian: Dalian University of Technology, 2016.
[33] Fang J, Fu Y, Shang C. The roles of reactive species in micropollutant degradation in the UV/free chlorine system [J]. Environmental ence & Technology, 2014,48(3):1859-1868.
[34] Ge L, Chen J, Qiao X, et al. Light-Source-Dependent effects of main water constituents on photodegradation of phenicol antibiotics: mechanism and kinetics [J]. Environmental Science & Technology, 2009, 43(9):3101-3107.
[35] Fang J, Fu Y, Shang C. The roles of reactive species in micropollutant degradation in the UV/free chlorine system [J]. Environmental Science & Technology, 2014,48(3):1859-1868.
[36] Liang H, Li T R, Zhang J, et al. 3-D hierarchical Ag/ZnO@CF for synergistically removing phenol and Cr(VI): Heterogeneous vs. homogeneous photocatalysis [J]. Journal of Colloid and Interface Science, 2020,558:85-94.
[37] Ahmed S, Ahmed Z. Development of hexagonal nanoscale nickel ferrite for the removal of organic pollutant via Photo-Fenton type catalytic oxidation process [J]. Environmental Nanotechnology Monitoring & Management, 2020,14:100321.
[38] Ferreira L C, Jose R, Fernandes, et al. Tavares. Photocatalytic degradation of an agro-industrial wastewater model compound using a UV LEDs system: kinetic study [J]. Journal of Environmental Management, 2020,269:110740.
[39] Sun P, Lee W N, Zhang R, et al. Degradation of DEET and caffeine under UV/Chlorine and simulated sunlight/chlorine conditions [J]. Environmental Science & Technology, 2016,50(24):13265-13273.
[40] Zheng J, Gao Z, He H, et al. Efficient degradation of Acid Orange 7in aqueous solution by iron ore tailing Fenton-like process [J]. Chemosphere, 2016,150(5):40-48.
[41] Xu L P, Li H, Mitch William A, et al, et al. Enhanced phototransformation of tetracycline at smectite clay surfaces under simulated sunlight via a lewis-base catalyzed alkalization mechanism [J]. Environmental Science & Technology, 2019,53(2):710-718.
Degradation of bisphenol S by photo-assisted electrolysis manganese slag/H2O2heterogeneous system.
XU Zi-hao, LI Ying-jie*, XIONG Yu-lu, HOU Zhi-chao, LI Jin-suo, TIAN Sen-lin
(Faculty of Environmental Science and Engineering, Kunming University of Science and Technology, Kunming 650500, China)., 2021.41(5):2123~2132

electrolytic manganese slag;bisphenol S;heterogeneous photo-Fenton reaction system;photocatalysis degradation;•OH;kinetic model
X705
A
1000-6923(2021)05-2123-10
徐子豪(1996-),男,河南驻马店人,昆明理工大学硕士研究生,主要研究方向为水环境中光催化技术.
2020-09-07
国家重点研发计划(2018YFC0213405);国家自然科学基金资助项目(21707058);云南省优秀青年基金(2019FI004);省级大学生创新创业训练计划项目(202010674052)
* 责任作者, 副教授, yjli@kmust.edu.cn
