[(6-取代-嘧啶-4-基氧)苯基]-3-甲氧基-丙烯酸甲酯的合成与抑菌活性
2021-01-20李玉江郭晓河董黎红
陶 乐, 李玉江, 郭晓河, 王 强, 董黎红, 张 倩
(河南省科学院高新技术研究中心,郑州 450002)
病害常年损失在10%以上,农作物由此平均每年减少产量约500 Mt. 如果不及时防治,病害在短时间内发展很快,受害面积逐步扩大. 由于农作物上的病菌在抗药性上越来越强,所以高效、低毒农药的研制是迫在眉睫的问题. 研制新型农药既能有效延缓病原群体抗药性的产生,也能对植物病害防治起到关键作用.嘧菌酯[1-4]是杀菌剂中的一类低毒、高效、广谱、内吸性杀菌剂,其来源于天然产物Strobilurin,是线粒体呼吸抑制剂. 它对几乎所有真菌类(子囊菌纲、担子菌纲、卵菌纲、半知菌类)病害都显示出很好的活性,具有保护、治疗、铲除、渗透、内吸活性等特点;同时,嘧菌酯还具有高度选择性,对作物具有很高的安全性[5-7],对环境基本无污染,可以茎叶喷雾、种子处理等方式使用[8],它具有保护、治疗和铲除三重功效[9-10],可通过结合色素b络合物,抑制电子链磷酸化产生能量[11]. 但是嘧菌酯难溶于水,不易被吸收[12]. 天然化合物的发现为新的化学合成打开了一扇大门,科学家正是基于此才成功地人工合成了许多结构类似的具有生物活性的杀菌剂. 在创制新农药的方法中,以天然化合物为基础,对其结构进行一定的修饰是一条非常有效的途径[13-17].本文为了丰富抗菌化合物库,改善化合物的溶解性,提高吸收率,合成了一系列[(6-取代-嘧啶-4-基氧)苯基]-3-甲氧基丙烯酸甲酯化合物(化合物6~11). 通过体外抗菌活性测试,发现[(6-取代-嘧啶-4-基氧)苯基]-3-甲氧基丙烯酸甲酯都有一定的抑菌活性,为进一步设计的新型抑菌分子提供了新的思路.[(6-取代-嘧啶-4-基氧)苯基]-3-甲氧基丙烯酸甲酯的合成路线如下所示:

1 实验部分
1.1 仪器与试剂
邻羟基苯乙酸(1)购自上海源叶生物科技有限公司,二甲基亚砜、吐温、马铃薯葡萄糖琼脂(PDA)均购自天津科密欧化学试剂有限公司,所用其他试剂均为市售分析纯.
质谱仪为高分辨质谱仪Bruker micro TOF-Qii;核磁共振波谱仪为Agilent-NMR-vnmrs400型,TMS为内标.
1.2 合成
1.2.1 苯并呋喃-2-(3 氢)-酮(2)的合成 依次将邻羟基苯乙酸(1)(304 g,2 mmol)、甲苯(2 L)、冰醋酸(0.5 L)、五氧化二磷(500 g)加入反应器中,加热回流反应6 h后,冷至室温,慢慢加入冰水,用乙酸乙酯萃取3 次,合并有机相,再用饱和食盐水萃取,有机相用无水硫酸钠干燥,减压浓缩至干,无须提纯可直接用于下一步反应. 取出小部分柱层析得到化合物2 白色针状结晶. 熔点:48~50 ℃,1H NMR(CDCl3,400 Hz),3.72(s,2H,CH2),7.08~7.32(m,4H,Ph-H).
1.2.2 3-α-甲氧基)亚甲基苯并呋喃-2(3氢)-酮(3)的合成 取上一步原料,加入原甲酸三甲酯(265 g,2.5 mmol)和氯化锌(13.6 g,0.1 mol),升温至110 ℃继续反应4 h,反应结束后降温. 反应体系中加入乙酸乙酯和水洗涤,分出有机相,减压浓缩,得到化合物3. 产物无须提纯,直接用于下一步反应. 取出小部分柱层析得到化合物3 为黄绿色固体,熔点:27~29 ℃,1H NMR(CDCl3,400 Hz),4.13(S,3H,CH3),7.06~7.13(m,2H,Ph-H),7.18~7.21(m,1H,CH),7.53~7.56(m,2H,Ph-H).
1.2.3 2-(2-羟基苯基)-3,3-二甲氧基丙酸甲酯酚钠盐(4)的合成 将上步原料加入甲醇(2 L),冰盐浴下加入甲醇钠(130 g,2.4 mmol),继续搅拌反应2 h后,反应液减压浓缩直接用于下一步反应. 取少量浓缩物加入稀盐酸中和至pH=6,然后用乙酸乙酯和水萃取,有机相减压浓缩至干,柱层析提纯得到无色透明油状物化合物4.1H NMR(CDCl3,400 Hz):3.38(s,3H,OCH3),3.68(s,3H,OCH3),4.95(s,1H,CH),6.76~6.85(m,2H,Ph-H),7.15~7.18(m,2H,Ph-H).
1.2.4 2-[2-(6-氯嘧啶-4-基氧)苯基]-3-甲氧基丙烯酸甲酯(5)的合成 室温条件下,依次将碳酸钠(106 g,1 mol)、4,6-二氯嘧啶(300 g,2 mol)、1,4-二氧六环(2 L)加入到反应瓶里,搅拌一会儿后向上述反应液中慢慢加入化合物4的酚钠盐,加热反应至60 ℃,继续反应6 h,趁热减压滤掉盐,冷至室温后加入水和乙酸乙酯,分出有机相,无水硫酸钠干燥,减压浓缩,得到浅黄色固体5.1H NMR(CDCl3,400 MHz),δ:3.59(s,3H,OCH3),3.73(s,3H,OCH3),3.95(s,3H,OCH3),6.06(s,1H,CH),7.15~7.44(m,4H,Ph-H),7.44(s,1H,Pyr-H),8.44(s,1H,Pyr-H),13C NMR(CDCl3,400 MHz),δ:171.586,170.721,167.397,160.346,157.705,150.344,132.456,128.942,125.876,125.382,121.899,107.099,90.828,61.730,54.035,51.363;HRMS:m/z[M+H]+.
1.2.5 2-[2-(6-甲氧基嘧啶-4-基氧)苯基]-3-甲氧基丙烯酸甲酯(6)的合成 将化合物5(1.03 g,3.4 mmol)、甲醇(10 mL)、甲醇钠(0.18 g,3.4 mmol)依次加入到反应器内,加热回流搅拌反应完全后,冷至室温,加入水和乙酸乙酯,分出有机相,减压蒸出有机相,柱层析得到白色结晶性粉末化合物6(0.84 g,83%).1H NMR(CDCl3,400 MHz),δ:3.60(s,3H,CH3),3.87(s,3H,CH3),6.46(s,1H,CH),6.62(s,1H,Pyr-H),7.18~7.73(m,8H,Ph-H),8.37(s,1H,Pyr-H),13C NMR(CDCl3,400 MHz),δ:171.397,170.076,165.355,15,9.330,157.834,154.032,150.670,134.178,133.541,131.917,129.040,129.002,126.194,125.534,115.152,107.274,107.046,92.854,62.565,51.454;HRMS:m/z[M+H]+305.113 2.
1.2.6 (E)-[2-[6-苯氧基)嘧啶-4-基氧)苯基]-3-甲氧基丙烯酸甲酯(7)的合成 将化合物5(3.1 g,10 mmol)、甲苯(25 mL)、苯酚(1.1 g,12.0 mol)、碳酸钾(1.38 g,10 mmol)、DMF(2 mL)、三乙烯二胺(DABCO)(0.2 g)组成的混合物搅拌,在100 ℃反应6 h. 冷至室温后,加入水和乙酸乙酯,分出有机相,无水硫酸钠干燥,减压蒸干,柱层析得到浅黄色固体7(3.51 g,96%).1H NMR(CDCl3,400 MHz),δ:3.64(s,6H,OCH3),3.78(s,6H,OCH3),6.24(s,2H,CH),7.17~7.52(m,9H,Ph-H),7.45(s,1H,Pyr-H),8.42(s,1H,Pyr-H).13C NMR(CDCl3,400 MHz),δ:171.442,170.843,167.397,160.483,158.039,153.159,150.169,132.539,130.300,129.033,125.845,125.663,121.929,118.666,115.235,107.062,92.035,61.836,51.447;HRMS:m/z[M+H]+367.128 8.1.2.7 (E)-[2-[6-对-硝基-苯氧基)嘧啶-4-基氧]苯基]-3-甲氧基丙烯酸甲酯(8)的合成 将化合物5(3.1 g,10 mmol)、甲苯(25 mL)、对硝基-苯酚(1.7 g、12.0 mol)、碳酸钾(1.38 g,10 mmol)、DMF(2 mL)、三乙烯二胺(DABCO)(0.2 g)组成的混合物搅拌,在100 ℃反应6 h. 冷至室温后,加入水和乙酸乙酯,分出有机相,无水硫酸钠干燥,减压蒸干,柱层析得到黄色固体(8)(3.78 g,92%).1H NMR(CDCl3,400 MHz),δ:3.62(s,3H,OCH3),3.78(s,3H,OCH3),6.18(s,1H,CH),7.19~7.43(m,6H,Ph-H),7.48(s,1H,Pyr-H),8.29~8.32(m,2H,Ph-H),8.42(s,1H,Pyr-H),13C NMR(CDCl3,400 MHz),δ:171.655,169.939,167.382,160.559,157.888,157.311,150.048,144.857,132.623,129.109,125.838~125.921,125.382,121.823~121.921,115.493,106.948,92.756,61.882,60.288,51.469,20.922,14.069;HRMS:m/z[M+H]+.
1.2.8 (E)-[2-[6-对-氨基-苯氧基)嘧啶-4-基氧]苯基]-3-甲氧基丙烯酸甲酯(9)的合成 在装有化合物(8)(2.0 g,5 mmol)的反应瓶里分别加入铁粉(0.56 g,10 mmol)、浓盐酸(2 mL)、乙醇(10 mL)和水(2 mL),60 ℃条件下搅拌反应2 h,补加浓盐酸(2 mL),继续反应5 h,冷至室温,加入水和乙酸乙酯,分出水相用碳酸钠饱和溶液中和至碱性,乙酸乙酯萃取,减压浓缩至干,柱层析得到黄色化合物(9)(1.74 g,94%).1H NMR(CDCl3,400 MHz),δ:3.62(s,3H,OCH3),3.78(s,3H,OCH3),6.18(s,1H,CH),7.19~7.43(m,6H,Ph-H),7.48(s,1H,Pyr-H),8.29~8.32(m,2H,Ph-H),8.42(s,1H,Pyr-H),13C NMR(CDCl3,400 MHz),δ:172.057,171.192,167.389,160.392,158.063,150.199,144.204~144.318,132.418,128.911,125.458~125.747,121.982,115.789,107.046,91.245,61.753,51.378;HRMS:m/z[M+H]+412.113 9.
1.2.9 (E)-[2-[6-{(E)-[2-[6-(2-氰基苯氧基)嘧啶-4-基氧]苯基]-3-甲氧基丙烯酸甲酯基}嘧啶-4-基氧]苯基]-3-甲氧基丙烯酸甲酯(10)的合成 依次将化合物5(3.0 g,10 mmol)、甲苯(30 mL)、邻羟基苯酚(1.90 g,5 mol)、碳酸钾(1.38 g,10 mmol)、DMF(2 mL)、三乙烯二胺(DABCO)(0.2 g)加入到反应瓶里,在110 ℃搅拌反应6 h. 冷至室温后,加入水和乙酸乙酯,分出有机相,无水硫酸钠干燥,减压蒸干,柱层析得到微黄色固体(10).1H NMR(CDCl3,400 MHz),δ:3.60(s,6H,OCH3),3.75(s,6H,OCH3),6.28(s,2H,CH),7.06~7.48(m,12H,Ph-H),7.46(s,2H,Pyr-H),8.42(s,1H,Pyr-H),13C NMR(CDCl3,400 MHz),δ:171.503,170.903,167.473,160.529,158.115,153.228,150.230,132.600,130.353,129.093,125.898,125.731,121.977,118.719,115.296,107.137,92.095,61.905,51.522;HRMS:m/z[M+H]+655.203 5.
1.2.10 (E)-[2-[6-萘氧基)嘧啶-4-基氧]苯基]-3-甲氧基丙烯酸甲酯化合物(11)合成 将化合物5(3.1 g,10 mmol)、甲苯(25 mL)、萘酚(1.73 g,12.0 mol)、碳酸钾(1.38 g,10 mmol)、DMF(2 mL)、DABCO(0.2 g)组成的混合物搅拌,在120 ℃反应6 h. 冷至室温后,加入水和乙酸乙酯,分出有机相,无水硫酸钠干燥,减压蒸干,柱层析得到浅黄色固体11(2.7 g,65%).1H NMR(CDCl3,400 MHz),δ:3.59(s,3H,OCH3),3.74(s,3H,OCH3),6.18(s,1H,CH),6.70~7.40(m,11H,Ph-H),7.46(s,1H,Pyr-H),8.41(s,1H,Pyr-H),13C NMR(CDCl3,400 MHz),δ:171.928,171.472,167.405,160.453,158.305,150.215,148.325,134.846,132.516,128.995,128.076,126.908,126.566,126.468,126.088,125.769,125.587,125.526,122.055,121.383,117.702,107.084,91.458,61.798,51.439,20.952,14.099;HRMS:m/z[M+H]+417.144 5.
1.3 化合物体外抗菌活性测试
离体抑菌活性测试方法:离体抑菌活性测试方法采用菌丝生长速率法[18].
一定量的测试化合物溶于二甲基亚砜中,配成一定浓度的溶液,用吐温将该溶液稀释成浓度500 mg/L的测试液. 吸取1 mL上述溶液,加入到9 mL马铃薯葡萄糖琼脂(PDA)培养基中,待培养基完全凝固后接入供试菌种,在(25±1)℃黑暗环境下培养72 h之后,对菌落直径进行测量,并与空白对照组进行比较,得到离体抑制率.
菌丝生长抑制率=(空白对照菌落增长直径-药剂处理菌落增长直径)/空白对照菌落增长直径×100%.
2 结果与讨论
2.1 目标化合物的合成
本文采用邻羟基苯乙酸(1)为起始原料,经水解、闭环、甲氧基亚甲基化、开环、醚化、消除和缩合七步反应合成出嘧菌酯类似物,以邻羟基苯乙酸(1)为原料,在合成水杨酸内酯(2)、化合物3、化合物4的过程中,每一步不需要分离提纯,可以直接用于下一步反应,工艺简单,收率较高. 特别是以化合物5为起始原料,将甲苯、不同的取代基萘酚溶于适用的溶剂中,采用1,4-二氮杂双环[2.2.2]辛烷(DABCO)这个功能特殊的有机碱做催化剂,以较高的产率生成了目标产物. 本合成方法避免了以往嘧菌酯类似物合成方法普遍存在的合成成本高、操作步骤复杂、反应在高温下进行、操作难度大、能耗高、催化剂价格高、催化能力弱等问题.
2.2 目标化合物的抑菌活性
目标化合物[(6-取代-嘧啶-4-基氧)苯基]-3-甲氧基丙烯酸甲酯的抑菌活性初筛结果(表1)表明,当药剂浓度为50 μg/mL,这些化合物对花生褐斑病菌、苹果轮纹病菌、小麦纹枯病菌的抑制率均较高,其中化合物6 对黄瓜枯萎病菌的抑制率较高;化合物8、化合物10 对花生褐斑病菌抑制率较高;化合物10 对苹果轮纹病菌抑制率较高;化合物10、化合物9、化合物6、化合物8 和化合物7 对小麦纹枯病菌抑制率较高;化合物7对玉米小斑病菌抑制率较高;化合物7对西瓜炭疽病菌抑制率较高;化合物6、化合物9和化合物7对水稻恶苗病菌抑制率较高. 因此,该类化合物可以有效抑制农作物上的致病菌,对于目前农作物耐药性愈发严重的情况具有潜在应用价值,开发前景良好.
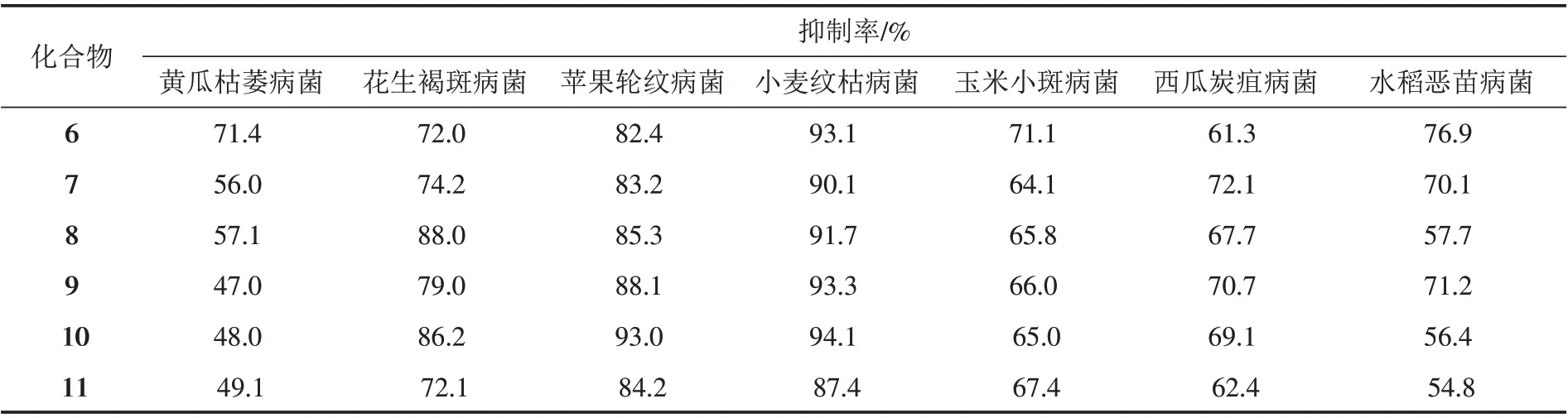
表1 化合物6~11在50 μg/mL浓度下有关离体抑菌活性测试的实验结果Tab.1 The experimental results of in vitro antibacterial activity test at the concentration of 50 μg/mL for compounds 6~11
从初筛结果可以看出,化合物6、化合物7、化合物8、化合物9、化合物10和化合物11对黄瓜枯萎病菌、花生褐斑病菌、苹果轮纹病菌、小麦纹枯病菌、玉米小斑病菌、西瓜炭疽病菌、水稻恶苗病菌都有一定的抑制活性,尤其对花生褐斑病菌、苹果轮纹病菌、小麦纹枯病菌的抑制效果较好,进一步研究正在进行.
