基于ICP-AES的不同产地干姜无机元素分析与评价
2020-12-10邹冬倩李鹏辉濮宗进周桂生黄胜良
邹冬倩,严 辉,*,李鹏辉,濮宗进,周桂生,郭 盛,杨 健,黄胜良
(1.南京中医药大学,江苏省中药资源产业化过程协同创新中心,国家中医药管理局中药资源循环利用重点研究室,江苏南京 210023;2.中国中医科学院中药资源中心,道地药材国家重点实验室培育基地,北京 100700;3.江苏融昱药业有限公司,江苏淮安 223001)
干姜(ZingiberisRhizoma)为姜科植物姜ZingiberofficinaleRosc.的干燥根茎,冬季采挖,除去须根和泥沙,晒干或低温干燥[1]。干姜始载于《神农本草经》,具有温中散寒、回阳通脉、温肺化饮的功效,临床上常用于脘腹冷痛、呕吐泄泻、肢冷脉微、寒饮喘咳等症[2-4]。干姜中的有效成分包括6-姜酚、8-姜酚、10-姜酚、姜烯酚及姜酮等酚类成分[5],以及姜醇、姜烯等挥发性成分[6]。现代药理研究表明,干姜具有抗炎、抗菌、抗氧化、抗肿瘤、保肝等作用[7-9]。
姜作为药食两用的中药,在中国已经有2000多年的食用历史,《论语》记载,孔子有“不撤姜食,不多食”之句。中国是姜的发源地之一,也是最早种植姜的国家。姜,适宜温暖湿润气候,不耐高温和强光,适宜土质肥沃、土层深厚、透气性好的沙壤土、壤土或粘壤土,这些生长特性决定了姜的分布产区[10-11]。除东北、西北等高寒地区以外,姜在全国各地均有分布,主产于四川、云南、贵州、广西、山东、湖南等地[12]。不同的地理生态环境,其无机元素的组成也同样存在差异[13-15]。随着研究的深入,发现土壤中的无机元素能够影响药用植物次生代谢产物的积累,进一步影响着药材的质量[16-17]。目前,关于干姜中的有效成分含量以及指纹图谱研究较多[18-20],但是针对不同产地的干姜中无机元素的组成研究不够充分[21-22]。而重金属元素也已成为公认的对人体有害的元素[23],同时值得关注的是,目前国内干姜主要产区多属于重金属土壤背景值较高的区域,具有潜在的重金属超标风险,因此对干姜药材中无机元素的组成规律的研究极为重要。
现今,关于中药中的无机元素的测定方法主要为石墨炉原子吸收法(GFAAS)、原子吸收分光光度法(AAS)、火焰原子吸收光谱法(FAAS)、电感耦合等离子体原子发射光谱法(ICP-AES),而ICP-AES是目前多元素测定最先进、最准确的技术手段[24],已广泛应用于食品、药品中的无机元素的检测[25-26]。ICP-AES能够检测光学光谱(165~800 nm),可以同时检测原子光谱中的多条谱线,并且能够同时检测多种原子和离子,ICP-AES的检测限较低,重现性较好,仪器的分析速度较快[27],因此采用ICP-AES法能够快速、准确地分析干姜中无机元素的组成。
本研究主要采用ICP-AES法对来自云南、四川、贵州、山东等地的干姜样品中无机元素含量进行测定,采用聚类分析和主成分分析对不同产地的样品进行化学计量学分析,以期分析不同产地样品的差异。对去皮与不去皮的样品中重金属元素的含量作比较,为干姜药材的产地加工提供理论依据。
1 材料与方法
1.1 材料与仪器
Al、As、B、Ba、Be、Cd、Co、Cr、Cu、Fe、Ga、Li、Mg、Mn、Ni、Pb、Sb、Sn、Sr、Ti、Tl、V、Zn(GSB 04-1767-2004),Na、P、K(GSB 04-1764-2004),In、Ge、Bi、Rh、Sc、Tb、Y(GSB 04-2826-2011),Hg(GSB 04-1728-2004) 国家有色金属及电子材料分析测试中心;硝酸(优级纯) 德国默克公司;去离子水 屈臣氏蒸馏水;28批干姜药材 经南京中医药大学严辉副教授鉴定为姜科(Zingiberaceae)植物姜(ZingiberofficinaleRosc.)的干燥根茎,标本存放于南京中医药大学标本馆。干姜样品采集于2017年4~6月,置于干燥阴凉密封罐中保存,干姜样品包含不同规格等级,以及相同规格等级的不同批次样品,其中S9与S11为不同批次的低硫母姜,S12、S15与S20为不同批次的高硫小黄姜,S17与S18为不同批次的低硫姜片,S23与S24为不同批次的低硫未去皮小黄姜,S27与S28为不同批次的低硫去皮小黄姜,详细信息见表1。
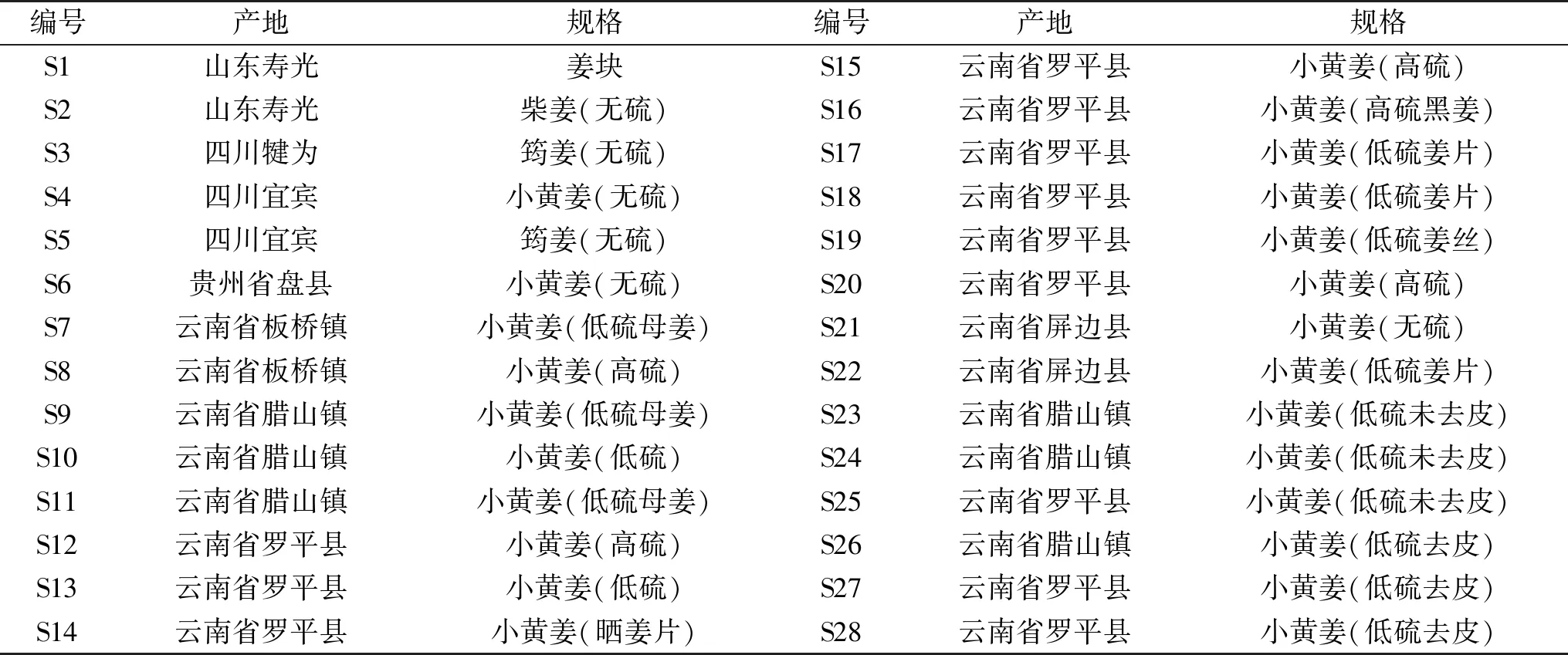
表1 28批不同产地干姜样品信息表
OptimaTM2100 DV电感耦合等离子体发射光谱仪 美国Perkin Elmer公司;HH-S6数显恒温水浴锅 巩义市予华仪器有限责任公司;Sartorius BT 125D十万分之一电子天平 北京赛多利斯仪器系统有限公司;SAGA-10TY超纯水器 南京易普易达科技发展有限公司;BJ-150高速多功能粉碎机 浙江德清拜杰电器有限公司;D2012高速台式离心机 大龙兴创实验仪器北京有限公司。
1.2 实验方法
1.2.1 供试品溶液制备 取干姜样品粉末(过3号筛)0.5 g,精密称定,置于50 mL塑料离心管中,加浓硝酸7 mL,放置于80 ℃水浴锅中,消解2 h。待溶液澄清透明或略带黄色时,消解完毕后,冷却至室温,用去离子水定容至50 mL,离心(13000 r/min,10 min),取上清液[28]。
1.2.2 对照品溶液制备 分别取多元素标准溶液,精密量取,用3% HNO3稀释,配制成适宜浓度的混合标准溶液,见表2。标准溶液中Li、Be、B、Tl、Pb、Na、Mg、Al、P、K、Sc、Ti、V、Cr、Mn、Fe、Co、Ni、Cu、Zn、Ga、As、Sr、Y、Rh、Cd、Sn、Sb、Ba、Tb浓度均为200 μg/L,Bi为400 μg/L,Hg为5 μg/L。随机选取一个样品测定其Ge、In等元素的响应信号(CPS),选择信号较低的并且原子质量与被测元素接近的元素作为内标。最终选择Ge 74和In 115作为内标。

表2 32种无机元素线性回归方程、相关系数、线性范围
1.2.3 仪器参数 等离子体射频功率1100 W,冷却气体流量15 L/min,辅助气流量0.94 mL/min,载气流量3.0 mL/min,观测方向为Axial,观测高度为15 nm,一次读数时间为5 s,进样延时30 s,泵速为15 r/min,样品提升速度1.0 mL/min,采样深度8 mm,分析模式采用全定量模式[29-31]。
1.2.4 标准曲线的制备 将标准品溶液逐级稀释,以3% HNO3为空白溶液,以Ge和In为内标,以元素浓度C(μg/L)作为横坐标(X),信号强度(CPS)作为纵坐标(Y),制作各元素的标准曲线。得到各无机元素的回归方程如表2所示,其中Li、Be、B、Tl、Pb、Al、Sc、Ti、V、Cr、Mn、Co、Ni、Cu、Zn、Ga、As、Sr、Y、Rh、Cd、Sn、Sb、Ba、Tb的回归方程的相关系数r>0.999。
1.3 数据处理
将28批干姜样品的32种无机元素含量作为变量,将测定数据导入SIMCA-P 14.0软件,进行主成分分析(PCA)和聚类分析(CA)。
2 结果与分析
2.1 方法学考察
2.1.1 精密度试验 将混合标准溶液,按上述方法连续重复测定6次,各元素含量的RSD在1.52%~4.96%,表明仪器精密度良好。

表3 28批不同产地干姜样品中32种无机元素含量(mg/kg)

续表
2.1.2 重复性试验 平行制备6份供试品溶液,按上述方法测定,各元素含量的RSD在2.46%~3.59%,表明仪器重复性良好。
2.1.3 稳定性试验 取供试品溶液,按上述方法测定,分别于0、1、2、4、6、8、12 h测定,各元素含量的RSD<4.59%,表明溶液在12 h内稳定。
2.1.4 加样回收率试验 精密称取样品S1样品,分别加入等量S1样品中各元素含量的对照品,平行3份,按上述方法测定,加样回收率为96.69%~112.22%,RSD<4.10%,说明该方法准确可靠。
2.2 样品测定结果
取28批样品,照1.2.1项下方法制备供试品溶液,按照1.2.3项下仪器参数上机测定,结果见表3。28批干姜样品中共检测到32种元素,其中Rh、Tb、Sb未检出,仅贵州盘县的样品检测出Tl、Sn,其他样品均未检测到这两种元素。干姜中含量较高的元素为K、P、Mg、Na、Mn含量范围分别为22587.83~92248.51、1778.29~4449.33、1848.98~4293.83、39.72~1216.93、79.16~3864.6 mg/kg。除Mn以外,还含有微量元素Fe(27.84~960.26 mg/kg)、Zn(14.3~55.45 mg/kg)。重金属元素Pb(0.21~1.93 mg/kg)、Cd(0.02~0.50 mg/kg)、As(<1.01 mg/kg)、Hg(<6.19 mg/kg)、Cu(2.40~7.96 mg/kg)。
2.3 不同产地干姜无机元素分析
2.3.1 聚类分析 在聚类分析谱系图中,纵坐标为距离,横坐标为样品编号,在距离为200时,所有的干姜样品被划分为两类,一类是来自山东省的样品,另一类是来自四川省、云南省、贵州省的样品。山东地区的样品与其他地区的样品无机元素组成差异大,而西南地区贵州、云南、四川的干姜无机元素组成相似,可能是由于地理环境的因素影响了干姜中无机元素的积累。

图1 28批干姜聚类分析谱系图
2.3.2 主成分分析 两个主成分的贡献率分别为PC1=0.903,PC2=0.023,分析发现来自四川、云南、贵州的样品较好地聚集为一类,来自山东的样品聚为一类。因此,四川、云南、贵州地区所产的干姜在无机元素的组成上较为相似,而山东地区所产的干姜与它们的差异较大。其中K、Na、P、Mg、Mn是对分类影响较大的几种变量。上述几种元素为干姜中含量较高的几种元素,其含量的变化对分类结果有较大的影响,主成分分析结果与聚类分析结果具有一致性。
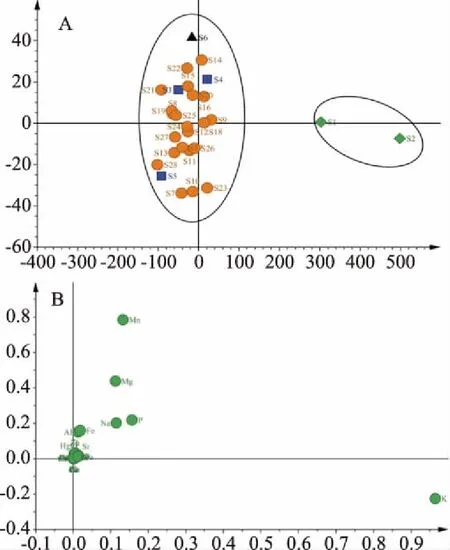
图2 28批干姜样品主成分得分图(A)与Loading-plot图(B)
2.4 云南干姜无机元素分析
2.4.1 云南干姜无机元素组成分析 根据干姜药材的本草考证研究结果,目前干姜的道地药材产区集中在云南的罗平、师宗。四川的犍为、沐川,贵州的六盘水等地,其中以云南地区为干姜药材(小黄姜)的主产区。因此,以云南省样品的各无机元素含量的平均值作为变量,分析云南省干姜的无机元素组成,所测的32种无机元素,K、P和Mg分别占84.22%、7.01%和6.98%,而Mn、Na、Fe和Al分别占0.70%、0.53%、0.20%和0.20%。

图3 云南干姜无机元素占比分析
2.4.2 云南未去皮干姜与去皮干姜无机元素含量对比 通过对未去皮干姜样品(S23、S24、S25)以及去皮的干姜样品(S26、S27、S28)中的重金属元素含量对比发现,其中Hg、Pb、As、Cd的含量在去皮样品中显著低于未去皮的样品,Cu含量在干姜去皮之后也呈现下降趋势。因此,干姜经过去皮处理之后,重金属及有害元素的含量下降,可能与姜皮对重金属元素的富集作用有关。目前,在四川犍为、云南等干姜主要产区同样发现去皮之后的干姜中重金属元素含量显著降低。而去皮之后干姜中的指标性化学成分含量与去皮之前并无显著性差异。去皮后干姜中挥发油、总酚含量均无显著变化,且去皮后能够降低干燥时间,降低干燥过程中的能源消耗,更有利于实际生产[32]。

图4 云南未去皮干姜与去皮干姜重金属元素含量比较
3 讨论与结论
28批干姜样品中,含量相对较高的元素有K、P、Mg、Mn、Na、Fe和Zn,其中以K、P含量最高。K平均含量高达34674 mg/kg,它是维持酸碱平衡,参与能量代谢以及维持神经肌肉的正常功能的重要元素;P平均含量高达2721 mg/kg,它是组成生命的重要物质,参与代谢过程和酸碱平衡的调节;干姜中同样含有较多人体所需的微量元素,如Fe、Zn、Mn等,因此干姜的营养价值也较高,具备进一步开发功能性食品的潜力。
《中国药典》2015版中对重金属含量一般要求为[1]:Pb≤5.0 mg/kg、Cd≤0.3 mg/kg、Hg≤0.2 mg/kg、Cu≤20.0 mg/kg、As≤2.0 mg/kg,但对干姜的重金属含量并无具体限定要求。《药用植物及制剂进出口绿色行业标准》[15]规定重金属总量应≤20.0 mg/kg,Cu≤ 20.0 mg/kg,Hg≤0. 2 mg/kg,Pb≤5.0 mg/kg,Cd≤0.3 mg/kg,As≤2.0 mg/kg。结合测定结果,Pb(0.21~1.93 mg/kg)、Cd(0.02~0.5 mg/kg)、As(<1.01 mg/kg)、Hg(<6.19 mg/kg)、Cu(2.4~7.96 mg/kg)。根据上述两种标准,所有样品中Pb、As、Cu均符合上述标准,样品S1~S4、S6~S8、S10、S12、S14~S16、S20~S25、S28中Hg含量超出标准,样品S1、S6、S9、S20~S25中Cd含量超出标准。干姜药材在经过去皮处理之后,重金属元素含量显著降低,各元素含量低于限定标准,能够增加药材的合格率。张利敏等[21]采用火焰原子吸收光谱法测定干姜中Cd含量为0.53 mg/kg,蒋云福等[33]采用火焰原子吸收分光光度法测定Cd含量为4.95 mg/kg,说明干姜中Cd元素含量相对较高,可能与西南地区的土壤具有一定的关联性。Hg含量较高,但波动较大,可能与Hg的记忆效应相关,在无任何消除汞记忆效应的措施下,0.5 μg/L的Hg即可产生明显的记忆效应,且随着Hg浓度的增加,记忆效应不断增强[34],在实验过程中并未采取消除Hg记忆效应的相关措施,可能导致样品测定结果波动较大。
本试验利用ICP-AES建立了干姜中32种无机元素的测定方法,分析了干姜中无机元素的组成。相关结果可为基于土壤无机元素特征的干姜药材质量溯源及品质评价研究提供参考。同时,干姜药材在产地加工时,进行去皮处理,既有利于降低重金属及有害元素的含量,也有利于缩短干燥时间,节约成本,同时也能为干姜的产地加工方式优化及食品开发应用提供一定的理论依据。
