肝硬化患者自发性门体分流发生率及预后分析
2020-10-22王涛李木松韩秋然李彩虹孙静伟
王涛 李木松 韩秋然 李彩虹 孙静伟
自发性门体间分流表现为在病理状态下,门脉循环与体循环系统之间的分支重新开放,大量新生毛细血管在门体间形成[1]。门静脉高压是肝硬化患者常见症状,主要是由于肝硬化患者门静脉各支血管内血流阻力增大、门体间侧支循环自发形成[2]。肝性脑病是肝硬化门脉高压并发症之一[3]。目前自发性门体分流在门静脉高压的肝硬化患者中并未有明确诊治指南[4]。封堵自发性门体分流、使分流入体循环的血液重新回归至门静脉是目前的主要治疗方式,但单纯封堵无法降门脉高压。经颈静脉肝内门体分流术(Transjugular intrahepatic portal shunt,TIPS)是一种介入栓塞微创手术,可有效降低门静脉高压[5]。因此本研究对肝硬化门静脉高压合并自发性门体分流患者在封堵自发性门体分流基础上给予TIPS手术联合治疗,分析患者预后情况。
资料与方法
一、病例资料
选择我院2017年3月—2018年10月接收的肝硬化伴门脉高压患者220例。纳入标准:①经腹部增强计算机断层扫描检查显示肝硬化、门脉高压;②符合肝硬化门脉高压诊治指南[6];③Child-Pugh分级B、C级[7];④入组前未接受过任何降低门静脉高压手术,未合并急性静脉曲张出血。排除标准:①合并凝血功能障碍、肝功能不全;②门静脉、肝动脉血管畸形;③合并心力衰竭、肺动脉高压及胆红素>3 mg/dL;④妊娠及哺乳期妇女;⑤合并肝癌及其他恶性肿瘤。本研究获医院伦理委员会批准,所有患者自愿签署知情同意书。
二、方法
联合手术方法:取仰卧位,给予所有患者2%利多卡因局部麻醉,首先经右侧股动脉穿刺,在正侧位行门静脉造影,通过造影结果观察门静脉、分流道、静脉曲张等情况。再让患者暴露右颈部,同样局部麻醉后经颈静脉穿刺,将Rups 100穿刺系统导入肝静脉入下腔静脉出口处,调零压力传感器,检测下腔静脉压,在门静脉左右支同时穿刺,于正侧位进行门静脉造影,测定门静脉压,以门静脉压力梯度=(门静脉压-下腔静脉压)值表示门静脉压力,观察门体分流情况及胃静脉曲张。(若造影结果显示不存在门体分流道,则表示该患者未伴有自发性分体分流,直接行TIPS)。存在门体分流道患者,通过造影结果分析门体分流类型是属于脾肾分流、脐静脉再通分流或其他类型,并根据门体分流道大小,对门体分流道使用弹簧钢圈、血管硬化剂或Amplatzer封堵器进行封堵。封堵完成后,再进行一次门静脉造影,若未见门体分流道,则置入血管Fluency支架建立人工分流道,支架大小:直径8 mm、10 mm,长60~100 mm,支架置入完成后再进行一次门静脉造影,测定门静脉压。所有患者进行1年术后随访。
三、观察指标
①所有患者自发性门体分流的发生情况;②术前、术后合并自发性门体分流患者门静脉压力梯度变化;③合并自发性门体分流患者术后1月、3月、6月、1年并发症发生情况、支架畅通率,并发症包括肝性脑病、腹水、上消化道出血,支架畅通情况以支架功能是否障碍表示,支架功能障碍判断方法:术后并发静脉曲张出血、腹水、超声提示支架内无血流信号、门静脉造影提示支架狭窄超过50%;④合并与未合并自发性门体分流患者术前一般资料及与术后1年内发生肝性脑病有关的多因素分析;⑤合并与未合并自发性门体分流患者术后1年内死亡情况。
四、统计学方法
采用SPSS 22.0软件分析数据,计量资料采用t检验,计数资料采用χ2检验。多因素采用logistic回归分析,患者1年内生存情况采用Kaplan-Meier生存曲线分析。以P<0.05为差异有统计学意义。
结 果
一、所有患者自发性门体分流的发生情况
所有肝硬化门静脉高压患者中有85例38.64%(85/220)合并自发性门体分流,其中脾肾分流患者37例43.53%(37/85)、脐静脉再通分流32例37.65%(32/85)、其他分流16例18.82%(16/85)。其他分流类型包括血栓性门静脉分流、门静脉右肾静脉分流、胆囊静脉曲张分流等。
二、术前、术后合并自发性门体分流患者门静脉压力梯度变化
术后85例合并自发性门体分流患者门静脉压力梯度(12.17±3.26)明显低于术前(35.43±6.71)(P<0.05)。
三、合并自发性门体分流患者术后1月、3月、6月、1年并发症发生率、支架畅通率
术后肝性脑病、腹水、上消化道出血的累积发生率随时间推移呈上升趋势,术后1年内肝性脑病累积发生率为32.41%(28/85)、腹水为36.47%(31/85)、上消化道出血为23.53%(20/85);术后支架畅通率降低,在术后1年内降至78.82%(67/85),表示术后1年内有18例患者支架功能发生障碍,67例患者支架功能未发生障碍,见表1。

表1 合并自发性门体分流患者术后1月、3月、6月、1年并发症发生率、支架畅通率(例)
四、合并与未合并自发性门体分流患者一般资料、术后肝性脑病发生率及多因素分析
合并自发性门体分流患者术前门静脉压力梯度高于未合并自发性门体分流患者(P<0.05);合并自发性门体分流患者中术前有肝性脑病病史的占比49.41%(42/85)高于未合并自发性门体分流患者22.96%(31/135)(P<0.05);合并自发性门体分流患者术后1年内肝性脑病累积发生率32.41%(28/85)与未合并自发性门体分流患者21.48%(29/135)比较无显著差异(P>0.05),见表2。
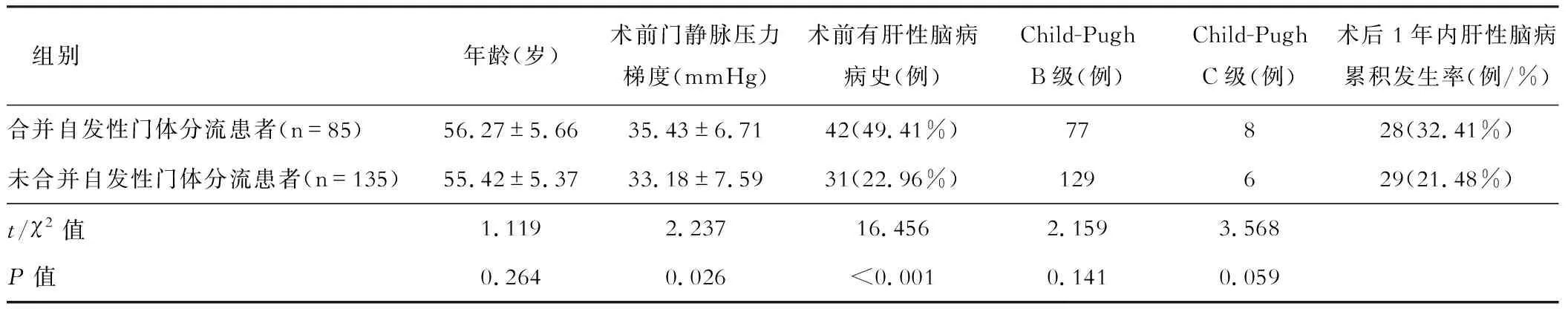
表2 合并与未合并自发性门体分流患者一般资料及术后1年肝性脑病发生率
将表2中P<0.05的指标纳入多因素分析,显示术前有肝性脑病病史是合并自发性门体分流的肝硬化门脉高压患者TIPS手术后1年内发生肝性脑病的独立危险因素(P<0.05),见表3。

表3 术后1年内发生肝性脑病的多因素分析
五、合并与未合并自发性门体分流患者术后1年内死亡情况
两组术后1年内死亡率比较无明显差异(P>0.05)。本研究随访1年中,合并自发性门体分流患者在术后1月未发现死亡,术后3月死亡3例,术后6月时死亡3例,术后1年时死亡5例;未合并自发性门体分流患者在术后1月死亡1例,术后3月死亡5例,术后6月死亡3例,术后1年死亡7例。
讨 论
肝硬化患者肝脏内血液循环系统障碍是临床主要病理特征之一,血流动力学紊乱会导致肝脏血管内形成血栓[8]。肝硬化患者肝脏内血管分布容易形成杂乱无序的分布状态,肝静脉、门静脉间形成大量侧支循环,即门体分流道[9]。自发性门体分流主要是由于门静脉高压造成的[10],这一症状会导致肝脏血液灌注量降低,继而出现肝脾肿大、腹水,甚至静脉破裂[11]。自发性门体分流常在门静脉高压手术时被发现,对分流道进行封堵是常用方法。
封堵方法可分为单纯应用海绵、弹簧钢圈或封堵器等进行封堵,球囊导管逆行性静脉栓塞手术、TIPS联合封堵[12]。球囊导管逆行性静脉栓塞手术是通过封堵胃底静脉曲张及门体分流道,达到治疗目的。此方法封堵后虽然降低了分流道侧支循环量,但同时也会使门静脉压力进一步升高,患者门脉高压情况仍未得到改善。TIPS是临床应用较广的降门脉高压方法,其适应证较广[13]。但TIPS术后可能并发肝性脑病,易致预后不良[14]。
本研究结果发现纳入的220例患者中合并自发性门体分流的有85例38.64%,与武文彬等的报道一致[15]。合并自发性门体分流患者的术后门静脉压力梯度明显低于术前,表示接受TIPS联合封堵治疗可有效降低患者的门静脉压力。随访1年发现,合并自发性门体分流患者术后随着时间延长肝性脑病、腹水、上消化道出血的累积发生率增加,术后1年时分别为32.41%、36.47%、23.53%,支架畅通率在术后1年时降至78.82%。未出现其他明显并发症。术后1年经合并与未合并自发性门体分流患者死亡率差异不大,并且两组中多数患者是因肝硬化本身处于Child-Pugh C级,死于肝功能衰竭,死于术后严重肝性脑病并发症的仅1例。表明虽然TIPS术后存在肝性脑病等并发症,但对患者死亡的影响较小。另外,合并自发性门体分流患者术后1年内肝性脑病累积发生率较高,但与未合并患者比较无显著差异,这表示给予TIPS联合封堵治疗不会使自发性门体分流患者肝性脑病发生率异常升高。多因素结果中术后肝性脑病与术前肝性脑病病史有关,与其他因素未体现明显关系,进一步表明在单纯封堵基础上增加TIPS治疗不会显著提高肝性脑病发病率,具有一定安全性。
综上所述,本研究中自发性门体分流发生率为38.64%,应用TIPS联合封堵,可能引起术后肝性脑病,但对术后死亡影响不大,且仅与术前肝性脑病病史有关,因此TIPS联合封堵法具有一定安全性。本研究所有患者术中均进行TIPS手术降门脉高压,未单纯使用封堵治疗自发性门体分流,避免了因仅行单纯封堵导致持续性门脉高压。但也无法得到单纯封堵与TIPS联合封堵的对比疗效,后续可通过回顾分析纳入更多合并自发性分流患者,探究不同封堵方法对患者肝性脑病发生率及预后的影响。
