评价含银敷料中银离子释放的体外创面模型的建立
2020-10-15
1 山东省医疗器械产品质量检验中心 (山东 济南 250101)
2 山东省药学科学院 (山东 济南 250101)
内容提要: 本文建立的含银敷料银离子释放体外创面模型,可模拟不同伤口创面类型。通过测量含银敷料与模拟伤口渗出液接触后,不同时间点内定量测定的银离子释放量及释放曲线的体外试验,科学直观地反映出敷料产品中释放的银离子有效成分、及累积离子量。通过动态测定含银敷料模拟临床使用状态下银离子的释放量,银离子的释放量直接反映了敷料的抗菌性能,因此本模型可有效评价含银敷料的安全性和有效性。
创面也称为伤口或者创伤,是正常皮肤(组织)在外界致伤因素或人体内在因素等作用下导致的损害,常伴有皮肤和人体组织损伤和连续性破坏完整性的破坏。根据愈合过程,可分为急性创面(切割伤、手术创面等)和慢性创面(如糖尿病溃疡、静脉性小腿溃疡等)。伤口感染是造成伤口延迟不愈的一个重要原因。创面的正确处理是外科手术治疗成败的关键, 而创面良好的愈合是创伤后人体功能康复的前提。加快创面愈合的研究中,对创面敷料的开发研制尤其重要。
敷料是覆盖于创面,为创面提供机械保护屏障,用于吸收或引流伤口分泌物的材料,其通过控制创面的微生物环境,直接或间接促进伤口愈合。医用敷料种类繁多,除传统的纱布、棉垫敷料等,近年来随着对“湿润伤口愈合”理论的认可,各类合成敷料、生物敷料等多种功能化、多样化的新型敷料得到广泛应用,如各类泡沫敷料、藻酸盐敷料。其中含银敷料由于其释放的银离子产生抗菌作用,具有良好的抗感染、促进伤口愈合功效,已在国内得到广泛临床应用。
1.含银敷料银离子释放模型的构建及应用
含银敷料以敷料为主,一般通过物理吸附或离子交换作用等方法,将含银物质负载于敷料基材。含银敷料吸收伤口渗出液后,释放银离子杀灭细菌、真菌及其他病原体,而获得抗菌性。理想的银离子释放应该是匀速、持续的。敷料基材的材料、组成及结构型式,含银物质的化学结构、含银量及其在基材中分布的均匀性,决定银离子释放量、释放速率及释放曲线,这些因素将影响银离子在体内吸收及分布代谢,反映含银敷料抗菌性能有效作用程度。因此怎样科学有效设计以上影响因素,对评价含银敷料抗菌性至关重要。
可通过体内和体外试验评价含银敷料的抗菌机制和有效性。体内试验如临床评价及动物试验,这两种方法成本高,周期长,且因试验对象的个体原因及创面差异等因素,重复性差,不能进行客观有效的结论。
本文建立的含银敷料银离子释放模型,目的是用来评价作为释放银离子的供体(即含银敷料)持续向模拟创面的“接受介质”释放银离子的情况。临床创面类型的多种多样,创面渗出液有少量、中量和大量,为充分模拟创面实际情况,本文建立了两类模型,即:饱和状态下评价模型(适用于大量渗出液的创面)和不饱和状态下评价模型(适用于少量、中良渗出液的创面)。
1.1 饱和状态下的评价模型(模型1)
模型1适用于有大量渗出液时伤口创面,是评价敷料吸收创面渗液后处在达到吸收饱和状态(即湿态下)的银离子释放的模型,可最大程度模拟临床创面实际状态。模型基本结构见图1。
1.1.1 敷料预湿
试验前将供试含银敷料裁剪成适宜大小的圆形(如图1所示),放入试验杯体前,用试验液将敷料进行预湿处理。预显敷料一是使其处于模拟伤口环境,二是使试验时不同敷料下的试验液的量保持一致。
预湿时加液量的确定:取3片敷料,分别称重,放入带37°C水的烧杯中,37°C干燥箱中保持30min,使其吸收水至饱和,用镊子夹住一角,悬垂30s,再称重,两次称重之差是该敷料的最大液体吸收量。
预湿水平的确定:试验前根据不同试验目的,及敷料适用伤口类型,用敷料的最大液体吸收量算出不同湿度程度(如75%, 50% 和 25%),向试样上加预期量的试验液。试验结果表明,预湿程度越高,银离子释放量也越高。
1.1.2 应用试验
试验温度:35°C,模拟人体伤口创面温度。
试验时,敷料创面接触面向下放入试验杯内开孔处,盖上压块,使敷料不会漂浮,并使敷料与培养基之间无气隔。从加液孔加入适量试验液,试验液离子含量相当于人体血清或创面渗出液(氯化钠和氯化钙的溶液,含142mmoL钠离子和2.5mmoL钙离子)。
根据不同试验目的,制备试样,设置不同的试验时间,如1h、2h、3h、4h、8h、12h、24h、48h等。在不同时间点取出试验液,消解处理后,用原子吸收法(AAS)测定试验液中释放出的银离子浓度。
1.2 不饱和状态下的评价模型(模型2)
模型2适用于有少量、中量渗出液的伤口创面,是评价敷料吸收创面渗液后处在未饱和状态下(即干态或半干态)的银离子释放的模型。通过建立一个创面模型,即一种模拟创面的纤维蛋白凝块,用于评价敷料与创面的接触,可最大程度模拟临床创面的实际状态。模型基本结构见图2。应用试验如下。
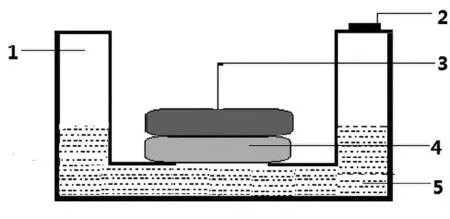
图1. 饱和状态下的评价模型1示意图(注:1.试验杯,可多次使用,用前在70%酒精振摇清洗,干燥至少1h;2.加液孔,带盖板,可取下添加试验液,试验时密闭防止液体挥发;3.压块,50mm×50mm×5mm的不锈钢块,重量约为98g;4.含银敷料;5.试验液。)
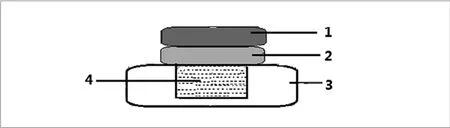
图2. 不饱和状态下的评价模型2示意图(注:1.压块,50mm×50mm×5mm的不锈钢块,重量约为98g;2.含银敷料;3.培养盘:直径为40mm,材质为聚甲醛或聚苯乙烯,内部开孔(孔径20mm,深度3mm),形成腔体积约为1mL的有底的盘形物;4.模拟创面。)
模拟创面:取纤维蛋白原3g,加入到牛血清白蛋白(BSA)磷酸盐缓冲液中,使纤维蛋白原浓度为30mg/mL,再取该溶液10mL,分别加入到培养盘中,然后各加入凝血酶1mL,迅速混匀。将混合物置(37±2)°C下1h,然后室温冷却 1h,使纤维蛋白凝块形成并凝固,即形成模拟创面。
如图2所示,将敷料放在培养盘内形成的模拟创面上,加压块,放入一个封闭容器中。
如需要,将敷料预湿(同1.1.1)。根据不同的试验目的,待敷料与模拟创面接触一定时间后,如1h、2h、3h、4h、8h、12h、24h、48h等,更换新的模拟创面,消解被更换下的模拟创面,用原子吸收法(AAS)测定试验液中释放出的银离子浓度。
1.3 结果表述
以不同时间点内定量测定的银离子释放量为横坐标,时间为纵坐标,可以得出含银敷料银离子体外试验释放曲线(见图3)。
2.模型的作用及意义
本文建立的两个不同状态下的体外试验模型,可分别模拟临床中不同类型的创面类型,最大程度模拟伤口渗出液量少量及大量的不同状态,最接近临床上含银敷料中银离子的实际释放情况。
通过该模型试验得出含银敷料银离子体外试验释放曲线,能科学直观反映出敷料产品中释放的银离子有效成分、累积离子量,可动态评价敷料模拟临床不同使用时期银离子的释放量,从而反映出含银敷料的抗菌性能,并由此可有效评价含银敷料的安全性和有效性。通过模型应用试验可以得出对含银敷料的抗菌功能的客观评价结论:①敷料产品声称的银离子含量与释放量没有相关性,即与抗菌性能的高低没有相关性;②不同敷料中银离子的释放量与抗菌性能有相关性,释放量越高,表明抗菌性能越好。

图3. 银离子体外试验释放曲线示例
评价含银敷料中银离子释放的体外模型,尤其适用于敷料开发研制阶段,在敷料基材的选择,含银物质的化学结构、添加量,与基材作用方式及其分布的均匀性等方面,都可使用本模型进行比较试验,根据预期值合理调整工艺及产品组份配方。同时也适用于不同含银敷料产品间的抗菌性能进行横向比较。
与动物体内试验或临床患者试验相比较,银离子释放体外模型克服了动物体内试验客观影响因素多,重复性差,成本高且不能定量评价等诸多不利因素。评价成本低、试验周期短、重复性好、数据结果直观、清晰,具有较好的经济性和适用性。
