分散液液微萃取-气相色谱串联质谱联用法测定生物样品中艾司西酞普兰
2020-10-12
(山西医科大学法医学院,山西 晋中 030600)
艾司西酞普兰(escitalopram)是丹麦Lunbeck公司研发的5-羟色胺再摄取抑制药,于2002年在瑞典上市,为消旋体西酞普兰的S-对映异构体,是新一代抗抑郁药[1],有研究[2-3]报道其不仅抗抑郁作用显著,而且具有较好的抗焦虑作用,因此被临床上广泛用于治疗抑郁症,其化学结构见图1。由于抑郁症患者本身就可能出现自伤、自杀或产生自杀企图,在使用此类药物治疗期间自杀事件时有发生。因此,中毒生物检材中艾司西酞普兰的检测尤为重要,不仅可在企图自杀事件中为临床抢救治疗提供合理方案,也可在中毒案件中为法医侦破案件提供充分的证据,有必要对其建立高灵敏度、高准确度、方便、高效的检测方法。

图1 艾司西酞普兰的化学结构Fig.1 Chemical structure of escitalopram
目前,艾司西酞普兰的检测方法主要有高效液相色谱法(high performance liquid chromatography,HPLC)[4]、高效液相色谱-串联质谱法(high performance liquid chromatography-tandem mass spectrometry,HPLC-MS/MS)[5]和气相色谱-串联质谱法(gas chromatography-tandem mass spectrometry,GC-MS/MS)[6]。生物检材中艾司西酞普兰的样品前处理过程中常采用液液萃取,此法耗时,需要大量有机溶剂,也有采用固相萃取手段,但成本较高,操作繁琐[7-9]。而离子液体分散液相微萃取是基于离子液体、分散剂和水的三元混合体系的样品前处理方法,富集效率高、快速简便,是一种环境友好和安全的萃取技术,被越来越广泛地应用于样品前处理中[10-11]。由于离子液体对有机物和无机物的溶解度高、蒸汽压低,与许多有机溶剂不混溶,大大减少了有机溶剂的使用[7]。本研究采用离子液体作为新型萃取剂,拟建立一种简单、方便、节省有机溶剂、环境友好且萃取率较高的超声辅助离子液体-分散液液微萃取-GC-MS/MS联用法以检测生物样品中艾司西酞普兰。
1 材料与方法
1.1 主要仪器与试剂
7890B-7000C气相色谱-三重四极杆串联质谱仪(配有G4513A自动进样器,美国Agilent公司),VORTEX-GENIE 2旋涡混合器(美国Scientific Industries公司),Research® plus单道移液器(德国Eppendorf公司),SB-5200DTD超声波清洗机(宁波新芝生物科技股份有限公司),Neofuge15R高速冷冻离心机[力新仪器(上海)有限公司],Simplicity 185超纯水系统(美国Millipore公司)。
艾司西酞普兰标准品(99.9%,北京普天同创生物科技有限公司);1-丁基-3-甲基咪唑六氟磷酸盐([C4MIM][PF6])、1-己基-3-甲基咪唑六氟磷酸盐([C6MIM][PF6])、1-辛基-3-甲基咪唑六氟磷酸盐([C8MIM][PF6])纯度均为99%,购自中国科学院兰州化学物理研究所;甲醇、乙腈均为色谱纯,丙酮为分析纯,实验用水为超纯水。
1.2 样品制备方法
空白血液和肝组织样本均来自健康家兔(山西医科大学动物中心)。
分别精密量取50 μL质量浓度为10 μg/mL的艾司西酞普兰标准品、100 μL[C6MIM][PF6]离子液体、850μL超纯水,加入预先装有100μL血液(或0.1g肝组织匀浆)的1.5mL聚四氟乙烯尖底离心管中,涡旋30 s,后加入250 μL乙腈溶液,涡旋30 s。超声4 min后,置于4℃冷冻离心机中以1556×g离心5min,然后将微量进样器轻轻插入下层离子液体中央,将吸取的下层液体置于1.5mL离心管中,用乙腈按体积比为1∶10进行稀释,1μL进样,供GC-MS/MS检测。
1.3 仪器条件
色谱条件:HP-5MS UI毛细管柱(30m×0.25mm,0.25 μm);载气为氦气(纯度99.999%);流速1 mL/min;升温程序为初始温度100℃,保持1.50 min,以25℃/min升至280℃,保持5 min;分流进样,分流比1∶10;进样量1μL,扫描起始时间2min。
质谱条件:电子轰击(electron impact,EI)离子源,电离能量70eV,离子源温度230℃,接口温度250℃;质量扫描范围(m/z)30~500,溶剂延迟3min;采用多反应监测(multiple reaction monitoring,MRM)模式,所选择的母离子质荷比为324,子离子质荷比分别为86(定量离子)和58,碰撞能量分别为5.00、6.00eV。
1.4 方法学验证
本研究对所建立检测方法的选择性、线性、检出限(limit of detection,LOD)、定量限(limit of quantification,LOQ)、精密度、准确度、提取回收率和基质效应进行验证[12],并应用于实际案例。
选择性:取10份不同来源的空白血液和肝组织,按1.2节方法进行样品制备、1.3节方法进行样品分析。要求空白基质中含有的物质对待测物的检测没有干扰。
线性:取空白检材(血液100μL、肝组织0.1g)各6份,配制质量浓度为5.56、11.11、55.56、111.11、555.56和 1 111.10 ng/mL(或质量分数为 0.025、0.05、0.25、0.50、2.50和5.00mg/g)的艾司西酞普兰加标样品,每个浓度平行3次。然后按1.2节方法进行样品制备、1.3节方法进行样品分析。以艾司西酞普兰含量为横坐标,峰面积为纵坐标,建立线性回归方程。
LOD和LOQ:取空白检材(血液100 μL、肝组织0.1 g)各7份,分别添加不同质量浓度的艾司西酞普兰储备液,配制成质量浓度为2.00、4.00、6.00、8.00、10.00、12.00和14.00ng/mL的血液样品以及质量分数为 2.00、4.00、6.00、8.00、10.00、12.00 和 14.00 μg/g的肝组织样品。按1.2节方法进行样品制备、1.3节方法进行样品分析。以信噪比(S/N)≥3时的样品最低浓度为LOD,以S/N≥10时的样品最低浓度为LOQ。
精密度和准确度:取空白检材(血液100μL、肝组织0.1 g)若干份,配制成质量浓度为5.56、111.11和555.56 ng/mL(或质量分数为0.025、0.50和2.50 mg/g)的艾司西酞普兰加标样品,各重复6次,按照本研究建立的方法进行样品前处理和检测。另取若干份空白检材(血液100μL、肝组织0.1g)按照本研究建立的方法进行样品前处理后分别添加艾司西酞普兰储备液,分别得到质量浓度为5.56、111.11和555.56ng/mL(或质量分数为0.025、0.50和2.50 mg/g)的加标样品后进样,各重复6次。连续3d重复上述操作,分别得到日内和日间精密度[以相对标准偏差(relative standard deviation,RSD)表示]。精密度和准确度控制在15%以内可视为良好。
提取回收率和基质效应:取不同来源的生物样品(血液100 μL、肝组织0.1 g)若干份,配制成质量浓度为5.56和555.56 ng/mL(或质量分数为0.025和2.50mg/g)的艾司西酞普兰加标样品,各重复6次,按照本研究建立的方法进行样品前处理和检测。另取若干份不同来源的生物样品(血液100μL、肝组织0.1g)按照本研究建立的方法进行样品前处理后分别添加艾司西酞普兰储备液,分别得到质量浓度为5.56和555.56 ng/mL(或质量分数为0.025和2.50 mg/g)的加标样品后进样,各重复6次。提取回收率=不同来源的生物样品提取前添加一定浓度的艾司西酞普兰峰面积平均值/不同来源的生物样品提取后添加对应浓度的艾司西酞普兰峰面积平均值;基质效应=不同来源的生物样品基质提取后添加一定浓度的艾司西酞普兰峰面积平均值/配制对应浓度的艾司西酞普兰峰面积平均值。提取回收率应高于50%,基质效应在85%~115%视为良好。
2 结果与讨论
2.1 超声辅助离子液体-分散液液微萃取条件筛选
2.1.1 萃取剂类型的筛选
分散液液微萃取的关键在于萃取剂的选择,合适的萃取剂要满足以下要求:(1)与水不互溶且密度比水大,这样方便在离心管底部形成回收富集相;(2)对待测物有良好的溶解性,萃取回收率较高[9]。因此,本实验考察了[C4MIM][PF6]、[C6MIM][PF6]和[C8MIM][PF6]3种离子液体对艾司西酞普兰的萃取效率影响。结果表明,[C6MIM][PF6]与其他两种萃取剂相比,萃取效果更优,差异具有统计学意义(P<0.05)。因此,最终选择[C6MIM][PF6]为本研究的萃取剂。
2.1.2 萃取剂体积的筛选
本研究考察了80、100和120 μL的离子液体体积。结果表明:萃取剂体积为100 μL时与其他两种体积相比,萃取效率最高,差异具有统计学意义(P<0.05)。因此,选择萃取剂体积为100μL。
2.1.3 分散剂类型的筛选
分散剂既要与水和萃取剂互溶,又要与萃取剂和样品混合形成乳浊液,分散剂的好坏直接影响萃取效率的高低。本研究选取甲醇、乙腈和丙酮作为分散剂。结果表明:在血液样品中用乙腈作为分散剂与其他两种分散剂相比,效果最佳,差异具有统计学意义(P<0.05);在肝组织样品中3种分散剂差异无统计学意义。综合考虑,选择乙腈作为分散剂。
2.1.4 分散剂体积的筛选
分散剂的体积直接影响萃取剂与待测物形成的混浊体系,本研究选择体积为220、250和270μL的乙腈进行比较。结果表明:乙腈体积为250 μL时与其他两种体积相比,血液和肝组织中目标物响应最高,差异具有统计学意义(P<0.05),故选择分散剂乙腈的体积为250μL。
2.1.5 超声时间的选择
本研究考察了不同超声时间(4、6、8、10和12min)对萃取效率的影响。一般来说,超声时间越长,萃取剂与待测物接触越充分,萃取效率越高。但是随着超声时间的延长,反应体系温度会上升,萃取效率反而有所降低。结果表明:在血液样品中,超声时间为4min时与其他4种超声时间相比,效果最佳,差异具有统计学意义(P<0.05);在肝组织样品中,5种超声时间的差异无统计学意义。综合考虑,选择超声时间为4min。
2.1.6 酸碱性条件的影响
本研究目标物艾司西酞普兰属于弱碱性物质,在弱碱性环境中更容易被有机溶剂提取,因此选择pH值为9、10和11进行考察。结果表明:反应体系pH值为10时,血液和肝组织中艾司西酞普兰响应最高,且与其他两种pH值相比差异具有统计学意义(P<0.05)。因此,选择反应体系pH值为10。
2.1.7 盐含量的影响
通过向待测溶液中加入不同质量分数(0、2%、4%、6%和8%)的氯化钠溶液,考察盐含量对萃取效率的影响。结果表明,盐的加入量对萃取效果影响不大,所以本研究选择不加盐。
2.2 方法学验证
选择性:空白血液和肝组织的总离子流色谱图(total ion chromatogram,TIC)见图2,空白血液中添加艾司西酞普兰的MRM色谱图见图3,空白肝组织中添加艾司西酞普兰的MRM色谱图见图4。采用超声辅助离子液体-分散液液微萃取-GC-MS/MS检测艾司西酞普兰的方法专属性强、特异性好,血液和肝组织中内源性物质对艾司西酞普兰的检测没有干扰。
线性、LOD和LOQ:血液样品中艾司西酞普兰在5.56~1 111.10 ng/mL范围内线性关系良好,相关系数(r)大于0.999;肝组织样品中艾司西酞普兰在0.025~5.00 mg/g范围内线性关系良好,相关系数(r)均大于0.999。本方法的LOD和LOQ能够满足法医毒物分析实际检案的需要。详见表1。
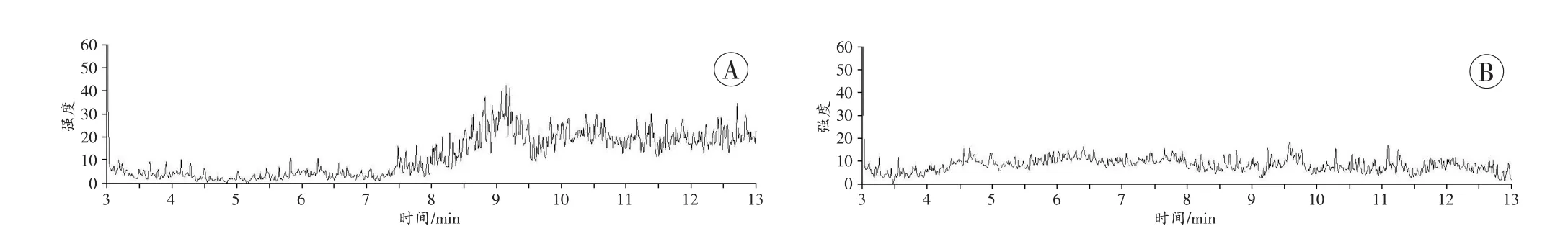
图2 空白血液和空白肝组织的TICFig.2 TIC of blank blood and blank liver
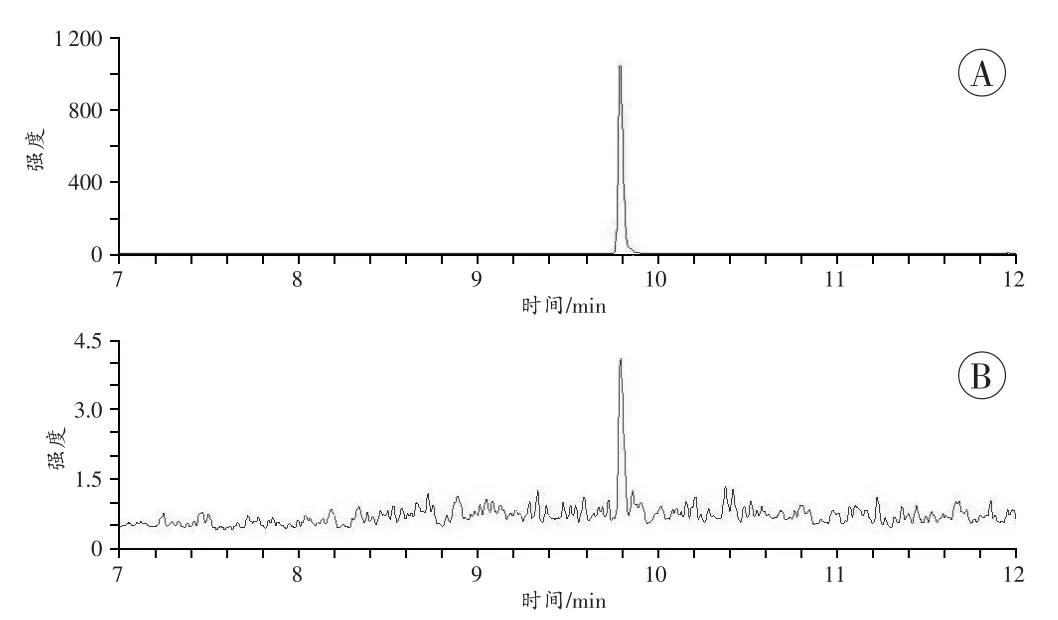
图3 空白血液中添加艾司西酞普兰的MRM色谱图Fig.3 MRM chromatogram of blood spiked with escitalopram

图4 空白肝组织中添加艾司西酞普兰的MRM色谱图Fig.4 MRM chromatogram of liver spiked with escitalopram

表1 艾司西酞普兰在血液和肝组织中的线性方程、LOD和LOQTab.1 Linear equation,LOD and LOQ of escitalopram in blood and liver
精密度及准确度:血液样品中艾司西酞普兰的日内精密度为12.66%~13.41%,日间精密度为14.01%~17.88%;肝组织样品中艾司西酞普兰的日内精密度为0.81%~1.00%,日间精密度为0.97%~1.41%。血液和肝组织样品的准确度均低于15%。详见表2~3。本研究中样品的精密度及准确度均符合方法学验证的要求。
提取回收率和基质效应:血液和肝组织样品中艾司西酞普兰的提取回收率均大于50%,基质效应在86.55%~114.90%(表2~3)。

表2 艾司西酞普兰在血液中的精密度、准确度、提取回收率及基质效应Tab.2 Precision,accuracy,extraction recovery rates and matrix effects of escitalopram in blood (%)
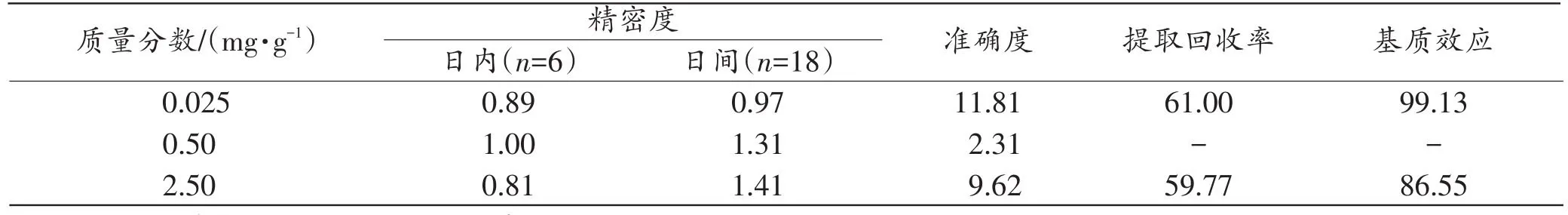
表3 艾司西酞普兰在肝组织中的精密度、准确度、提取回收率及基质效应Tab.3 Precision,accuracy,extraction recovery rates and matrix effects of escitalopram in liver (%)
2.3 案例应用
某年8月23日17:45,刘某(男,30岁)因“乏力、食欲缺乏7 h,意识障碍3 h”入住某医院,一般情况差,神志模糊,既往有1年抑郁症病史,于8月24日00:55经抢救无效死亡。为查明刘某的死亡原因,于8月30日在某司法鉴定中心进行尸体检验及药(毒)物检验。药(毒)物检验结果显示:从送检的白色药片中检出艾司西酞普兰成分;从送检的刘某心血、肝组织中均检出艾司西酞普兰成分;用超声辅助离子液体-分散液液微萃取-GC-MS/MS联用法检出刘某心血中艾司西酞普兰质量浓度为1.26μg/mL,肝组织中质量分数为0.44mg/g。
3 结 论
离子液体作为一种新兴化学试剂,因其蒸汽压低、液态范围宽、环境友好等优势在样品前处理领域有广阔的应用前景。本研究采用超声辅助离子液体-分散液液微萃取-GC-MS/MS联用法检测生物样品中艾司西酞普兰,该方法较传统液液萃取[13]、固相萃取[14]减少了有机溶剂的使用,降低了检测成本,且操作简单、快速,杂质干扰少,富集效率高,可满足生物检材中艾司西酞普兰的检测要求,并且环境友好优势突出,不仅可作为一种改良方法在药毒物定性定量分析中推广使用,而且本研究建立的方法还可为艾司西酞普兰相关案件提供技术支持。
