席夫碱-镍配合物的合成与表征
2020-09-11郭冬晴马洪伟程奥华
郭冬晴,马洪伟,李 婷,程奥华
(东北林业大学 化学化工与资源利用学院,黑龙江 哈尔滨 150040)
前 言
席夫碱是一类具有R1(R2)-C=N-R3结构的化合物。是由化学家Schiff在1864年首次发现的。席夫碱这种物质是由含胺类基团的物质和含活性羰基基团的物质缩合而形成的。席夫碱的核心为-C=N-基团,由于N原子具有孤对电子,可以与多种物质配合,因此在医药学[1]、催化、防腐蚀以及光致变色[2]方面,乃至分析化学检测鉴定离子方面都有重要应用。如杨丰科、韩健、王永春、陈芳合成了7种新型席夫碱,测得其许多产物可以抑制细菌活性,其中含S的席夫碱抑制细菌活性最强[3]。席夫碱还可以作为荧光探针对Al3+进行特异识别[4]。郭鹏,刘峥等制备了双席夫碱镍配合物-石墨烯-玻碳电极,用于定量检测胭脂红含量,提供了一种简单便捷、重现性好的检测胭脂红含量的新方法[5]。镧系元素席夫碱配位物一方面能发挥优良的发光性能,另一方面又发挥了席夫碱易与金属离子形成稳定配合物的特征,成为当今稀土领域最为活跃的研究领域之一[6~8]。席夫碱中的某些物质还含有液晶的某些性质,可以被用于合成某些有机试剂和新科技材料。而本文中所要研究的目标产物是席夫碱分类中举足轻重的一支。到目前为止,有关吡唑啉酮类席夫碱金属配合物的论文已经非常多了,但是脂肪族长链席夫碱合镍配合物未见有人发表,所以我们目前的主要任务是能设计并合成出新型的脂肪族长链席夫碱合镍配合物,并对其进行多种表征,来探究席夫碱合镍配合物的性质。目的是进一步拓宽席夫碱配合物的应用领域。
在无水溶剂的条件下以吡唑啉酮为母体,与己酰氯发生反应得到新型4-己酰基吡唑啉酮(HL)配体,以HL为母体,与苯胺反应合成新型4-己酰基吡唑啉酮缩苯胺席夫碱(HQ),通过非水溶剂法将4-己酰基吡唑啉酮缩苯胺席夫碱(HQ)与金属盐Ni反应成功合成金属配合物,最后用红外表征确定其官能团,用紫外光和荧光表征等方法对化合物的结构和组成进行表征,为席夫碱合镍配合物在实际应用上提供理论支持。
1 实验部分
1.1 试剂与仪器
1.1.1 试剂
1-苯基-3-甲基-5-吡唑啉酮和溴化钾试剂均为化学纯。己酰氯、盐酸、二氧六环、无水乙醇、苯胺、乙酸镍、氢氧化钠和氢氧化钙都为分析纯。
1.1.2 仪器
电子天平AR153CN;加热磁力搅拌器EMS-9;傅立叶变换红外光谱仪FTIR-8400;紫外可见光分光光度计UV-2550;荧光分光光度计F-4500。
1.2 HL的合成
取质量为26.1002g的苯基甲基氮茂酮白色固体(物质的量为0.15mol),放置于250mL磨口锥形瓶中,向锥形瓶中加入140mL二氧六环,安装冷凝回流装置,将所有药品加热至沸腾,使所有的固体全部溶解,然后溶液会慢慢变成桔黄色。等待几分钟,冷却后向溶液中加入20.0001g的白色粉末状的Ca(OH)2,等待一会儿,溶液第二次沸腾的时候,会发现该悬浮液的颜色慢慢变深了,然后向溶液中滴加20mL己酰氯,大概15min左右滴完,注意掌控滴入的速度,回流时间约1~1.5h。等到其变凉后,将所有的反应物一起倒入HCl中,使反应过程中得到的Ca配合物被破坏,等到锥形瓶中的物质由浆状物慢慢变为棕色液体的时候,进行过滤,过滤后洗涤,最后重结晶,出现暗红色物质。
1.3 席夫碱的合成
取50mL磨口锥形瓶洗净后晾干,称取质量为0.5461g的HL药品(物质的量为2mmol),置于洗净的锥形瓶中,移取20mL无水C2H6O,然后把锥形瓶放在磁力搅拌器上加热并搅拌至其中所有固体全部消失,溶液呈酒红色。然后向锥形瓶中移取2mL苯胺(物质的量为2mmol),然后安装冷却回流装置,调节加热搅拌速率,加热回流约5h左右,5h后使锥形瓶静置冷却。锥形瓶底部出现针状结晶,将锥形瓶中所有产物过滤至洁净干燥的小烧杯中,将小烧杯静置,直到小烧杯中再次出现晶体,过滤小烧杯中液体,得到产物为粉色晶体。
1.4 席夫碱-镍配合物的合成
首先取50mL磨口锥形瓶和小烧杯,洗净后晾干,然后称取乙酸镍固体粉末0.2488g(物质的量为1mmol),置于洁净干燥的小烧杯中,加入10mL无水C2H6O,然后把小烧杯放在磁力搅拌器上加热搅拌至小烧杯中所有固体全部消失,溶液呈浅绿色。
接下来称取0.6960g席夫碱固体,(物质的量为2mmol),置于洁净干燥的锥形瓶中,移取10mL无水C2H6O,然后置于磁力搅拌器上加热搅拌至其中所有固体全部溶解,液体呈橙色。将小烧杯中的乙酸镍溶液缓慢逐滴加入锥形瓶中,注意滴加速度应该尽可能缓慢。全部滴加完后,安装冷却回流装置,调节加热搅拌速率,加热回流约5h左右,5h后使锥形瓶静置冷却。锥形瓶底部出现针状结晶,将锥形瓶中所有产物过滤至洁净干燥的小烧杯中,将小烧杯静置,直到小烧杯中再次出现晶体,过滤小烧杯中液体,得到产物为浅绿色晶体。
2 结果与讨论
2.1 席夫碱及其镍配合物的红外光谱研究
实验测定的HQ与席夫碱-镍配合物的红外光谱图分别如图1、2所示。HQ中的各基团的特征表征峰如表1所示。由图表可知,在1630cm-1处出现了一个较强的吸收峰,此峰为-C=N-的伸缩振动峰。席夫碱中吡唑环上的羰基发生伸缩振动主要出现在1400cm-1处,与HL相比发生了红移。通过图表数据可以佐证合成了期望的脂肪族长链席夫碱。
席夫碱-镍配合物内的各基团的特征表征峰如表1所示。席夫碱吡唑环上的羰基发生伸缩振动主要显现在1540cm-1处,与HQ相比发生了红移。而-C=N-的伸缩振动则出现在1640cm-1处,与HQ相比发生了红移。510cm-1吸收峰为Ni-O的吸收振动峰。通过红外光谱的数据分析可以佐证合成了席夫碱-镍配合物。
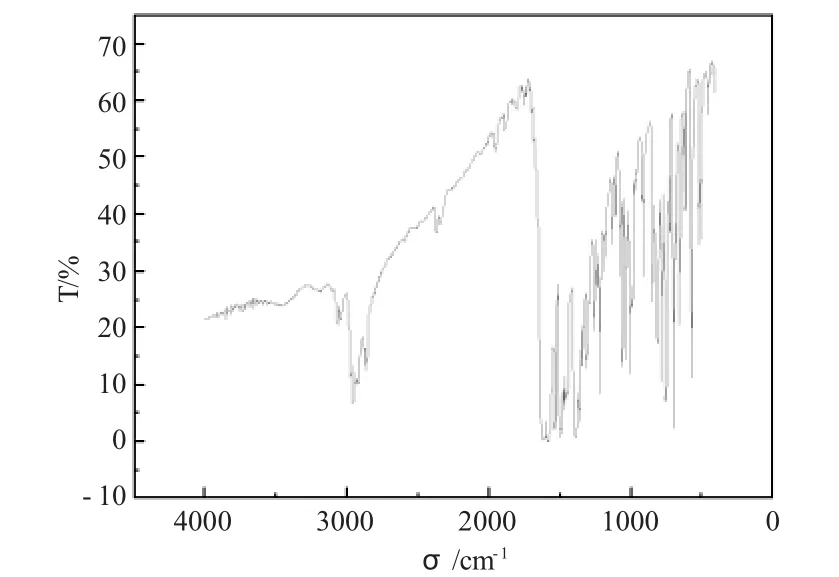
图1 席夫碱红外光谱图Fig.1 The IR spectrum of Schiff base
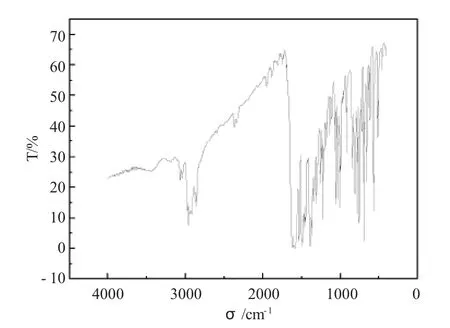
图2 席夫碱-镍配合物红外光谱图Fig.2 The IR spectrum of Schiff base-nickel complex

表1 产物的IR数据Table 1 The IR data of product
2.2 席夫碱及其镍配合物的紫外-可见吸收光谱研究
将合成的产物溶于无水C2H5OH,制得浓度为10~4mol/L溶液。实验测定的席夫碱和席夫碱-配合物的紫外光谱分别如图3、4所示。席夫碱的吸收峰如表2所示。3个峰分别位于234nm,257nm和305nm波长处,可以分别被认为是芳烃共轭体系中的π→π*跃迁,羰基中的π→π*跃迁和共轭体系的n→π*跃迁出现的吸收峰。与酰基吡唑啉酮相比,席夫碱羰基中的π→π*跃迁和共轭体系的n→π*跃迁出现的吸收峰发生了红移。
席夫碱-镍配合物的吸收峰如表2所示。三个峰分别位于233nm,255nm和306nm处,与席夫碱相比,金属配合物芳烃共轭体系中的π→π*跃迁和羰基中的π→π*跃迁产生的吸收峰发生了蓝移,共轭体系的n→π*跃迁出现的吸收峰发生了红移。

图3 席夫碱紫外光谱图Fig.3 The UV spectrum of Schiff base
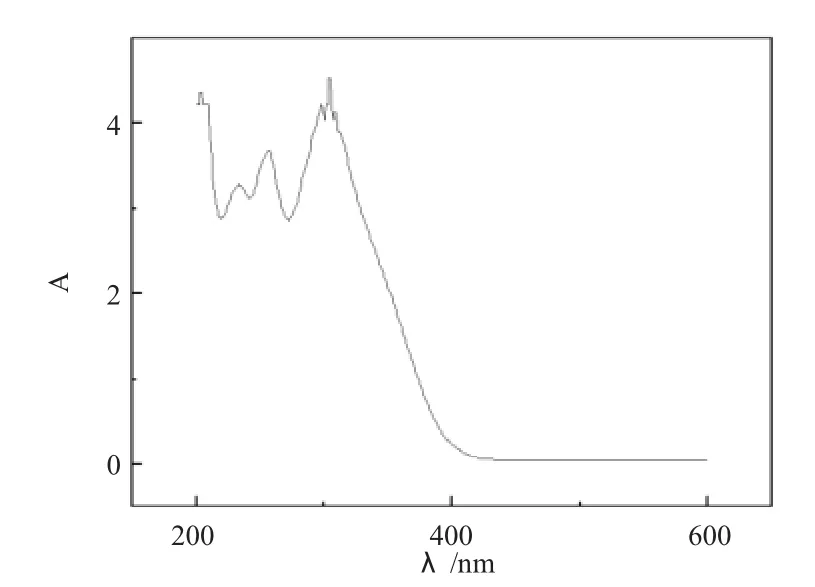
图4 席夫碱-镍配合物紫外光谱图Fig.4 The UV spectrum of Schiff base-nickel complexes
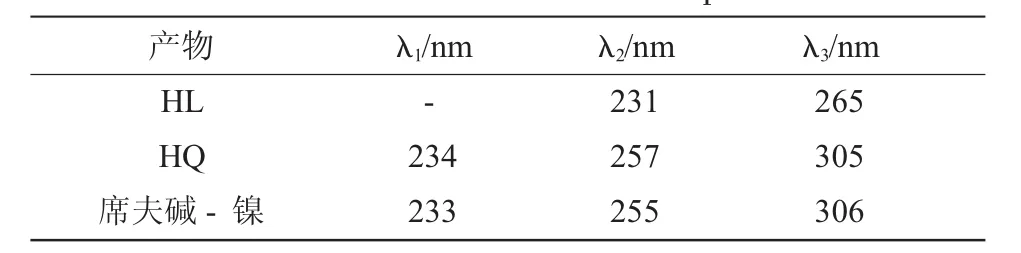
表2 样品的UV数据Table 2 The UV data of samples
2.3 席夫碱及其镍配合物的荧光光谱研究
实验测定的席夫碱的荧光光谱如图5、6所示,席夫碱-镍配合物的荧光光谱图如图7、8所示。席夫碱的最大激发峰(λEX)和最大发射峰(λEM)如表3所示。由图表可知实验制得的席夫碱具有较大的荧光强度。席夫碱-镍配合物的最大激发峰(λEX)和最大发射峰(λEM)如表3所示。由图表可知实验制得的席夫碱-镍配合物具有较大的荧光强度。
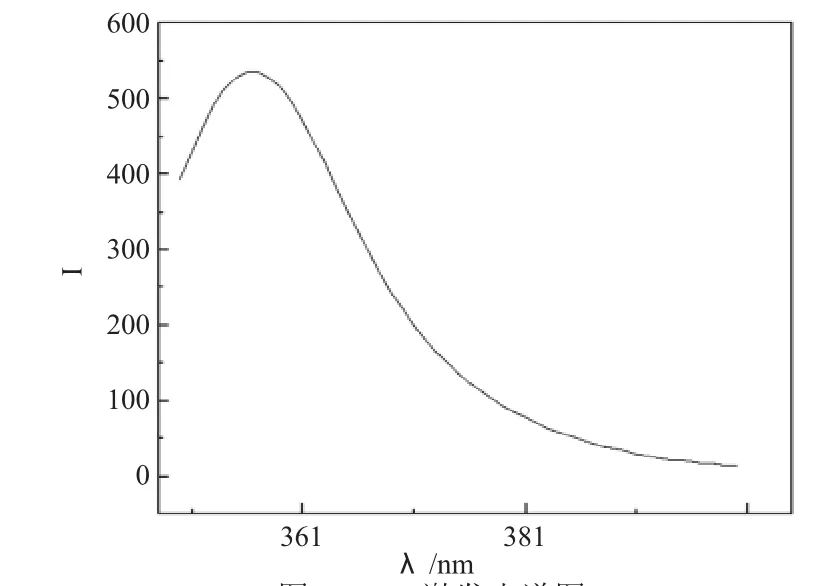
图5 HQ激发光谱图Fig.5 The excitation spectrum of HQ
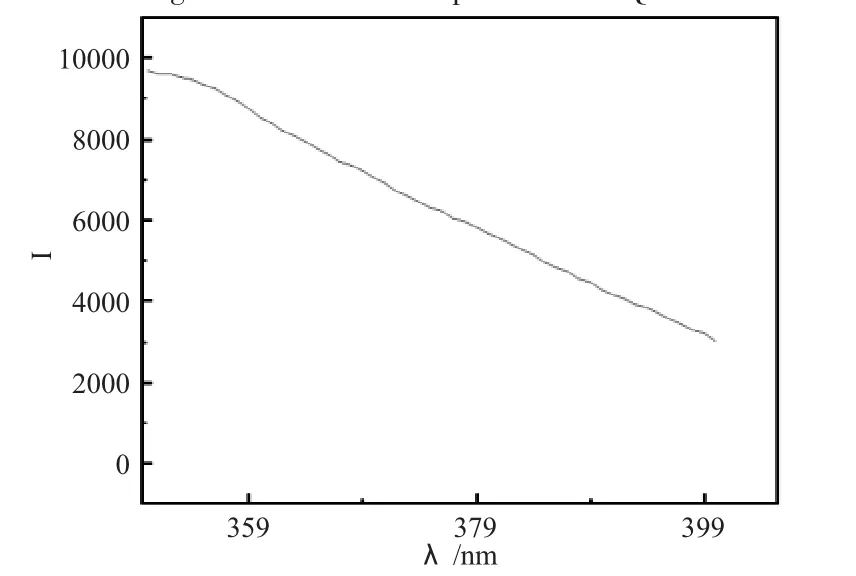
图6 HQ发射光谱图Fig.6 The emission spectrum of HQ
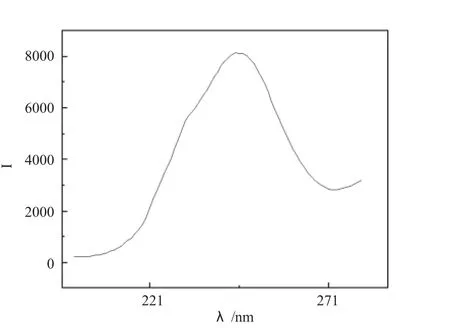
图7 席夫碱-镍激发光谱图Fig.7 The excitation spectrum of Schiff base-nickel complexes

图8 席夫碱-镍发射光谱图Fig.8 The emission spectrum of Schiff base-nickel complexes

表3 样品的FL数据Table 3 The FL data of samples
3 结论
本文主要介绍了HL、HQ以及金属镍配位物的合成及其在各个领域范围内的应用,并通过红外光谱、紫外光谱和荧光光谱对每一步的合成产物进行表征以探究它们的性质和结构。在红外光谱中,利用红外光谱特征峰的峰值能够分别佐证出HL的合成,席夫碱的合成以及席夫碱-镍配合物的合成,并且可以发现在510cm-1处有O-Ni键生成,这可以佐证配合物配位成功;在紫外光谱中得到目标产物的最强吸收波长出现在306nm处;通过荧光谱图可以找到金属配合物的最强激发波长是245nm,最强发射波长是349nm,荧光强度较大,这也说明了此化合物具有荧光性能,可以用作荧光材料,为以后探索席夫碱-镍配合物的其它应用提供了很好的实验依据。
