毛细管电泳法测定复方氨基酸注射液的游离磷酸盐
2020-08-28林东刘玉萍
林东,刘玉萍
(广州市药品检验所,广东 广州 510160)
磷是人体不可缺少的元素之一,在肠外营养液中常常添加磷酸盐作为补磷成分[1]。某些肠外营养液中的复方氨基酸注射液采用甘油磷酸钠作为补磷的成分,但甘油磷酸钠在工艺生产中,遇热易分解产生少量的游离磷酸盐。人体摄入过多游离磷酸盐时,可与钙结合成难溶于水的正磷酸钙,使体内的钙无法充分吸收、利用,容易引起骨折、牙齿脱落和骨骼变形,长期用药可引起血磷升高、血钙降低。因此,很有必要对游离磷酸盐限度进行控制。目前,测定游离磷酸盐的方法主要为分光光度法,操作较为繁琐,且重现性比较差[2]。本文参考文献[3]建立毛细管电泳检测法对某市售肠外营养液中复方氨基酸注射液的磷酸盐进行测定,结果显示方法准确可靠,可为复方氨基酸注射液中游离磷酸盐的含量测定提供参考。
1 仪器与试药
7100型安捷伦毛细管电泳仪及熔融石英毛细管(75 μm×80 cm,有效长度70 cm)。
3批复方氨基酸注射液(编号:A1;A2;A3);Anion Analysis Kit试剂盒[Beck Am Coulter公司生产,批号:M809229,包括有NaOH溶液(Conditioner-Na)、冲洗液(Rinse Solution)、聚阳离子表面活性剂(Anion Coating)、嘧啶二甲酸缓冲液(Anion Separation Buffer,加速剂)、酸性冲洗液(Anion Acid Rinse)、内标液(枸橼酸缓冲液)等试剂];KH2PO4(天津科密欧化学试剂有限公司,批号:20100318,105 ℃干燥至恒重);酶磷试液(Roche公司,批号:12917632);水为去离子水。
2 方法与结果
2.1 溶液配制
2.1.1 对照品溶液 取KH2PO4约0.1 g,精密称定,置200 mL量瓶中,加去离子水溶解并稀释至刻度,摇匀,得对照品储备液。分别精密量取对照品储备液1、3、5、8、10、12、15 mL,各置50 mL量瓶中,精密加入内标液0.5 mL,加去离子水溶解并稀释至刻度,摇匀,作为系列对照品溶液①~⑦。
2.1.2 游离磷酸盐供试品溶液 精密量取复方氨基酸注射液6 mL,置50 mL量瓶中,精密加入内标液(枸橼酸缓冲液)0.5 mL,加去离子水溶解并稀释至刻度,摇匀,作为游离磷酸盐测定溶液。
2.1.3 酶解甘油磷酸钠供试品溶液 参照进口注册标准操作:精密量取复方氨基酸注射液400 μL,置10 mL量瓶中,精密加入磷酸酶试液[取磷酸酶溶液40 μL和缓冲溶液(称取盐酸三乙醇胺1.85 g、MgCl20.4 g、加水80 mL使溶解,用1 mol/L NaOH溶液调节pH至7.4,用水稀释至100 mL,摇匀)]1 mL,摇匀,置37 ℃水浴中反应35 min,加入内标液0.1 mL,并用去离子水稀释至刻度,摇匀,作为总磷酸盐测定溶液。
2.2 毛细管电泳条件
以嘧啶二甲酸缓冲液为操作缓冲液,检测波长为232 nm,带宽4.0,参比波长为215 nm,带宽10.0,毛细管温度为20 ℃,分离电压为30 kV,进样端为负极,压力进样为3 447.3 Pa,进样时间为14 s。每次进样前,依次用NaOH溶液、冲洗液、聚阳离子表面活性剂、嘧啶二甲酸缓冲液(加速剂)冲洗毛细管柱180 s。每次进样后,依次用NaOH溶液、酸性冲洗液、冲洗液冲洗毛细管柱100 s。
2.3 系统适用性试验
取“2.1”项下的对照品溶液⑤10 mL、游离磷酸盐供试品溶液和酶解甘油磷酸钠供试品溶液进样分析,结果显示枸橼酸根、磷酸根离子的分离度为14.5(见图1),连续进样5次,其峰面积与内标峰面积比值的相对标准偏差为1.7%。
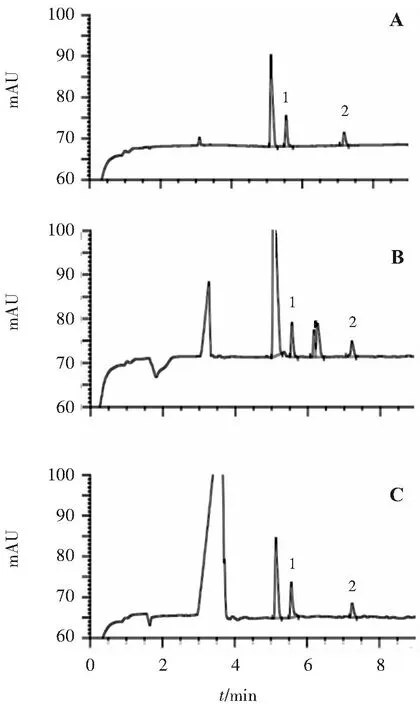
A.对照品溶液; B.游离磷酸盐供试品溶液; C.酶解甘油磷酸钠供试品溶液;1.磷酸根; 2.枸橼酸根(内标)。
2.4 标准曲线的制备
取系列浓度对照品溶液①~⑦按“2.2”项电泳条件分别进样,记录电泳图谱,以磷酸根(HPO32-)浓度为横坐标、磷酸根与枸橼酸根峰面积比值为纵坐标进行线性回归,得回归方程Y= 0.422 7x- 0.051 7,线性范围为 0.079 1~1.186 6 mmol/L,r为0.995 0。
2.5 精密度试验
取游离磷酸盐供试品溶液(编号:A3)与酶解甘油磷酸钠供试品溶液(编号:A3),分别重复进样6次,测得的结果代入线性回归方程计算磷酸根浓度,其RSD值分别为1.8%和2.0%。
2.6 加标回收率试验
精密量取“2.1”项下的对照品溶液⑤(浓度为0.791 1 mmol/L)0.5 mL与游离磷酸盐供试品溶液(编号:A1)0.5 mL,混匀,合并成1 mL的游离磷酸盐供试品加标试样,配制6份进样,测得的结果代入线性回归方程,计算加标回收率;精密量取“2.1”项下的对照品溶液⑤0.5 mL与酶解甘油磷酸钠供试品溶液(编号:A3)0.5 mL,混匀,合并成1 mL的酶解甘油磷酸钠供试品加标试样,配制6份进样,测得的结果代入线性回归方程,计算加标回收率,结果见表1。可见,平均回收率分别为99.2%和100.0%,符合方法学要求。
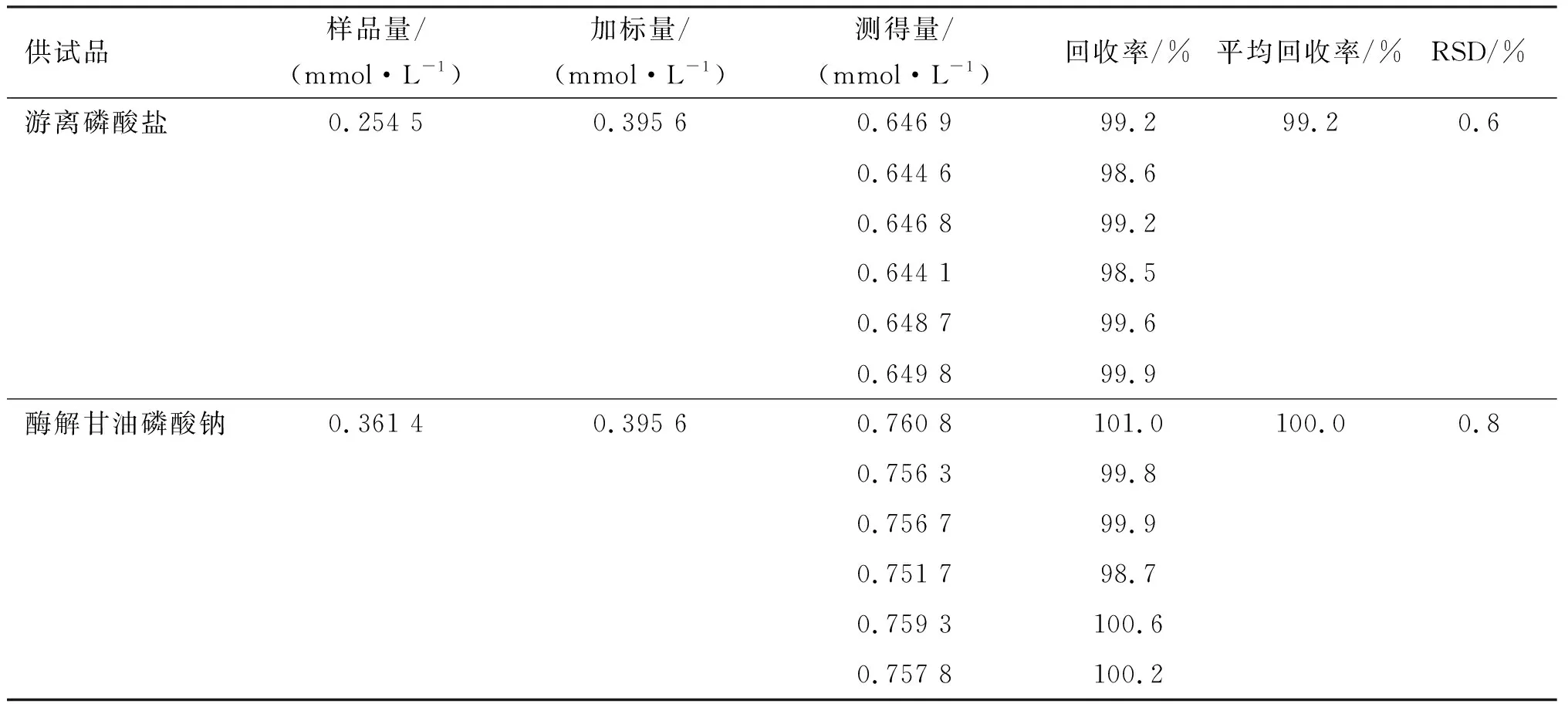
表1 加标回收率试验结果Table 1 Results of fortified recovery
2.7 样品测定
取按“2.1”项下方法配制的对照品溶液①~⑦、游离磷酸盐供试品溶液和酶解磷酸盐供试品溶液,分别进样,采用内标法加标准曲线测定复方氨基酸注射液中的游离磷酸盐和总磷酸盐含量,结果见表2。

表2 供试品中磷酸盐的测定结果Table 2 Determination Results of phosphate in test samples
3 讨论
根据参考文献[4],采用嘧啶二甲酸为间接紫外检测试剂,磷酸盐在232 nm无紫外吸收,而嘧啶二甲酸根离子通过检测器时,出现较大的背景吸收,当无紫外吸收的待测离子通过检测器时,由于降低背景吸收而出现负信号,达到检测目的。但由于本试验使用的是安捷伦7100型毛细电泳仪,无法通过仪器直接把负信号转变为正信号,因此在仪器中设定215 nm的参比波长,来实现正信号转化。
参照文献[3]方法,笔者适当延长进样前后的冲洗时间,有效地提高了基线稳定性及保留时间的迁移。另外,也需要注意仪器所在环境的湿度,过高易产生电流泄漏,同样会对基线造成影响[5]。
以甘油磷酸钠为补磷成分的复方氨基酸注射液,在进口注册标准中主要对磷酸盐有含量测定的要求,但并未对其游离磷酸盐限度进行合理控制,由产品处方可知磷酸盐的主要来源是甘油磷酸酸钠。工艺生产过程中,甘油磷酸钠受热易分解成游离磷酸盐,过量的磷酸盐对人体造成危害。因此,如何控制甘油磷酸钠制剂中的游离磷酸盐比例,建议相关企业做进一步研究。
本方法相较于传统的紫外分光光度法,操作上更为简便、高效、消耗试剂少,可作为复方氨基酸注射液中游离磷酸盐质量分数的测定方法,效率更高。
