双刺参胶囊中紫丁香苷及人参皂苷Rg1、Re、Rb1的含量测定
2020-07-20钟方丽王晓林
邸 松,钟方丽,王晓林,王 璐,高 园
(吉林化工学院化学与制药工程学院,吉林吉林 132022)
双刺参胶囊是由刺玫果、刺五加及人参三味中药材经过适当工艺加工而成的保健食品,其拟申报的保健功能为缓解体力疲劳。苏联学者N·布赫曼以“第三状态”描述了其所发现的非健康非疾病的状态,即亚健康状态[1]。疲劳是亚健康人群一种常见的状态[2],长期处于该状态下的人群,其免疫系统存在明显异常甚至受损[3]。
保健食品是一种适用于特定人群使用,具有调节机体功能,不以治疗疾病为目的食品[4]。中药类保健食品,是在中医“药食同源”基础上[5],以中药为主要成分的具有保健养生功能的特殊食品[6]。刺玫果含有丰富的黄酮及皂苷类成分,具有抗疲劳、抗衰老、增强免疫力、保肝、促智等药理作用[7]。刺五加主要含有三萜、木脂素、皂苷类成分等,具有增强机体免疫力、缓解体力疲劳、保护神经中枢系统等药理活性[8]。人参皂苷是人参的主要活性成分,具有抗衰老、抗抑郁等多种保健功效[9]。在国家公布的《关于进一步规范保健食品原料管理的通知》中,人参、刺玫果及刺五加均属于可用于保健食品的药食同源类药材[10]。大量文献表明,三者提取物中的皂苷类成分均具有较强的抗疲劳功效[11-13],其中人参三醇型皂苷(人参皂苷Rg1、人参皂苷Re)、二醇型皂苷(人参皂苷Rb1)[14]及紫丁香苷[15]为主要活性成分。梁少雄[16]和姜丽萍等[17]采用高效液相色谱法分别测定了参苓白术散和复方双参颗粒中人参皂苷Rg1、Re、Rb1的含量;姚路路等[18]和奉艳花等[19]采用乙腈-水梯度洗脱,分别测定刺五加甘草颗粒和壮药愈疡散中紫丁香苷的含量。在工业生产中,质量检测仪器需长时间工作,在检测过程中流动相流速、柱温箱温度、检测器灵敏度会出现不同程度的波动,且随着仪器使用时间加长,波动将逐渐明显,所以对于方法的耐用性要求较高。研究者大多只建立了检测方法,未对方法的耐用性进行评价。
本研究采用高效液相色谱法,在建立双刺参胶囊中4种有效成分的含量测定方法的同时,对检测方法的耐用性进行评价,为双刺参胶囊的进一步研究及质量标准的制定提供了基础数据,也为后续工业生产过程中质量检测奠定基础。
1 材料与方法
1.1 材料与仪器
双刺参胶囊 自制;人参、刺五加、刺玫果 中药饮片,吉林国安药业有限公司;人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1纯度>98.5%,成都曼思特生物科技有限公司;紫丁香苷 纯度>99.5%,成都曼思特生物科技有限公司;乙腈、甲醇 色谱纯,天津市大茂化学试剂厂;其余试剂 均为国产分析纯。
Agilent-1260型高效液相色谱仪 配有DAD阵列检测器,安捷伦科技有限公司;1201型高效液相色谱仪 配有UV检测器,大连依利特分析仪器有限公司;FA2004N型电子分析天平 上海精密科学仪有限公司;SK5210HP型超声波清洗器(超声功率:200 W,工作频率:53 kHz) 上海科导超声仪器有限公司。
1.2 实验方法
1.2.1 双刺参胶囊的制备 取人参粉、刺玫果粉、刺五加粉按处方量混合,加入5倍量90%乙醇,于80 ℃水浴提取2次,每次1 h。合并滤液,60 ℃减压浓缩为稠膏,干燥,粉碎成细分,加入适量淀粉混合均匀,制粒、干燥,加入颗粒质量1%的硬脂酸镁,混匀,灌装至1#胶囊中,既得双刺参胶囊(每粒0.35 g)。
1.2.2 溶液制备
1.2.2.1 供试品溶液的制备 取10粒双刺参胶囊内容物,将内容物混合研碎,精密称取1.0 g,置于烧瓶中,加20 mL甲醇,超声处理(功率200 W,频率53 kHz)30 min,放冷后过滤,滤渣经甲醇洗涤,将滤液及洗涤液转移至25 mL容量瓶中,定容至刻度,即得。
1.2.2.2 对照品溶液的制备 分别称取干燥至恒重的人参皂苷Rg1、Re、Rb1各约10 mg,精密称定,分别置于10 mL容量瓶中,加入甲醇溶解并定容。分别吸取上述溶液各3.0 mL,置于10 mL容量瓶中,混合,定容,即得质量浓度分别为0.369、0.306、0.339 mg/mL的人参皂苷Rg1、Re、Rb1的混合对照品溶液。
称取干燥至恒重的紫丁香苷对照品约2 mg,精密称定,置于50 mL棕色容量瓶中,加入适量甲醇溶解,定容,即得质量的浓度为0.046 mg/mL的紫丁香苷对照品溶液。
1.2.3 检测方法的建立
1.2.3.1 人参皂苷Rg1、Re、Rb1色谱条件的选择 人参皂苷因为具有较多的药、食功效[20],进而有比较成熟的含量检测方法,本实验通过文献查阅[21-23],使用Nano-Micro UniSil 5-120 C18色谱柱(250 mm×4.6 mm,5 μm),检测波长203 nm,柱温35 ℃,进样量10 μL,分别考察乙腈-水、乙腈-0.4%磷酸水梯度洗脱,根据目标峰的分离度、保留时间、拖尾因子等因素优选出适用于双刺参胶囊中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1含量测定的色谱条件。
1.2.3.2 紫丁香苷色谱条件的选择 柱温30 ℃,进样量10 μL,流速1.0 mL/min,检测波长265 nm,分别使用依利特ODS2、BDS-C18及APS色谱柱,考察乙腈-水(10∶90)、乙腈-水(15∶85)等度洗脱及乙腈-水梯度洗脱,根据目标峰的理论板数、保留时间、峰形等因素确定其色谱条件。
1.2.4 含量测定的方法学考察
1.2.4.1 标准曲线的绘制 分别吸取人参皂苷混合对照品溶液、紫丁香苷对照品溶液1.0、2.0、4.0、6.0、10.0 mL于10 mL容量瓶中,定容,分别在对应色谱条件下进样,记录峰面积,以各成分的质量浓度作为横坐标,对应的峰面积作为纵坐标进行线性回归,得到标准曲线方程。
1.2.4.2 检测限及定量限的确定 吸取紫丁香苷及人参皂苷混合对照品溶液,加入甲醇按比例进行稀释。在色谱条件下进样,分别记录各成分峰面积,当信噪比为3和10时,计算各成分对应的质量浓度,即为各成分所对应的检测限和定量限。
1.2.4.3 精密度实验 精密吸取人参皂苷混合对照品溶液及紫丁香苷对照品溶液、供试品溶液各10 μL,在相应色谱条件下连续进样6次,记录各成分的峰面积,并计算RSD值。
1.2.4.4 重复性实验 取同一批次双刺参胶囊,按照供试品溶液制备方法进行溶液制备。按照色谱条件进样6次,分别记录人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1及紫丁香苷的峰面积,并计算RSD值。
1.2.4.5 稳定性实验 吸取同一供试品溶液,分别在0、6、12、24、36、48 h进样,记录目标峰的峰面积,计算RSD值。
1.2.4.6 系统耐用性实验 在选定的流动相条件下,通过测定条件(检测波长、流动相流速及检测温度)及色谱柱的改变,对样品再次进行含量测定,以测定的含量为依据,进行耐用性考察。
1.2.5 加样回收率实验
1.2.5.1 人参皂苷Rg1、人参皂苷Re及人参皂苷Rb1的回收率实验 称取已知含量的双刺参胶囊内容物6份,每份1.0 g,精密称定,分别加入1.47 mg的人参皂苷Rg1、1.90 mg的人参皂苷Re及3.67 mg的人参皂苷Rb1,按照供试品溶液制备方法制备供试品溶液,在人参皂苷检测的色谱条件下进样,记录各目标峰的峰面积,计算回收率。
1.2.5.2 紫丁香苷的回收率实验 称取适量已知紫丁香苷含量的双刺参胶囊内容物9份,每份1.0 g,精密称定,每3份为一组,分别加入已知含量50%、100%及150%的紫丁香苷,按照供试品溶液制备方法进行溶液制备,在色谱条件下进样,记录紫丁香苷的峰面积,计算紫丁香苷回收率。
1.2.6 双刺参胶囊中有效成分的含量测定 称取双刺参胶囊内容物3份,每份1.0 g,精密称定,按照供试品溶液制备方法制备供试品溶液。分别在对应各成分的色谱条件下进样,测定人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1及紫丁香苷的含量。
1.3 数据处理
每组实验重复3次,取平均值,数据处理采用安捷伦1260型高效液相脱机工作站,及Origin作图整理。
2 结果与分析
2.1 供试品溶液制备方法的选择
实验考察了超声次数对各成分转移率的影响,取1.0 g样品,加入甲醇超声(功率200 W,频率53 kHz)处理30 min,放冷至室温,过滤,使用甲醇洗涤滤渣,合并滤液及洗液后定容为25 mL。剩余滤渣重复上述操作3次,得到4组供试品溶液,分别在色谱条件下进样,测定结果显示经过1次超声处理,供试品中的4中皂苷类成分转移至溶剂中的转移率均大于96.5%,可视为完全转移。故最终选择超声处理1次制备供试品溶液。
2.2 检测方法的确定
当人参皂苷的检测选用流动相乙腈-0.4%磷酸水梯度洗脱时,人参皂苷Rg1及人参皂苷Re无法分离。在检测紫丁香苷时,选用依利特ODS2色谱柱时采用乙腈-水等度洗脱无目标峰出现,采用乙腈-水梯度洗脱时目标峰拖尾严重;选用BDS-C18色谱柱时,各组流动相下目标成分的分离度小于1.5;选用APS色谱柱,采用乙腈-水等度洗脱时,紫丁香苷对应峰分离度较低。最终确定人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1含量测定的色谱条件为:Nano-Micro UniSil 5-120 C18色谱柱,以乙腈-水为流动相,按一定梯度洗脱,梯度洗脱程序见表2,柱温35 ℃,检测波长203 nm,进样量10 μL,流速1.0 mL/min;紫丁香苷含量测定的色谱条件为:APS色谱柱,以乙腈-水作为流动相梯度洗脱(表3),柱温30 ℃,检测波长265 nm进样量10 μL,流速1.0 mL/min。在对应色谱条件下,各成分的保留时间、分离度、理论塔板数及拖尾因子见表4。对应的HPLC色谱图见图1。高效液相色谱法测定相关成分含量时,系统适应性要求分离度应大于1.5,主峰拖尾因子不得大于2.0,理论塔板数应大于3000,从表4中可以看出,4种有效成分目标峰的理论塔板数均大于20000,分离度均大于2.12,说明色谱柱柱效较好,4种物质目标峰与相邻峰完全分离。由4种物质的拖尾因子可知,人参皂苷Rg1和人参皂苷Re对称性较好,人参皂苷Rb1和紫丁香苷略有拖尾现象。

表2 人参皂苷Rg1、人参皂苷Re、 人参皂苷Rb1的梯度洗脱程序Table 2 Gradient elution procedure of ginsenoside Rg1,Re,Rb1
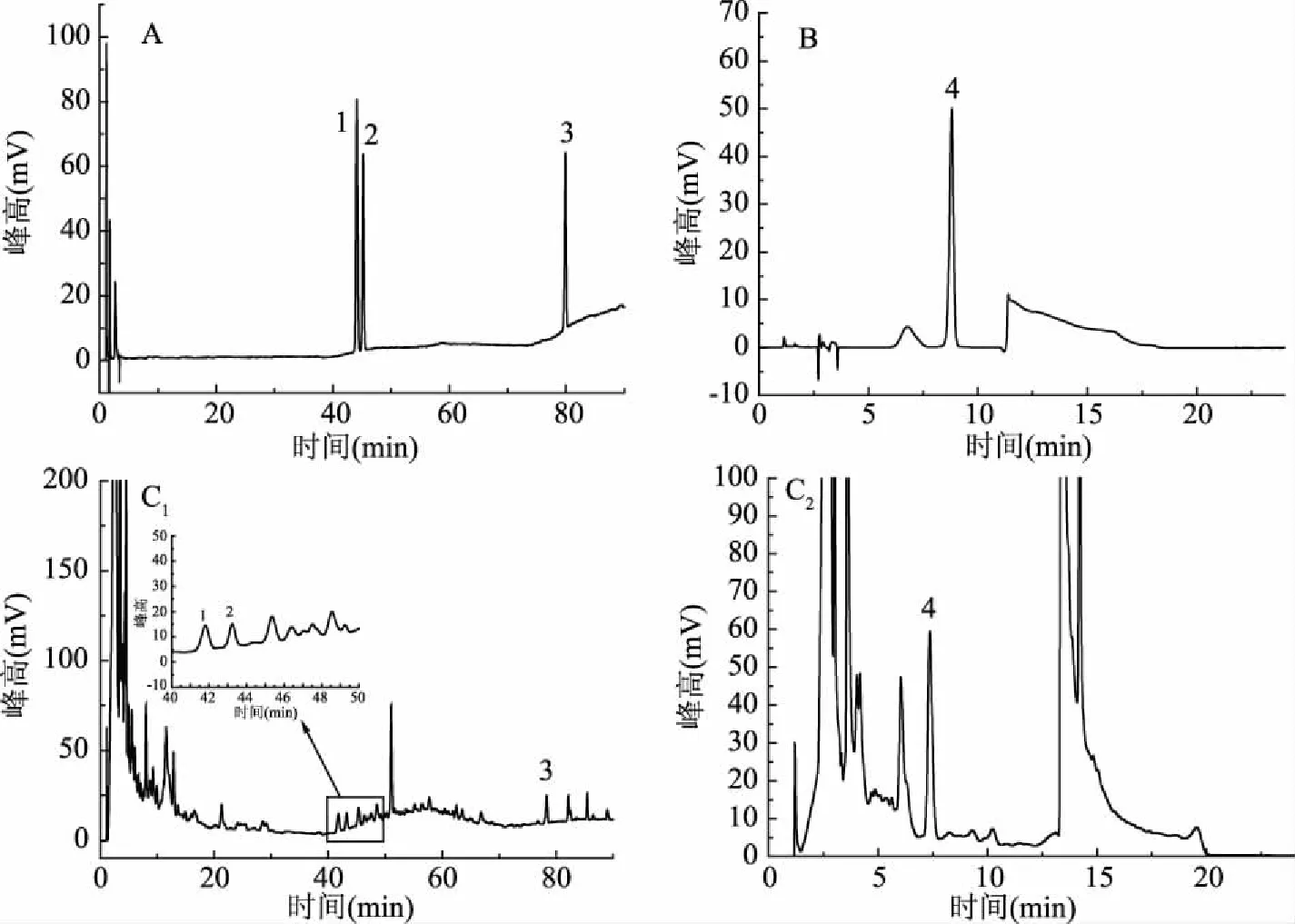
图1 双刺参胶囊的HPLC谱图Fig.1 HPLC spectra of Shuangcishen capsules注:A:人参皂苷混合对照品色谱图(波长:203 nm);B:紫丁香苷色谱图(波长:265 nm);C:供试品溶液色谱图(C1波长:203 nm;C2波长265 nm);1:人参皂苷Rg1;2:人参皂苷Re;3:人参皂苷Rb1;4:紫丁香苷。
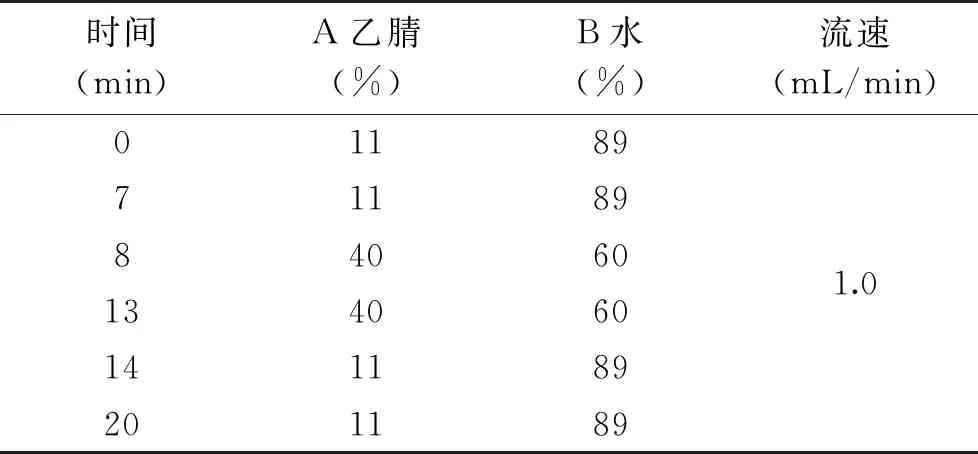
表3 紫丁香苷的梯度洗脱程序Table 3 Gradient elution procedure for syringin

表4 4种成分的色谱数据Table 4 Chromatogram data of four kinds of components
2.3 含量测定的方法学考察实验结果
2.3.1标准曲线绘制的实验结果 4种有效成分均以质量浓度为横坐标,峰面积为纵坐标绘制标准曲线,拟合方程、线性范围、检测限及定量限见表5。由实验结果可知,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1及紫丁香苷的进样质量浓度分别为15.30~306.00、16.95~339.00、18.45~369.00、4.60~46.00 μg/mL范围内与其峰面积值呈良好的线性关系,其检测限分别为:0.77、0.89、0.93、0.12 μg/mL,其定量限分别为:2.21、2.71、2.74、0.38 μg/mL。
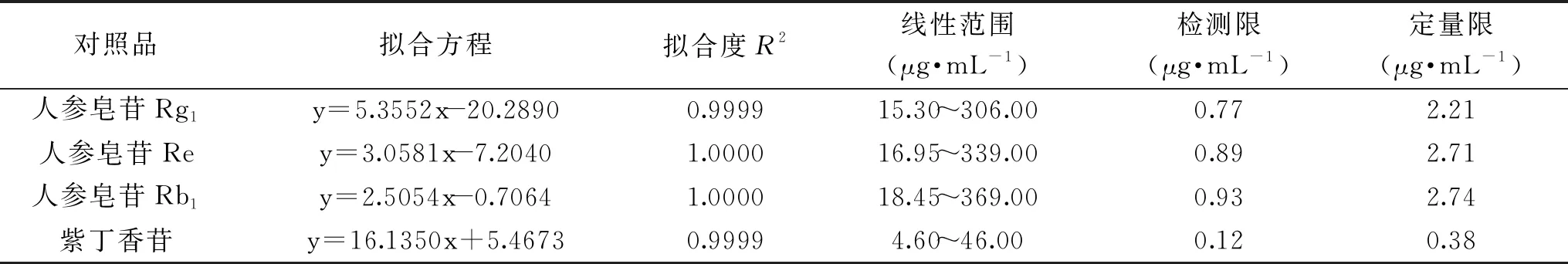
表5 标准曲线绘制实验结果Table 5 Standard curve drawing test result
2.3.2 精密度、重复性及稳定性实验结果 实验结果显示,在上述色谱条件测定双刺参胶囊中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1及紫丁香苷,仪器精密度良好,方法重复性较好,供试品溶液在48 h内稳定,满足测定要求。详细实验结果见表6。
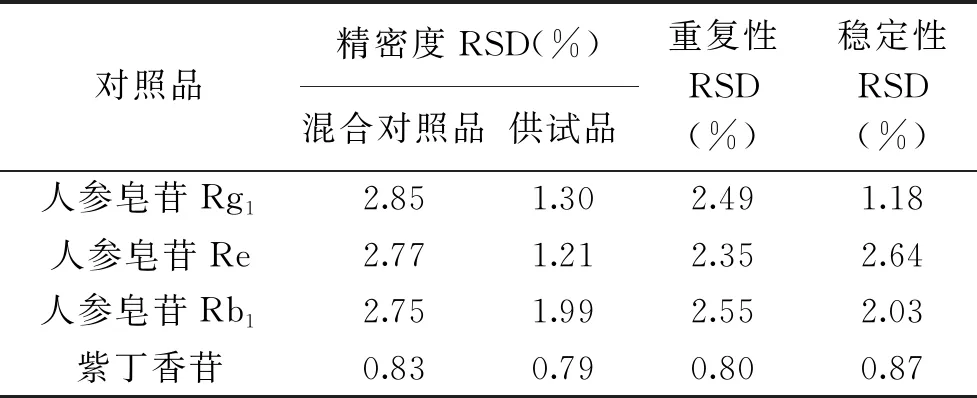
表6 方法学考察实验结果(n=6)Table 6 Methodological investigation result(n=6)
2.3.3 系统耐用性实验结果 在测定条件微小调整后对样品进行含量测定,相应色谱条件下的样品含量测定值对应的RSD值均小于3%,表明测定方法耐用性良好,实验结果见表7、表8。
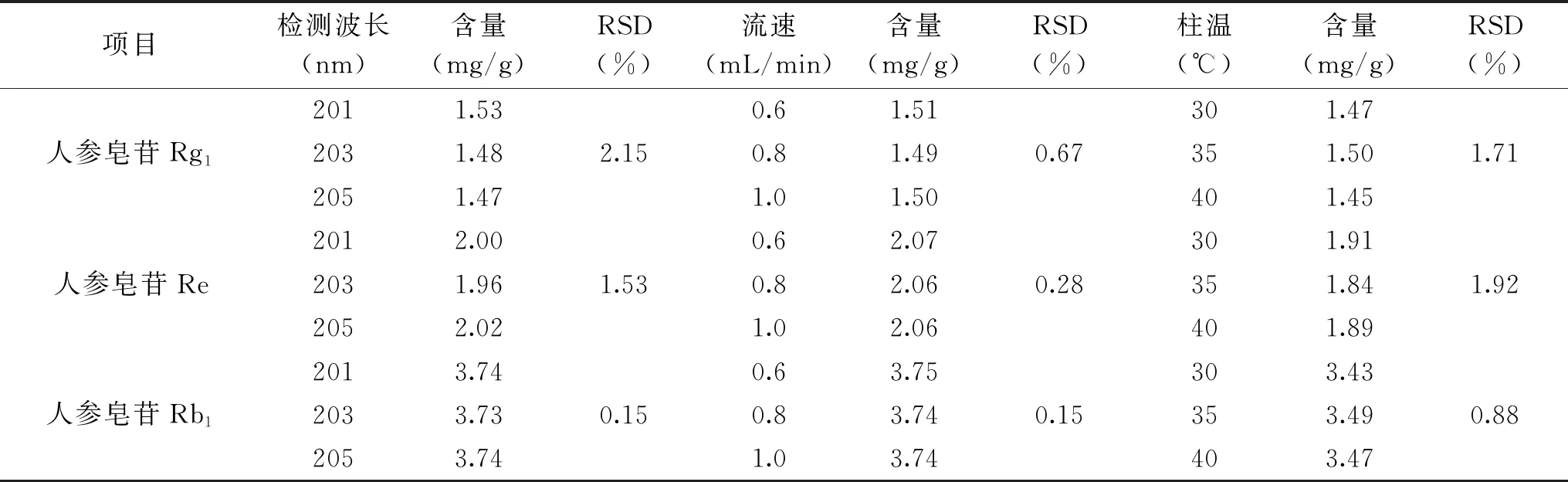
表7 人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1系统耐用性实验结果Table 7 System durability test results of ginsenoside Rg1,Re,Rb1
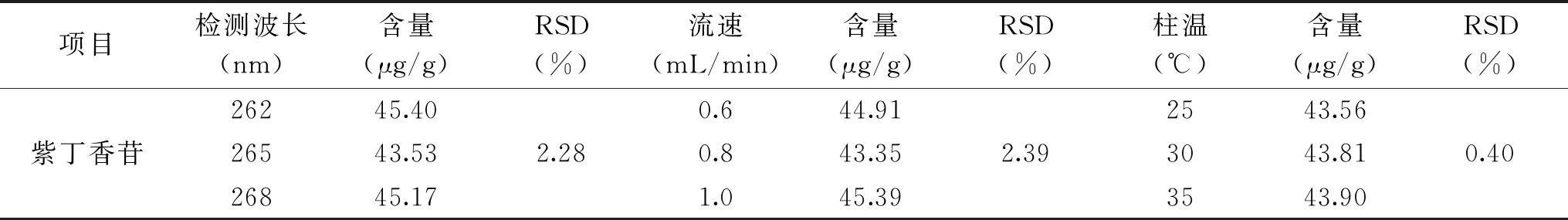
表8 紫丁香苷系统耐用性实验结果Table 8 System durability test result for syringing
2.3.4 加样回收率实验结果 根据表9、表10可知,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1及紫丁香苷的平均加样回收率分别为100.13%、100.50%、102.33%、101.55%,RSD值分别为0.67%、0.99%、0.29%、0.68%,说明该方法准确度高,可用于双刺参胶囊中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1、紫丁香苷的含量测定。
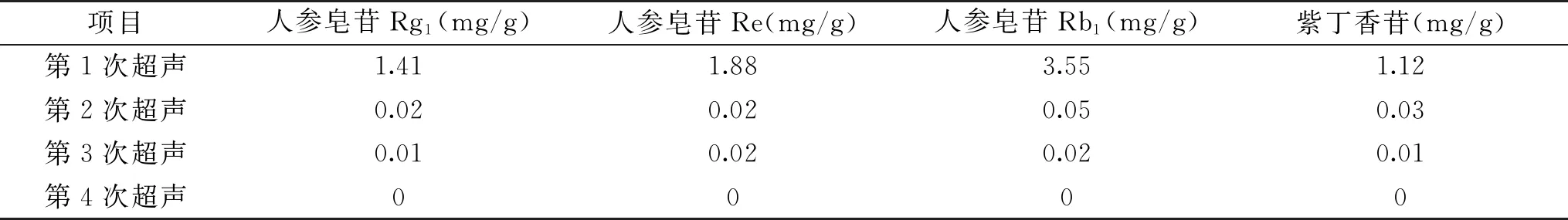
表1 供试品溶液制备方法实验结果Table 1 Preparation method test results of test solution
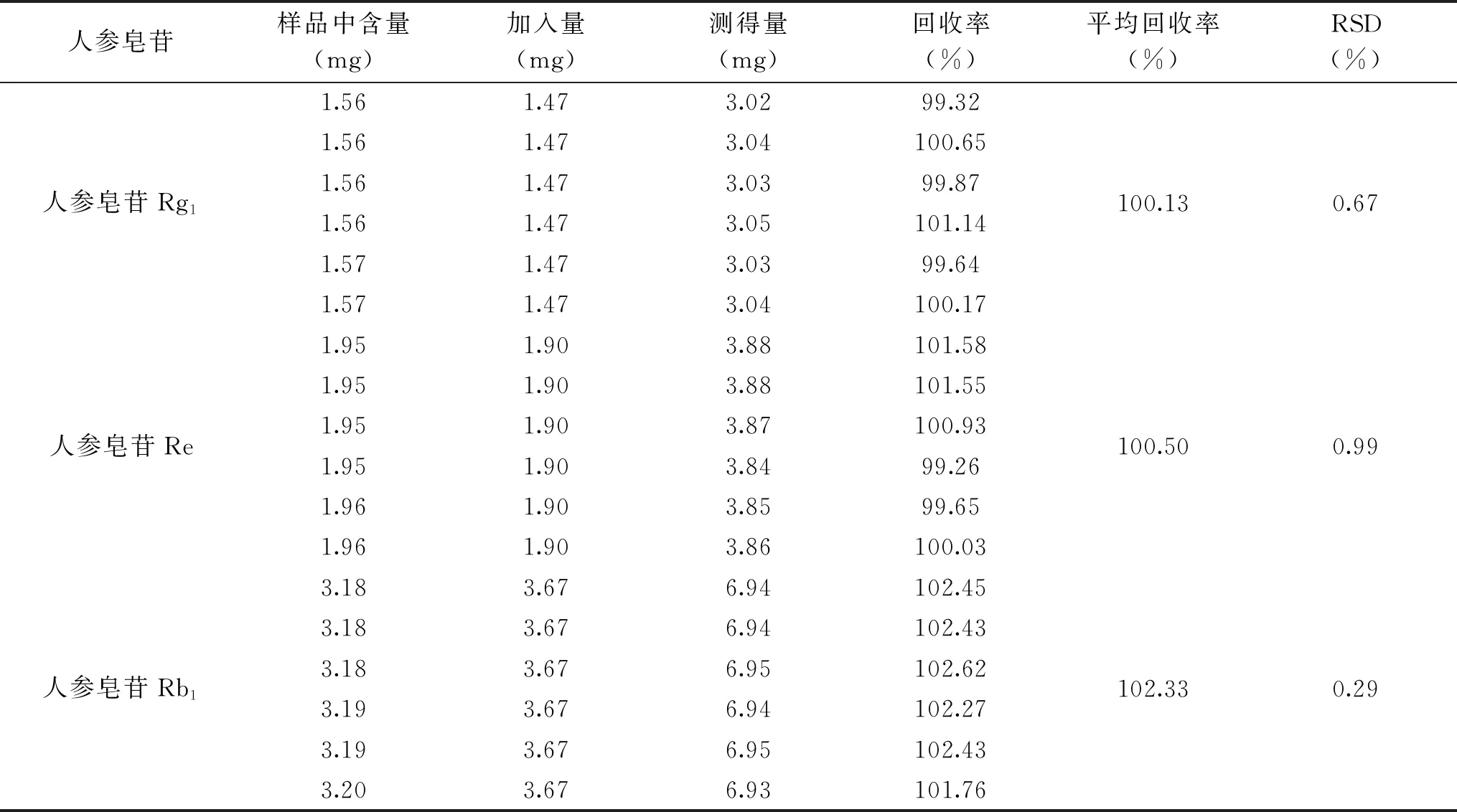
表9 人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1加样回收率实验结果(n=6)Table 9 Test results of ginsenoside Rg1,Re,Rb1 loading recovery(n=6)
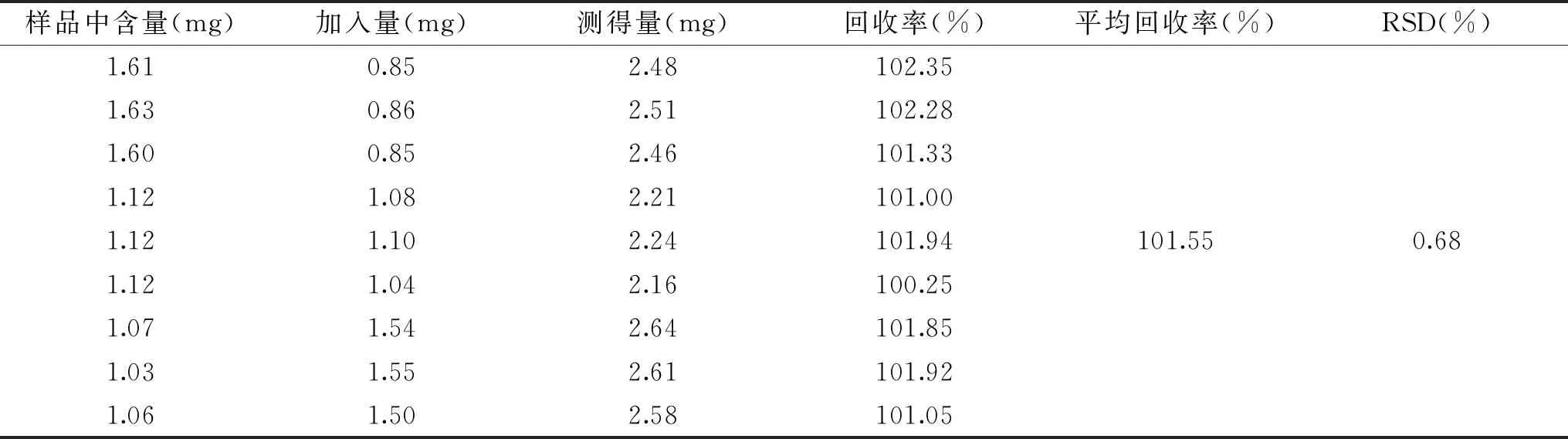
表10 紫丁香苷加样回收率实验结果(n=9)Table 10 Syringin recovery test results(n=9)
2.3.5 样品中各有效成分含量测定的实验结果 3批双刺参胶囊含量测定结果显示,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1的含量分别为137.90、189.58、356.83 mg/100 g(相当于每粒含0.48、0.66、1.25 mg),紫丁香苷为114.99 mg/100 g(相当于每粒含0.40 mg),实验结果表明双刺参胶囊中含有抗疲劳活性成分人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1及紫丁香苷,且不同批次样品中4种有效成分含量相差不大。实验数据见表11。
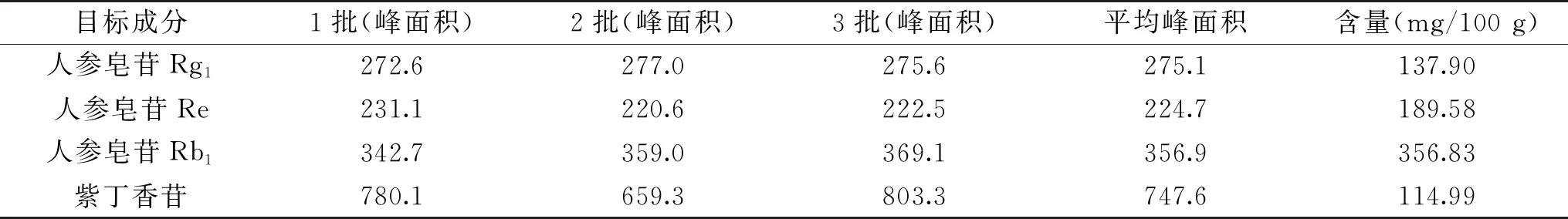
表11 样品含量测定的实验结果Table 11 Test results of sample content determination
3 结论
本研究选用人参、刺五加、刺玫果三种药食同源药材,制备了抗疲劳保健食品双刺参胶囊。采用HPLC建立了双刺参胶囊中4种有效成分含量测定的方法。在检测条件下,测得每粒双刺参胶囊中含有人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1及紫丁香苷分别为0.48、0.66、1.25、0.40 mg,且各有效成分分离度均大于2.0,理论塔板数均大于20000,符合相关含量测定标准。该方法简便准确,重复性好,方法稳定可行,可用于双刺参胶囊质量控制。
双刺参胶囊属中药类抗疲劳保健食品,在后续的研究中,将会借鉴中药制剂的“一测多评”法,使用超高效液相色谱仪,在缩短检测时间的基础上,探索可同时测定双刺参胶囊中更多有效成分含量的方法,为双刺参胶囊的进一步研究提供基础。
