IRMOF-3接枝柠檬醛的合成与抗菌性能
2020-06-17苏健裕管靖玮方立明徐振波肖雨茜
苏健裕 管靖玮 方立明 徐振波 肖雨茜
(1.华南理工大学 食品科学与工程学院,广东广州 510640;2.华南理工大学 材料科学与工程学院,广东 广州 510640)
自20世纪弗莱明发现盘尼西林以来,抗生素的滥用导致细菌的耐药性不断增加,已成为临床医学的棘手难题,开发新型抗菌材料、降低产生耐药菌的风险迫在眉睫[1]。柠檬醛是山苍子精油中的主要抑菌成分,具有较好的广谱抑菌性能[2- 3],但易挥发和氧化变质[4]。目前,研究者们大多采用微乳液[5]、微胶囊[6- 7]等包埋方法来提高柠檬醛的稳定性,这能在一定程度上降低柠檬醛的挥发与变质速率,但所制备的柠檬醛具有一定的时效性。金属有机框架(MOF)化合物以金属离子为中心,与有机配体通过化学配位构建多孔三维框架结构。MOF材料的 孔隙度高、比表面积大,其开放的金属位点具有一定的抗菌能力[8- 10]。现有研究中,尚未发现柠檬醛与金属离子有增加细菌耐药性的风险,因此,MOF接枝柠檬醛有可能可以提高柠檬醛的稳定性,同时结合MOF中金属离子的抑菌能力,得到新型的高性能抗菌剂。IRMOF-3是以Zn4O6+为金属位点、2-氨基对苯二甲酸为有机配体,通过水热法或表面活性剂法合成的一种MOF。水热法一般采用高温长时反应方式,反应时间在24~72 h不等,且产物较少,多为微米级。添加表面活性剂的方法可加速晶体成核速度,反应时间有所缩短(8~18 h),但是反应需要高温,且产物粒径分布不均匀,表面活性剂难去除。文中采用醋酸锌法,在温和条件下快速合成IRMOF-3。与水热法和表面活性剂法比较,醋酸锌法制备的IRMOF-3纳米颗粒细小、均匀,晶体结构完整。在此基础上,通过可酸响应的席夫碱键反应,在IRMOF-3纳米颗粒表面接枝柠檬醛(IRMOF-3-C),以期合成具有良好抗菌性与稳定性的抗菌剂。
1 材料与方法
1.1 材料与试剂
柠檬醛(纯度98%)、2-氨基对苯二甲酸(纯度98%)、吡啶、二环己基碳二亚胺(DCC)、聚乙烯吡咯烷酮(PVP),均购自美国Sigma公司;六水合硝酸锌(纯度99%),购自广州化学试剂厂;二甲基亚砜(DMSO)、N,N-二甲基甲酰胺(DMF)、二氯甲烷(CH2Cl2)、甲醇、无水乙醇,购自天津大茂化学试剂厂;LB肉汤培养基、琼脂粉,购自广东环凯微生物科技有限公司;ATCC 23235金黄色葡萄球菌(Staphylococcusaureus)、ATCC 43894大肠杆菌(Escherichiacoli),来自American Type Culture Collection。
1.2 仪器设备
主要仪器设备如下:高分辨场发射扫描电子显微镜(德国Zeiss Merlin)、X射线多晶衍射仪(德国Bruker D8 ADVANCE)、傅里叶变换红外光谱仪(德国Bruker VERTEX 70)、液相色谱质谱联用仪(德国BrukerAgilent 1100/Esquire HCT PLUS)、同步热分析仪(德国NETZSCH STA449 F3)、生化培养箱(上海一恒科学仪器有限公司LRH-250)、生物安全柜(力康生物医疗科技控股有限公司HFsafe900)。
1.3 实验方法
1.3.1 IRMOF-3的合成
根据文献[11- 13]中的IRMOF-3合成方法,采用水热法、表面活性剂法和醋酸锌法分别制备了3种IRMOF-3。
水热法:将二氨基对苯二甲酸(0.297 g,1.64 mmol)与六水合硝酸锌(1.308 g,4.40 mmol)超声溶解于80 mL DMF并转移到反应釜,在100 ℃下加热18 h后冷却,离心收集并用DMF洗涤3次后,用CH2Cl2置换DMF,每12 h换液1次,3 d后干燥。
表面活性剂法:将PVP(0.20 g)溶解于含有无水乙醇(5 mL)和DMF(5 mL)的混合溶剂中,然后将六水合硝酸锌(66.93 mg)和二氨基对苯二甲酸(16.29 mg)溶解在4 mL的DMF中并加入上述溶液。将溶液超声分散10 min后,转移到反应釜中,并在105 ℃下加热8 h(加热速率1.5 ℃/min)。最后,通过离心(10 000 r/min,15 min)分离产物。产物用DMF反复洗涤5次后,放置于透析袋中80 ℃过夜去除未结合的有机配体和PVP。最后,用CH2Cl2置换DMF,12 h换液1次,3 d后干燥。
醋酸锌法:将醋酸锌(0.176 g,0.8 mmol)超声分散于10 mL DMF中,2-氨基对苯二甲酸(0.054 g,0.3 mmol)超声分散于15 mL DMF中。将2-氨基对苯二甲酸溶液置于磁力搅拌器上搅拌,并将醋酸锌溶液快速倒入溶液中,搅拌反应1 min,离心并用DMF洗涤3次,再用CH2Cl2置换DMF,每12 h换液1次,3 d后干燥。
以上3种合成方法的超声和离心处理条件一致,超声处理条件均为40 kHz、240 W,离心处理条件均为10 000 r/min、15 min;洗涤干燥条件均为:用CH2Cl2置换DMF,12 h换液1次,3 d后在25 ℃下真空干燥24 h。
1.3.2 IRMOF-3-C的合成
通过柠檬醛中的醛基与2-氨基对苯二甲酸中的氨基发生席夫碱反应,将柠檬醛接枝在IRMOF-3颗粒表面,具体操作如下:将10 mg的IRMOF-3在10 mL的DMSO中进行超声分散(40 kHz,240 W),30 min后,加入柠檬醛(11.36 mg)、吡啶(0.1 mL)和DCC(20 mg),在氮气气氛下避光,室温搅拌4 h后离心(10 000 r/min,15 min),收集产物并用DMF洗涤多次,再将其浸泡在CH2Cl2中,每12 h换液1次,置换3 d。
1.3.3 IRMOF-3-C的表征
(1)扫描电子显微(SEM)表征[14]
SEM主要用来表征IRMOF-3以及IRMOF-3-C的表观形貌。将制备好的颗粒在乙醇中超声分散30 min(40 kHz,240 W),选取适宜的浓度,取5 μL液体滴在光滑的硅片表面,干燥后喷金60 s制得电镜样品。
(2)X射线衍射表征(XRD)[15]
XRD主要用来表征IRMOF-3和IRMOF-3-C的晶型结构。采用Cu靶Kα辐射,管压40 kV,管流40 mA,扫描速度0.2°/s,采样宽度0.02°,扫描范围5°≤θ≤60°。测试前将样品室温真空干燥24 h后过200目筛。
(3)傅里叶红外光谱(FT-IR)表征[16]
FT-IR主要用来表征材料接枝前后官能团的化学结构变化。采用KBr压片法进行测试,首先将IRMOF-3和IRMOF-3-C研磨至粉末状,再分别与KBr以约1∶200的质量比研磨至混合均匀,制得透明的固体KBr压片用于测试。
(4)电喷雾质谱(ESI-MS)表征[17]
ESI-MS用来进一步测定接枝是否成功。将IRMOF-3-C(10 mg)在3 mL含10 %甲醇的水溶液中超声处理30 min(40 kHz,400 W),过0.22 μm的滤膜,取1 mL过滤的上清液进行ESI-MS测定。
1.3.4 菌悬液的制备[18]
将冻存的大肠杆菌与金黄色葡萄球菌在LB液体培养基中接种过夜,培养活化菌株,将菌株转移到LB固体培养基上画板培养24 h,挑取单菌落接种在LB液体培养基中过夜培养,离心(5 000 r/min,5 min)后用生理盐水洗涤、重悬,调整到与0.5麦氏比浊管相同的浊度(约为1.5×108CFU/mL)使用。
1.3.5 最小抑菌浓度的测定[19]
最小抑菌浓度(MIC)是指在药物作用于细菌后能完全抑制细菌生长的最低浓度。将在LB液体培养基中分散好的柠檬醛、IRMOF-3与IRMOF-3-C在96孔板中进行二倍稀释,并加入稀释好的菌液使每个孔中的菌浓度为1×105CFU/mL,制备梯度材料浓度(4.000、2.000、1.000、0.500、0.250、0.125、0.063、0.031 mg/mL)的样品,将其放置在37 ℃的培养箱中培养24 h后取出,测600 nm处的吸光度(OD600)来判定MIC。设置只有菌的阴性对照组、无菌的空白对照组与只加材料的对照组。
1.3.6 最小杀菌浓度的测定[20]
最小杀菌浓度(MBC)表示与阳性对照(未处理)相比,杀灭99.9%的细菌所需的最小颗粒浓度。通过将MIC菌液培养在LB固体培养基上,并在37 ℃下孵育24 h来测定MBC值。所有测定均在生物安全柜中进行。
1.3.7 细菌形态的观察
将经过2倍MIC的IRMOF-3-C处理的菌液(实验组)和生理盐水(对照组)处理后的菌液于4 000 r/min下离心5 min,弃上清液,用磷酸缓冲盐溶液(PBS)洗涤两次除去残留的培养基后,加入用PBS稀释的含2.5%戊二醛的溶液,于4 ℃固定12 h,再用PBS溶液洗涤两次。分别用30%、50%、70%、85%、90%、95%梯度浓度的乙醇脱水,每个梯度中静置5 min,再用100%乙醇脱水两次,每次静置15 min。将细菌真空干燥并喷金60 s后,用场发射电镜观察细菌形态。
2 结果与分析
2.1 IRMOF-3与IRMOF-3-C的形貌分析
研究中采用了3种方法来合成IRMOF-3并进行形貌分析。水热法合成的IRMOF-3(如图1(a)所示)颗粒粒径约为12~18 μm,结构基本规整,大体呈六面体,棱角分明。但是,由于在静止条件下长时间高温加热反应,晶核形成时间长,导致粒径偏大、尺寸分布不均匀。加入表面活性剂PVP并采用高温法合成IRMOF-3(如图1(b)所示)可以加速成核,缩短反应时间,得到较小的粒径(约为200~600 nm)。然而,表面活性剂的加入会影响颗粒形貌,导致颗粒呈球状。采用醋酸锌为锌源,在室温搅拌下合成IRMOF-3(如图1(c)所示)时,由于醋酸锌可以加速2-氨基对苯二甲酸的去质子化,加快成核速度,所以能在室温、搅拌等简单条件下快速合成得到粒径50 nm左右的六面体颗粒,且粒径均一,表面平整。因此,可选择醋酸锌法合成IRMOF-3纳米颗粒,并在其表面接枝柠檬醛。图1(d)显示,接枝后的颗粒表面形貌较接枝前没有显著区别,保持了原有的粒径大小与六面体结构。




图1 IRMOF-3与IRMOF-3-C的SEM图Fig.1 SEM images of IRMOF-3 and IRMOF-3-C
2.2 IRMOF-3与IRMOF-3-C的晶型分析
采用XRD对水热法、表面活性剂法和醋酸锌法合成的IRMOF-3进行了晶体学研究,结果见图2。可以看出,3种方法合成的颗粒的晶型与模拟的IRMOF-3的出峰位置基本相同,表明其晶型结构一致。接枝柠檬醛后,IRMOF-3-C的XRD出峰位置基本无变化,表明接枝柠檬醛的过程中溶剂与催化剂未破坏IRMOF-3的晶型结构。

图2 IRMOF-3与IRMOF-3-C的XRD图谱Fig.2 XRD patterns of IRMOF-3 and IRMOF-3-C
2.3 IRMOF-3与IRMOF-3-C的化学结构分析

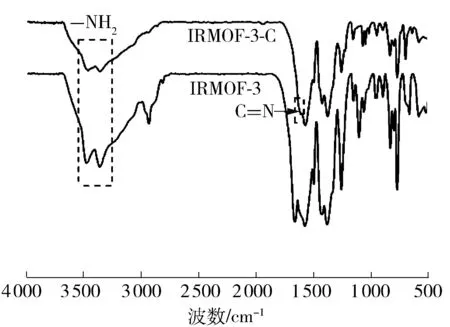
图3 IRMOF-3与IRMOF-3-C的红外谱图Fig.3 FT-IR spectra of IRMOF-3 and IRMOF-3-C
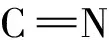
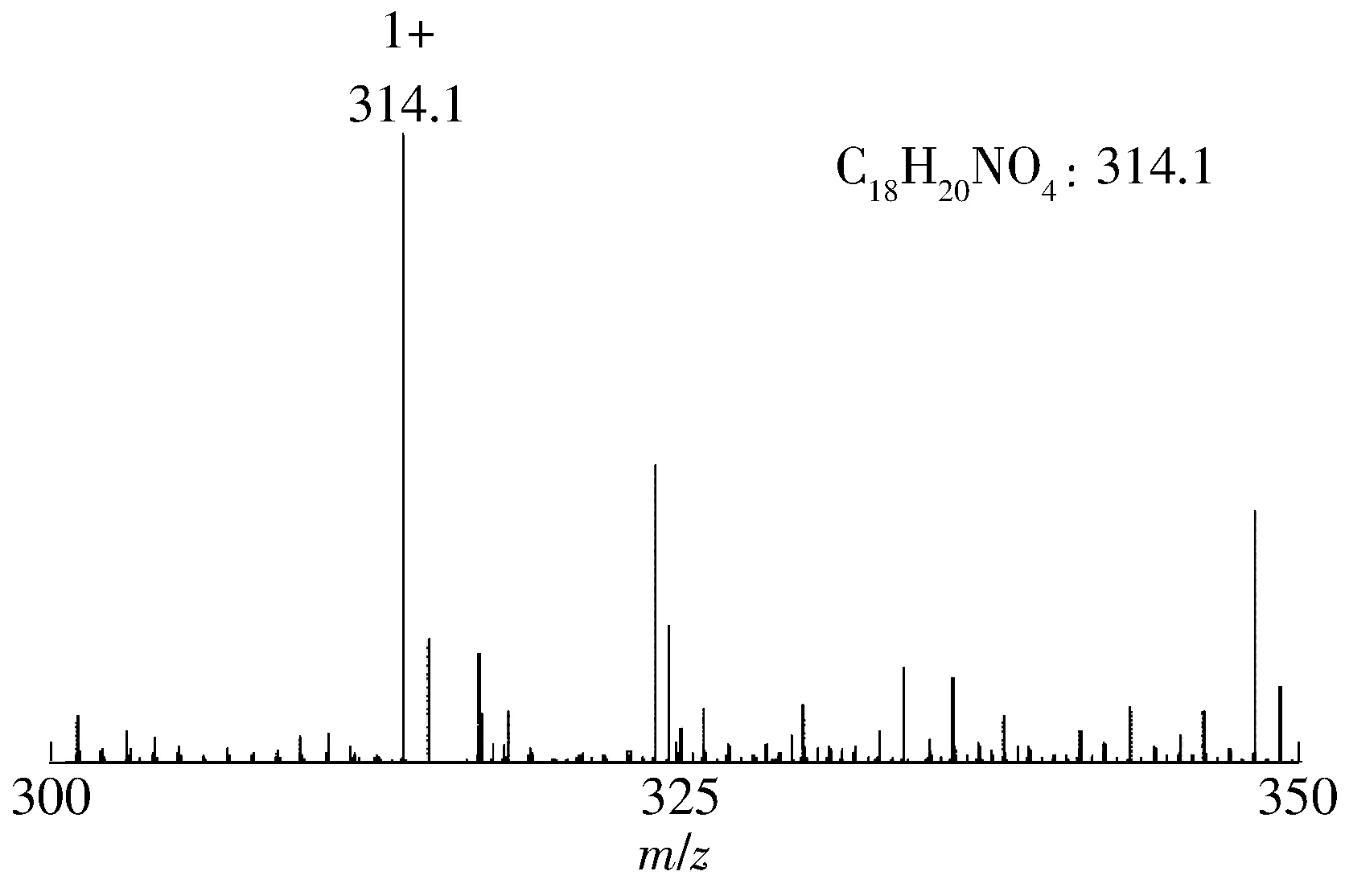
图4 IRMOF-3-C的电喷雾质谱图Fig.4 ESI-MS spectrum of IRMOF-3-C
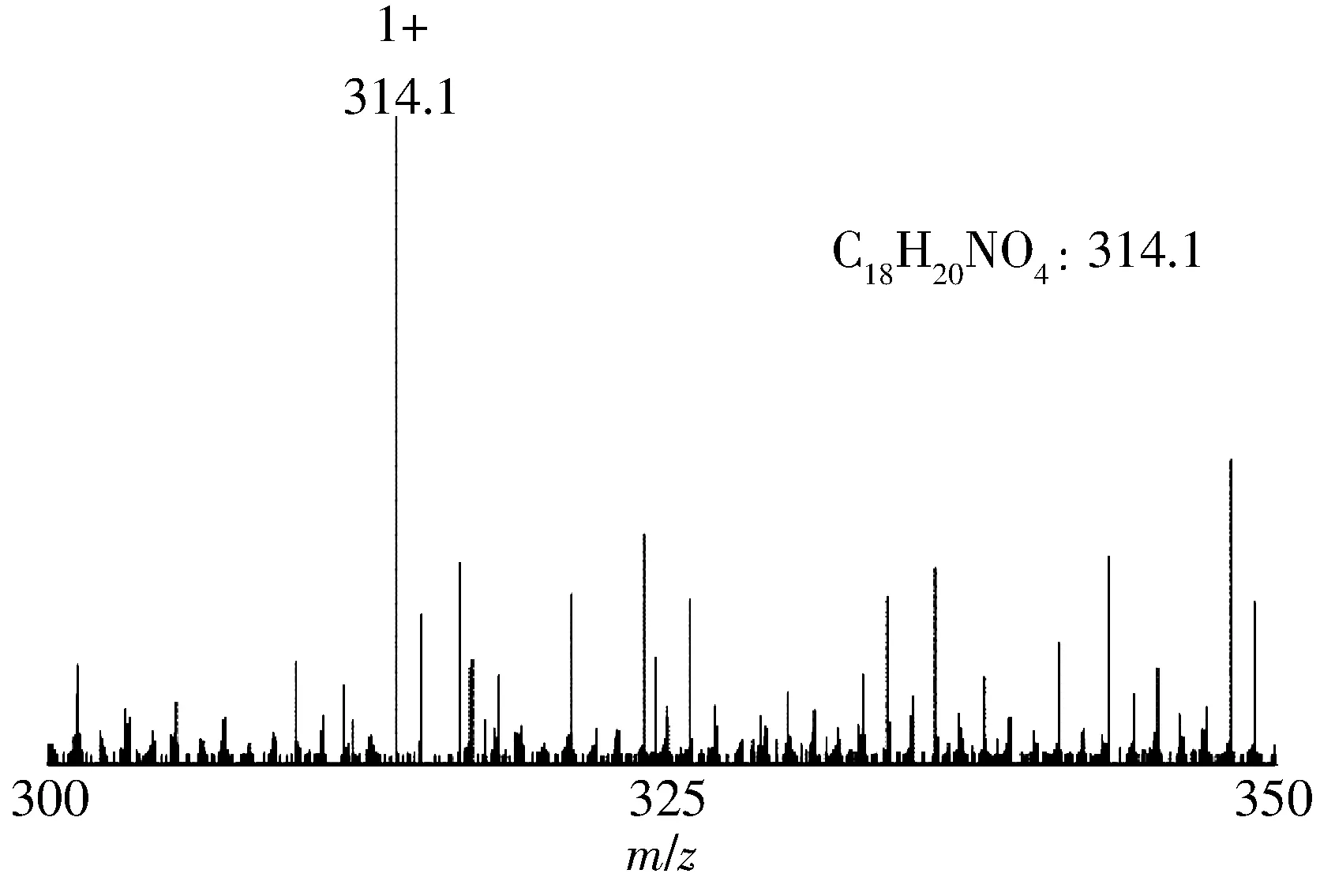
图5 室温放置7 d后IRMOF-3-C的电喷雾质谱图
Fig.5 ESI-MS spectrum of IRMOF-3-C after stored for 7 days at room temperature
2.4 抗菌性能
选择大肠杆菌(革兰氏阴性菌)与金黄色葡萄球菌(革兰氏阳性菌)为实验菌株来评价柠檬醛、IRMOF-3与IRMOF-3-C的抗菌性能,结果(见图6和7)显示,与柠檬醛相比,IRMOF-3-C表现出较强的抑菌能力,这主要是因为柠檬醛不溶于水,在水中分散性极差且易挥发,影响了其抗菌能力。而IRMOF-3-C通过席夫碱键接枝柠檬醛,增加了柠檬醛的分散性,并且席夫碱键对酸敏感,可以在酸性环境下断裂,使得柠檬醛中的醛基从IRMOF-3上恢复并释放。细菌的生长会形成微酸环境[19,21],在抗菌过程中IRMOF-3-C一方面通过酸响应释放柠檬醛抗菌,另一方面通过Zn2+的金属位点抗菌[14,22],从而增强了抗菌效果。细菌在IRMOF-3-C溶液中培养12 h后的SEM形貌观察结果也显示,大肠杆菌的菌体凹陷结构坍塌细胞壁被破坏(见图8(a)),金黄色葡萄球菌的菌体也呈干瘪状态且细胞壁表面出现明显的裂痕(见图8(b));反之,与在生理盐水中培养的细菌对照(见图8(a)和8(b)右下角插图),大肠杆菌和金黄色葡萄球菌均呈饱满的形态,表面的细胞壁致密无裂痕。据此推断,在细菌培养环境下,柠檬醛与Zn2+从IRMOF-3-C上释放,两者作用于细菌细胞壁,使其破损而起到杀菌作用(如图9所示)。而IRMOF-3-C抗金黄色葡萄球菌的效果低于大肠杆菌,是因为革兰氏阳性菌的细胞壁较厚、组织紧密坚固,而柠檬醛与金属离子是通过破坏细胞壁来发挥杀菌作用[23- 25]所致。
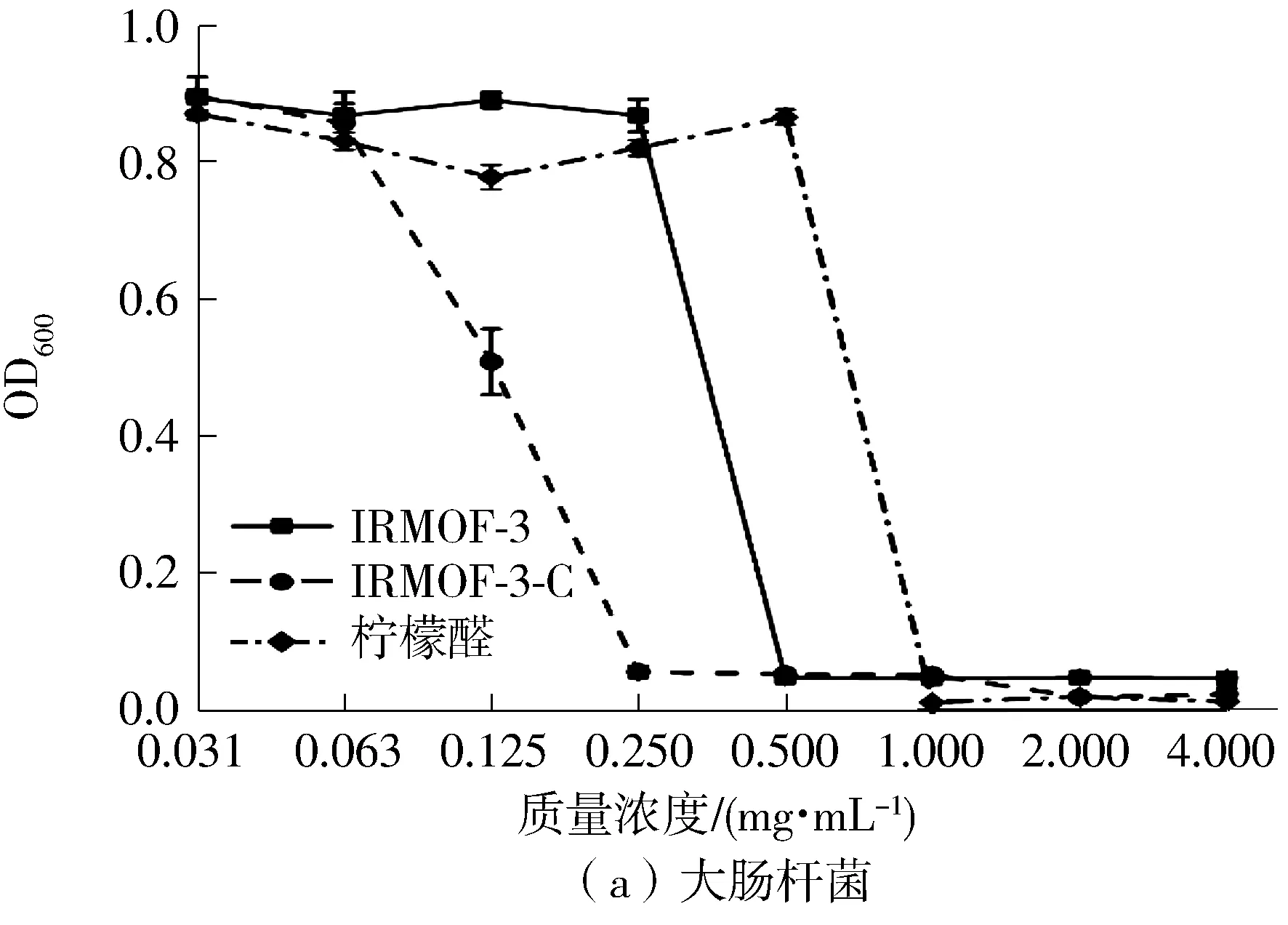
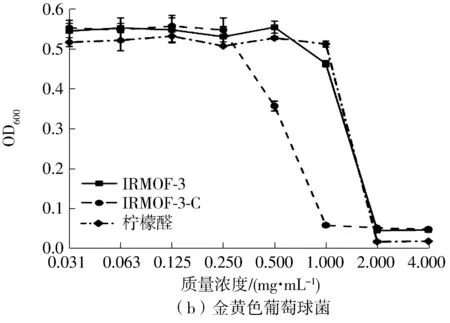
图6 柠檬醛、IRMOF-3与IRMOF-3-C对大肠杆菌与金黄色葡萄球菌的OD600测定结果
Fig.6 OD600values of citral,IRMOF-3 and IRMOF-3-C againstEscherichiacoliandStaphylococcusaureus

图7 柠檬醛、IRMOF-3与IRMOF-3-C对大肠杆菌与金黄色葡萄球菌的MBC测定
Fig.7 MBC determination of citral,IRMOF-3 and IRMOF-3-C againstEscherichiacoliandStaphylococcusaureus
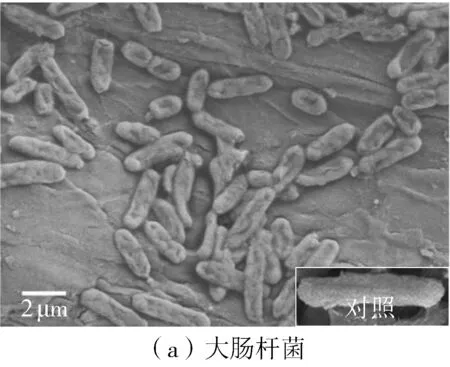

图8 大肠杆菌与金黄色葡萄球菌在IRMOF-3-C和生理盐水中培养12 h后的SEM照片1)
Fig.8 SEM images ofEscherichiacoliandStaphylococcusaureusafter being cultured in IRMOF-3-C and saline solutions for 12 h,respectively
1)各小图右下角插图为在生理盐水中培养12 h后的照片
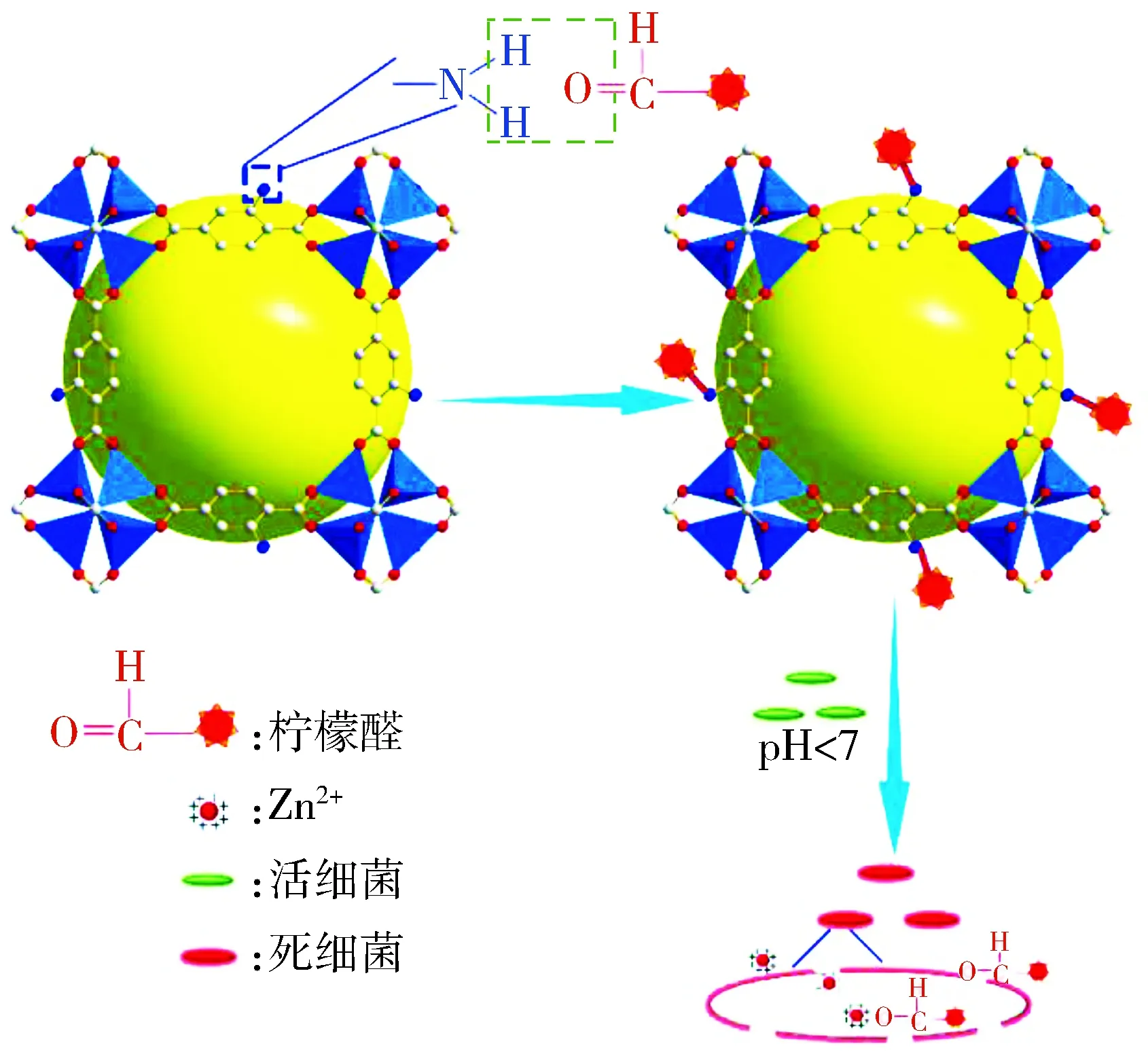
图9 IRMOF-3 接枝柠檬醛的抗菌机理示意图
Fig.9 Schematic drawing of the antibacterial mechanism of IRMOF-3 grafted with citral
3 结语
文中探讨了水热法、表面活性剂法与醋酸锌法合成的IRMOF-3颗粒的形貌结构,并采用醋酸锌法一步合成了纳米级的IRMOF-3。利用柠檬醛上的醛基与IRMOF-3的有机配体2-氨基对苯二甲酸上的氨基发生的席夫碱反应,形成了具有酸响应功能的席夫碱键,提高了柠檬醛的稳定性。金黄色葡萄球菌与大肠杆菌的MIC与MBC测试结果显示,IRMOF-3-C的抗菌效果优于IRMOF-3,这可能是由于细菌生长的微酸环境导致席夫碱键断裂,释放出柠檬醛,从而提高了材料的抗菌性。文中结果为改善柠檬醛稳定性、提高其抗菌适用性以及研发高性能抗菌材料提供了新的思路。
