药桑叶多糖的脱蛋白工艺与抗氧化活性研究
2020-05-29杨斌旺刘平古刘龙飞刘晋文崔汉钊汪河滨
杨斌旺,刘平古,刘龙飞,刘晋文,崔汉钊,汪河滨
(1.塔里木大学生命科学学院,新疆阿拉尔843300;2.新疆生产建设兵团南疆化工资源有效利用工程实验室,新疆阿拉尔843300)
药桑(Morus nigra L.)属半栽培半野生资源,在植物分类学上属桑科(Moraceae)桑属(Morus L)黑桑种[1],分布于新疆南疆地区的一种古老树种,具有独特药用价值。药桑叶中含有丰富的黄酮、生物碱、多糖、蛋白质等物质[2-4],其中多糖是药桑叶中的主要活性成分之一,研究报道证实药桑叶多糖具有明显的降血糖、抗肿瘤、降血脂、抗氧化等功效[5-10]。
药桑叶多糖是极性极大的大分子物质,用水或稀碱提取的多糖常含有蛋白质,采用乙醇沉淀多糖时蛋白也同时沉淀出来,因此纯化多糖时首先要去除蛋白质。Sevage法是目前脱蛋白常采用的方法之一,但该法脱蛋白效率低,次数多,多糖的损失率大[11-13],因此有必要对其脱蛋白工艺进行优化。本研究在单因素试验基础上采用正交试验方法确定药桑叶多糖Sevage法除蛋白的最佳工艺条件,并进行多糖DPPH自由基抗氧化活性试验,以期为药桑叶多糖在药品和功能食品方面的高效开发与综合利用提供理论参考。
1 材料与方法
1.1 材料与试剂
药桑叶:于2018年6月采自新疆阿克苏地区库车县;D-无水葡萄糖标准品:上海源叶生物科技有限公司;牛血清白蛋白标准品:北京索莱宝科技有限公司;考马斯亮蓝G-250标准品:上海康德生物科技有限公司。正丁醇、石油醚、苯酚、磷酸:天津永晟精细化工有限公司;硫酸:天津市北联精细化学品开发有限公司;无水乙醇、氯仿:天津市致远化学试剂有限公司,均为分析纯试剂。
1.2 仪器与设备
CP224C电子分析天平:奥豪斯仪器(上海)有限公司;GZX-9240MBE电热恒温鼓风干燥箱:上海博讯实业有限公司医疗设备厂;德国Heidolph Hei-VAP旋转蒸发仪;DZKW-S-6电热恒温水浴锅:北京市光明医疗仪器有限公司;S54型紫外分光光度计:上海棱光技术有限公司;TDZ4-WS台式低速离心机:湖南湘仪实验室仪器开发有限公司;LGJ-10C冷冻干燥机:北京四环科学仪器厂有限公司。
1.3 方法
1.3.1 药桑叶粗多糖的提取
药桑叶→粉碎过筛→乙醇脱色、脱脂→热水浸提→离心、抽滤→滤液→醇沉→冷冻干燥→药桑叶粗多糖[14-15]
1.3.2 药桑叶粗多糖脱蛋白
称取药桑叶粗多糖500 mg置于200 mL容量瓶中,加水溶解并稀释至刻度摇匀,得2.5 mg/mL的储备溶液,备用。量取定量药桑叶粗多糖溶液,分别与不同体积的Sevage试剂(预先配置好的体积比为4∶1的氯仿-正丁醇溶液)混合、振摇,将混合液置于离心机中,调节至4 000 r/min,离心10 min。离心后,除去下方的有机溶剂和交界处的变形蛋白质,重复上述操作几次,即得到脱蛋白后的药桑叶多糖,冷冻干燥,备用。
1.3.3 多糖含量测定
多糖含量的测定采用苯酚硫酸法[16-17]。称取105℃干燥至恒重的D-无水葡萄糖10 mg置于100 mL容量瓶中,加水溶解并稀释至刻度摇匀,得0.1 mg/mL葡萄糖标准液,作为对照溶液,备用。量取6.3 mL 80%的苯酚溶液转移至100 mL容量瓶中,加蒸馏水至刻度配置成5%苯酚溶液,摇匀后放置于棕色试剂瓶中(现配现用)。分别吸取葡萄糖标准液 0、0.6、0.8、1.0、1.2、1.4、1.6 mL,用水补至2 mL,依次加入5%苯酚溶液1.0 mL,然后加入3.0 mL的浓硫酸溶液,摇匀,沸水浴30 min后,冷却至室温(25℃左右)。不加标准葡萄糖溶液为空白,测定波长为490 nm处的吸光度值。以纵坐标为吸光度值(A),以横坐标为葡萄糖浓度(C)绘制葡萄糖标准曲线。得到的回归方程A=26.355C-0.017 7,R2=0.997 6。在0~0.03 mg/mL范围内具有良好的线性关系。药桑叶多糖含量测定:吸取2 mL多糖水溶液测定其吸光度,根据回归方程计算其浓度。多糖的损失率计算公式如下:

1.3.4 蛋白质含量测定-考马斯亮蓝法(Bradford法)
蛋白质含量的测定采用考马斯亮蓝法(Bradford法)[18]。称取牛血清蛋白5 mg,加入蒸馏水溶解,定容至5 mL的容量瓶中,吸取定容好的溶液1 mL,用蒸馏水稀释定容到10 mL容量瓶中,即制成0.1 mg/mL的标准溶液,备用。称取0.01 g的考马斯亮蓝G-250,溶于90%乙醇中,加入10 mL的85%(m/v)的磷酸,最后用蒸馏水定容至100 mL,摇匀即得到考马斯亮蓝储备液。精确吸取牛血清蛋白标准溶液0.1、0.2、0.3、0.4、0.6、0.8 mL加入试管中,分别加水定容至1.0 mL,以不加蛋白标准溶液作为空白组,然后加入5.0 mL考马斯亮蓝染液,将各个试管中的溶液纵向倒转混匀,室温(25℃左右)5 min后,测定波长595 nm处的吸光光度值。以横坐标为标准蛋白质浓度(C),以纵坐标为吸光度(A),绘制蛋白质标准曲线。得到的回归方程为A=42.349C+0.013 5,R2=0.983 9。在 0~0.015 mg/mL 范围内具有良好的线性关系。计算蛋白质除去率公式如下:

1.4 单因素试验对药桑叶多糖除蛋白效率的影响
1.4.1 Sevage试剂用量对药桑叶多糖除蛋白效果的影响
固定脱蛋白时间为20 min,脱蛋白次数为3次,考察多糖溶液与Sevage试剂的体积比分别为1∶1、1∶2、1∶3、1∶4时,对药桑叶多糖除蛋白效果的影响,然后测定多糖损失率和蛋白除去率。
1.4.2 脱蛋白时间对药桑叶多糖除蛋白效果的影响
固定多糖溶液与Sevage试剂的体积比为1∶2,脱蛋白次数为3次,考察振摇时间分别为10、20、30、40 min时,对药桑叶多糖除蛋白效果的影响,然后测定多糖损失率和蛋白除去率。
1.4.3 脱蛋白次数对药桑叶多糖除蛋白效果的影响
固定多糖溶液与Sevage试剂的体积比为1∶2,脱蛋白时间为20 min,考察脱蛋白次数分别为2、3、4、5次时,对药桑叶多糖除蛋白效果的影响,然后测定多糖损失率和蛋白质除去率。
1.5 药桑叶粗多糖脱蛋白正交试验
在单因素试验的基础上,对多糖溶液与Sevage试剂的体积比(A)、脱蛋白时间(B)、脱蛋白次数(C)3个因素进行正交试验,设计正交表,考察3个因素对药桑叶多糖除蛋白效果的影响,从而确定最佳除蛋白工艺条件。正交试验因素水平设计见表1。

表1 正交试验因素水平表Table 1 Factors level table of orthogonal test
1.6 药桑叶多糖体外抗氧化活性测定
阳性对照组:取抗坏血酸(VC)适量,用95%的乙醇定容置5 mL的容量瓶中,再配置成浓度分别为0.05、0.1、0.15、0.2 mg/mL 的溶液。
试验组:取等量相同浓度脱蛋白前、后的药桑叶多糖溶液,用95%的乙醇定容到5 mL的容量瓶中,配置成浓度分别为 0.05、0.1、0.15、0.2 mg/mL的样品溶液。
以不同浓度VC溶液做阳性对照组,取0.2 mmol/L的DPPH溶液和溶液样品各2.0mL加入到试管内,混匀后,在恒温(28℃)条件下,放置到避光处,反应30 min,空白对照为蒸馏水,在517 nm处测定吸光度[19-20]。每个样品做3次平行试验。DPPH自由基清除率计算公式如下:
DPPH 自由基清除率/%=[1-(A1-A2)/A0]×100
式中:A0为95%乙醇与DPPH溶液反应后的吸光度值;A1为含不同浓度样品与DPPH溶液反应后的吸光度值;A2为不同浓度下样品溶液与95%乙醇溶液取2 mL的吸光度。
2 结果与分析
2.1 多糖溶液与Sevage试剂的体积比对药桑叶多糖除蛋白效果的影响
Sevage试剂用量对脱蛋白效果的影响见图1。

图1 Sevage试剂用量对脱蛋白效果的影响Fig.1 Effect of Sevage reagent dosage on deproteinization
从图1可知,随着多糖溶液与Sevage试剂的体积比减小(即Sevage试剂用量的增加),多糖损失率增加。多糖溶液与Sevage试剂的体积比为1∶2时,蛋白除去率较好,蛋白除去率达到75.47%,多糖损失率达到20.96%。综合蛋白除去率和多糖损失率考虑,选取最佳多糖溶液与Sevage试剂的体积比为1∶2。
2.2 脱蛋白时间对药桑叶多糖除蛋白效果的影响
脱蛋白时间对脱蛋白效果的影响见图2。
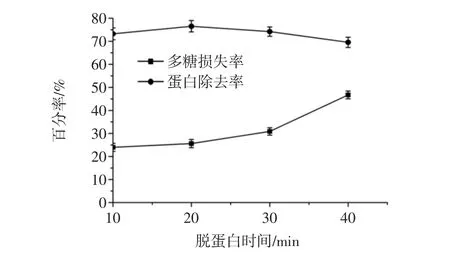
图2 脱蛋白时间对脱蛋白效果的影响Fig.2 Effect of deproteinization time on deproteinization
从图2可知,随着脱蛋白时间的增加,多糖损失率越增加。脱蛋白时间为20 min时,蛋白的除去率最高,蛋白除去率可达76.54%,在10 min时多糖损失率最少,达到21.81%。综合蛋白除去率和多糖损失率考虑,选取脱蛋白时间为20 min。
2.3 脱蛋白次数对药桑叶多糖除蛋白效果的影响
脱蛋白次数对脱蛋白效果的影响见图3。
从图3可知,随着脱蛋白次数的增加,多糖损失率增加。在脱蛋白次数为3次时,蛋白质除去率最高,可达74.92%。综合蛋白除去率和多糖损失率考虑,选取最佳脱蛋白次数为3次。
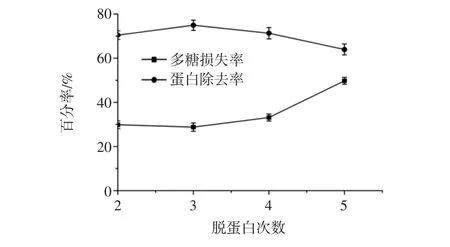
图3 脱蛋白次数对脱蛋白效果的影响Fig.3 Effect of the number of deproteinization on the deproteinization effect
2.4 正交试验优化结果
将药桑叶粗多糖的除去率的权重系数设为0.5,药桑叶粗多糖脱蛋白后多糖含量的权重系数也设为0.5,进行统计分析。综合评分H=0.5X×100/74.55+0.5Y×100/88.98[21]。
式中:X为药桑叶粗多糖的除去率,%;Y为药桑叶粗多糖脱蛋白后多糖含量,%。
正交试验见表2,方差分析见表3。
由正交试验结果的最优脱除条件为A2B1C1,即多糖溶液与Sevage试剂体积比为1∶2、脱蛋白时间为20 min、脱蛋白次数为3次。在所选试验范围,各因素对药桑叶多糖除蛋白效率的影响大小是C(脱蛋白次数)>B(脱蛋白时间)>A(多糖溶液与Sevage试剂的体积比)。根据方差分析,脱蛋白次数对药桑叶粗多糖除蛋白效率极为显著,脱蛋白时间较为显著。在此工艺优化条件下,重复试验3次,结果测定出平均蛋白质除去率为76.54%,多糖损失率为20.80%,综合评分为95.55%。
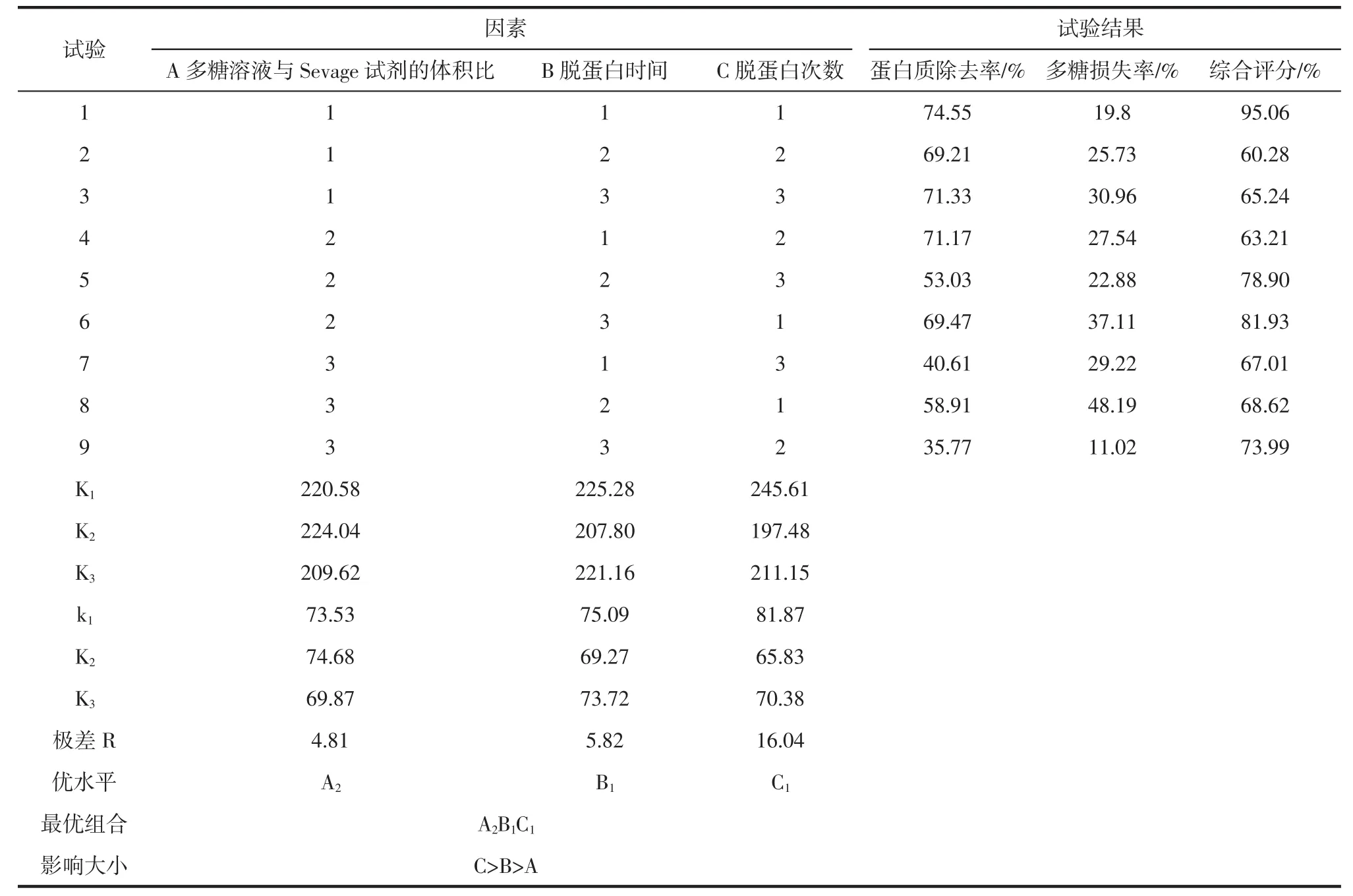
表2 正交试验Table 2 Orthogonal test
2.5 抗氧化活性结果
脱蛋白前、后的药桑叶多糖溶液和VC溶液对DPPH自由基的清除率见图4。
经Origin8.5进行线性拟合得到图4,根据图4知,药桑叶多糖溶液浓度在一定范围内,其对DPPH自由基的清除能力清除能力随着样品浓度的增加而显著增加。同浓度VC溶液和脱蛋白前后的药桑叶多糖溶液清除DPPH自由基的能力对比可得出:VC>脱蛋白后>脱蛋白前。当溶液浓度达到1.2 mg/mL时,脱蛋白前、后的药桑叶多糖对DPPH·清除率分别达到72.56%、84.78%,脱蛋白后的清除效果明显增加,说明脱蛋白后的药桑叶多糖具有良好的体外抗氧化能力。
3 结论
本次试验利用单因素方法研究了不同影响因素对Sevage法脱除蛋白质效果的影响,Sevage试剂用量采用正交试验方法确定了Sevage法最佳除蛋白工艺为:多糖溶液与Sevage试剂的体积比为1∶2、脱蛋白时间20 min、脱蛋白次数3次,蛋白质除去率为76.54%,多糖损失率为20.80%。在一定浓度范围内,DPPH自由基试验中发现药桑叶多糖表现出良好的抗氧化活性,为高效开发药桑叶多糖药品及功能食品奠定了基础。
