降脂模型研究进展
2020-05-26胡乃华余琳媛龚莉虹代旭阳李芸霞
王 成,胡乃华,余琳媛,龚莉虹,代旭阳,李芸霞
(成都中医药大学 药学院,教育部中药材标准化重点实验室,中药资源系统研究与 开发利用省部共建国家重点实验室培育基地,成都 611137)
随着全球人民生活水平的提高和饮食习惯的改变,高脂血症(hyperlipidemia,HLP)已逐渐成为严重危害全人类身体健康的“第一杀手”,且发病率呈逐年上升趋势[1]。目前,HLP及其并发症占据了全球死亡率的50%[2]。在中医古籍中,虽然没有对“高脂血症”这病症的明确记载,但早在秦汉时期的《黄帝内经》中已有“脂者”、“油脂”、“脂膜”等关于脂的相关论述,且还用“膏人”、“肥人”等词来形容血浆脂质过高的人[3]。古代中医认为,HLP发生的原因是五脏六腑的气化、运输、疏泄、宣发等生理功能失调,致使体内津液集聚,痰湿化生,流注经脉,渗入血中[4]。在现代医药领域,HLP又称为脂质代谢紊乱,是血液中任何或所有血脂和/或脂蛋白水平异常升高,是一种最常见的血脂异常形式。有研究表明,HLP是导致脂肪肝、动脉粥样硬化、冠心病、糖尿病、脑梗死等多种疾病的首要病因[5]。
相比于降脂作用快速确切的西药,我国传统中药治疗HLP有着独特的优势和广阔的发展前景。据不完全统计,目前已知的具有降血脂功效的中草药有100多种,中医临床上用于治疗HLP的中成药有200余种[6],由此可见,运用我国中医药理论对改善和治疗HLP有着广阔的前景。但是,因降脂单味中药、复方和中成药等具有分类庞杂、种类繁多和成分复杂的特点,依靠单一的降脂模型和研究技术很难对发挥作用的有效化学成分及具体降血脂的机制进行全方面、深层次的研究。HLP的预防和治疗已成为亟待解决的难题之一,高脂模型对于脂代谢性疾病以及HLP继发的心脑血管性疾病的研究具有重大意义[7]。因此,建立一个完美的、理想的高脂模型是筛选降脂中药和研究HLP中医发病机理的关键因素之一。目前国内外已建立了多种高脂模型,主要分为高脂细胞模型、高脂哺乳动物模型和高脂斑马鱼模型三种。本文就针对当今常用的三种高脂模型进行归纳总结,为今后进一步探索HLP的发病机制和筛选有效的降脂中药提供一定的选择依据。
1 高脂细胞模型
1.1 HepG2细胞模型
人源性肝癌细胞系(human hepatocellular liver carcinoma cell line,HepG2)因其具有生长周期短、高分化性、分化稳定性和长生不老性等特点,被广泛应用于抗氧化、降脂保肝、抗肝癌和抗脂肪变性等研究[8]。又因其保留了完整的与人类生物代谢相关的酶,可以正常表达与脂质代谢相关的mRNA转录水平及蛋白水平,目前也被广泛用来评价中药的降脂活性。
郝正亮等[9]利用1.0×10-5mol/L的磷酸三苯酯(triphenyl phosphate,TPP)诱导HepG2细胞,TPP作用于HepG2细胞24 h后用脂质分析试剂盒和油红O脂肪染色对其进行验证。结果显示,经TPP作用后,显著升高甘油三酯(triglyceride,TG)的含量,增加细胞中脂滴的堆积面积,成功诱导高脂HepG2细胞模型。还有研究表明[10],氧化性低密度脂蛋白(oxidation low density lipoprotein,Ox-LDL)可以通过升高载脂蛋白AI(apolipoprotein AI,apoAI)和降低载脂蛋白B(apolipoprotein B,apoB)的表达而快速使HepG2细胞在48 h建立成高胆固醇模型,与正常组相比,模型组细胞内的裂解总胆固醇(total cholesterol,TC)、裂解游离胆固醇(free cholesterol,FC)、上清TC和上清FC均有显著性差异,表明成功建立高胆固醇HepG2细胞模型。此外,李玉平等[11]对Ox-LDL诱导的高胆固醇HepG2细胞模型的最佳浓度和最佳诱导时间进行了摸索。结果表明,50 mg/mL的Ox-LDL诱导HepG2细胞48 h是造高胆固醇模型的最佳条件。但是,由于Ox-LDL毒性较大,容易对细胞造成凋亡等不可逆转的损伤[12],目前人们更多的选择游离脂肪酸中含量最多的油酸来诱导HepG2细胞脂肪堆积模型。在油酸的干预下,HepG2细胞中SREBP-1c过度表达,p-AMPK蛋白受到抑制,致使细胞内TC和TG显著性增加[13],成功建立HepG2细胞脂肪堆积模型。
1.2 L02细胞模型
因HepG2细胞来源于人肝胚胎肿瘤细胞,与正常人肝细胞有一定的差异,将其用于建立降脂中药筛选模型存在较大的分歧。与此同时,另一传代株人正常肝细胞进入人们的视野。L02细胞是一种来自于正常人胚胎肝组织且能够贴壁生长的一种细胞,能完全模拟人类脂质代谢过程。因此,用其复制的高脂细胞模型较HepG2细胞更具可行性和说服性。
殷锦锦等[14]探讨使用游离脂肪酸(free fatty acids,FFA,棕榈酸和油酸混合物)来建立L02细胞脂肪变性模型。方法是往1640培养基中添加FFA共同培养L02细胞24 h,后采用油红O染色对细胞内脂滴形态进行观察,同时检测TG、丙二醛(malondialdehyde,MDA)以及细胞凋亡率来鉴定模型是否成功。结果显示,高脂模型组细胞内有大量脂滴形成,TG显著性升高,MDA含量和细胞凋亡率均没有明显增高,成功诱导高脂L02细胞模型。还有学者对FFA里油酸和棕榈酸的比例及其它最佳条件进行了系统性研究。Gómez-Lechón等[15]经全面研究发现,当FFA中油酸和棕榈酸的比例为2∶1时,最适合用来建立高脂L02细胞模型。但是,随着对FFA的深入研究,一些学者发现FFA是一种毒性特别强的二性分子,容易引起生物膜的损伤[16],后来有学者建议用毒性更小的脂肪乳剂来建立高脂L02细胞模型。此外,袁勇等[17]还探索出当造模液中脂肪乳剂为1.0 mL/L,造模时间为48 h时,是建立L02细胞非酒精性脂肪肝(nonalcoholic fatty liver disease,NAFLD)模型的最佳条件,适用于更深入和更全面的探索HLP和NAFLD的发病机制,筛选出防治HLP和NAFLD的有效中药。
1.3 3T3-L1细胞模型
3T3-L1前脂肪细胞是G.J.Todaro从17~19 d Swiss系小鼠胚胎里3T3细胞中分离得到。用该细胞进行脂质代谢方面的研究时,需要利用适当的诱导剂对其进行刺激,使其定向分化成充满脂滴的脂肪细胞才能进行下一步的实验探索。诱导分化前3T3-L1前脂肪细胞间质稀少,体积小,呈梭形,包浆中不含有TG的油滴[18]。诱导分化后则变成成熟的脂肪细胞,贴壁完好,楞角分明,大量的TG脂滴积聚于细胞核的周围。3T3-L1脂肪细胞是目前国际上公认的可用于研究HLP、肥胖以及筛选降脂中药和抗肥胖药物的细胞模型[19]。
肥胖是一个全球性的健康问题,它被认为是HLP、高血压和动脉粥样硬化(atherosclerosis,AS)等心血管疾病发生的危险因素。有研究发现,与脂质代谢相关的基因为肥胖等代谢综合征的药物治疗提供了丰富的潜在靶点,Roh等[20]通过在DMEM培养基中加入诱导剂(10μg/mL胰岛素,2.5μmol/L地塞米松和0.5 mmol/L 3-异丁基-1-甲基黄嘌呤),诱导3T3-L1细胞分化成脂肪细胞,成功筛选出具有抗肥胖活性的植物提取物。此外,Lee等[21]在含有高葡萄糖、10%胎牛血清和青霉素/链霉素等的DMEM培养基中,加鸡尾酒培养3T3-L1细胞48 h,也使其成功诱导分化成脂肪细胞。
此外,还有一些细胞也可以用来建立高脂细胞模型。如1954年从非恶性的人体组织中建立的具有无限传代特点的人肝Changliver细胞、小鼠巨噬RAW264.7细胞株、来自大鼠肝的肝BRL细胞、人单核/巨噬细胞株THP-1、奶牛肝细胞和草鱼肝细胞等。
常用高脂细胞建模方法的比较见表1。
2 高脂哺乳动物模型
2.1 大鼠
因具有成本低、易于饲养、抗病力强、实验操作简单和模型稳定性好等优点,大鼠已成为目前国内外研究人体脂质代谢使用率最高的一种动物。此外,大鼠所含血液丰富,一次采血即可对多项指标进行检测,可以较好的对脂质的吸收、合成和分解等代谢过程进行深入研究。
目前,在诱导大鼠形成高脂模型来进行血脂代谢紊乱的实验中,喂养高脂饲料或高脂高胆固醇饲料是普遍选取的方法。Moselhy等[22]在普通饲料中添加了2%的胆固醇和0.4%的胆酸钠制作成高脂高胆固醇饲料,用于评价麦角甾醇联合烟酸对高脂饮食(high fat diet,HFD)大鼠的潜在降脂和降胆固醇作用。结果显示,HFD组大鼠TC、TG、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDLc)、极低密度脂蛋白胆固醇(very low density lipoprotein cholesterol,VLDL-c)以及致动脉粥样因子水平均明显高于正常组,高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-c)水平低于正常组。麦角甾醇或烟酸的灌胃组,TC、TG、LDL-c均比模型组低。研究表明烟酸和麦角甾醇可以预防高胆固醇血症和冠心病。然而,高TC的食物对大鼠并没有吸引力,甚至还易出现“厌食”的情况,以致于不能精确掌握每日进食量,进而影响实验结果准确性。因此,有的学者建议用灌胃高脂乳剂法替代高脂高胆固醇饲料饲养法,这样既可以避免进食的不一致性,还可以根据实际需求增减高脂成分的含量,缩短造模时间。此外,还有学者将与脂质代谢相关酶的活性物质作为复制高脂模型的材料。如灌胃铅可以显著性抑制细胞色素P450的活性,进而影响甾醇独立基团调控肝酶对脂质的代谢[23]。Liu等[24]通过对大鼠进行为期75 d的醋酸铅水溶液灌胃,成功研究了葛根素可以通过降低细胞在代谢过程中产生的活性氧簇,更新抗氧化酶活性,阐明葛根素对铅诱导的高脂血症和肝损伤的保护作用机制。

表1 常用高脂细胞建模方法Table 1 Common hyperlipidemia cell modeling method
2.2 小鼠
小鼠因价格便宜、易于饲养、造模成本低、血脂稳定和采样方便等优点,也被广泛运用于筛选降脂中药的实验研究中。但是,小鼠能采集的血量少,极大程度的限制了相关指标的检测。此外,小鼠血浆中不含血浆胆固醇酯转移蛋白[25](cholesteryl ester transfer protein,CETP),对饮食中的胆固醇和高糖无反应,很难继续发展为AS,因此,只能单纯的用于HLP研究。
近年来,C57BL小鼠和敲除了与脂蛋白代谢相关蛋白的小鼠被大量应用于复制高脂模型。与建立高脂大鼠模型相似,建立高脂小鼠模型时,高脂饲料喂养法和灌胃法也是常用方法。此外,自从第一个转基因小鼠制备成功,转基因动物模型也被广泛用于HLP和AS的研究。长期用高脂饲料喂养转基因C57BL/6J小鼠,可导致血脂异常、肥胖和2型糖尿病等疾病[26]。Saravanan等[27]连续用高脂饲料(脂肪含量35.8%)对C57BL/6J小鼠进行为期70 d的造模饲养,利用此模型评估一种单萜酚类化合物百里酚对高脂血症、2型糖尿病的作用。结果表明,40 mg/kg的百里酚具有良好的抗高脂血症、高血糖的作用,可保护C57BL/6J小鼠免受HFD的侵袭。还有学者发现连续28 d给小鼠灌胃1,3-二氯丙醇,可以通过调节腺苷酸活化蛋白激酶(AMP-activated protein kinase,AMPK)信号通路来诱发HLP。Lu等[28]通过此种方法成功复制高脂小鼠模型,且还发现HDL-c的降低程度与1,3-二氯丙醇呈一定的剂量依耐性。载脂蛋白E(apolipoprotein E,ApoE)是一种多态性蛋白,能调节脂代谢有关酶的活性,参与脂蛋白的转化和代谢过程。ApoE主要存在于乳糜颗粒、极低密度脂蛋白(very low density lipoprotein,VLDL)和部分HDL中,对ApoE基因多态性的研究也是目前医学研究的热点之一。ApoE变异或者缺失,会导致血脂代谢紊乱和AS等疾病。Patterson等[29]利用基因靶向技术,制备了ApoE-/-转基因小鼠,用于研究瑞舒伐他汀对ApoE基因缺失小鼠高脂血症深静脉血栓的影响。与正常小鼠相比,ApoE-/-小鼠的TC升高4倍,TG升高2倍。在正常饮食下,即可形成高胆固醇血症,在高脂高胆固醇饮食下,可加速AS的病变发生。由此可见,利用基因靶向技术所制备的转基因小鼠可大大节约造模时间。
2.3 家兔
家兔的脂蛋白代谢与人类相似,血浆中具有丰富的CETP,不具有肝ApoB mRNA编辑活性[30],对外源性胆固醇吸收率高,血中脂质清除率低,是研究人类脂质代谢和AS最常用的动物模型,同时也是最早被用于复制HLP和AS模型的动物。又因家兔肝脂酶活性较低,不需要格外添加任何诱导剂,单纯饲喂高胆固醇饲料即可快速发展成HLP和AS,其TC在一个月可升高11.8倍,在两个月可升高17.7倍[31]。因此,家兔提供了一个独特的系统来研究膳食胆固醇对高胆固醇血症、AS和肝功能障碍的影响[32]。
相比于大鼠和小鼠,家兔对高胆固醇食物显得尤为敏感。大多数HLP和AS兔模型都是通过高脂饲料喂养所得到。Heikal等[33]采用HFD(含1%胆固醇)对雄性新西兰家兔喂养8周,成功造成高血脂家兔模型,用于研究非布索坦的抗高脂血症的作用及作用机制。基因敲除为研究脂质代谢提供了另一种制备兔模型的方法,但即便如此,ApoE-/-兔仍需要饲喂高胆固醇饲料才能诱导高脂血症。最近Lu等[34]使用CRISPR/Cas9系统锚定低密度脂蛋白受体(low density lipoprotein receptor,LDLR)外显子7,试图产生一种可自发形成HLP的LDLR-KO兔。结果显示,LDLR-KO兔在正常的饮食下均可自发性诱导高胆固醇血症和AS。提示LDLR-KO家兔可以作为研究高胆固醇血和AS的模型,用于模拟人类原发性高胆固醇血症,使心脑血管病的研究更加精确。
2.4 豚鼠
有研究表明[35],豚鼠的脂蛋白代谢与人类的代谢有显著的相似之处。与人类一样,豚鼠也是少数几种LDL-c含量最高的物种之一。其相似主要体现在LDL/HDL比值高、肝中游离胆固醇浓度高于酯化胆固醇、肝胆固醇合成、酯化和分解代谢很相似等[36]。豚鼠性情温顺,采血量大,对TC的敏感性高于大鼠[37]。此外,切除卵巢的豚鼠还可以较好地模拟绝经后女性的脂蛋白代谢[38]。
豚鼠对高脂饲料、高胆固醇饲料显得尤为敏感,通常在普通饲料中添加少量的胆固醇便可造成高胆固醇血症。Yang等[39]采用高脂饲料(添加5%的猪油和0.3%的胆固醇)饲喂豚鼠,14周后测定血脂、ApoB100、MDA、超氧化物歧化酶(superoxide dismutase,SOD)、一氧化氮含量。对主动脉粥样硬化病变进行组织学检查,结果显示,模型组TC、TG、LDL-c、ApoB100水平是对照组的9.45倍、6.01倍、12.72倍、14倍,模型组HDL-c相比与对照组显著降低72%,出现严重血脂异常,且模型组MDA含量高于对照组8.2倍,SOD活性降低60.8%,并伴有组织学改变和内皮功能障碍。由此可见,豚鼠也是一种比较理想的研究脂代谢的模型动物。
此外,用来复制高脂模型的动物还有长爪沙鼠[40]、金黄地鼠[41]、食蟹猴[42]、悬猴、鹌鹑、鸡、家鸭、beagle犬、五指山小型猪和鸽子等,研究者应根据实验需求选择合适的动物模型进行研究。
常用高脂哺乳动物模型的比较见表2。
3 高脂斑马鱼模型
斑马鱼是一种原产于南非地区的热带硬骨鱼,因其基因组序列与人类有着87%的高度相似性[43],体积小,胚胎透明,易于大规模饲养,繁殖能力强和实验周期短,被广泛作为高通量筛选药物的经典模型[44-45]。又因其血脂构成、脂质吸收、脂质代谢、器官和组织与人类基本一致,近年来被大量应用在与脂质代谢和脂质异常相关的疾病研究中,如HLP、糖尿病、脂肪肝、AS等,是研究单体中药降血脂作用的理想模式生物[46]。
3.1 斑马鱼幼鱼
Stoletov等[47]利用斑马鱼幼鱼身体透明、器官清晰可见和能够以高分辨率在体内对器官和生物过程进行非侵入性的可视化的特性,对活体高胆固醇血症斑马鱼幼鱼的血管脂质堆积、脂蛋白氧化和脂肪条纹的形成情况进行了实时的研究报道。该团队在高胆固醇饲料中添加一种红色的Cholesteryl BODIPY 576/589 C11活体荧光探针,用来牢固标
记幼鱼体内的胆固醇,以便在激光共聚焦显微镜下对活体斑马鱼中的胆固醇走向以及在血管壁内的沉积进行实时的动态观察。结果显示,诱导出稳定的红色荧光磷脂堆积、血管脂质大量沉积、脂肪条纹形成,表明高胆固醇血症模型成功建立。但是,由于这种活体荧光探针价格昂贵,容易猝灭,对实验设备要求较高、结果不稳定和重现性差,后来Zhou等[48]建立了一种可以快速高通量筛选降脂药物的斑马鱼高脂模型。该团队通过对5 dpf(days post fertilization,dpf)斑马鱼幼鱼喂养0.1%的蛋黄粉24 h和48 h,对斑马鱼尾静脉油红O染色,对其在解剖立体显微镜下成像所得到的图片进行定量分析,发现斑马鱼的肠道和血管中的脂质会随着时间的增加而堆积,快速建立了斑马鱼HLP模型,并且该团队利用这模型对几种常见的不同作用机制的降血脂药物进行了筛选和疗效评价。后来,余琳媛等[49]采用这种造模方法来筛选传统降脂中药制首乌中具有降脂保肝作用的有效化学成分。结果显示,大黄素能显著降低斑马鱼的死亡率,降低TG水平,可明显改善斑马鱼幼鱼肝脂质的沉积,由此推测制首乌中具有降脂作用的主要有效成分是大黄素。
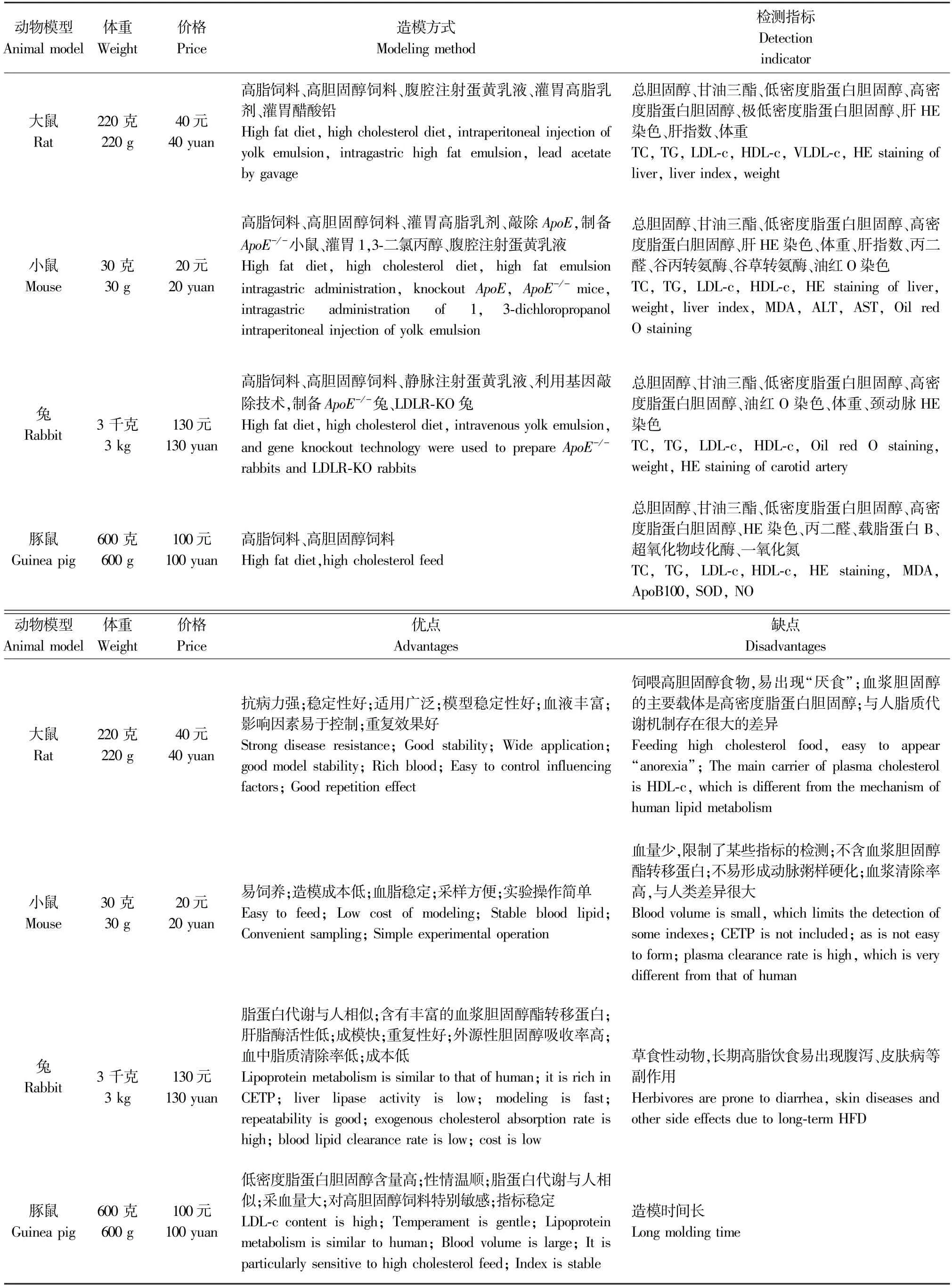
表2 常用高脂哺乳动物模型比较Table 2 Comparison of commonly used hyperlipidemia mammal models
3.2 斑马鱼成鱼
由于斑马鱼幼鱼HLP模型的检测指标大多都是通过油红O染色和活体荧光探针来反应,这些都是间接地反应血脂的相对变化,不能真实地反映出机体的脂质代谢情况,况且从斑马鱼幼鱼中提取血液也是不切实际的。但是,可以通过抽取斑马鱼成鱼的血浆来直接检测血脂的变化情况[50]。韩冰等[51]用含4%胆固醇饲料去喂养3月大的斑马鱼成鱼20 d,通过对肝进行油红O染色和测定血清TC、TG和LDL-c含量与空白组相对比,其结果显示高胆固醇组的血清TC、TG和LDL-c含量均有显著性升高,肝中出现大量的脂肪滴累积,表明成功建立高脂斑马鱼成鱼模型,为下一步研究和开发新的降血脂中药奠定基础。
高脂斑马鱼幼鱼和成鱼造模方法的比较见表3。
4 高脂模型在筛选降脂中药中的作用
长期高脂高胆固醇饮食会打破机体脂质吸收和消化之间的平衡关系,导致脂肪、胆固醇和复合糖类长期大量的在血管内壁上聚集和过度沉积,导致动脉壁增厚变硬,血管腔变窄,致使动脉内膜形成粥样斑块,影响血流速度,进而产生一系列更为严重的心血管疾病。因此,及早进行预防和筛选有效的降脂药是降低患者心血管事件发生的有效控制手段。目前对于HLP的治疗首选他汀类药物,但是如果长期服用调血脂西药,其以转氨酶升高为特征的肝损害和以肌酸激酶升高为特征的横机纹溶解等副作用会逐渐凸显出来。因此,一些天然产物,特别是我国具有悠久的历史和显著的疗效的传统降脂中药,因具有多靶点、多途径、多环节、疗效好、毒副小等的优点,可以很好地与西药作用的单一性相弥补而受到了格外的关注。因此,建立可用于筛选和研究降血脂中药的脂质代谢紊乱动物模型显得尤为重要。
现代中医认为,HLP的病因病机主要是恣食肥甘,痰浊淤阻引起。运用传统中药来预防和治疗HLP,主要是依据中医基础理论中的辨证论治,故筛选和研究降脂中药时需要根据其病因病机及证候选择不同的实验方法来复制高脂模型[52]。目前,已有很多学者通过不同的高脂模型筛选出具有调血脂作用的中药。如何首乌[49]、柴胡[53]、天麻[54]、虎杖[55]、决明子[56]等,具有降血脂、降血压、抗脂肪肝、抗AS等功效,可用于治疗高血压、HLP、AS等疾病。随着我国医疗技术的快速发展,我国对HLP的治疗不但可以从中医的证候表征入手,还可以结合现代中医药理论知识从基因蛋白水平治疗HLP。
理想的降脂模型不单单有助于筛选降脂中药和其机制的研究,还应该有助于HLP中医发病机理的研究,只有明白机理才能准确的选择相应的治法和药物。但是,我国暂时还没有大规模、多中心、深层次的研究,以及我国中药成分的多样性和中医理论的复杂性,目前还未彻底了解其发挥疗效的具体机制和HLP的中医发病机理。因此,对于降血脂模型的建立,还需要我们不断改进、完善和创新,以寻求更完美的生物模型,更加深入全面地阐明HLP的发病机理和降脂中药的治疗机制。
5 结语和展望
综上所述,目前有多种多样的方法来建立HLP模型,各种模型均有其优缺点。高脂细胞模型相对于其他模型,具有实验周期短、可控性强、成本低等优点,但生物体终究是一个有机整体,其各个组织器官之间都存在着联系,单纯用细胞模型来研究只能说明药物是对这种细胞的作用效果,无法代替整个有机体。而动物模型即可以用来探讨降脂中药对整个机体的作用机制,特别其斑马鱼模型还可以高效、快速的进行高通量筛选。因此,我们应该将细胞模型与动物模型紧密结合起来,使两种模型相互补充,共同促进对HLP发病机制及防治中药的研究。

表3 高脂斑马鱼造模方法比较Table 3 Comparison of modeling methods for hyperlipidemia zebrafish
复制的高脂模型成功与失败,受到了多种因素的制约。饲喂方式的不同(饲喂法和灌胃法)、高脂饲料占比的不同以及脂肪乳剂配方的不同,都会影响造模的成功率。此外,影响造模效果的因素还有动物的品系、性别和年龄等。在建立高脂动物模型时,一般多选用雄性动物。因HLP的发生与肾上腺素等激素有关,而雄性动物较雌性动物竞争更为激烈,所以雄性动物更易形成HLP。所以应该根据具体的实验情况,选择合适的HLP实验动物模型。
随着新理论、新技术和新概念的出现,人们对高脂模型的要求随之提高。研究人员在进行研究时必须谨慎,因为某些模型的脂质代谢可能被证明与人类完全不同,因此,可能不适合研究降血脂中药的作用机制。笔者认为,在众多的模型中挑选出适合于研究HLP的模型时,需要结合自身实验的目的、指标和经费等客观条件,特别要着重注意以下几点。第一,选择建立的模型应尽可能与人类疾病相符合;第二,尽量选用自身影响因素小的模型,实验结果最好是可以多次重现,以避免实验结果的偶然性和不精确性;第三,应注意选择模型的实用性、经济型和可操作性。笔者相信,结合现代医学的研究手段,中医药治疗HLP将会有更加广阔的发展前景。
