由酸性氯化铜蚀刻废液制备氢氧化铜工艺技术研究
2020-03-07汤政涛刘后传张启凯吕照辉戚健剑于少明
汤政涛,刘后传,张启凯,吕照辉,戚健剑,于少明
(1.合肥工业大学化学与化工学院,安徽合肥230009;2.泰兴冶炼厂有限公司,江苏泰兴225400)
随着电子工业的发展,印刷电路板(Printed Circuit Board,PCB)作为主要承载器件已广泛应用于计算机等电子产品中。根据美国印刷电路协会报道,2016 年世界PCB 市场达到约582 亿美元,且近三年仍在上升[1-2]。PCB产量日益剧增,给人们生活带来了极大的便利。但同时,PCB 生产过程产生的废弃物也给环境造成了威胁,如:在其蚀刻过程中会产生大量蚀刻废液,若不经处理直接排放不仅造成严重的环境污染,也会造成资源的巨大浪费[3]。目前,我国PCB 行业产生的蚀刻废液60%为酸性氯化铜蚀刻废液[4],其主要成分为HCl、CuCl2等。对其处理方法主要包括两大类:一类是以蚀刻废液为原料合成铜的化合物,如氧化亚铜[3]、氧化铜[5-6]、碱式氯化铜[7]、碱式碳酸铜等[8];另一类是对蚀刻废液进行再生处理。
Cu(OH)2是一种蓝色或淡蓝色粉末,易受热分解。氢氧化铜具有一定的表面活性和触杀性,在农药和医药方面得到了广泛应用。此外,氢氧化铜还广泛应用于能量储存、催化、传感器等领域[9-10]。Cu(OH)2的制备方法较多,主要有沉淀法、溶胶-凝胶法、模板法等[9-10]。
目前,以酸性氯化铜蚀刻液为原料,制备Cu(OH)2的研究报道较少。卞永辉等[11]通过向酸性蚀刻废液中加入氢氧化钠制备氢氧化铜。该法操作简单,所得产品纯度高,但对Cu2+回收率未作报道。郑淑玉[12]、金正新等[13]对以碱性含铜蚀刻废液为原料制备氢氧化铜进行了研究,其中郑淑玉等虽回收了99.9%的Cu2+,但Cu(OH)2产品纯度只达到81%;金正新制得Cu(OH)2产品纯度达97%以上,但洗涤步骤较繁琐,另需添加稳定剂来保护产品。
本实验以酸性含铜蚀刻废液和NaOH为主要原料,在不添加任何助剂的条件下,制得纯度合格的氢氧化铜产品,但难洗涤,需要消耗大量洗涤水。为解决此问题,本实验首先确定适宜的pH 值,在不影响产品纯度前提下,研究不同沉淀剂配比n(NaOH)∶n(HFD)对产品洗水用量的影响,重点研究了不同助剂与产品洗水用量之间的关系,解决Cu(OH)2产品洗涤难的问题。本工艺制得的Cu(OH)2产品纯度高,洗涤方便,滤液中的氯化钠可回收利用,为清洁环保工艺。
1 实验部分
1.1 实验材料
原料:酸性氯化铜蚀刻废液(其中Cu2+含量为128.1 g/L;盐酸浓度为1.74 mol/L),江苏泰兴冶炼厂有限公司。沉淀剂:氢氧化钠,分析试剂:硫酸、硝酸、硫代硫酸钠、碘化钾、氨水、冰乙酸、淀粉等均为分析纯,国药集团化学试剂有限公司。
1.2 实验方法
移取适量酸性氯化铜蚀刻废液,加入一定量的助剂,混合均匀。按一定的滴加速度加入一种混合的沉淀剂,将溶液pH 调至适宜值,在一定温度下搅拌反应1.5 h,陈化10 min,后经过滤、洗涤、干燥得到产品Cu(OH)2,对其进行表征和化学分析等。本工艺流程示意图如图1所示。
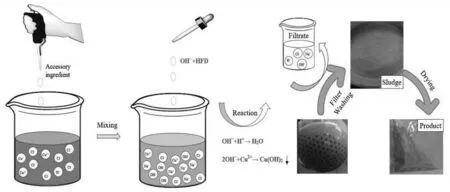
图1 工艺流程示意图
1.3 产品分析与表征
1.3.1 氢氧化铜纯度分析
采用间接碘量法,详见标准Q/320581 GVH 002-2016《工业用氢氧化铜》。
1.3.2 XRD表征
采用日本理学电机公司制造的D/MAX2500V 型X射线衍射仪分析物相组成,Cu 靶、Kα辐射,石墨单色器滤波,扫描速度为10°/min,扫描范围为20°~80°。
1.3.3 TG表征
采用德国耐驰仪器制造有限公司制造的TG209 F3热重分析仪,在30℃~800℃范围的氮气环境下对样品进行热稳定性测试,升温速率10℃/min。
1.3.4 SEM
采用美国FEI 公司制造的QUANTA200FEG 型扫描电子显微镜分析产品的形貌,无水乙醇为分散剂,60 W功率超声分散30 min。
2 结果与讨论
2.1 pH对Cu2+回收率及产品纯度的影响
实验在反应温度25℃、沉淀剂滴加速度10 s/滴、反应时间1.0 h、陈化时间10 min 条件下,考查了6 组不同pH 对产品的纯度及蚀刻废液中铜的回收率的影响,所得实验结果如图2 所示。
从图2可以看出,当pH<13时,所得产品的纯度<96%,在此范围内随着pH 升高,Cu2+回收率及产品纯度均随之提高。pH=12.5时,Cu2+回收率接近100.0%,这主要是由于向蚀刻液中加入碱液过程中,在pH 5~8 的范围内首先形成了碱式氯化铜(CuCl2·3Cu(OH)2);pH=9时,CuCl2·3Cu(OH)2逐渐向Cu(OH)2转化[5,14],此时反应体系是二者共存的状态,因而pH=11~12.5时,所得产品纯度偏低。
当pH=13 时,所得产品铜含量最高且纯度≥97.0%,滤液中检测不到Cu2+的存在,Cu2+回收率接近100.0%。这是因为在pH=13时,CuCl2·3Cu(O H)2中与Cl-结合的Cu2+完全转化为氢氧化铜,使得产品中基本只含有氢氧化铜单一组分,此时产品纯度达到97%以上。在该条件下,体系中Cu2+与O H-结合生成氢氧化铜而被完全回收。
当pH ≥13时,所得产品的纯度有所降低,Cu2+回收率急剧降低。这是因为pH ≥13时,体系中的O H-浓度偏高,生成的氢氧化铜沉淀会以Cu(O H)+、Cu(O H)3-、Cu(O H)42-等络离子的形式溶于过量的碱中,滤液中Cu2+浓度增加[12],使Cu2+回收不完全。笔者通过实验探究发现,在pH=14 条件下,制备氢氧化铜产品时,所得滤液为深蓝色溶液,化学分析表明,有2.8%的Cu2+进入到滤液中。
2.2 不同助剂对产品洗水用量的影响
实验考查了4 种助剂(分别记为A、B、C、D)对产品的形貌及洗水用量的影响,所得实验结果如表1、图6所示。

表1 不同种助剂对制得产品洗涤效果的影响
从表1数据可以看出,增加助剂对过滤时间影响不大,但对产品洗涤有较大影响。不加助剂时,所得产品呈密实的泥状沉淀,洗涤困难,消耗大量洗涤水。这是因为生成了类似胶体大小的氢氧化铜颗粒,使洗涤难度增加[15]。加入助剂后,产品的洗涤困难得到了改善。这是因为助剂的作用机理与表面活性剂类似,可能在颗粒周围起到结构导向剂的作用[16],改变了产品形貌。加入A 或B 助剂时,所得产品为密实的泥状物,洗水量有所减少。加入C或D助剂时,产品由原先的颗粒状转化为纤维状,如图6。在不加助剂时,合成的氢氧化铜产品颗粒更细小,部分团聚成大颗粒;在加入助剂C后,合成的氢氧化铜产品呈纤维状,纤维相互堆积,使得产品表现出蓬松的状态,该状态下产品中杂质容易被洗去,有效地减少了洗水量,节约洗涤用水量达58.6%以上。
2.3 沉淀剂配比对产品纯度及洗水用量的影响
在助剂C条件下,加入一种氢氧化钠与HFD混合的沉淀剂来制备氢氧化铜产品。实验考查不同配比的混合沉淀剂对产品纯度及洗水用量的影响。所得实验结果如图3所示。
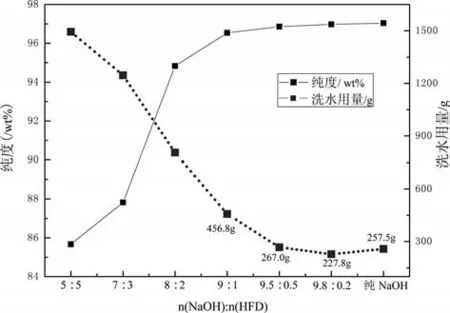
图3 不同沉淀剂配比n(NaOH):n(HFD)对产品纯度及洗水用量的影响
从图3 可以看出,随着沉淀剂配比增大,所得氢氧化铜产品的纯度随之增大,最后趋于一个稳定值97.0%;随着HFD加入量的减少,产品洗涤越来越容易,洗水用量呈现先降低后升高的趋势。n(NaOH):n(HFD)=9.8∶0.2时,洗水用量最少,且制得的产品符合工业用氢氧化铜Q/320581 GVH 002-2016标准要求。
2.4 产品表征及质量分析
(1)XRD 分析
图4 为回收的氢氧化铜产品XRD 图。从图4 可以看出,合成产品在2θ 为23.8°、34.0°、35.9°、38.0°、39.8°、53.2°、64.7°等处出现了衍射峰,分别对应(021)(002)(111)(041)(130)(150)(152)晶面,与氢氧化铜PDF 标准卡片(JCPDS No.13-0420)完全吻合,除氢氧化铜衍射峰外无杂质峰,说明本实验制得的产品为纯度较高的氢氧化铜。
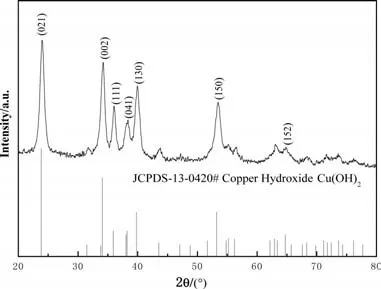
图4 氢氧化铜产品的XRD图
(2)热重分析
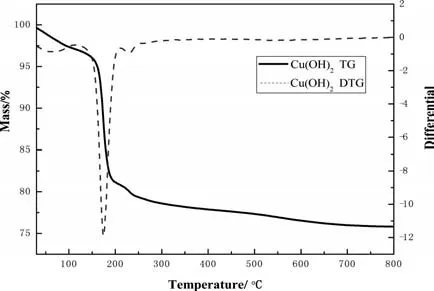
图5 氢氧化铜产品的热重分析曲线
图5为本实验制得的氢氧化铜热重分析曲线。图5显示产品在75℃前有微量失重,失重率约为1.0%,这是由于颗粒失去表面吸附水造成的。在75℃~300℃为主要失重带,在此温度区间曲线迅速下降,后缓慢下降,在300℃后趋于平缓。此过程主要是由于Cu(OH)2分解出OH-,进而失去一分子H2O。300℃左右基本分解完全,失重率达18.5%左右。氢氧化铜受热发生如下脱水分解反应:
Cu(OH)2→CuO+H2O ↑
理论失重率18.45%,与实验失重率相符。因此为得到纯度较高的氢氧化铜,干燥时温度不得高于90℃。与金[13]所述类似,本实验在干燥温度70℃条件下制得纯度较高的氢氧化铜产品。
(3)SEM分析
图6 为助剂C 加入前后氢氧化铜产品的SEM 照片。从图6可以看出,添加助剂C后合成的氢氧化铜产品分散性良好,为纤维状,长度在2~4 μm 之间,宽度在0.1~0.2 μm 之间,由纤维堆积成的微团,粒径在4~11 μm 之间;纤维无序堆积使微团变得蓬松;不加助剂时,制备的氢氧化铜呈颗粒状,粒径更加细小,团聚形成的大颗粒比较密实,粒径在1~8 μm 之间。
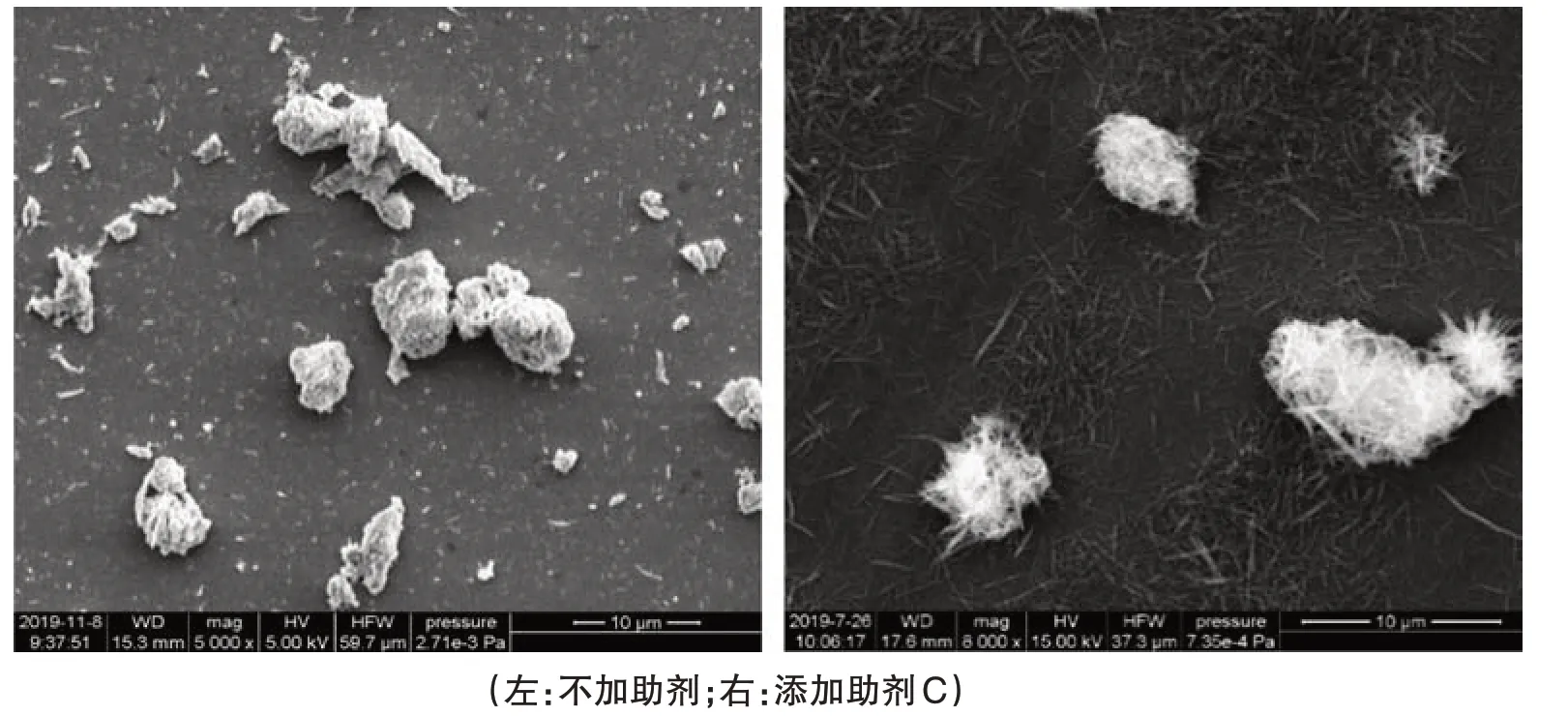
图6 助剂C加入前后氢氧化铜产品SEM照片比较
3 结论
(1)实验以酸性含铜蚀刻废液为主要原料,确定在助剂C,沉淀剂配比n(NaOH)∶n(HFD)=9.8∶0.2,沉淀剂滴加速度10 s/滴,反应温度25℃,反应时间1.0 h,陈化时间10 min 条件下制备的氢氧化铜最佳。Cu(OH)2产品纯度达97.0%以上,蚀刻废液中Cu2+的回收率≥99.9%。助剂C及HFD的引入,不仅显著改变了产品形貌,且有效解决了产品呈胶状、难洗涤等问题,节约洗水用量58.6%以上。
(2)XRD 测试结果表明,本工艺制备的产品为单一组分Cu(OH)2,纯度较高,结晶度高。TG分析结果表明,氢氧化铜在90℃左右开始失水。
(3)SEM测试结果表明,不加助剂条件下制备的氢氧化铜产品团聚成密实的颗粒状,粒径在1~8 μm 之间,在添加助剂C 条件下制得的氢氧化铜产品,有效地改变了产品的形貌,使产品呈现纤维状及纤维堆积而成的微团形貌。纤维状氢氧化铜长度在2~4 μm 之间,宽度在0.1~0.2 μm之间;由纤维堆积成的微团,粒径在4~11 μm 之间。
