热脱附-气质联用法分析檀香及其燃香烟气成分
2020-02-18涂永元黄玉香邱
涂永元黄玉香邱 飞
[1.国家燃香类产品质量监督检验中心(福建), 福建 永春 362600; 2.永春县产品质量检验所,福建永春 362600; 3.福建省香产品质量检验中心,福建 永春 362600; 4.泉州医学高等专科学校,福建 泉州 362100; 5.华侨大学分子药物研究院,福建 泉州 362021; 6.华侨大学生物医学学院,福建 泉州 362021; 7.分子药物教育部工程研究中心,福建 泉州362021]
檀香Santalum albumL.又称真檀、旃檀、白檀香,是一种生长极其缓慢的热带芳香植物。檀香经济价值高,兼具多种用途,素有“香料之王”的美誉,作为一味芳香药物具有调理脾胃、理气温中、消除风肿之功效[1];在宗教中,檀香质地坚硬、耐腐蚀,常用于佛像的雕造[2];在民俗文化中,檀香因其焚烧时独有的木香味,而被更多地用于传统燃香产品的制香配方中,可令人身心放松、消弭焦虑、提振精神。
檀香市场供不应求,价格常年居高不下,为迎合大众对于檀香香气的喜爱,近年来随着上游产业香精香料合成技术的日趋成熟,模仿檀香香气的合成香精越来越多地掺入到各类燃香产品中,这些化工添加型的产品因其包含的化学结构信息不同,香气仍有差异,混淆檀香功效价值,本质上仍无法与天然成品檀香相比拟。前期初步研究表明[3],檀香型燃香产品产生的烟气中含有较多复杂未知成分,由于缺乏深入有效的化学分析和文献报道,其烟气对人体健康和环境的影响无从判断,使得人们对于燃香产品的使用始终存在顾虑。因此,面对日趋混乱的燃香市场,为防止檀香类燃香产品质量降低、防范市场未知风险,分析檀香原料及其燃烧烟气成分将具有积极的意义。本研究以大量应用于燃香产品的药用原料檀香作为研究对象,采用热脱附-气质联用法(TD-GC/MS)分析檀香原料和燃烧檀香烟气中的挥发性成分,探索建立快速分析檀香的新途径、新方法,并比较分析檀香及其燃烧烟气挥发性成分的信息,力图真实地反映檀香燃烧后烟气来源。
1 材料
UNITY-xr+ULTRA-xr 热脱附分析仪(英国Markes 公司);7890B-5977B 气相色谱-质谱联用仪(美国Agilent 公司);Tenax-TA 玻璃采样管(英国Markes 公司);2,6-二苯呋喃多孔聚合物(粒径0.18~0.25 mm,60~80 目);1.8 m×1.8 m×1.8 m 的密闭玻璃方箱(自制)。檀香对照品(批号121240-201002,中国食品药品检定研究院);市售檀香样品(产地云南,批号170101,安徽聚草中药饮片有限公司,使用前将样品粉碎后过30 目筛,收集粉末备用);氮气、氦气(质量分数99.999%,佛山德力梅塞尔气体有限公司);正构烷烃混标(C7~C40,1 000 mg/L 于正己烷溶液,美国o2si 公司)。
2 方法
2.1 热解析条件 采样管脱附温度250 ℃;采样管脱附时间10 min;传输线温度200 ℃;干吹时间1 min;冷阱初始温度-20 ℃;冷阱脱附温度300 ℃;冷阱脱附时间5 min;载气为氮气。
2.2 气质联用仪条件 HP-5 ms Ultra Inert 色谱柱(30 m×0.25 mm×0.25 μm);初始温度50 ℃,以5 ℃/min 升至250 ℃;载气氦气,载气体积流量1 mL/min;离子源温度230 ℃,传输线温度280 ℃,四级杆温度150 ℃;电离方式为EI;电离能量70 eV;溶剂延迟1 min,扫描范围m/z40~450。
2.3 数据处理
2.3.1 定性定量分析 所得数据经NIST 17[NIST/EPA/NIH Mass Spectral Library(EI)]、NIST Standard Reference Database 1 A v17 标准库和https://webbook.nist.gov/chemistry/数据检索,参照上述谱库非极性或弱极性气相色谱柱保留指数数据,给出差异小于1%的保留指数鉴定结果;采用峰面积归一化法。
2.3.2 保留指数计算 单一线性程序升温的条件下保留指数计算式为
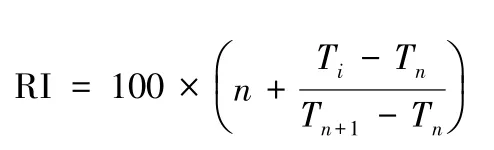
式中,RI 为测组分的保留指数;Ti为待测组分的保留时间,单位min;Tn、Tn+1为待测组分前后正构烷烃的保留时间,单位min;n为正构烷烃的碳原子数。
2.4 样品前处理及采集方法
2.4.1 檀香对照品、样品前处理 取微量粉碎过的檀香样品置于空玻璃管中间,用适量石棉封堵样品两端,石棉外侧再分别用U 型别针固定,最后用进样密封帽套紧玻璃管,放入热脱附仪中,在“2.1”“2.2”项条件下于氮气氛围中直接热脱附,进样至GC/MS 分析获得数据;同法分析檀香对照品。
2.4.2 檀香样品燃烧后烟气成分的采集 参照GB/T 26393—2011[4]TVOC 采样模型,取0.6 g 粉碎好的檀香样品置于1.8 m×1.8 m×1.8 m 密闭玻璃采样室中点燃,再用连有Tenax-TA 采样管的大气采样仪,以0.2 L/min 速率收集25 min 檀香燃烧产生的烟气。采样结束后,将Tenax-TA采样管放入热脱附仪中,在“2.1”“2.2”项条件下进行脱附,进样至GC/MS 分析获得数据;采集样品前以同样方法收集上述玻璃采样室空白空气,以扣除空白数据干扰。
3 结果与讨论
3.1 热脱附条件优化
3.1.1 采样管脱附温度的优化 将1.5 mg 样品按“2.4.1”项下方法处理,放入待脱附的玻璃管中,脱附温度分别设置为200、225、250、275、300 ℃,发现样品脱附后的化合物个数和总峰面积呈上升趋势。当样品脱附温度为275、300 ℃时,与250 ℃化合物个数、总峰面积趋于相同,化合物为120 个左右,总峰面积在3.1×109左右,并且低沸点化合物个数增多,样品在高温解析时可能有部分化合物降解,因此选择250 ℃较为适宜。不同采样管脱附时间(5、10、15 min)对样品脱附也有一定的影响,达到10 min 时已基本能够保证样品脱附完全。
3.1.2 冷阱脱附温度优化 在上述优化的采样管脱附温度条件下,设置不同冷阱捕集温度(-30、-20、-10、0、10 ℃),当温度低于-20 ℃时检出化合物个数、总峰面积趋于稳定,因此选择-20 ℃作为冷阱捕集温度。在此条件下设置不同冷阱脱附温度(225、250、275、300 ℃)和冷阱脱附时间(2、5、10 min),考察检出化合物个数及总峰面积变化情况,并且在每次实验后用空白采样管2 次热脱附检查冷阱是否有残留化合物。结果表明,当冷阱脱附温度为300 ℃,脱附时间为5 min 时,总峰面积趋于平稳,化合物个数最多。
3.1.3 采样管吸附时间优化 在恒温恒湿条件下,将两根老化好的Tenax-TA 采样管首尾串联,分别以0.2 L/min 采样速率收集采样室样品燃烧气体15、25、35 min,当采样25 min 时第一根检出化合物个数、总峰面积趋于平稳,采样35 min 时第二根开始检出化合物,证明此时第一根管采样管已接近饱和,并且部分化合物穿透现象明显增加,因此选择25 min 采样时间较为适宜。
3.1.4 对面积归一化法结果的影响 取上述1.5 mg 样品,按“3.1”项下方法重复热脱附6 次,样品总峰面积RSD为8.35%,主要成分α-檀香醇峰面积RSD 为3.79%,β-檀香醇峰面积RSD 为2.97%;按“2.4.2”项下条件用Tenax-TA 采管采样6 次燃烧后烟气成分,样品总峰面积RSD 为6.2%,主要成分α-檀香醇峰面积RSD 为7.26%,β-檀香醇峰面积RSD 为9.33%。由此可知,样品总峰面积以及主要化合物峰面积RSD 值都小于10%,因此该方法重复性较好,对檀香成分面积归一化产生的结果影响较少,并可大致获得样品主成分含有量信息。
3.2 实际样品分析 檀香对照品、檀香样品燃烧前后总离子流图(TIC)见图1,可知檀香燃烧前后色谱峰保留时间基本一致,但燃烧后杂峰变多。以面积归一化法计算各组分含有量,结果见表1。
3.3 檀香对照品、样品及燃烧烟气化学成分分析
3.3.1 檀香对照品、样品挥发性成分 根据相关文献报道[5-8],α-檀香醇和β-檀香醇是赋予檀香独特香气、发挥多种生物活性的特征性、有效成分。由于目前尚无法通过工艺合成的方式实现檀香醇工业量产,也无相关对照品,因此本研究以上述檀香对照品作为参考物质,以是否含有主成分α-檀香醇、β-檀香醇作为判断檀香真伪的关键性指标。结果表明,檀香对照品和檀香样品中识别的挥发性成分分别有27 种和24 种,占比分别为63.48% 和75.91%,大部分物质保留时间都集中分布在24~30 min,主要由酚类、醇类、萜类、醛类、酸类组成;对照品和样品的主成分都为α-檀香醇和β-檀香醇,其中含有量最高的是α-檀香醇,在对照品和样品中为21.46%、23.19%,其次是β-檀香醇,分别为16.35%、14.56%;除上述2 种主成分外,含有量较多的共有成分有反式-α-香柠檬醇(对照品和样品含有量分别为6.12%、5.59%)、(Z)-表-β-檀香醇(分别为4.18%、4.10%)。
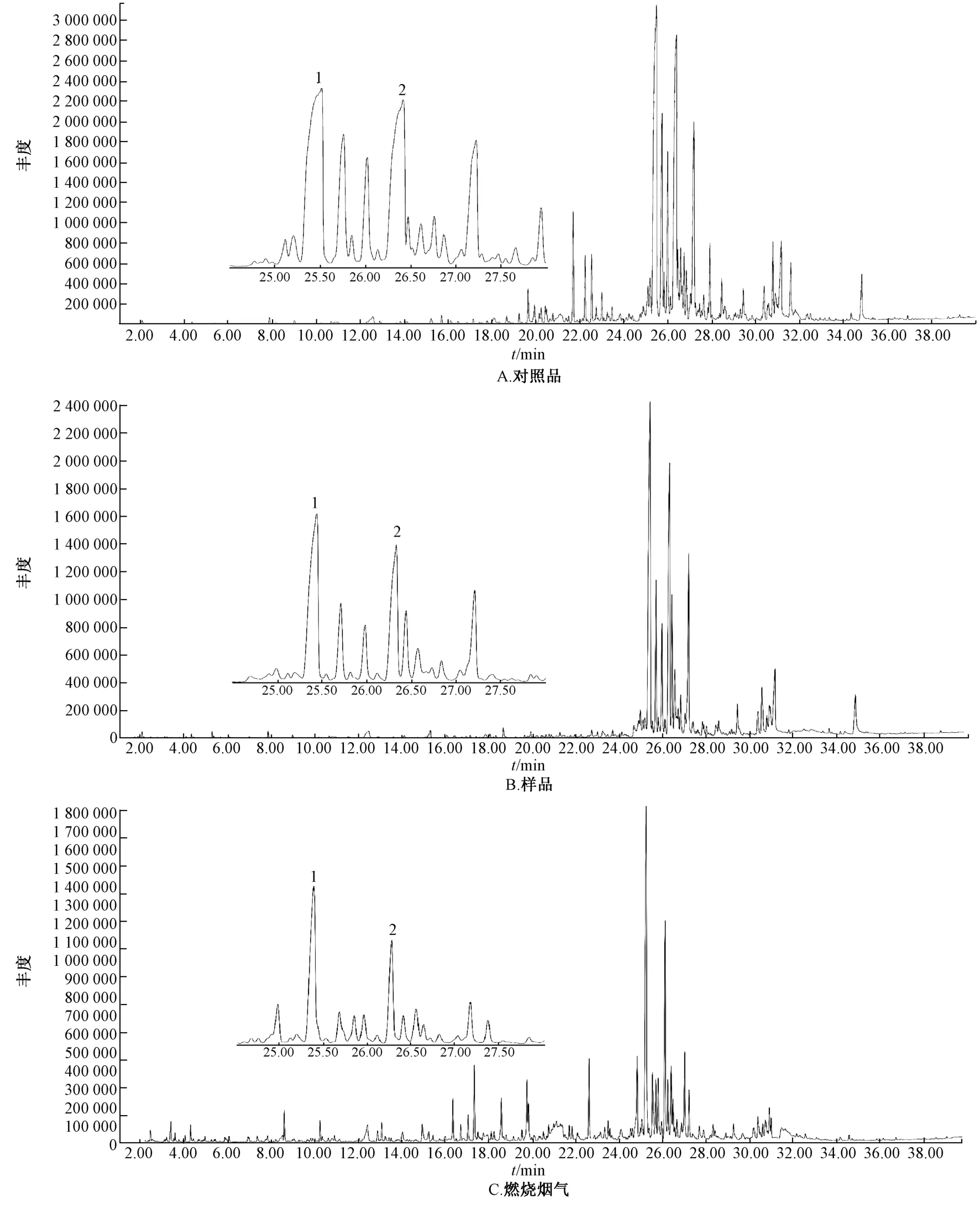
图1 各样品挥发性成分的总离子流色谱图
3.3.2 燃烧烟气成分 以市售檀香样品作为燃烧烟气研究对象,表明它能被Tenax-TA 采样管吸附并被识别出的成分共有37 种,相对含有量占64.54%,成分分布较为分散,由酚类、醇类、萜类、醛类、酮类、酸类等复杂物质组成。对于保留时间在25 min 以后的识别成分,样品燃烧前后数量基本相同,但该时间段总含有量由燃烧前的72.71%降至燃烧后的43.83%,其中除酚类成分外各成分相较于燃烧前均有所下降,关键物质α-檀香醇和β-檀香醇总含有量则由燃烧前37.75%降至燃烧后的24.05%,但仍为檀香燃烧后最高;对于保留时间在25 min 之前的识别成分,烟气中种类、含有量增加明显,化合物由11 个增加至25 个,总含有量由燃烧前3.01%升高至燃烧后的20.71%,该段时间新增物质主要为酚类,由燃烧前的4 种增至17 种,相对含有量达17.89%。整体上看,烟气中酚类总含有量由燃烧前的5.68%上升到25.50%,约为燃烧前的4.5 倍,是检出烟气中种类最多、含有量增加最大的一类组分,这很可能是由于其本身特有的木脂素类化合物在高温下热裂解结果所致[9]。2 段保留时间物质比较的结果表明,燃烧作用有使檀香中高沸点、大分子的化合物分解成低沸点、结构更加稳定、小分子物质的趋势。
3.4 燃烧烟气中含有的生物活性物质 檀香样品燃烧后烟气成分虽然复杂,但其含有的生物活性物质众多,药用潜力大,可供后续该类产品的生物医学研究参考。檀香集药用、香料、收藏价值于一身,离不开其物质基础α-檀香醇和β-檀香醇,α-檀香醇具有化学预防作用,被广泛应用
于抗辐射、抗肿瘤尤其是抗皮肤癌的治疗中[10],并具有抗氧化、抗高血糖[11]以及镇静作用[12],而β-檀香醇具有抗癌[13]、抗病毒、抗流感[14]作用。燃烧后烟气中的酚类物质众多,酚类化合物普遍具有消毒防腐作用[15],可用于环境消毒,其中相对含有量最高的丁香醛具有清除电离自由基、抗辐射、抗氧化损伤、抗凋亡作用[16];其他酚类物质(如愈创木酚、4-乙基愈创木酚、丁香酚、5-叔丁基连苯三酚等)也都具有很强的抗菌、抗氧化活性[17-20],并且具有芳香气息,常用于日用品的调香,可以平衡或提高檀香燃烧后整体香气,使得香气层次更加丰富[21]。
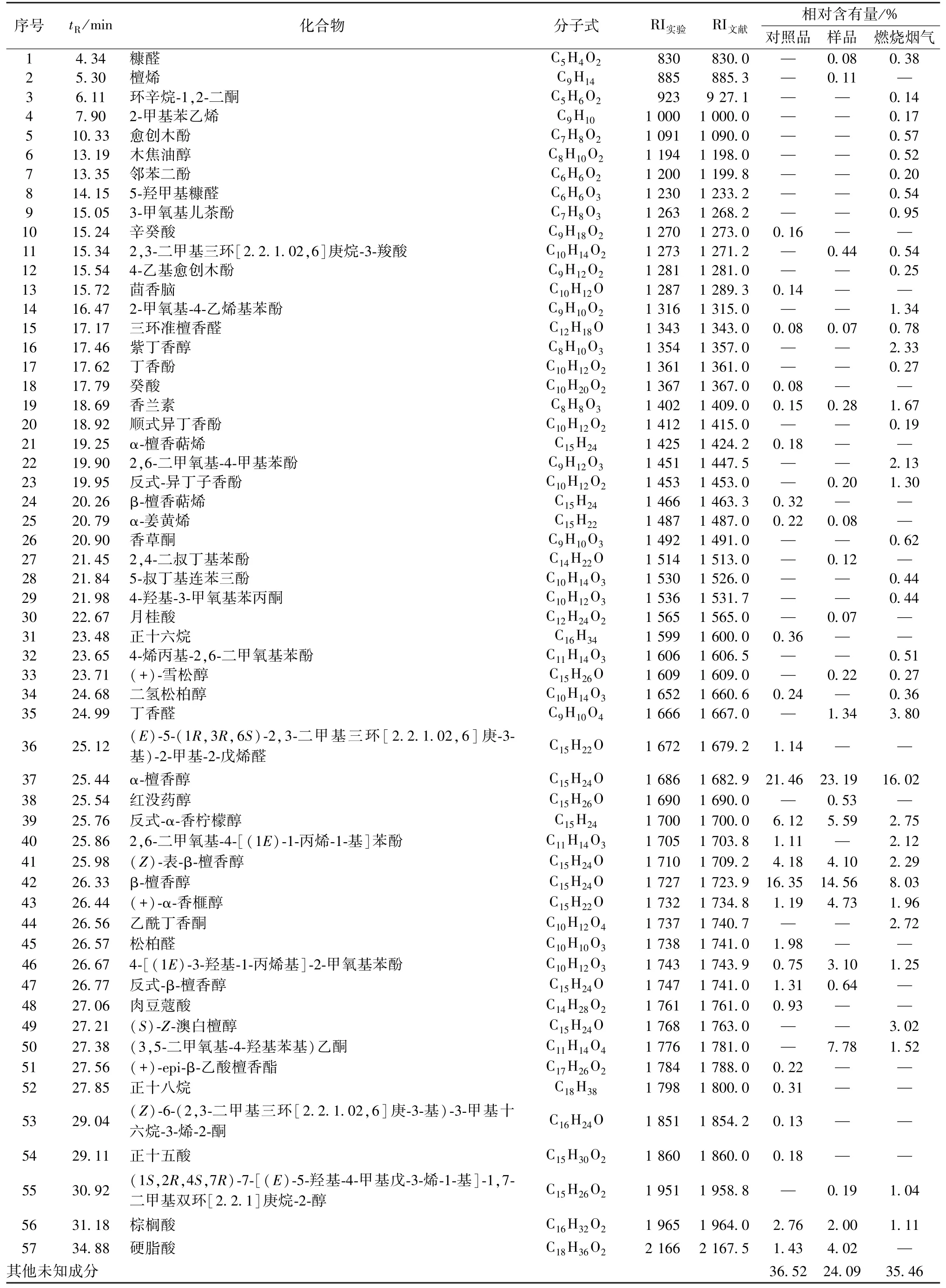
表1 各样品挥发性成分及其相对含有量
4 结论
由于檀香的特征性成分α-檀香醇、β-檀香醇具有挥发性,可采用直接热脱附法分析鉴别,样品仅需简单粉碎后直接放入脱附管,经加热元件高温解析,可使样品中挥发性、半挥发性有机物直接析出并用于气质检测。所得数据经NIST 17 标准谱图库比对、保留指数判断,结合对照品挥发性成分信息,测得α-檀香醇、β-檀香醇相对含有量分别为23.19%、14.56%,识别的样品化合物与对照品主成分信息基本相符,并且相较于显微鉴定法、薄层色谱法[22]、水蒸气蒸馏法、溶解提取法[5-7]等通用的檀香鉴定方法,该方法几乎无样品前处理过程,操作快捷简便,实用性强,仅需提供微量样品便可辨识出大部分主要挥发性成分,应用于檀香快速鉴别时有参考价值;在烟气成分检测方面,通过热脱附Tenax-TA 采样管收集后分析出占总含有量64.54%的37 种复杂物质,并且由于木脂素、纤维素等热解,致使酚类成分种类和相对含有量增加最多,这也使得檀香烟气在原有生物活性的基础上具有更强的杀菌潜力。因此,檀香作为常见香料,对其深入研究将有利于燃香产品的质量提升和标准规范,也可为后期该类产品开发利用提供有价值的参考信息。
