蕲蛇Ⅱ型胶原蛋白海藻酸钙-壳聚糖纳米胶囊的制备
2020-02-18钱苏海蔡斯琦丁兴红丁志山范永升
钱苏海,蔡斯琦,丁兴红,丁志山,范永升
(浙江中医药大学,浙江 杭州 310053)
蕲蛇为蝰科动物尖吻蝮Agkistrodon acutus的干燥体,其性味甘、咸、温,归肝经[1],广泛应用于治疗风湿顽痹,如类风湿关节炎、肢体麻木、关节肿胀等。前期研究发现,蕲蛇Ⅱ型胶原蛋白具有良好的治疗类风湿关节炎作用[2-4],但其腥味重,化学性质不稳定,药物作用时间短,制约了临床推广应用。
以壳聚糖-海藻酸盐为囊材包埋蛋白是一种新型制药技术,它有助于保持蛋白类药物的生物活性[5-6],提高胶囊稳定性和载药量,并可调节药物释放速度,实现缓释性能,具有良好的临床应用前景。目前,尚无制备蕲蛇Ⅱ型胶原蛋白壳聚糖-海藻酸盐纳米胶囊的报道,故本实验通过反相乳化法制备该制剂,正交试验优化其工艺,并对其理化性质进行表征,药物释药性能进行考察,从而为相关新型给药系统的研发提供实验基础。
1 材料
Zetasizer Nano ZS90 激光粒度分析仪、Zeta 电位仪(英国Malvern 公司);H-7650 透射电子显微镜(日本Hitachi公司);酶标仪(美国Thermo 公司);磁力搅拌器(德国IKA 公司)。海藻酸钠、乙酸、氢氧化钠、PBS 缓冲液,氯化钙均为分析纯(上海阿拉丁试剂有限公司);透析袋(截留分子量10 000)、壳聚糖(生物技术级,脱乙酰度≥95%)(上海麦克林生化科技有限公司);水为双蒸水(美国Millipore 公司)。蕲蛇Ⅱ型胶原蛋白[7](自制,含有量95%)。
2 方法
2.1 纳米胶囊制备 100 mg 海藻酸碾碎,转移到0.5%乙酸中溶解,加入Ⅱ型胶原蛋白冻干粉超声溶解,再加入CaCl2溶液超声乳化完全,缓慢滴加0.5 mol/L NaOH 将pH值调至7.5,得到海藻酸钙Ⅱ型胶原蛋白纳米胶囊,将其洗涤离心后加到壳聚糖溶液中磁力搅拌2 h,即得。
2.2 透射电镜观察 将分散于去离子水的蕲蛇Ⅱ型胶原蛋白纳米胶囊滴于200 目喷碳铜网上,室温干燥后滴加数微升2% 磷钨酸钠负染液,静置后滤纸吸去负染液,干燥30 min后进行电镜观察。
2.3 粒径、Zeta 电位测定 应用激光纳米粒径仪检测粒径、Zeta 电位,观察粒径分布范围。
2.4 载药量、包封率、释药性能测定
2.4.1 载药量 精密称取纳米胶囊适量(C2)于研钵中研细,适量PBS 缓冲液(0.1 mol/L,pH=7.2)混匀,待其充分溶胀后再剧烈搅拌30 min,使蕲蛇Ⅱ型胶原蛋白充分溶出,滤液定容后采用羟脯氨酸法测定羟脯氨酸质量浓度,乘以系数7.46 即为其含有量(C1),计算载药量,公式为载药量=C1/C2×100%。
2.4.2 包封率 取纳米胶囊约100 mg 于50 mL 量瓶中,PBS 缓冲液(0.1 mol/L,pH=7.2)定容,待其充分溶胀后离心取上清液,羟脯氨酸法测定上清液蕲蛇Ⅱ型胶原蛋白质量(C3),沉淀置于研钵中研细,加适量PBS 缓冲液剧烈搅拌30 min,以使蕲蛇Ⅱ型胶原蛋白充分溶出,羟脯氨酸法测定其质量(C4),计算包封率,公式为包封率=[C4/(C4+C3)]×100%。
2.4.3 释药性能 100 mg 海藻酸碾碎,转移到150 mL 0.5%乙酸中,加入100 mg Ⅱ型胶原蛋白超声乳化,得到微乳溶液,将它和纳米胶囊置于含有人工胃液浸液的透析袋内,放入生理盐水中,在不同时间点取样,羟脯氨酸法测定蕲蛇Ⅱ型胶原蛋白质量浓度,计算药物累积释放率,同时加入等量新鲜人工胃液保持恒定体积。
3 结果
3.1 制备工艺优化 因素水平见表1,结果见表2,方差分析见表3。

表1 因素水平

表2 试验设计与结果
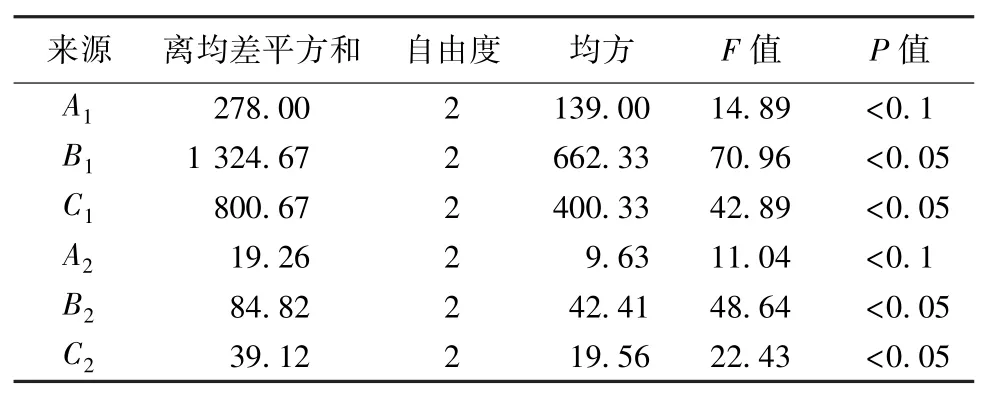
表3 方差分析
由表可知,蕲蛇Ⅱ型胶原蛋白与海藻酸比例对粒径、Zeta 电位影响最大,壳聚糖溶液浓度次之,CaCl2溶液浓度影响最小;最优工艺 为A3B2C3,即CaCl2溶液浓度20 mmol/L,蕲蛇Ⅱ型胶原蛋白与海藻酸比例1∶1,壳聚糖溶液浓度1%。再进行3 批验证试验,测定平均粒径为(210±5.12)nm,PDI 为0.16±0.03,Zeta 电位为(-25.46±0.56)mV,粒径分布见图1。
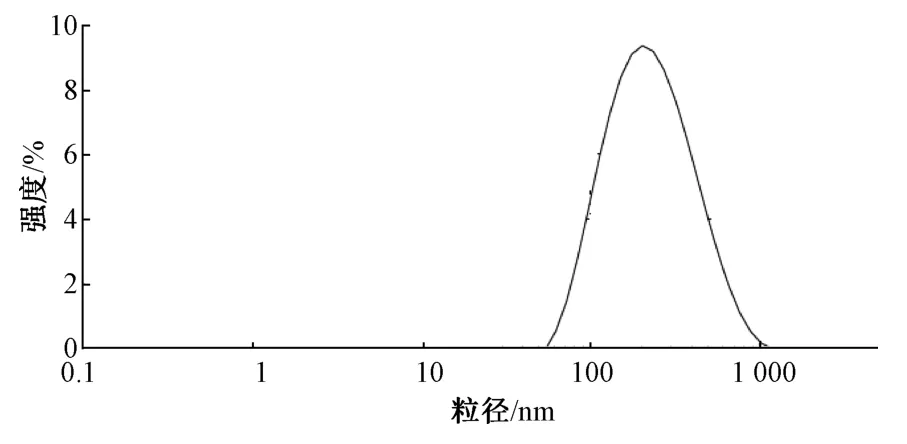
图1 蕲蛇Ⅱ型胶原蛋白纳米胶囊的粒径分布
3.2 微观形态 图2 显示,纳米胶囊大小均匀,分散性好,表面光滑饱满。

图2 纳米胶囊透射电镜图
3.3 载药量、包封率 纳米胶囊平均包封率、载药量分别为(83.69±4.31)%、(16.35±1.35)%。
3.4 释药性能 图3 显示,纳米胶囊24 h 累积释放率为(81.86±3.15)%,实现了缓释作用;蕲蛇Ⅱ型胶原蛋白释放的总体趋势是先快后慢,12 h 时微乳释放率不大于55%,而此时纳米胶囊已达到95%。

图3 样品释药性能曲线
4 讨论
本实验通过正交设计[8]获得蕲蛇Ⅱ型胶原蛋白纳米胶囊最优参数,此时所得制剂性能优良,具有良好的稳定性和粒径分布范围,并且表面光滑饱满,这是因为在形成过程中蕲蛇Ⅱ型胶原蛋白首先被海藻酸表层富集,之后海藻酸中α-L-古罗糖醛酸单元与CaCl2中钙离子发生交联反应,逐步形成带负电荷海藻酸钙囊壳,它在带正电荷的壳聚糖溶液中受静电作用而进一步成型[9]。进一步研究发现,该制剂具有的良好药物包封性能,这是因为胶囊囊芯中蕲蛇Ⅱ型胶原蛋白在海藻酸钙与壳聚糖的共同包埋下,由于海藻酸与钙离子交联度反应而使囊膜致密性增加,两者一起形成致密的纳米胶囊网络结构,导致它从基质渗透到外界环境溶液的难度加大,避免了药物泄漏损失,从而具有良好的包封率[10-11]。另外,还测得其平均载药量大于15%,具有一定的临床应用价值。
蕲蛇Ⅱ型胶原蛋白缓释纳米胶囊具有良好的缓释效果,这可能是由于海藻酸与蕲蛇Ⅱ型胶原蛋白之间受氢键与静电作用,使得其结构更致密,可抑制药物扩散速率[12],从而实现了该作用。
