硫酸新霉素及相关物质体外抗菌活性与毒性的研究*
2020-01-06朱晓玥黄敏文赵述强袁耀佐
朱晓玥,黄敏文,赵述强,张 玫,时 乐,袁耀佐**
1 江苏省食品药品监督检验研究院,南京 210019;2 国家药品监督管理局化学药品杂质谱研究重点实验室,南京210019;3 南京中医药大学,南京 210023
硫酸新霉素为氨基糖苷类抗生素,能有效抑制革兰阴性菌,为国内外临床上常用的抗生素之一[1]。硫酸新霉素是从新霉素链霉菌的代谢产物中分离得到的混合物,主要成分为新霉素B 和C,以及少量新霉素A。新霉胺为硫酸新霉素产品的主要非活性杂质,而巴龙霉素和核糖霉素作为工艺杂质在新霉素中也有检出[2]。硫酸新霉素有耳毒性和肾毒性,对人体健康危害较大。因此,在硫酸新霉素国家评价性抽验过程中,按照杂质谱控制(impurity profiles)理念“针对药品中的每一个杂质,依据其生理活性制定相应的质控限度”[3],先建立用于硫酸新霉素杂质谱的膜抑制LC-MS 方法,推定其他主要杂质,共检出12 个杂质(另文发表),然后采用不同模型,考察硫酸新霉素及主要相关物质的抗菌活性及毒性差异,为质量标准中的杂质控制提供数据支撑。
1 实验材料
1.1 仪器与试药
比浊仪(Densichek plus,生物梅里埃公司);电子天平(XS205,梅特勒);听力检测系统(TDT auditory systems,Tucker Davis Technologies Incorporated,Gainesville,FL,USA,软件为powere Sig Gen32 software);DP2-BSW 荧光显微镜(Olympus 公司)。
对照品:硫酸新霉素(批号130309-201512)、硫酸巴龙霉素(批号130371-200305)、硫酸核糖霉素(批 号130348-9301)、新霉胺(批 号130411-200908)均购自中国食品药品检定研究院;硫酸新霉素B(批号180803,纯度66.007%)、硫酸新霉素C(批号180801,纯度60.776%)均为宜昌三峡制药有限公司提供。水解酪蛋白琼脂培养基(MHA,批号20180606)、水解酪蛋白培养基(MHB,批 号20180605)均购自青岛海博生物技术有限公司。
1.2 菌株
大肠杆菌(ATCC25922,批号E0006B)、金黄色葡萄球菌(ATCC25923,批号A0246B)均购自广东环凯微生物科技有限公司。
1.3 动物
健康SPF 级成年豚鼠(南京江宁青龙山动物繁殖场,生产许可证号:SCXK(苏)2017-0011);斑马鱼胚胎以野生成鱼交配获得(国家斑马鱼资源中心)。
2 方法与结果
2.1 硫酸新霉素及相关物质体外抗菌活性考察
2.1.1 常量肉汤稀释法 参照美国临床实验室标准化协会(CLSI)标准[4],以硫酸新霉素为例:取32支无菌试管,分大肠杆菌组和金黄色葡萄球菌组,编号为1~16,各试管中供试品溶液的浓度(以主药计)依次为128、64、32、16、8、4、2、1、0.5、0.25、0.125、0.062 5、0.031 25、0.015 625、0.007 812 5、0.003 906 25 μg·mL-1。将供试菌分别先用MHB 培养基校正菌体浓度至0.5 麦氏比浊度,再用MHB 肉汤稀释100倍至受试菌浓度约为5×105CFU/mL。另取两管分别为阳性对照(不添加药物只添加菌体)和阴性对照(只添加培养基,不添加药物及菌体)。在1 至16 管和阳性对照管内分别加入受试菌1 mL,混合均匀。将接种好的试管封口置37 ℃培养18 h,观察无明显浑浊管及其相邻澄清管所对应的药物浓度,即为最低抑菌浓度(MIC)区间。结果见表1。硫酸新霉素及相关物质对大肠杆菌和金黄色葡萄球菌的体外抗菌活性强弱顺序均为:硫酸新霉素B>硫酸新霉素>硫酸新霉素C>硫酸核糖霉素>巴龙霉素>新霉胺。
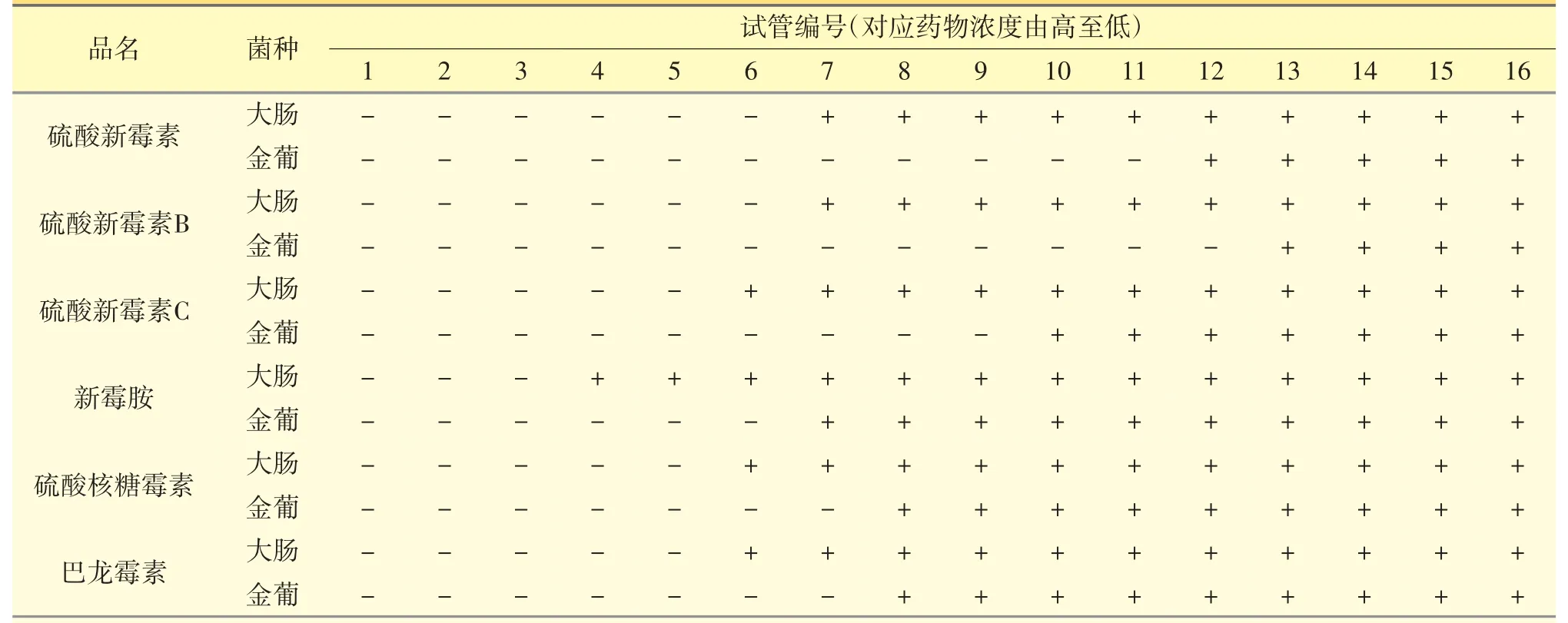
表1 各受试药物最低抑菌浓度(MIC)
2.1.2 纸片扩散法 结合CLSI 推荐的纸片扩散法[5]及用2015 年版《中国药典》四部抗生素微生物检定法(通则1201)进行抑菌效果检测。分别将硫酸新霉素及相关物质用MHB 肉汤配制成1.024 mg·mL-1的供试品溶液(均以主药计)。精取上述供试品溶液2 μL 分别浸润药敏纸片并晾干,将晾干后的各药敏纸片放于含有敏感细菌的固体培养基表面,37 ℃培养18 h,测定抑菌圈直径大小(如图1)。硫酸新霉素及相关物质对大肠杆菌和金黄色葡萄球菌体外抗菌活性强弱顺序均为:硫酸新霉素B>硫酸新霉素>硫酸新霉素C>硫酸核糖霉素>巴龙霉素>新霉胺,与常量肉汤稀释法的结果吻合。
2.2 硫酸新霉素及成分B、C 对豚鼠听力损伤考察
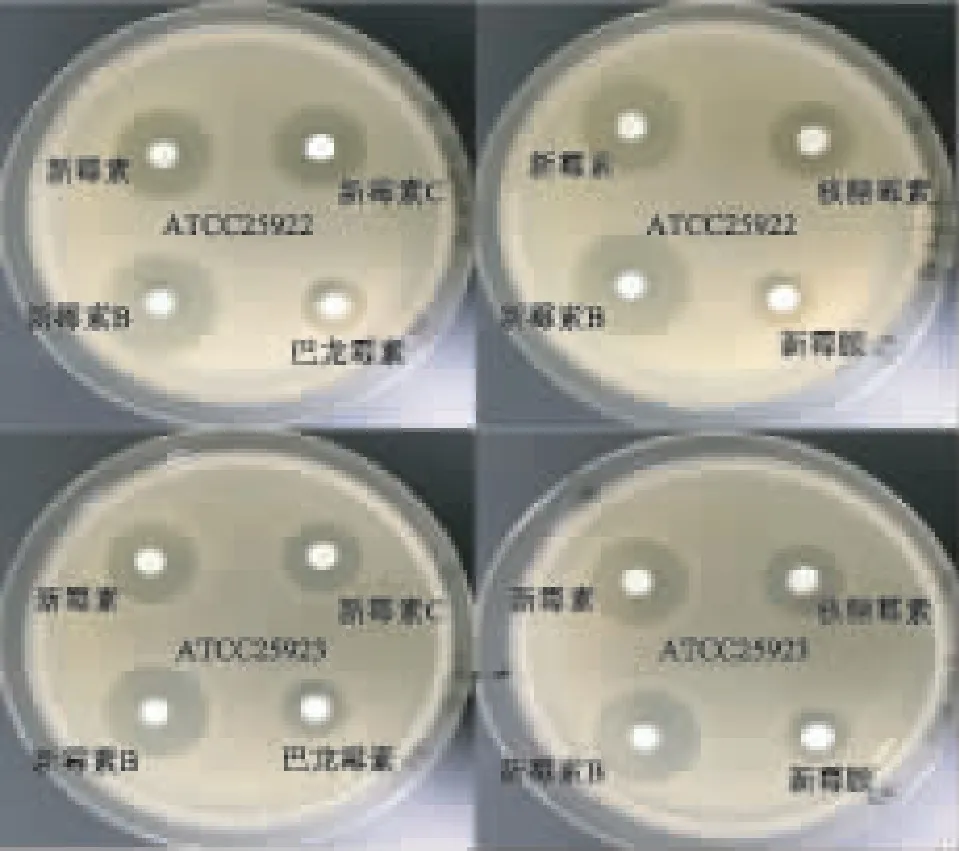
图1 各供试品溶液的体外抗菌活性直观对比图(纸片扩散法)
选体重250~350 g 雄性豚鼠,适应性饲养3 天,随机分为空白组、硫酸新霉素组、硫酸新霉素B 组(下称B 组)、硫酸新霉素C 组(下称C 组)。各组每天分别腹腔注射,剂量为:硫酸新霉素组100mg·kg-1,B 组80mg·kg-1,C 组15mg·kg-1;给药体积均为5mL·kg-1;空白组给予等体积的生理盐水。各组常规饮食,避免其他听力损伤因素的干扰,连续给药28天。末次给药后第2 天,受试动物颅顶正中皮下为正极,给声侧耳廓后下为负极,接地电极于鼻翼。发出300 Hz 为主的短声刺激信号,间隔90ms,带通滤波50~3000Hz,叠加200 次,扫描时程20 ms。声刺激强度从90 Db SPL 开始,以5 Db 逐次递减,观察Ⅰ波以判定两侧耳的ABR 听阈值。结果显示,与空白组比较,硫酸新霉素组和B 组ABR 听阈值明显升高,有显著性差异(P<0.01);与空白组比较,C 组听阈值未见明显升高(P>0.05)。与硫酸新霉素组比较,B 组ABR 听阈值低,有统计学差异(P<0.05);C 组ABR听阈值显著低于硫酸新霉素组(P<0.01)。见图2。
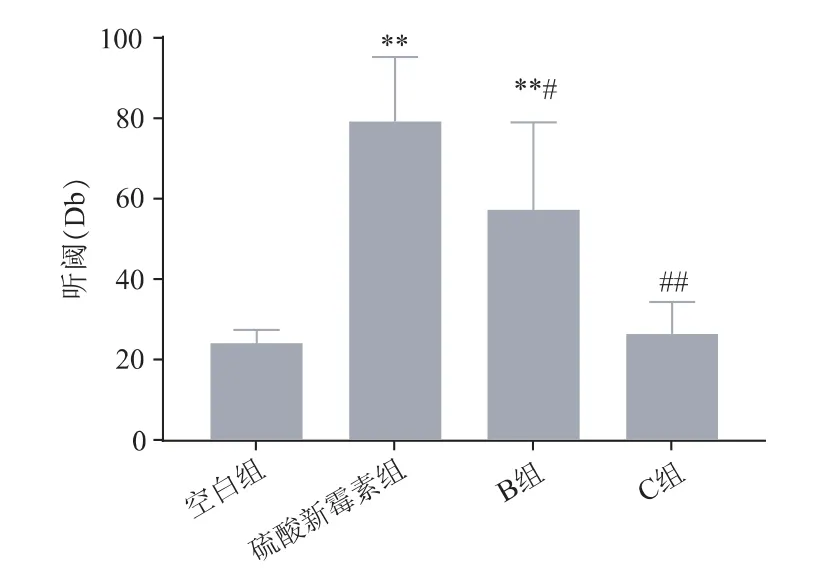
图2 硫酸新霉素及成分B、C 对豚鼠ABR 听阈的影响
2.3 硫酸新霉素及成分B、C 对斑马鱼的毒性考察
2.3.1 斑马鱼药物致死率研究 取成熟斑马鱼,黑暗10 h、照明14 h 条件下饲养,产卵时按雌雄1∶1 放入交配鱼缸,获取受精卵。实验挑选健康受精卵于6孔板中(试验前24 h 停止喂食)。实验分组同“2.2”项。给药的3 个组给予系列浓度受试药物,空白组加入小鱼培养液。斑马鱼暴露给药后每天以同样浓度药液换液1/2,分别在24、48、72 h 时间点观察斑马鱼反应及存活情况。结果显示,在100~250μg·mL-1浓度范围内,硫酸新霉素组与B 组在48 h 全部死亡;C组只有在浓度250 μg·mL-1下48 h 出现死亡,其他浓度72 h 才出现死亡。由于给药3 天后幼鱼基本死亡,故以72 h 为观察终点。用χ2检验(Fisher 精确概率法)对比各给药组给药72 h 后的累积死亡率,结果显示,硫酸新霉素组的毒性与B 组相比,无显著差异,两组毒性均明显高于C 组(P<0.001,P<0.001)。
2.3.2 斑马鱼器官毒性研究 实验分组同“2.2”项。取成熟斑马鱼,光照交替培养,产卵后选取健康胚胎,按每组给予30 枚胚胎,置于0.5、0.2、0.1 μg·mL-1不同浓度的试验药物中,每天更换药液1 次。胚胎发育至72 h 时,将测试液替换为人工海水,胚胎发育至第7 天时进行毛细胞染色,在荧光显微镜下观察毛细胞形态并拍摄。毛细胞染色结果显示,0.5 μg·mL-1剂量的硫酸新霉素组和B 组即可对毛细胞产生较大破坏(毛细胞数量较少),而C 组各剂量对毛细胞影响不大。见图3。
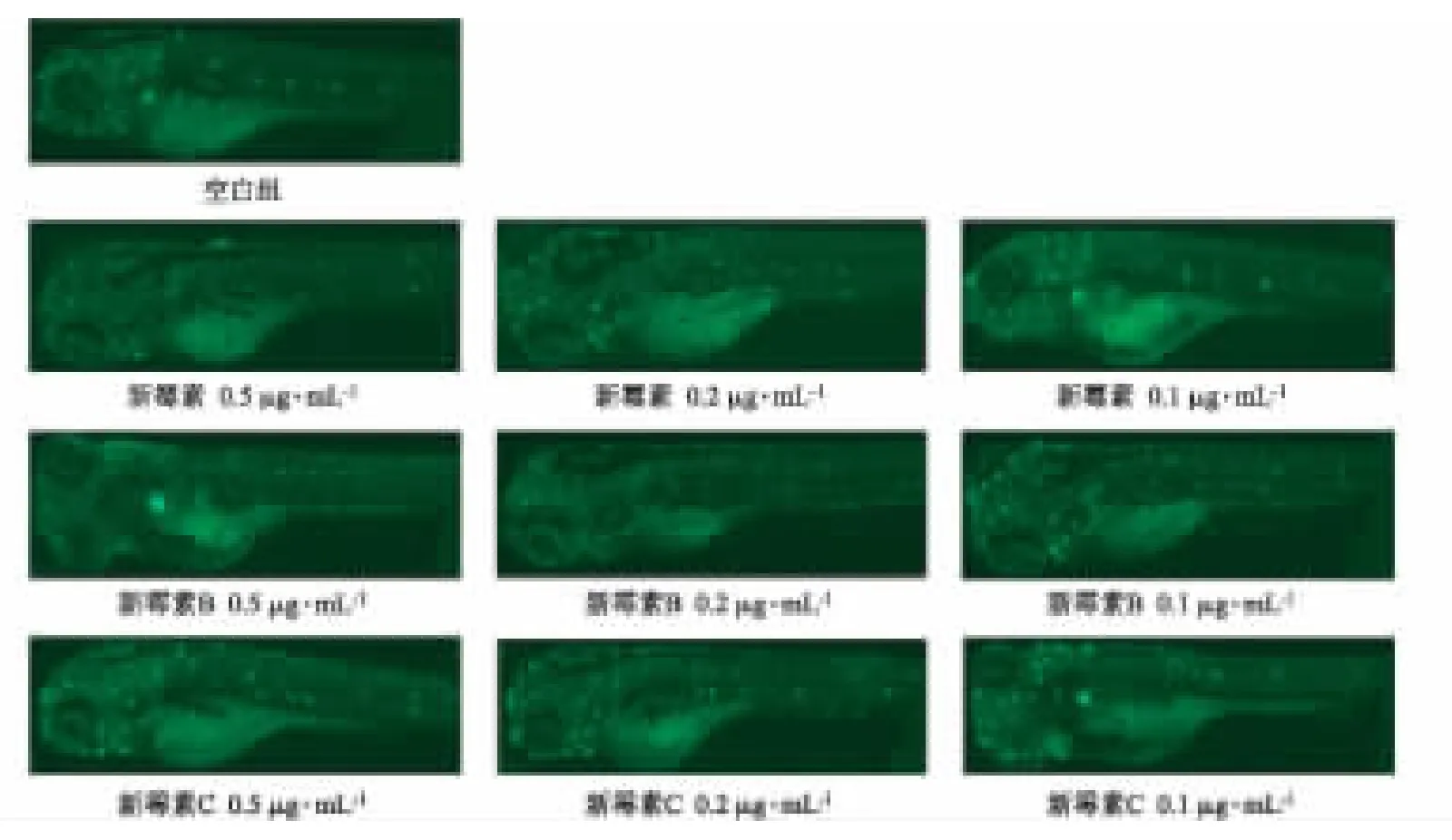
图3 斑马鱼毛细胞染色结果 注:荧光点代表毛细胞
3 讨论
3.1 体外抑菌活性的研究
常量肉汤稀释法和纸片扩散法为经典的体外抗菌活性测定方法,具有操作简单、定性结果肉眼可见、无需特殊仪器判定等优势。本研究采用上述两种方法研究了硫酸新霉素及成分B、C,新霉胺、核糖霉素及巴龙霉素的体外抗菌活性,获得了它们的抗菌效果信息并相互验证了它们的抗菌活性的强弱顺序。作为硫酸新霉素主要杂质的新霉胺抗菌作用较弱,采用微生物检定法按照平均装量计算硫酸新霉素含量时会产生较大偏差,提示应该控制新霉胺的含量。而成分B、C 抗菌效果与硫酸新霉素略有差别,临床应用过程中应重点关注各自不良反应,合理使用抗生素并作个体化治疗。
3.2 动物模型的毒性研究
氨基糖苷类抗生素的严重副作用为耳毒性,毛细胞为感受声波刺激的感觉上皮细胞,ABR 的Ⅰ波起源于与毛细胞相连接的听神经树突的突触后电位,毛细胞的损伤会引起ABR 的Ⅰ波的变化[6],因此ABR 是检测听觉系统损伤较为敏感的方法。在硫酸新霉素中,其成分B 约占80%,成分C 约占15%[7],本次实验为客观评估B、C 在硫酸新霉素引起的耳毒性中所带来影响的大小,故按照此比例设定剂量。结果显示,C 组ABR 听阈值与空白组相当,硫酸新霉素组和B 组ABR 听阈值明显升高。有理由推测,成分B 是引起硫酸新霉素耳毒性副作用的主要因素。
斑马鱼因具有与哺乳动物相似的生物结构及生理功能而被广泛用于毒理学研究[8]。结合药物致斑马鱼死亡率和器官毒性的结果,3 种物质的毒性排序为硫酸新霉素>B>C,与豚鼠听力损伤的研究结果一致,由此可进一步推测成分B 是硫酸新霉素中的主要毒性所在,而成分C 的毒性较弱。
3.3 对质量标准提高的一些思考
综合体外抗菌活性及毒性实验的结果,表明新霉胺抑菌作用较弱,成分C 的毒性与空白组相当,成分B 比硫酸新霉素毒性较低,提示可能存在其他毒性杂质。EP9.0 版采用HPLC-PAD 法测定硫酸新霉素的有关物质并明确了相关杂质限度[9]。2015 年版《中国药典》仅采用薄层色谱法对硫酸新霉素原药中的新霉胺控制限度[10],与国外药典比较存在较大差距。随着杂质谱控制理念广泛应用于新药研发,结合硫酸新霉素有关物质测定的相关文献报道的启示,建议在硫酸新霉素质量标准中增加对有关物质的控制,明确新霉素C、新霉胺、单杂及总杂的限度,提高该药质量。
