草果挥发油β-环糊精包合物的制备与评价
2019-12-30马小双张锐乖李文艳
马小双 张锐乖 李文艳


摘要:研究了草果挥发油β-环糊精包合物的最佳制备工艺条件并考察其表征和稳定性。先用水蒸气蒸馏法提取草果挥发油,以提取率为指标,用正交试验选出最佳提取工艺条件。用饱和水溶液法进行草果挥发油的包合,以β-环糊精为壁材,以包合率和包合产率为指标,通过正交试验,优选草果挥发油最佳的包合工艺条件。使用薄层色谱法(TLC)、紫外分光光度法(UV)和显微成像法对包合效果进行了评价,并考察了包合物在强光、高温、高湿环境下的稳定性。结果表明:优草果挥发油提取条件为蒸馏时间6h、液比1:8、浸泡时间1.5h。最佳草果挥发油包合工艺条件为草果挥发油与β-环糊精体积比为1:10、包合温度为40℃、包合时间为1.5h、β-环糊精与水的体积比为1:10。通过用TLC、UV和显微成像法表征分析后,形成草果挥发油β-环糊精包合物,并通过稳定性考察,其具有一定的杭光照性、热稳定性、湿稳定性。试验得出的最佳提取挥发油工艺和草果挥发油包合工艺操作简便,提取率高,包合物稳定性好。
关键词:草果;挥发油;β-环糊精;包合物;稳定性
中图分类号:S576 文献标识码:A 文章编号:1674-9944(2019)22-0198-06
1 引言
草果(Amomumtsaoko)又名草果子《小儿卫生总微论方》,为姜科豆蔻属(AmomurnRoxb)植物草果(A.tsaoko Crevostet Lemarie)的干燥成熟果实[1]。主产于广西、云南、贵州等地,主要化学成分为挥发油、柠檬醛、樟脑油、α-松油醇、香叶醇和橙花叔醇等,具有燥湿健脾、温胃止痛和止呕截疟的功能,用于寒湿内阻、脏腹胀满、呕逆和不思饮食等症[2]。其中,挥发油中的1,8-按油素具有驱风、镇静、抗菌、抗病毒、杀灭寄生虫及发汗作用;柠檬醛具有平喘、祛痰和抑菌的作用;樟脑油具有刺激神经,使头脑清醒灵活的作用;α-松油醇、香叶醇、橙花叔醇有明显的镇静和抗菌作用[3]。草果挥发油具有独特的香味,可以作香料使用,广泛用于食品、化妆品和香精香料中[3]。草果作为香料,挥发油为其最主要活性成分,2015版《中国药典》把测定挥发油总量作为评价草果品质的重要指标。
国内对草果挥发油的提取工艺[4~6]、化学成分[7,8]、药理作用[9,10]等的研究比较广泛,但有关草果挥发油β-环糊精包合物制备的相关文献比较少也不全面,而对其他草本植物挥发油包合物制备的文献比较多。刘宇等[11]对油樟叶挥发油β-环糊精包合物的制备工艺进行了研究及稳定性考察,采用饱和水溶液法制备包合物,进行正交试验,以包合产率和包合率为筛选指标,优选出最优包合工艺。裴贵珍等[12]对孜然挥发油β-环糊精包合物的制备与评价。李颖[13]等用星点设计-效应面法优化鱼腥草挥发油-β-环糊精包合物的制备工艺。
国外有关课题组[14]运用水蒸气蒸馏法从草果挥发油中鉴定出了73种成分,主要成分为1,8-按油素、ρ-对丙基苯甲醛、香叶醇、香叶醛、α-松油醇、α-水芹烯、橙花醛、橙花叔醇、β-蒎烯等。国外有关课题组在前期工作中已采用水蒸气蒸馏法和GC-MS技术分离鉴定了广西草果挥发油的成分,且与以往的国内外相关研究报道相似,但在化合物含量和部分化合物类型上有所差异。这种差异有可能是由于草果的采集地点、提取方法以及果型的不同所造成的。而本试验选用云南马关县的草果,属于文山特色品种,国内外都没有相关文献研究报道。
中药挥发油疗效显著,但在传统中药剂型的制备过程中并未得到关注,利用环糊精包合技术可达到增加挥发性成分的溶解度和溶出度、提高其生物利用度及稳定性、固体化和降低毒副作用等目的[15]。尤其适用于中药挥发油的制剂研究,目前,表征药物β-环糊精包合物的方法较多,可分别从热分析、光谱学、色谱学等方面的性质差异对其进行验证[16,17]。β-环糊精有很好的水溶性和稳定性,草果挥发油经β-环糊精包合后,为白色固体粉末,使草果挥发油中浓烈的气味基本被掩盖,且包合工艺操作简便,挥发油利用率高。
2 实验仪器与试剂
2.1 材料与试剂
材料:云南马关县草果、β-环糊精。
试剂:无水乙醇、正已烷、乙酸乙醋、香草醛、硫酸、蒸餾水、自来水等。
2.2 仪器与设备
200g手提式高速万能粉碎机:DFT-200型,温岭市林大机械有限公司;电子调温电热套:DZTW型;北京市永光明医疗仪器有限公司;电热恒温水浴锅:北京市永光明医疗仪器有限公司;循环水真空泵:SHZ-DⅢ;巩义市予华仪器有限责任公司;恒温鼓风干燥箱:DGG-9240A型;上海齐欣科学仪器有限公司;超声波清洗机:WF-250EH型;薄层点样器:SP-Ⅱ型,上海科哲生化科技有限公司;紫外可见分光光度计:T9型,北京普析通用仪器有限责任公司;照相显微镜:DMO500型;药品稳定实验箱:云南特安呐制药股份有限公司;尼龙筛、挥发油测定器、圆底烧瓶、冷凝管、铁架台、量筒、烧杯、玻璃棒、布氏漏斗、抽滤瓶、冰箱、分析天平、硅胶G薄层板、展开槽、毛细管、密封玻璃瓶、称量瓶、移液管、吸尔球、保鲜膜等。
3 实验方法
3.1 草果挥发油的提取(水蒸气蒸馏法)
按《中国药典》2015年版一部附录挥发油测定法(甲法)进行口将干燥的草果粉碎,过2号筛,称取草果粗粗粉80.00g,置于1000mL圆底烧瓶中,选择蒸馏时间、料液比、浸泡时间3个因素进行L9(33)正交试验,因素水平见表1。加入一定量的水,浸泡一定时间,连接挥发油测定器分别进行不同时间的蒸馏,精确读取挥发油的量[4]。
试验根据采用3因素3水平进行正交试验L9(33),如表1。
3.2 草果挥发油β-环糊精包合物的制备
3.2.1 操作方法
选择草果挥发油与β-环糊精的配比、包合温度、包合时间、β-环糊精与水的比例4个因素进行L9(34)正交试验,因素水平见表2。取β-环糊精适量,加蒸馏水配置成饱和溶液,置于恒温水浴锅上,搅拌的同时滴加草果挥发油,设定一定的搅拌时间,搅拌结束后,将形成的包合物混悬液置冰箱冷藏24h后,抽滤,弃去滤液,用15mL水乙醇洗涤包合物3次,直到无油渍,抽干后用恒温鼓风干燥箱50℃干燥,最后得到白色粉末状包合物。
3.2.2 包合物中实际含油量测定
包合率及包合物产率的测定,按《中国药典》2015年版一部附录挥发油测定法(甲法)进行。精密量取草果包合物,置于500mL圆底烧瓶中,加入蒸馏水300mL,连接挥发油测定器,使沸腾2h左右,直至油量不再增加后停止加热,放置至室温,读取挥发油实际含油量。并计算包合产率和包合率。
包合产率(%)=W包合物/(Wβ-环糊精+W挥发油)
包合率(%)=(包合物中实际含油量)/(挥发油加入量×空白回收率)
综合评分=包合率×80%+包合产率×20%
3.2.3 空白回收试验
精密量取3份挥发油1mL,分别置于500mL圆底烧瓶中,按“3.2.2”项下方法测定,分别读取油量,算出空白回收率。挥发油空白回收率=收集挥发油量/加入挥发油量×100%。
3.2.4 验证试验
取草果挥发油3份,按筛选出的最佳的包合工艺制备草果挥发油与β-环糊精包合物,对其制备工艺进行验证。
3.3 草果挥发油β-环糊精包合物表征研究
3.3.1 薄层色谱法
取草果挥发油1mL,用适量无水乙醇溶液溶解作为样品工;同理,取包合物适量按药典法提取挥发油,作为样品n;取包合物和β-环糊精各1g,用无水乙醇溶液20mL溶解,作为样品Ⅲ和Ⅳ;将样品点于硅胶G薄层板上,用正已烷,乙酸乙酯(17:3)为展开剂展开,以5%香草醛硫酸溶液为显色剂,烘干显色[11]。
3.3.2 紫外分光光度法
用精密移液管取草果挥发油1mL,用10mL无水乙醇稀释溶解,即样品溶Ⅰ;称取1g包合物,用10mL无水乙醇超声溶解15min,过滤,取上清液,用10ml容量瓶定容,即样品溶液Ⅱ,称取1gβ-环糊精,与样品溶液Ⅱ的处理方法相同,即样品溶液Ⅲ;将草果挥发油与β-环糊精物理混合,加入10mL无水乙醇超声溶解15min,与样品溶液Ⅱ的处理方法相同,即样品溶液Ⅳ。将草果挥发油、包合物、β-环糊精、草果挥发油与β-环糊精混合物四个样品在紫外分光光度计中进行200~800nm全波长扫描,观察吸收曲线变化[18]。
3.3.3 显微成像法
称取未研磨的β-环糊精、研磨的β-环糊精、包合物、草果挥发油和β-环糊精混合物各一定的量制成溶液,分别滴于载玻片上,用显微镜观察其成像并捕捉照相[18]。
3.4 草果挥发油包合物的稳定性考察
3.4.1 光稳定性试验
分别称取草果挥发油β-环糊精包合物、按照制备投料比混匀所得的草果挥发油与β-环糊精的混合物各3份,每份3g,置于称量瓶中,放于药品稳定实验箱均照射10d(强度4000Lx),于第0、5、10d时取样,按“3.2.2”项下方法测定挥发油相对含量[11]。然后所测得的挥发油含量/包合物(混合物)中挥发的原含量,得出包合物与混合物中草果揮发油的含量百分比。
3.4.2 高温试验
分别称取草果挥发油β-环糊精包合物、按照制备投料比混匀所得的草果挥发油与β-环糊精的混合物各3份,每份3g,置于称量瓶中,放于60℃恒温干燥箱内放置10d,于第0、5、10d时取样,测定挥发油相对含量[11]。
3.4.3 高湿试验
分别称取草果挥发油β-环糊精包合物、按照制备投料比混匀所得的草果挥发油与β-环糊精的混合物各3份,每份3g,置于称量瓶中,放在温度为25℃相对湿度为75%的药品稳定实验箱中。于第0、5、10d时取样,按“3.2.2”项下方法测定挥发油相对含量[11]
4 实验结果与分析
4.1 草果挥发油提取结果与分析
根据“3.2.2 "项下方法提取草果挥发油结果如表3,从表3中可以看出:A3>A2>A1,B2>B3>B1,C3>C1>C2;提取工艺条件为A3B2C3,确定草果挥发油最佳提取工艺条件:蒸馏时间为6h;料液比为1:8;浸泡时间为1.5h。极差R值RA>RC>RB,确定各因素对草果挥发油提取率的影响主次顺序依次为A>C>B,即蒸馏时间>浸泡时间>料液比。
4.2 草果挥发油包合的结果与分析
4.2.1 饱和水溶液法正交筛选结果
包合草果挥发油正交的筛选,从表4中可以看出:A3>A2>A1,B1>B3>B2,C2>C3>C1,D1>D2>D3;草果挥发油的包合工艺条件为A3B1C2D1,即直观分析结果,确定草果挥发油包合物最佳的包合工艺条件为草果挥发油:β-环糊精为1:10;包合温度为40℃;包合时间为1.5h;β-环糊精:水为1:10。极差R值RA>RC>RD>RB,各因素对草果挥发油包合物包合的影响主次顺序依次为A>C>D>B;即草果挥发油:β-环糊精>包合时间>β-环糊精:水>包合温度。
4.2.2 空白回收试验结果
读取3份草果挥发油油量分别为0.80mL,0.85mL,0.90mL,挥发油空白回收率为85.00%。
4.2.3 验证试验结果
3份草果挥发油的包合率分别为58.74%,56.24%,52.65%;包合得率分别为66.54%,60.21%,64.82%,结果表明,该挥发油的包合工艺条件稳定,具有重现性和可操作性。
4.3 草果挥发油包合物表征结果与分析
4.3.1 薄层色谱法
草果挥发油(Ⅰ)、包合后提取的挥发油(Ⅱ)、包合物(Ⅲ)以及β-环糊精(Ⅳ)的TLC色谱图如图1所示。由图1可看出,样品Ⅰ和样品Ⅱ在相同的位置上出现了相同颜色的斑点,且Rf值基本相同,样品Ⅲ和样品Ⅳ中没有斑点出现,表明草果挥发油包合物已经形成,其表面并无挥发油残留,而且包合前后草果挥发油主要的化学成分未见明显的变化,所以包合物质量较好,说明包合过程对挥发油成分无影响。
4.3.2 紫外分光光度法
草果挥发油(Ⅰ)、包合物(Ⅱ)、β-环糊精(Ⅲ)及草果挥发油与β-环糊精混合物(Ⅳ)的UV谱图如图2所示。由图2可看出,样品Ⅱ和Ⅲ溶液无草果挥发油的特征吸收峰,而样品工和W溶液在相同位置上有草果挥发油类似的吸收峰,说明草果挥发油已经被β-环糊精包合在疏水性空腔结构中,已经构成一种新的物质。
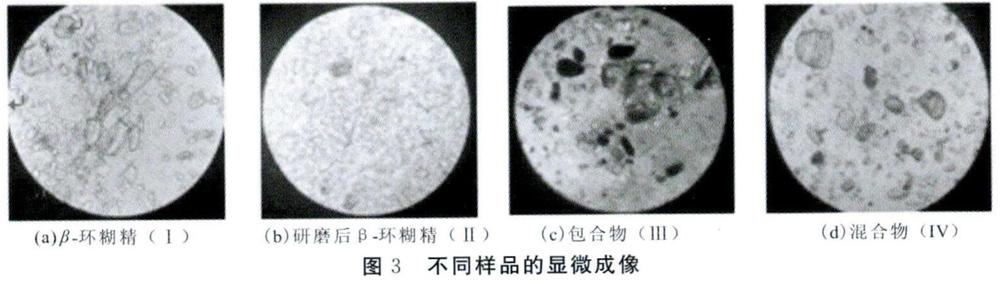
4.3.3 显微成像法
β-环糊精(Ⅰ)、研磨后β-环糊精(Ⅱ)、包合物(m)及草果挥发油和β-环糊精混合物(Ⅳ)的显微成像图如图3所示。由图3可看出,未研磨β-环糊精和研磨后β-环糊精为无色半透明立方体状结晶颗粒,颗粒粒度相对较大且清晰可辨,而草果挥发油β-环糊精包合物为黑色不透明不规则团状物质,草果挥发油和β-环糊精混合物为半透明立方体状结晶颗粒。试验表明β-环糊精仅在外力作用下并未发生变化,而β-环糊精包合草果挥发油后,其形态颜色均发生改变,显示新物质已经形成。
4.4 稳定性考察结果与分析
4.4.1 光稳定性试验结果
光稳定性试验结果见表5,由表5可知,在强光下照射10d,测定草果挥发油β-环糊精包合物和混合物在不同取样时间的样品挥发油含量,结果表明,草果挥发油β-环糊精包合物和混合物中的挥发油含量都有所下降,但混合物中的挥发油含量下降快速,草果挥发油β-环糊精包合物的抗光解性明显优于混合物。
4.4.2 高温试验结果
高温稳定试验结果见表6,由表6可知,在60℃恒温干燥箱内放置10d,测定草果挥发油β-环糊精包合物和混合物在不同取样时间的样品挥发油含量,结果表明,草果挥发油β-环糊精包合物和混合物中的挥发油含量都有所下降,但混合物中的挥发油含量下降明显,草果挥发油β-环糊精包合物的抗高温性明显优于混合物。
4.4.3 高湿试验结果
高湿稳定性试验结果见表7,由表7可知,在温度为25℃相对湿度为75%的药品稳定实验箱中放置10d,测定草果挥发油β-环糊精包合物和混合物在不同取样时间的样品挥发油含量,草果挥发油β-环糊精包合物和混合物中的挥发油含量都有下降趋势,但混合物中的挥发油含量下降趋势明显,草果挥发油β-环糊精包合物的抗高湿性明显优于混合物。
5 结论与讨论
因揮发油具有易挥发、易升华、不稳定的特点,故不宜单独用于中药制剂,将其制成包合物以克服上述缺点。草果挥发油具有抗氧化、调节胃肠功能、抗菌、抗肿瘤以及改变药物通透性等作用,但稳定性较差,对光敏感,强光下易分解。将草果挥发油制成包合物后,可减少挥发油的挥发,使其挥发油的稳定性提高。
本试验是按《中国药典》2015年版一部附录挥发油测定法(甲法)进行,用水蒸气蒸馏法提取草果挥发油,选择蒸馏时间、料液比、浸泡时间3个因素进行L9(33)正交试验,以提取率为指标,选出最佳提取工艺条件。试验结果,最优草果挥发油提取条件为蒸馏时间6h、料液比1:8、浸泡时间1.5h,用水蒸气蒸馏法提取的草果挥发油提取率可高达2.50%左右,3个因素中蒸馏时间是主要因素,浸泡时间次之,最后是料液比。
将提取好的草果挥发油用β-环糊精(β-CD)包合,包合方法为饱和水溶液法,用正交试验优选最佳工艺,以挥发油包合率、包合物产率为评价指标。最佳草果挥发油包合条件为:草果挥发油与β-环糊精体积比为1:10,包合温度40℃;包合时间1.5h;β-环糊精与水的体积比为1:10。最终草果挥发油的包合率可到达55.87%左右,包合物得率可到达63.85%左右,各因素对草果挥发油包合物包合影响的主次顺序依次为草果挥发油:β-环糊精>包合时间>β-环糊精:水>包合温度。通过用薄层色谱法(TLC)、紫外分光光度法(UV)和显微成像法表征分析后,表明草果挥发油包合物已经形成,其表面并无挥发油残留,而且包合前后草果挥发油主要的化学成分未见明显的变化,所以包合物质量较好。并通过稳定性试验,即将草果挥发油β-环糊精包合物和混合物在光照、高温、高湿条件下放置一段时间,测定草果挥发油β-环糊精包合物和混合物在不同取样时间的样品挥发油含量。试验结果表明,草果挥发油β-环糊精包合物和混合物中的挥发油含量都有所下降,但混合物中的挥发油含量下降快速,而草果挥发油β-环糊精包合物的挥发油含量下降缓慢,其草果挥发油β-环糊精包合物稳定性明显优于混合物,具有一定的抗光照性、热稳定性、湿稳定性,以达到增加药物溶解度、稳定性,提高生物利用度的目的。
本试验的客分子为草果挥发油,具有较强的挥发性。经β-环糊精包合,将草果挥发油制成包合物后,使液态油状草果挥发油改变成固体粉末的包合物,便于配方,还可具有缓释作用。避免了挥发油挥发,增强了其稳定性,同时因为β-环糊精的特性,又使其在水中的溶解度增加,从而提高了其生物利用度。而提取草果挥发油的原料为云南文山马关县的草果,马关县具有发展草果产业的天然优势,种植的草果质量好。草果挥发油的用途广泛,用β-环糊精包合草果挥发油,使其挥发油的稳定性提高,提高了云南草果的经济效益和社会效益。
参考文献:
[1]药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社.2010:165.
[2]徐国钧.常用中药品种整理和研究(第3册)[M].福州:福建科学技术出社,1997:217.
[3]代敏,彭成.草果的化学成分及其药理作用研究进展[J].中药与临床,2011,2(4):55~59
[4]闵勇,张薇,樊爱萍,等.微波辅助提取草果挥发油工艺研究[J].食品工业科技,2011(6):238.
[5]赵怡,张国英,肖中华,等.超临界CO2流体萃取法提取草果挥发油化学成分的研究[J].中国药学杂志,2004(09):69~70.
[6]熊将,花儿.正交实验优化超临界CO2提取草果挥发油工艺[J].食品科学,2012,33(24):48.
[7]丁艳霞,谢欣梅,崔秀明.不同方法提取草果挥发油的化学成分[J].河南大学学报(医学版),2009,28(4):284.
[8]闵勇,张薇,姚立华,等.云南省不同产地草果叶中挥发油化学成分研究[J].安徽农业科学,2011,39(6):3298~3300.
[9]冯雪,姜子涛.李荣.调味香料草果挥发油的抗氧化性能及清除自由基能力[J].中国调味品,2010,3(35):48.
[10]谢小梅,龙凯,钟裔荣,等.高良姜草果防霉作用的实验研究[J].药物研究,2002,11(5):45.
[11]刘宇,殷中琼,魏琴,等.油樟叶挥发油β-环糊精包合物的制备工艺研究及稳定性考察[J].中国中药杂志,2013,38(13):2105~2108.
[12]裴贵珍,陈文,马世俊,等.孜然挥发油β-环糊精包合物的制备与评价[J].中成药,2015,37(2):416~419.
[13]李颖,曾茂贵,游鹏程,等.星点设计-效应面法优化鱼腥草挥发油-β-环糊精包合物的制备工艺[J].中草药,2014,45(13):1855~1862.
[14]Yang Y,Yan R W,Cai X Q,et al.Chemical composition and anti-microbial activity of theessentialoil of Amomumtsao-ko[J].JSciFood Agric,2008,88(12):2111.
[15]Gao S,Sun J,Fu n,et al.Preparation,characterizationandpharma-cokineticstudiesoftacrolimus-dimethyl-β-cyclodextrininclu-sioncomplex-loadedalbuminnanoparticles[J].IntJ Pharm,2012,427:410~416.
[16]王大伟,刘琪,刘明,等.LNG-HP-β-CD包合物制备、表征及其紫外稳定性研究[J].光谱学与光谱分析,2011,31(3):808~811.
[17]Srinivasan K,Sivakumar K,Stalin T.2,6-Dinitroaniline andβ-cyclodextrin inclusion complex properties studied by different an-alytical methods[J].Carbohydr Polym,2014(113):577~587.
[18]毛軒睿,邵金华,孔童.等.野黄桂叶挥发油包合物的制备及评价[J].食品与机械,2018,34(12):205~210.
收稿日期;2019-10-11
作者简介:马小双(1982-),女,讲师,硕士,研究方向为中药资源的开发与应用。
