不同品种及排酸成熟时间对南方黄牛肉色和色素物质含量的影响
2019-11-28王文浩

摘要:为研究不同品种南方黄牛牛肉肉色间的差异及不同排酸时间对牛肉肉色的影响,以1周岁左右的黎平黄牛与西门塔尔牛为试验对象,在相同饲养环境条件下育肥6个月后屠宰测定背最长肌不同排酸时间(0、1、3、5、7、9 d)下的肉色变化,揭示不同黄牛品种肌肉肉色的差异。结果发现,随排酸的进行,2种肉牛牛肉pH值、总肌红蛋白和氧合肌红蛋白含量在一定时间内不断减少,高铁肌红蛋白含量不断增加,黎平牛肌肉L*值在排酸前7 d不断提高,且在测定的所有时间点都高于西门塔尔牛;黎平牛肌肉的a*和b*值变化幅度与西门塔尔牛相比较小。说明西门塔尔牛肌肉pH值达到较低水平要稍慢于黎平牛。排酸成熟能够显著改变2种牛肉的肉色,黎平牛肌肉肉色较西门塔尔牛鲜红、稳定性好。
关键词:南方黄牛;肉色;排酸时间;黎平黄牛;西门塔尔牛;肌红蛋白
中图分类号:TS251.5+2 文献标志码: A
文章编号:1002-1302(2019)18-0228-04
收稿日期:2018-06-05
基金项目:江西省教育厅科学技术项目(编号:GJJ161007);宜春地方发展研究中心项目(编号:2210816027)。
作者简介:王文浩(1988—),男,江苏射阳人,博士,讲师,主要从事动物生产相关研究。E-mail:wwh11@126.com。
牛肉中富含蛋白质,在氨基酸组成上比猪肉更接近人体需求,可提高人体免疫力,对于青少年的生长发育及术后、病后调养具有重要的作用。因其蛋白质含量高、脂肪含量低、味道鲜美,深受大众喜爱,享有“肉中骄子”的美称。我国幅员辽阔,各地区生态差异较大,形成了分布广泛、各具特色的地方黄牛品种。其中,南方黄牛是我国特有的种质资源。目前,市场上牛肉的嫩度、风味都比较差,因为其中主要为冷冻肉或热鲜肉,这2种牛肉的汁液流失多,难以满足消费者的需求。通常牛在屠宰后,牛肉最终转变成可食用肉一般要经过僵直、解僵以及成熟3个阶段。肉类成熟即指动物被宰杀后,生活时的正常生化平衡被打破,在动物体内组织酶的作用下,发生一系列复杂的生化反应,结果产生外观上的僵硬状态(僵直),经过一段时间这种僵硬现象逐渐消失,肉质变软,持水力和风味得到很大改善的变化过程[1]。
因此屠宰后排酸过程的控制对于牛肉品质的改善有着非常重要的意义,相关研究表明,排酸过程中肉pH值降低,能够抑制大部分微生物的生长,同时在酶作用下肉中部分肌浆蛋白分解成多肽和氨基酸,能够增加风味和改善口感。而肉色是显示肉品质量的重要指标,直接影响消费者的购买欲望,因此肉色可以用来衡量牛肉的经济价值[2]。肉的颜色取决于肌红蛋白和血红蛋白,后者主要存在于血液中,放血屠宰时随血液流失,前者(肌红蛋白)是肌浆内的球状血红素蛋白质,从充分放血的牲畜胴体中获得,为主要呈色物质,因此肌红蛋白决定了肉的颜色。有研究表明,在肉品成熟过程中肉色会发生剧烈的变化[3-4]。目前,国内外对猪肉色泽的研究较多,而对牛肉肉色的研究鲜有报道。
本研究对南方本地黄牛和国外引进的大型肉牛品种西门塔尔牛在不同排酸成熟时间进行了宰后肉色的指标测定,从肌肉中色素物质入手,发现2种肉牛在排酸过程中肉色的变化规律,旨在通过对牛肉肉色的研究,为南方黄牛肉质的改善和营养价值的提高提供理论基础。
1 材料与方法
1.1 试验动物与饲料
随机选取1周岁的黎平黄牛和西门塔尔牛(均为公牛),各10头,在相同的饲养环境条件下进行6个月的短期育肥试验,试验时间为2017年5—10月,所有试验动物饲养于宜春学院生命科学与资源环境学院生态牧场。饲料配方按照57.0% 玉米粉、12.0%菜籽粕、11.5%小麦麸、7.0%棉籽粕、5.0%大豆粕、1.4% 磷酸氢钙、1.1%植物油、1.0%添加剂预混料、0.5%小苏打、0.5%食盐等原则进行设计。日粮配方按照精饲料、粗饲料质量比为2 ∶1、2%体质量的日采食量原则进行配制,其中粗饲料为全青贮玉米饲料,主要成分包括95.27% DM(干物质)、4.42%CP(粗蛋白)、1.74%EE(粗脂肪)、4.37%Ash(粗灰分)、0.06%Ca(钙)、0.05%P(磷)、55.77% NDF(中洗纤维)和32.96%ADF(酸洗纤维)。上述饲料均购自宜春学院生命科学与资源环境学院农学系生态农场。
1.2 试验设计与样本采集
育肥期结束后,集中屠宰,宰前12 h禁食,2 h停水。每头牛经电击致晕,屠宰、剥皮后劈半称取酮体质量,将酮体从跟腱处悬挂在低温(0~4 ℃)排酸室,进行排酸,分别在排酸后的0、1、3、5、7、9 d(即宰杀后0、1、3、5、7、9 d)取每头牛12~13肋间背最长肌,进行肉色的测定。
1.3 试验仪器
美能达cR400型色差仪(日本柯尼卡公司);RH-N50型肌肉嫩度仪(广州润湖仪器有限公司);PHB-1型便携式pH计(上海三信仪表厂)。
1.4 测定方法
1.4.1 pH值 pH值利用便携式pH计进行测定,测定方法为探头伸入到肉样中,确保其电极和肌肉组织液完全接触,待其读数稳定后进行记录,每个肉样测定3次,取平均值,使用前须对仪器进行校准。
1.4.2 肉色 便携式色差仪经白板校准后,测定黎平黄牛和西门塔尔公牛不同排酸时段0、1、3、5、7、9 d背最长肌肉表面的a*值(红度)、H值(色相角)、L*值(亮度)、C值(彩色度)以及b*值(黄度)。L*、a*、b*值的测定方法为使肌肉表面與色差仪的镜头呈垂直状态,色差仪镜口与肉面紧扣,确保不漏光,并且单个样品重复测定3次,尽量使每次的测定位置都均匀分布在肌肉切面,并计算C和H。公式如下:C=[(a*)2+(b*)2]0.5;H=arctg(b*/a*)。
1.4.3 肌肉中色素物质的检测 将20 mL磷酸钠缓冲液(浓度为0.04 mol/L,pH值为6.8)与10 g肉样混匀研磨成浆,匀浆液在4 ℃条件下静置1 h后在离心机上离心30 min,离心转速为3 300 r/min。上清液经滤纸过滤后用上述磷酸钠缓冲液定容到25 mL,随后分别在572、565、545和525 nm波长处利用分光光度计测定其吸光度。
高铁肌红蛋白(MMb)百分含量=(-2.514R1+0.777R2+0.800R3+1.098)×100%;
氧合肌红蛋白(OMb)百分含量=(0.882R1-1.267R2+0.809R3-0.361)×100%;
总肌红蛋白(TMb)含量(mg/g)=-0.166D572 nm+0.086D565 nm+0.088D545 nm+0.099D525 nm。
其中:R1、R2、R3分别是吸光度比值D572 nm/D525 nm、D565 nm/D525 nm、D545 nm/D525 nm。
1.5 统计分析
数据统计分析采用SPSS 19.0软件,数据多重性比较利用Duncans法,试验数据采用“平均值±标准误”表示。
2 结果与分析
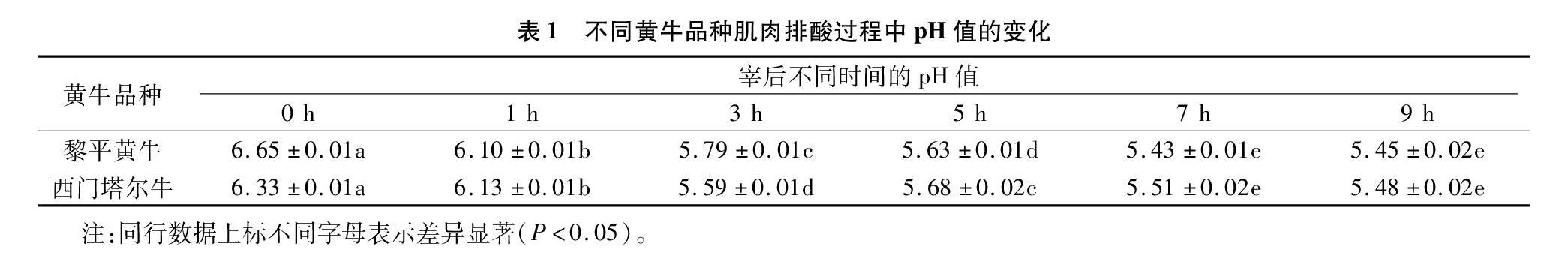
由表1的pH值可知排酸过程中肌肉嫩度的变化情况,宰后当天黎平牛肌肉的pH值高于西门塔尔牛;宰后0~3 d黎平牛和西门塔尔牛肌肉pH值均表现为显著下降趋势,3 d后黎平牛肌肉pH值持续下降,7 d后趋于稳定,而西门塔尔牛肌肉pH值在3 d后趋于稳定;宰后7~9 d黎平牛和西门塔尔牛pH值达到相同水平。
由表2可知,2种黄牛肌肉排酸过程中,宰后当天黎平牛肌肉的L*值与西门塔尔牛相当;西門塔尔牛和黎平牛肌肉的L*值在屠宰后0~5 d表现近似,均为明显上升趋势,黎平牛和西门塔尔牛肌肉的L*值在5 d后趋于稳定;宰后黎平牛肌肉的L*值在测定的所有时间点都要高于西门塔尔牛。
由表2中2种黄牛肌肉排酸过程中a*值的变化看出,宰后当天黎平牛肌肉的a*值低于西门塔尔牛;宰后0~7 d黎平牛肌肉a*值大致表现为先显著上升后下降的趋势,在宰后1 d 达到最高峰,7~9 d 趋于平衡,变化不明显。西门塔尔牛肌肉a*值在0~3 d持续上升,1~9 d变化不明显,但在9 d时与黎平牛肌肉a*值相当。
表2中2种黄牛肌肉排酸过程中肌肉b*值的变化显示,宰后当天黎平牛肌肉的b*值和西门塔尔牛一致;宰后0~7 d黎平牛肌肉b*值表现为明显的先快速上升后缓慢上升的趋势,在7 d时达到最高峰,随后开始下降。西门塔尔牛肌肉b*值在0~7 d表现为先上升后下降的趋势,在3 d时达到最高峰,但在9 d时与黎平牛肌肉b*值相当。
由表2还可以看出,2种黄牛肌肉排酸过程中,宰后当天黎平牛肌肉的C值低于西门塔尔牛;宰后0~9 d黎平牛肌肉C值表现为明显的先快速上升后平稳的趋势,在7 d时最大。西门塔尔牛肌肉C值在0~7 d表现为明显的先上升后下降的趋势,在排酸后3 d达到最高峰,7~9 d上升缓慢,在排酸后9 d与黎平牛肌肉C值相当。
此外,由表2可以看出,宰后当天黎平牛肌肉的H值高于西门塔尔牛;宰后0~9 d黎平牛肌肉H值表现为先显著地快速上升后平稳最后下降的趋势,在宰后7 d达到峰值。西门塔尔牛肌肉H值在0~7 d表现为先显著上升后下降的趋势,在宰后5 d达到最高峰,7~9 d变化不明显,趋于平稳,但在宰后9 d与黎平牛肌肉H值相当。
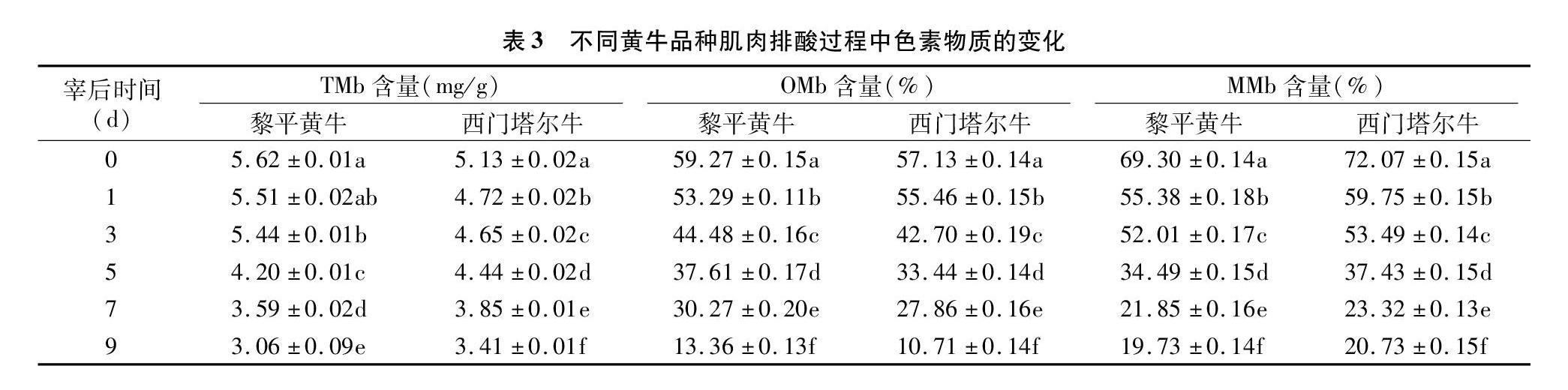
由表3可知,2种黄牛肌肉排酸过程中,黎平牛和西门塔尔牛的TMb含量均表现为明显的下降趋势,宰后前3 d黎平牛的TMb含量高于西门塔尔牛,随后几天西门塔尔牛的TMb含量高于黎平牛。
由表3中2种黄牛肌肉排酸过程中氧合肌红蛋白含量的变化看出,黎平牛和西门塔尔牛的OMb含量均表现为明显的下降趋势,但是黎平牛肌肉中OMb的含量下降明显缓于西门塔尔牛。
由表3还可以看出,2种黄牛肌肉排酸过程中,黎平牛和西门塔尔牛的MMb均表现为明显的上升趋势,但是黎平牛肌肉中MMb的含量上升明显缓于西门塔尔牛。
3 讨论
动物被屠宰后肌肉中pH值降低的原因是宰后各种无氧代谢相关的生化反应仍然继续发生,大量乳酸等物质不断产生。动物体内pH值一般在7.0左右,宰后由于乳酸产生导致pH值逐渐下降。本研究发现,黎平牛和西门塔尔牛在宰后0~7 d的过程中,其pH值持续下降,在7 d后趋于稳定,达到极限值5.5左右。如果宰后pH值>6.8,说明牛肉被腐败菌污染,腐败菌使肉中蛋白质分解从而产生有毒元素并发出恶臭味道[5]。此外,肉色、持水性、微生物繁殖速度及蛋白质溶解度变化都受pH值下降影响。有研究发现,pH值下降速度与温度、品种有关[6]。
本研究中西门塔尔牛肌肉pH值优先达到较低水平,但是肌肉pH值稳定时,黎平牛pH值要低于西门塔尔牛,肌肉pH值降低,抑制了大部分微生物生长,由此推断黎平牛冷鲜肉保存期较西门塔尔牛要长。有关学者研究发现,pH值与肌肉颜色(L*值、a*值、b*值)密切相关,主要由于pH值升高(大于蛋白质等电点)时,肌肉持水性增加,从而提高肌肉表面的吸光能力,肉色加深[7],pH值升高到一定极限值时,可以改变肌红蛋白功能而使肌肉呈现暗红色[8]。据报道,肌红蛋白是决定肉色的主要因素,肌红蛋白以如下3种状态存在:还原型、氧合型、高铁型,这3种不同状态的肌红蛋白可以相互转换,分别呈现出暗紫色、鲜红色以及棕褐色[9]。肉颜色的稳定性是由Fe2+的肌红蛋白保持程度所决定的[10]。随着熟化时间的延长,氧合肌红蛋白氧化生成高铁肌红蛋白MMb,肉品发生褐变[11]。本研究中随着熟化时间的延长,氧合肌红蛋白OMb的含量持续下降,致使肌肉的颜色变为褐色。
L*为明度系数,主要受肌肉中脂肪沉积量和肌红蛋白含量的影响,其值为0~100不等,值越大亮度越大。随着排酸时间的持续,2个试验组的肉牛肌肉L*测定值都在一定时间内增大,这是因为在排酸的过程中,随着pH值的不断下降,肌肉蛋白变性、肌肉收缩、汁液渗出、结合水减少导致肉表面反射特性改变[12]。本研究中总肌红蛋白的含量随着熟化时间的延长持续下降,这种情况考虑与肌肉保水性的不同有关,本试验也注意到在排酸过程中肌肉出现了不同程度的渗水现象,并且肌红蛋白是水溶性蛋白,主要存在于肌浆中,因此TMb的损失与肌肉的保水性有关。排酸5 d后,2种肉牛肌肉的pH值变化幅度变缓,与肌肉L*值的变化规律相一致。黎平牛肌肉的L*值在排酸的各个时间点均高于西门塔尔牛,说明黎平牛肌肉较西门塔尔牛鲜亮,更易受到消费者的青睐。
a*为红度值,其值由负到正变化表示肉色由绿色逐渐变为红色。近期研究表明,冷鲜肉肉色测定中最重要的肉色指标是红度值,通常情况下随着贮藏时间的延长红度值会不断减少,但如果肌肉采用真空包装并存放在0 ℃,红度值在14 d之内都不会改变。该研究中还证明了肉色褐变的速度会随着存放地温度的升高而加速,除此之外,肉色褐变的速度还会受到空气中氧浓度的影响,相关研究证明了红度值与肉色稳定性存在密切关系,肉色会受到贮藏时间、贮藏温度和包装方式的影响[13]。本研究中2种肉牛的肌肉摆放于4 ℃ 冷库进行排酸成熟,温度较低,空气中氧气浓度变化不大。肉色的a*值均大于0,即都为红色,黎平牛肌肉的a*值在宰后1 d后变化幅度较小,并且黎平牛肌肉中氧合肌红蛋白的含量下降趋势较西门塔尔牛缓慢,这就说明黎平牛牛肉肉色稳定性较好。
b*为黄度值,其值由负变到正表示肉色由蓝色逐渐变为黄色。本研究中2种肉牛肌肉的黄度值均大于0,表现为黄色。黄度值主要由于在宰后初期,氧合蛋白和肌红蛋白含量相对较高,比值越高,黃度值越高,随着时间的延长,肌红蛋白和氧合肌红蛋含量下降。Mancini等的结论与本研究的结果不矛盾,屠宰放血后的肌肉由于缺氧主要存在还原型肌红蛋白,此时肌肉呈现暗紫色[14];本研究中排酸前期,肌肉的总肌红蛋白和氧合肌红蛋白含量均处于较高的水平,此时肌肉呈鲜红色,该色是最理想的肉色,也是消费者最喜爱的肉色。随着暴露时间的延长和高温、紫外线的作用,肌红蛋白的球蛋白部分变性,失去了保护血红素的功能,使得氧合型肌红蛋白变成棕褐色的高铁型肌红蛋白[15]。黎平牛肌肉的b*值在宰后1 d后变化幅度较小,说明黎平牛牛肉肉色稳定性较好。C和H值是由a*和b*值通过公式计算出来的,变化规律与a*和b*值相一致,不多作讨论。
4 结论
通过宰后排酸成熟,西门塔尔牛肌肉pH值相较黎平牛优先达到较低水平,从而抑制了微生物的繁殖。排酸成熟能够显著地改变2种牛肉的肉色,随排酸时间的延长,肉色变化程度越不明显。经排酸成熟处理,在肉色上,黎平牛肌肉较西门塔尔牛鲜红;在肉色稳定性上,黎平牛肌肉较西门塔尔牛稳定性好。
参考文献:
[1]Li K,Zhang Y M,Mao Y W,et al. Effect of very fast chilling and aging time on ultra-structure and meat quality characteristics of Chinese Yellow cattle M. Longissimus lumborum[J]. Meat Science,2012,92(4):795-804.
[2]Neath K E,Del Barrio A N,Lapitan R M,et al. Difference in tenderness and pH decline between water buffalo meat and beef during postmortem aging[J]. Meat Science,2007,75(3):499-505.
[3]Holmer S F,Mckeith R O,Boler D D,et al. The effect of pH onshelf-life of pork during aging and simulated retail display[J]. Meat Science,2009,82(1):86-93.
[4]Ngapo T M,Riendeau L,Laberge C,et al. Marbling and ageing - Part 1. Sensory quality of pork[J]. Food Research International,2012,49(1):396-405.
[5]Machado M,Lage J F,Ribeiro A F,et al. Quality of aged meat of young bulls fed crude glycerin associated with different roughage sources[J]. Acta Scientiarum.Animal Sciences,2015,37(2):167-172.
[6]Weglarz A. Meat quality defined based on pH and colour depending on cattle category and slaughter season[J]. Czech Journal of Animal Science,2010,55(12):548-556.
[7]Fletcher D L,Qiao M,Smith D P. The relationship of raw broiler breast meat color and pH to cooked meat color and pH[J]. Poultry Science,2000,79(5):784-788.
[8]Jung S,Ghoul M,de Lamballerie-Anton M. Influence of high pressure on the color and microbial quality of beef meat[J]. LWT - Food Science and Technology,2003,36(6):625-631.
[9]Luno M,Roncales P,Djenane D,et al. Beef shelf life in low O2 and high CO2 atmospheres containing different low CO concentrations[J]. Meat Science,2000,55(4):413-419.
[10]馬汉军,周光宏,徐幸莲,等. 高压处理对牛肉肌红蛋白及颜色变化的影响[J]. 食品科学,2004,25(12):36-39.
[11]梁成云,刘笑笑,孟令丽,等. 日粮VE水平对熟化过程中牛肉肉色和抗氧化酶活性的影响[J]. 食品科学,2008,29(8):61-64.
[12]Papaleo Mazzucco J,Melucci L M,Villarreal E L,et al. Effect of ageing and u-calpain markers on meat quality from Brangus steers finished on pasture[J]. Meat Science,2010,86(3):878-882.
[13]Olivera D F,Bambicha R,Laporte G,et al. Kinetics of colour and texture changes of beef during storage[J]. Journal of Food Science and Technology,2013,50(4):821-825.
[14]Mancini R A,Hunt M C. Current research in meat color[J]. Meat Science,2005,71(1):100-121.
[15]Lawrie R A. Chemical and biochemical constitution of muscle[M]//Toldra F. Lawries meat science. Oxford:Woodhead Publishing,1998:58-95.
