传统与补料发酵玫瑰醋香气成分的分析
2019-07-20陈笑钗李婷黄炳文蒋予箭
陈笑钗,李婷,黄炳文,蒋予箭*
(1.浙江五味和食品有限公司,浙江 湖州 313213;2.浙江工商大学 食品与生物工程学院,杭州 310018)
不同的发酵工艺使食醋香气成分在量上有很大差异[1]。形成食醋香气的成分主要包括酸类、酯类、醇类等挥发性成分。固相微萃取(SPME)技术是近年来发展起来的一种样品前处理技术,常与GC-MS联用来分析和鉴定风味物质[2,3],它集萃取、浓缩、进样为一体,选择性和重现性好,灵敏度高,提高了分析检测的效率和准确性。近年来多研究食醋香气物质的定性分析,但关于浙江玫瑰醋所得成品的香气主要组成成分及定量分析的方法研究少有报道。
已经研究了补料发酵技术对玫瑰醋生产工艺改良的可行性,在控温(31±1) ℃发酵条件下,初始酸度2.5 g/dL时补加1/2体积的稀释至酒精度6%酒液,醋酸发酵结束时,酸度最高上升到(5.48±0.27) g/dL,与传统工艺最高酸度达(4.81±0.15 ) g/dL对比,酒精转化醋酸的效率得到提高,醋酸生成量增加。并且补料工艺对玫瑰醋色泽形成无显著影响。补料工艺玫瑰醋符合产品标准,且酸度比传统发酵高,提高了产品得率,经过感官品评分析,补料产品保留了传统工艺玫瑰醋的主要风味特性[4,5]。玫瑰醋补料发酵技术路线见图1。
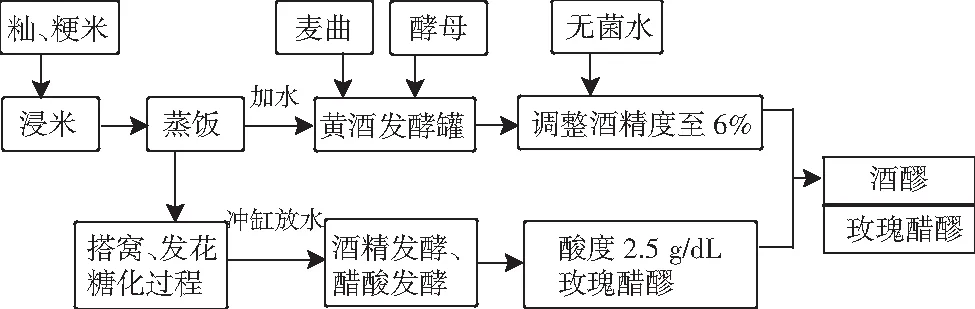
图1 工艺流程Fig.1 Technological process
本文对固相微萃取条件进行了优化,考察萃取头、萃取时间、萃取温度对玫瑰醋样品中挥发性风味物质萃取的影响[6],采用内标法对香气成分定量,测定其有效性及回收率,建立玫瑰醋挥发性香气物质的测定方法,对传统及补料发酵生产的浙江玫瑰醋香气成分组成进行了分析。
1 材料与方法
1.1 材料与试剂
β-苯乙醇、乙酸乙酯、苯甲醛、2-乙基丁酸、乙酸:均为色谱纯;氯化钠、无水乙醇:均为分析纯。
1.2 主要仪器与设备
AR2140型电子分析天平 奥豪斯国际贸易有限公司;7890A-5975C型气相色谱-质谱联用仪 美国Agilent公司;固相萃取纤维头(50/30 μm DVB/CAR/PDMS、85 μm PA) 美国Supelco公司;HH-6数显恒温水浴锅 常州国华电器有限公司;AL204型电子分析天平 深圳市科衡仪器电子有限公司。
1.3 实验方法
1.3.1 香气物质测定方法的建立
1.3.1.1 萃取头的老化
在使用固相萃取纤维头之前,必须进行老化,老化至无杂质的干扰峰出现。在气相色谱的进样口处,将萃取头于240 ℃老化30 min。
1.3.1.2 SPME样品前处理
取样品10 mL置于20 mL顶空瓶中,用带有硅橡胶隔垫的瓶盖密封。先将顶空瓶放入恒温水浴锅平衡30 min,然后将萃取头插入顶空瓶中距离液面1 cm处,在一定温度下吸附一定时间。之后抽回纤维头,从顶空瓶中拔出萃取头,取出后将萃取头量程调为4 cm,插入GC-MS仪的气相色谱进样口,推出纤维头,于240 ℃下解吸2 min,进行GC-MS分析。
1.3.1.3 GC-MS分析条件
气相色谱条件:色谱柱:DB-WAX,60 m×0.25 mm×0.5 μm(柱长×内径×膜厚);进样口温度:240 ℃,不分流进样,载气为氦气,恒流模式,柱流速:1 mL/min;柱温:30 ℃保持6 min,以2 ℃/min升到140 ℃,然后以4 ℃/min升到220 ℃,保持10 min。
质谱条件:离子源EI,离子源温度230 ℃,四级杆温度150 ℃,质量数扫描范围33~500 amu。
1.3.1.4 SPME萃取参数条件优化
a.萃取头的选择
实验选择食品香气分析中2种常用的纤维萃取头,非极性复合涂层50/30 μm DVB/CAR/PDMS和强极性85 μm PA萃取头,以固相微萃取后进样测定的化合物总色谱峰面积和色谱峰数为指标,比较以上2种萃取头对浙江玫瑰醋样品的萃取效果。
b.SPME的萃取条件优化
结合文献可知,固相微萃取的萃取时间及温度的选择对萃取效果有很大的影响,在萃取挥发性风味物质时,加入适当浓度盐类可有效提高挥发性成分在顶空的浓度[7]。在萃取温度40 ℃,萃取时间30 min,样品中添加150 g/L浓度NaCl的基础上,比较不同萃取温度(30,40,50,60,70 ℃),不同萃取时间(20,30,40,50,60 min),不同NaCl质量浓度(150,200,250,300,350 g/L)对玫瑰醋香气物质萃取效果的影响。
1.3.2 玫瑰醋中香气成分的定性分析
采用计算机检索谱库,由Xcalibur软件系统完成,未知化合物通过计算机检索与NIST DEMO 2.0谱库相匹配,对正反匹配度都大于800(最大值为1000)的鉴定结果给予定性,结合化学成分的保留时间、质谱图谱、实际成分和保留指数等鉴定化合物结构,从而确定浙江玫瑰醋的香气组成成分。
1.3.3 玫瑰醋中香气成分的定量分析
1.3.3.1 内标物的配制
内标物的选择原则有:(1)与被分析物质的物理化学性质要相似(如:沸点、极性、化学结构等);(2)被分析试样中不存在的纯物质;(3)能完全溶于被测物品(或溶剂)中,且不与被测样品起化学反应,并与试样中各组分的色谱峰能完全分离[8]。本实验选择2-乙基丁酸作为内标物。准确吸取2 mL的2-乙基丁酸于100 mL容量瓶中,用20%乙醇定容,配制的内标物浓度为159.18 mg/L。
1.3.3.2 混合标准溶液的配制与相对响应因子的测定
选择食醋中常见的几种代表性酸类、酯类、醇类和醛类物质,测定它们对内标物2-乙基丁酸的相对响应因子。除醛类外,其他的羰基化合物和杂环化合物以与醛类物质的相对响应因子计算[9]。
选择β-苯乙醇、乙酸、乙酸乙酯、苯甲醛组分,配制体积百分比1.0 mL/L的标准储备液。测定相对响应因子时将标样稀释10倍,则标准液中各组分浓度为0.1 mL/L。
采用加标法测定各组分的相对校正因子,取一定量的混合标液加入到玫瑰醋样品中,通过峰面积的增大量来计算该组分的校正因子。以2-乙基丁酸为内标物,将内标物和标样等体积混合后,吸取100 μL加入到10 mL醋样中,在1.3.1.3的GC-MS分析条件下进样,计算各香气组分的相对校正因子,得出各组分的保留时间和峰面积。相对校正因子(fi)的计算公式:
(1)
式中:ΔAi和ΔWi分别表示组分标品i的增加含量和对应增加的峰面积;As和Ws表示内标物s的含量与峰面积。
待测风味物质的含量计算公式:
(2)
式中:Wi和Ai分别是被测组分的含量与峰面积;Ws和As分别为内标物的含量与峰面积。
1.3.4 香气测定方法有效性评价
取同一玫瑰醋样品,分别萃取5次后进样,选取相对含量较大,出峰时间间隔较大的多种香气组分,对其保留时间和相对含量进行再现性和回收率测定。
2 结果与分析
2.1 香气成分测定萃取条件优化
2.1.1 萃取纤维头的选择
萃取头是SPME装置的核心组成部位,不同固定相构成的萃取头型号会影响对物质的萃取吸附能力。本实验比较了50/30 μm DVB/CAR/PDMS和85 μm PA 2种纤维头在相同的吸附条件(40 ℃吸附30 min)和解吸附条件(240 ℃解吸2 min)下,对浙江玫瑰醋挥发性风味物质的萃取效果,结果见图2。

图2 不同萃取纤维头对萃取效果的影响Fig.2 The extraction effect of different extraction fiber heads
由图2可知,50/30 μm DVB/CAR/PDMS纤维头的萃取效果明显较好,总峰面积为1.54×109,几乎是85 μm PA总峰面积的1.48倍。从检出的有效化合物个数来看,50/30 μm DVB/CAR/PDMS检出了56种化合物,而85 μm PA检出了43种化合物。型号为50/30 μm DVB/CAR/PDMS复合涂层的萃取头对玫瑰醋样品来说,进行风味萃取更为合适,分离出的化合物较全面,色谱分析响应值较高,且风味强度较大,故选择此型号作为萃取玫瑰醋风味物质的萃取头。
2.1.2 萃取时间的选择
选用50/30 μm DVB/CAR/PDMS萃取头,萃取温度为40 ℃的条件下,以可检出的总峰面积及化合物色谱峰数为指标,比较5个不同吸附时间对萃取效果的影响,结果见图3。
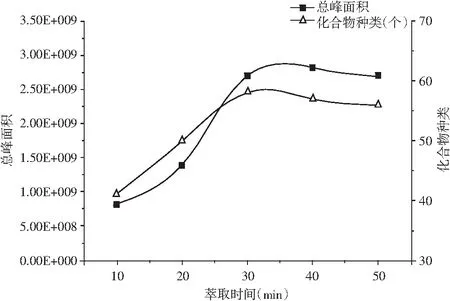
图3 萃取时间对总峰面积和色谱峰数的影响Fig.3 The effect of extraction time on total peak area and chromatographic peak number
由图3可知,随着萃取时间延长,萃取物质总峰面积随之增加,吸附时间从10 min延长到30 min,总峰面积及检测到的有效化合物个数增加较为明显,之后增加幅度减小,趋于平衡,这是因为固相微萃取是一个吸附-解吸附的过程,30 min时基本达到平衡,此时间与GC-MS分析样品所需时间较接近,可以提高单位时间内样品分析效率。
2.1.3 萃取温度的选择
萃取温度是影响萃取效果很重要的因素,一方面温度升高可以提高顶空固相微萃取的吸附效果,另一方面温度超过合适范围会引起萃取头固有组分的解吸,使萃取头的吸附能力下降,因此选取合适的萃取温度尤为重要[10]。选用50/30 μm DVB/CAR/PDMS萃取头,萃取时间为30 min的条件下,以总峰面积和检出的色谱峰数为指标,比较不同萃取温度(30,40,50,60,70 ℃)对玫瑰醋挥发性成分萃取效果的影响,结果见图4。

图4 萃取温度对总峰面积和色谱峰数的影响Fig.4 The effect of extraction temperature on total peak area and chromatographic peak number
由图4可知,萃取温度升高时萃取量(总峰面积)有所增加,但萃取温度升高到50 ℃以后,总峰面积增加比较平缓,但检出有效化合物数量在减少。可能原因是过高的温度引起一些物质发生化学变化,故选择萃取温度50 ℃作为本次实验的最佳温度。
2.1.4 添加盐浓度的选择
适当加入NaCl等盐类,可以增大溶液的离子浓度,同时减小液体对挥发性物质的束缚,增大有机物质的逸出活度,提高仪器的响应值及降低挥发性物质的检出限[11],提高萃取时的吸附效率。选用50/30 μm DVB/CAR/PDMS萃取头,50 ℃萃取30 min的条件下,比较NaCl不同质量浓度水平对萃取效果的影响,结果见图5。
由图5可知,当NaCl质量浓度从150 g/L增加到300 g/L时,检测到的化合物种类呈增多的趋势,增加到350 g/L时检测到的化合物种类有所减少,可能原因是盐浓度过高,与有机物发生反应。因此,调整样品中NaCl质量浓度为300 g/L较为合适。
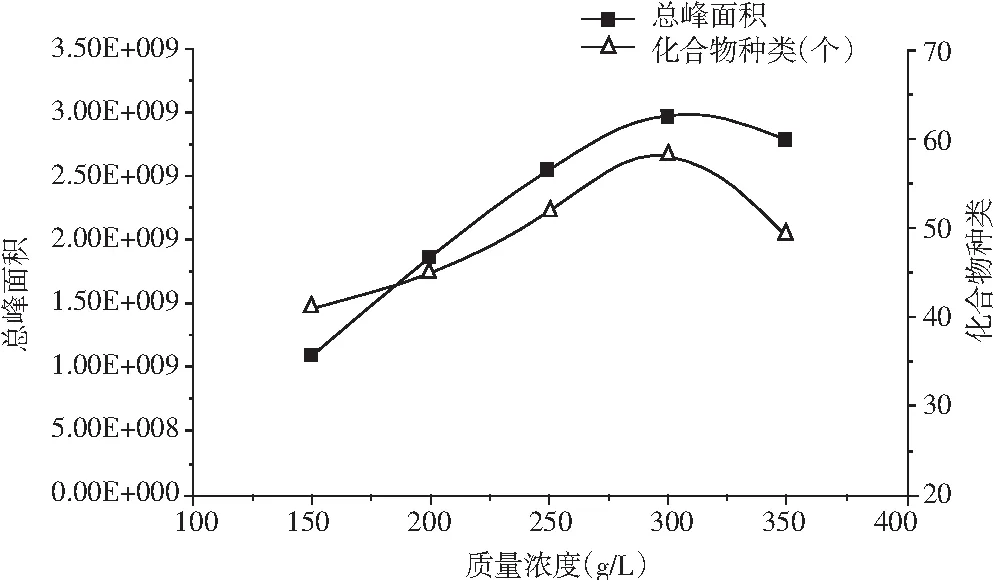
图5 盐离子浓度对总峰面积和色谱峰数的影响Fig.5 The effect of NaCl concentration on total peak area and chromatographic peak number
2.2 SPME萃取方法的有效性验证
采取上述优化的操作条件(萃取时间30 min,萃取温度50 ℃,NaCl浓度300 g/L),对某玫瑰醋样品萃取5次,分别进样,选择相对含量较大的多种香气物质,对其保留时间和相对含量进行重现性及方法回收率分析,结果见表1和表2。

表1 保留时间重现性结果Table 1 The results of retention time repeatability

表2 标样的回收率实验Table 2 The results of standard sample recovery experiment
结果表明,各香气物质保留时间的相对标准偏差RSD<1%,说明该香气测定方法出峰时间较稳定,实验精密度高。方法回收率在83.32%~98.62%,样品回收率能满足测定要求。
2.3 浙江玫瑰醋中香气物质组成测定
2.3.1 气相色谱-质谱联用(GC-MS)进样分析谱图及定性分析
原料及其酒精发酵、醋酸发酵和成熟过程都可以产生浙江玫瑰醋的香气成分[12]。经1.3.1.2方法对样品进行顶空固相微萃取预处理后,对1种传统发酵玫瑰醋和1种初始酸度2.5 g/dL补料1/2体积的补料发酵玫瑰醋进行气相色谱-质谱联用(GC-MS)进样分析,传统发酵玫瑰醋所得谱图见图6,补料发酵玫瑰醋所得谱图见图7。经1.3.2对挥发性成分定性分析,得到色谱峰对应成分及相对峰面积,见图8。

图6 传统发酵玫瑰醋GC-MS谱图Fig.6 GC-MS spectrogram of traditional fermented rose vinegar
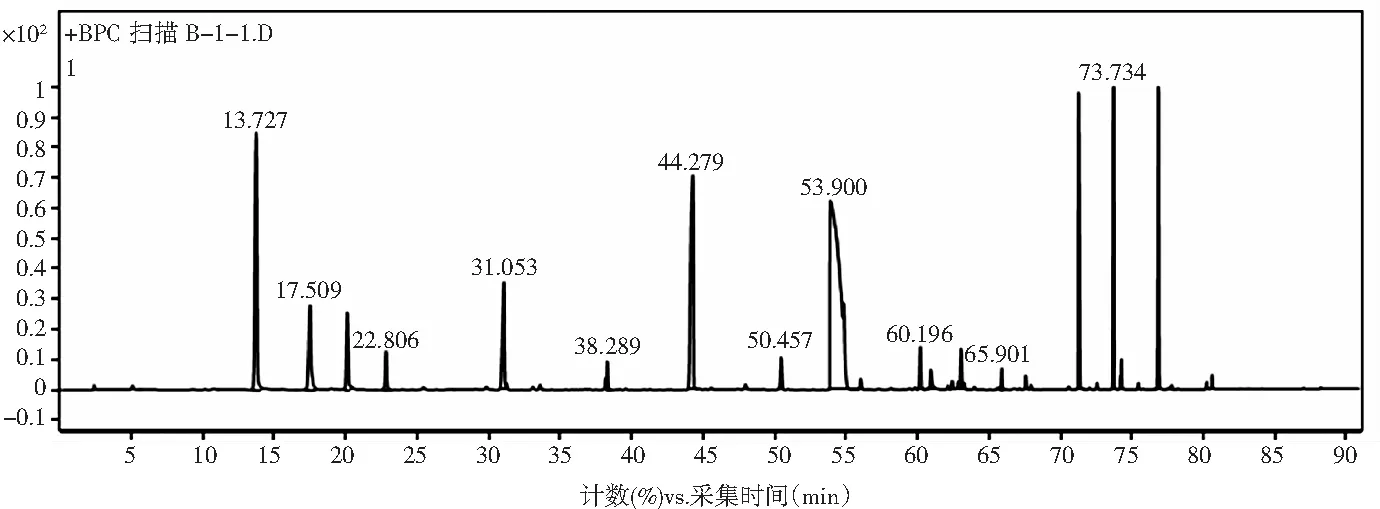
图7 补料发酵玫瑰醋GC-MS分析谱图Fig.7 GC-MS spectrogram of fed-fermented rose vinegar

图8 补料与传统发酵玫瑰醋的香气物质相对含量的比较Fig.8 Comparison of relative content of aroma components in fed-fermented and traditional fermented rose vinegar
由图8可知,酸类、酯类、醇类是组成玫瑰醋香气成分的主要物质,占可检出挥发性物质含量的80%左右,补料发酵玫瑰醋的醇类和酚类物质相对含量比传统发酵低,而酯类、酸类、酮类、醛类成分的相对含量较传统发酵醋样高,酯类含量明显高于传统发酵,可能原因是黄酒醪液的加入促进了玫瑰醋发酵的酯类物质生成,酯类物质多,可以形成一种果香味。
2.3.2 玫瑰醋中香气物质组成分析
按照1.3.3香气物质定量方法,以计算出的相对校正因子对玫瑰醋中检测的香气成分进行定量分析,结果见表3。

表3 不同发酵工艺的玫瑰醋香气成分定量结果Table 3 Quantitative results of aroma components of rose vinegar with different fermentation process μg/L

续 表 μg/L
采用内标法对不同发酵工艺玫瑰醋的香气成分进行定量[13],在保持原有香气成分的基础上,由于补料的加入,对风味的丰富有一定有利的影响,但补料发酵对玫瑰醋风味成分含量有较大的影响,主要有以下几方面的变化:
(1)补料工艺对醇类的组成影响不大,但对其含量影响较大。传统发酵玫瑰醋醇类主要组分为乙醇、2,3-丁二醇、β-苯乙醇。补料工艺醋样中乙醇占香气总含量的0.13%,传统发酵乙醇占0.26%,表明醋酸发酵比较彻底。β-苯乙醇在2种样品中均大量存在,苯乙醇是苯丙氨酸经降解产生醛,然后再还原生成的[14]。而β-苯乙醇具有清甜玫瑰香气,气味持久,不仅是组成黄酒的重要香气成分,也对玫瑰醋的香气贡献较大,补料发酵降低了2,3-丁二醇的含量,但使其他高级醇的含量更为丰富,异丁醇、异戊醇、二异丁基甲醇含量也有提高,由于补料促进醋酸发酵,提高底料利用率,增加了醇类的合成反应。
(2)酯类的形成主要是微生物产生的酶系催化的有机酸和乙醇的酯化。补料发酵后玫瑰醋总酯含量比传统发酵有所增加,在种类上比传统工艺增加了2-乙基己酸乙酯、乳酸异戊酯、异丁酸乙酯、异戊酸乙酯、己酸-2-苯乙酯这5种酯类成分,原因可能是补料可以促进对酯类物质的生成,另外补料本身含有丰富的酯类物质。酯类化合物的形成途径主要是发酵和后熟的过程中有机酸和醇的酯化反应[15],酯类的产生与乙醇的增加是同时进行的。由表3可知,乙酸乙酯、乙酸异戊酯、乙酸苯乙酯是构成玫瑰醋香气的主要酯类成分,在传统发酵中这3种成分占酯类含量的92.81%,补料发酵占79.17%。由于黄酒补液使补料发酵后玫瑰醋的辛酸乙酯、丁二酸二乙酯、苯乙酸乙酯含量比传统发酵提高,它们的含量增多使得改良后玫瑰醋的香气更加馥郁芬芳[16]。
(3)补料发酵酸类比例达到所测香气物质总量的65.92%,而传统发酵为51.83%。玫瑰醋的醋酸发酵主要生成乙酸和其他一些不挥发性酸,表明补料发酵提高乙酸生成量,除乙酸外,对其他酸类成分的提高也有影响。己酸和辛酸是醋酸发酵阶段的产物,丙酸是酵母蛋白代谢的副产物[17]。而丙酸和正己酸在补料发酵中未检出,可能是由于补料后使醋酸发酵效率提高,它们与部分醇类发生酯化的结果。
(4)醛、酮类物质虽然在玫瑰醋香气物质组成中所占比例较小,但对浙江玫瑰醋风味有着重要影响,许多醛类作为玫瑰醋发酵过程中重要的底物和产物,都具有独特的香味。由表3可知,组成玫瑰醋香气成分的醛类主要是苯甲醛和呋喃甲醛,补料发酵后呋喃甲醛含量比传统发酵提高93.53 μg/L,苯甲醛含量提高98.87 μg/L,含量变化较大。Callejon等的研究结果表明醋中3-羟基-2-丁酮的含量更多与醋酸发酵类型有关[18]。补料发酵将玫瑰醋中3-羟基-2-丁酮含量提高1053.10 μg/L,表明3-羟基-2-丁酮的含量可以用来鉴别玫瑰醋发酵工艺,补加酒液使其含量改变。
3 小结
采用固相微萃取(SPME)与GC-MS联用测定玫瑰醋中香气挥发性成分的组成及含量,优化萃取条件使萃取的物质浓度高,有效测定玫瑰醋中组成香气的酯类、酸类、醇类、醛类、酚类等物质,结果如下:
得到玫瑰醋香气成分萃取条件为萃取头50/30 μm DVB/CAR/PDMS,50 ℃条件下萃取30 min,样品中添加盐浓度300 g/L,此条件下萃取的玫瑰醋挥发性香气物质强度大,色谱分析响应值较高。方法回收率在83.32%~98.62%,能满足实验的要求。
补料醋样除酯类物质种类变化较大外,其余香气组分种类与传统工艺基本一致。乙醇、2,3-丁二醇和β-苯乙醇组成了玫瑰醋主要的醇类成分;乙酸乙酯、乙酸异戊酯、乙酸苯乙酯是构成玫瑰醋香气的主要酯类成分;组成玫瑰醋香气成分的醛类主要是苯甲醛和呋喃甲醛。
补液的加入使玫瑰醋香气物质的含量发生改变,大部分香气物质含量得到了较大提高,尤其是酯类、酸类、酮类的含量。补料发酵在种类上比传统发酵增加了2-乙基己酸乙酯、乳酸异戊酯、异丁酸乙酯、异戊酸乙酯、己酸-2-苯乙酯这5种酯类成分,由于黄酒补液使补料发酵后玫瑰醋的辛酸乙酯、丁二酸二乙酯、苯乙酸乙酯含量比传统发酵增多,使得改良后玫瑰醋的香气更加馥郁芬芳。
