未来疗法:用细胞治病
2019-04-17爱丽丝·帕克
爱丽丝·帕克
2018年9月4日,哥倫比亚大学分子疗法方向的博士后杰布·德容,在饲喂300个由干细胞培育而成的“迷你脑”。
2017年的一天,当妮雪儿·奥巴尔得知自己怀上第二个孩子时,她怎么也没有料到,这次怀孕,或者说她肚子里的宝宝会创造历史。
时年40岁的奥巴尔是夏威夷的一名餐饮协调员。怀孕18周时,她在未婚夫克里斯托弗·康斯坦丁诺的陪同下前往医院做超声波检查,却发现有些不正常——胎儿的心脏偏大,此外,器官周围还开始出现积液。这些迹象表明,为了向快速生长的身体泵血,胎儿的心脏负荷格外大,而且已经开始衰竭。
个中缘由,医生洞若观火。奥巴尔和康斯坦丁诺都是甲型地中海贫血症的基因携带者,这种遗传性血液病可导致人体的红细胞数量偏低,乃至危及生命。红细胞携带的血红蛋白与氧气结合并从肺部输送,以供给其他细胞,所以红细胞计数偏低意味着全身细胞中的氧气水平较低。虽然奥巴尔和男友均没有受到此症的影响,但根据他们的基因结合情况,他们的孩子有可能患上此病。
当奥巴尔怀上他们的第一个孩子(男孩)加布里埃尔时,医生告诉这对伴侣,他们的孩子如果得了这种病,结局会很惨。“从医生那里得到的信息就是,大多数胎儿会在子宫内死亡,即便顺利出生也活不了多久。”奥巴尔说道。不过加布里埃尔很幸运,他从父母那里继承的DNA没有引发细胞突变从而使他患病。
但怀孕18周时,他们的第二个孩子(女孩)经超声波检查,被正式诊断出患有甲型地中海贫血症。他们没有太多选择:女儿需要在母体内接受输血,方能提高她顺利出生的几率。而且即便活着出生,余生也需要定期输血,依靠健康捐献者的血液来补充自身血液的低含氧量。
他们的基因顾问师提了另外一个建议,不过成功的几率不高。当时顾问师刚刚了解到,加州大学旧金山分校正在试验一种有望治疗甲型地中海贫血症的激进方法:对子宫内的胎儿实施干细胞移植。
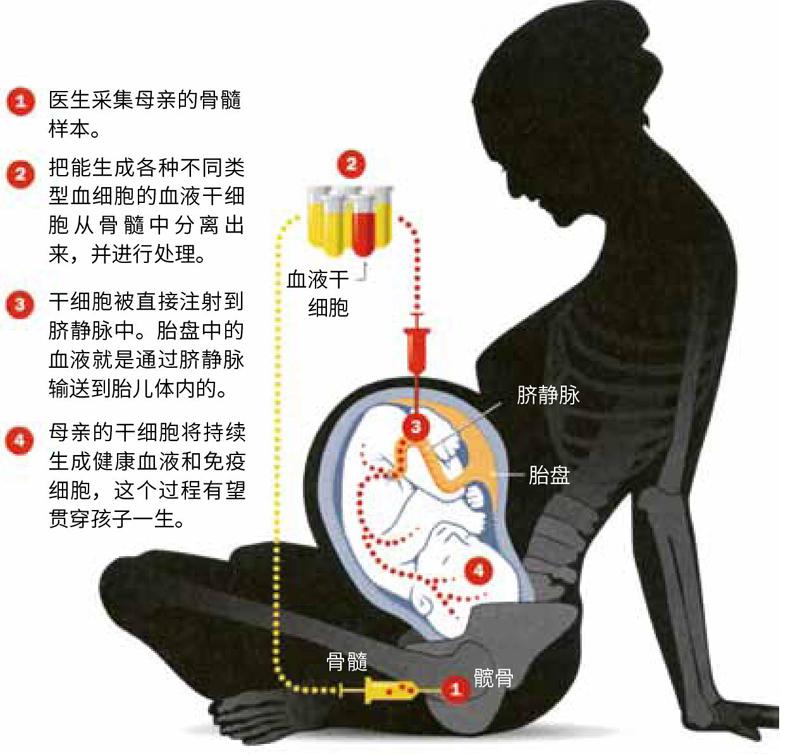
此前研究人员也曾尝试过利用子宫内干细胞移植来治疗这种血液疾病,但鲜有成功。他们把从孕妇骨髓中提取出的血液干细胞(可生成各种不同类型的血细胞,)在实验室里经过处理后,直接注射到胎儿与母体胎盘相连接的脐静脉中。理想情况下,孕妇的健康干细胞开始分裂并取代胎儿有缺陷的血细胞。但抽取骨髓对于孕妇来说会有风险,因此以前凡是涉及甲型地中海贫血症的试验,所用的干细胞均来自胎儿父亲,可这些干细胞往往会被排斥。因此,这项新试验就产生了一个道德问题:母亲冒险去挽救胎儿是否值得?而在加州大学旧金山分校外科学教授蒂皮·麦肯齐看来,这种疗法值得尝试。
奥巴尔是有顾虑的,但如果干细胞能像预期的那样,给女儿一个活下来的机会,甚至可以无病无痛地过正常人的生活,她和康斯坦丁诺还是愿意尝试一下的。他们的女儿将成为全球首个接受干细胞移植的胎儿,她将在严密的临床监控下,被注入来自母亲的干细胞。

一名医生正在检查奥巴尔刚出生3周的女儿埃莉安娜。小宝宝在妈妈肚子里时便接受了干细胞移植,来治疗遗传自父母的甲型地中海贫血症。
虽然长期以来,取自骨髓的血液干细胞都是治疗白血病、淋巴瘤等血癌的基石,不过,麦肯齐试验性地从孕妇体内提取干细胞来治疗一个正在子宫内孕育的胎儿,是目前少有的几种用细胞而非药物来治疗众多疾病的试验之一。一项项颇具前景的研究,则使此类基于干细胞的疗法慢慢地用于最终的临床治疗。
有了这些从骨髓中提取的干细胞,科学家就可以利用人体与生俱来的本领:细胞再生。成人的很多器官和组织,包括脂肪细胞和血液,都自备了隐匿的干细胞,这些干细胞的唯一职责就是在细胞和组织受到损伤或衰亡时进行再生。而且这种细胞是能够采集的,以用于研究和体外培育。
然而,有些器官里的这种干细胞储量并不大,大脑和心肌尤其如此。20多年前,科学家在试管婴儿诊所捐献的用于科研的胚胎中,发现了此类颇具可塑性的细胞,进而掌握了实验室条件下在人体的任何类型细胞中培育此种细胞的方法。这也使得在治疗心脏病、糖尿病甚至精神疾病等病症时,用健康的组织或器官取代受损的,能够治愈且不需服药或动手术,最终将成为可能。
可是,利用从人类胚胎中获取的干细胞来治病引发了严重的伦理问题,因为要提取胚胎干细胞需要终止妊娠,这给人的感觉就是结束一个人的生命。所以多年来美国联邦政府都立法禁止科学家利用政府资金来从事针对此类细胞的研究。而从2006年开始,科学家们发现,可以运用迂回战术来绕开这一伦理障碍。日本一个由京都大学教授山中伸弥领导的小组研究发现,从任何人身上提取一个皮肤细胞,擦掉其作为皮肤细胞的生长痕迹,能将其还原为胚胎期的空白状态——实质上是把它改造成了一个胚胎干细胞,而且不牵涉复杂的道德起源问题。这种颇具可塑性的细胞被称为“诱导性多能干细胞”(iPS),能够在实验室的培养皿中,在研究人员小心翼翼的操作下,再辅以适当的要素,生成心肌、大脑神经或可用胰岛素泵泵入体内的胰细胞。
将这些疗法用于人体的探索之路刚起步时有过一些失误。2009年,美国食品药品监督管理局(FDA)批准了第一例胚胎干细胞临床试验,其中包括把用干细胞培育而成的神经细胞植入瘫痪病人体内,以恢复其脊柱神经的功能。最初是在小鼠身上做试验,谁知植入小鼠体内的细胞形成了肿块,甚是令人担忧。虽然这些肿块并非肿瘤,但足以引起人们对于该疗法安全性的警觉,FDA遂叫停了试验。虽然试验后又重启,可开展此项研究的那家公司最终决定停止研究。
在经过多年的研究和实践之后,如今科学家正准备试验的是,心脏病发作后,干细胞能否转变为心肌,以取代坏死的组织;或者是,注入Ⅰ型糖尿病患者体内的新细胞,能否取代无法产生足量胰岛素的胰细胞,来行使这项功能。诸如此类。研究者甚至希望有朝一日能借助由干细胞培育的新的神经元来治疗帕金森等脑部疾病,这些神经元可替代脑部受损的运动神经——正是后者的受损,导致患者不由自主地颤抖。
“借助干细胞,我们现在能够从病因入手寻求疗法,而非简单地头痛医头脚痛医脚。”迪帕克·斯里瓦斯塔瓦说道,他是加州格莱斯顿研究所罗登贝瑞干细胞中心主任,也是加州大学旧金山分校的一名教授。
干细胞不仅能够取代病患细胞,催生很多新疗法,它们还为研究各种病症提供了一种极为重要的方法。此前,由于科学家们没有太多的活体细胞用于研究,在这方面一直没取得什么进展。如今美国的一些实验室正在孵化所谓的“迷你脑”,它由数万个培育自iPS细胞的脑细胞构成,用作研究从孤独症到精神分裂症等精神疾病的模型。在某一領域内,有些疗法并没有如医生料想的那样取得广泛成功,但这方面的学问能够推动新的疗法产生。
每个星期三是杰布·德容饲喂300个“迷你脑”的日子。这位哥伦比亚大学分子疗法方向的博士后,每次都要先清理每个球状脑组织过去一周产生的废弃物。他小心翼翼地用一根吸液管将只有几微米大小的废弃物吸出,唯恐把各个“迷你脑”的细胞弄混了,然后滴入粉里透橙的液体食物,这种液体里面含有生长因子、养分、葡萄糖以及能合成蛋白质的氨基酸。一趟下来,德容要忙活好几个小时。
“迷你脑”大小介于一粒罂粟子和一颗胡椒籽之间,它们躺在一个神经精神学实验室特制的冰盒底部,肉眼几乎看不见。由iPS细胞培育而成的它们,能为人类提供第一扇窗口,来了解精神疾病发生时到底是哪里出了问题。
人类对于精神疾病的治疗依然远远落后于其他疾病的主要原因在于,想要获取活体大脑用于试验几乎是不可能的。神经学家只好拿小鼠大脑或去世的精神病患者的大脑组织切片作为替代品,来获取第一手数据。现在,哥伦比亚大学“精准医学计划”主管、督导德容的“迷你脑”项目的桑德尔·马克斯,希望这个项目能促成一项突破性研究,让人类首次利用干细胞来发现并试验精神疾病的新疗法。
迄今为止,这种“迷你脑”包含了与任何人类细胞DNA中相同的两万个基因,而且能制造出任何脑细胞能够制造的全部重要蛋白质——由于它们缺乏一整个大脑的所有构造,马克斯和德容更倾向于管它们叫“类器官”。德容照料的这些球状脑组织,均是从阿米什社区居民(注:阿米什人是新教的一个信徒分支,以拒绝现代设施,过简朴生活而闻名)身上提取细胞,制成iPS细胞后再培育而成的。这些居民当中有些是健康人,其他人则因受一种罕见的遗传性脑部疾病影响,有自闭症谱系障碍、智力低下和癫痫发作等症状。而将干细胞培育成类脑器官,就是为了研究这种遗传偏差到底如何影响了正常的脑部发育。“现在我们可以在实验室里研究和观察脑细胞是如何生长和发育的。”德容说。当下,他和他的团队正在研究类器官重复人的实际病程时,两者到底如何相似,以期能够利用这些“迷你脑”,最终制造出有效消除基因变异影响的药物来。
再造人体组织和部分器官来替代病患部分,科学家在这方面也取得了进展。例如,气管或尿道遭肿瘤摧毁的癌症病人,能利用自身的细胞生长出新的来,从而降低了器官移植引发的排异风险。
“胰岛素发现于1920年,我希望在发现它100年的时候,人们无需再注射它。”
——道格拉斯·梅尔顿,哈佛干细胞研究所
早期有个治疗黄斑变性的试验,完成于2014年。这个试验显示,干细胞疗法对于患者有着积极的效果。得了黄斑变性的患者,其视网膜色素上皮细胞会逐渐退化,最终使患者失明。在这个试验中,研究人员从试管婴儿胚胎中提取胚胎干细胞,将它们在视网膜色素上皮细胞内进行培育后,再移植到患者眼中,以取代他们已经失能的视网膜。据报道,将近两年之后,为数不多的试验参与者中——他们在试验之初便被认定为失明——逾半数人的视力有所改善。
各种疗法也开始借助iPS技术,用成人细胞充当胚胎细胞,此举也规避了附着在真正胚胎细胞上的伦理问题。
这一过程对于人体心脏的康复来说尤为重要。成人的心肌细胞不再分裂,或者说极少分裂,这意味着心脏组织在受损时(就像心脏病发作时那样)不会再生,而是会变为瘢痕组织,妨碍心脏泵血。加州格莱斯顿研究所的斯里瓦斯塔瓦发现,一个正在发育中的胎儿,其心肌细胞会很活跃地分裂,以长成心脏。他把在此过程中被开启的四个基因隔离起来,在胎儿出生时把它们关闭,以阻止心肌细胞继续分裂。等把这些基因移植到健康成人的心肌细胞中之后再重启它们,如此一来,心肌细胞又可以再次分裂了。而胚胎基因即使是被移植到瘢痕心脏组织中,重启之后也能促使心肌细胞进行分裂,生成新的肌肉。“在造物主的工具箱里,到底是哪种工具被用于胚胎期心脏的形成,这一点我们总算是弄明白了。”他说,“然后,我们在成人体内将同样的(遗传)信息重新排列,这样重新编程后,细胞再次分裂,长出新的心肌。”
斯里瓦斯塔瓦表示,这种方法不仅可用于生成新的心肌,而且也可能生成其他类型的细胞。2016年底,他参与成立了生物制药公司Tenaya Therapeutics,对这项技术进行完善。现在公司正准备运用该技术对病人进行试验治疗。
在美国,此类基于干细胞的生物科技公司正如雨后春笋般冒出,它们主攻不同类型的病症。在马萨诸塞州剑桥市的生物科技公司Semma Therapeutics,哈佛干细胞研究所的联合负责人道格拉斯·梅尔顿正在研究一种新方法,可以从像他两个孩子那样的Ⅰ型糖尿病患者身上获取细胞,然后将它们改造成一种可用胰岛素泵泵入体内的胰细胞。他的最新研究显示,这种产自iPS细胞的细胞,能够监测血糖的波动水平并对其作出反应,而且能有效地测量出它们到底分泌了多少胰岛素。不过对于Ⅰ型糖尿病来说,这种方法并不能确保万事大吉,因为患者的免疫系统会攻击泵入的胰细胞。所以梅尔顿和Semma的同事们研究出一种方法,将新分裂的、可分泌胰岛素的胰细胞用一种可“溜过”免疫系统的薄膜保护起来,使其免受伤害。梅尔顿希望在接下来的两年里,能对其研发的泵入系统,以及用干细胞制成的可分泌胰岛素的胰细胞进行测试。
与许多新兴科技一样,干细胞技术所代表的疗法在开发过程中也潜藏着阴暗面。2017年,美国《新英格兰医学杂志》报道了一项研究。在这项研究中,研究者从黄斑变性患者身上的脂肪细胞中提取干细胞,培育成视网膜细胞后再移植给患者,以治疗此病。可是,有3名参与此项研究的患者在接受治疗后视力严重受损,研究也被叫停。此后的调查发现,志愿者向开展研究的公司都交了钱,作为试验性治疗的费用,这可不符合临床试验的做法。调查还发现,这项研究在招募志愿者和告知志愿者试验情况等方面,均存在着不规范的地方。志愿者到底被移植了哪种类型的细胞也存疑待查。

2018年9月4日,神经生物学家徐斌(音)、桑德尔·马克斯、杰布·德容(左起)在检查培育中的“迷你脑”。
一开始,对于要利用自身的干细胞来治疗腹中胎儿的甲型地中海贫血症,由此成为全球首个这么做的孕妇,奥巴尔是有些害怕的,可当她看到输血过程时就放心了。“我在视频中看到了干细胞机器,还看到了白色圆点,这些白色圆点就是我的干细胞。”她的女儿接受了5次输血,都是通过奥巴尔的腹部注射到脐静脉上。“我看了整个过程,就是觉到很震惊,这真的很酷!”她说。
对于奥巴尔来说,只要能根治女儿的病,成为首个“吃螃蟹者”的风险值得去冒。这个疗法似乎也确实有效:医生曾警告说,她的女儿刚出生时可能会全身发青,看上要去比一般的新生儿虚弱。不过,她的女儿不仅撑过了10个月的妊娠期,而且在2018年2月1日出生后的第一声啼哭也很响亮,这让奥巴尔那颗悬着的心立刻放松下来。虽然在以后的日子里,这个名叫埃莉安娜的孩子会因为娘胎里的病而显示出一些发育迟缓的迹象,但奥巴尔和康斯坦丁诺对于孩子的将来抱定了乐观的态度。
麦肯齐开展的这项干细胞试验具有历史性意义。就目前而言,它对科学界的影响尚不明确,但婴儿的名字已经反映出她对这个家庭的意义所在。奥巴尔说:“我想给她起一个能表示她是一名斗士,不屈不挠地进行抗争的名字。”首次进行子宫内输血时,一位值班护士名叫埃莉安娜。奥巴尔得知,这个名字的意思是“上帝已回應”。“就是它了!”她说。
[译自美国《时代周刊》]
干细胞研究进展
医生正在利用母亲的干细胞来治疗胎儿的血液疾病,这些血液疾病往往会导致死胎。医生是这样开展治疗的: