抗非小细胞肺癌药物奥希替尼研究进展
2019-03-04饶晓明李海燕李凯
饶晓明,李海燕,李凯
奥希替尼(Osimertinib,TagrissoTM,AZD9291)是阿斯利康公司研发的一种口服第三代表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)[1]。2017年3月30日被FDA完全批准上市[2],此前2015年11月13日被FDA加速批准上市[3],所谓加速批准是指FDA可以根据应答率等替代终点来批准某个用于治疗临床需求未满足的重大疾病的药物上市[4]。奥希替尼主要针对EGFR T790M基因突变的非小细胞肺癌(NSCLC),该突变常常发生在对第一、第二代EGFR-TKI耐药的病人中[5]。2015年11月13日,FDA基于奥希替尼在EGFR T790M 突变阳性的NSCLC病人中的两项II期临床试验,即实验肿瘤反应率和反应持续时间的结果而加速批准其上市[4]。奥希替尼的推荐剂量为80 mg/d,除非病人有不可接受的毒副作用或者病情发生进展,可空腹或与食物同服,对于有吞咽困难的病人,奥希替尼可溶于约50 mL的水中后迅速服用。中国食品药品监督管理局(CFDA)于2017年3月22日批准奥希替尼上市申请[6],距其全球首次上市仅仅1年4个月左右,为EGFR T790M基因突变阳性的局部晚期或转移性NSCLC病人提供了一个更好的选择,可进一步改善该类病人的预后。本文就奥希替尼的作用机制、研究历程、药效学、药动学、不良反应,耐药机制进行综述,促进广大医药工作者对其的进一步认识。
1 作用机制
奥希替尼的分子式:C28H33N7O2,化学名:N-[2-[2-(二甲胺基)乙基-甲氨基]-4-甲氧基-5-[4-(1-甲基吲哚-3-yl) 嘧啶-2-yl]氨基]苯基]prop-2-烯酰胺[3],结构式如图1所示[5]。奥希替尼结构中含有丙烯酰胺基,能够与EGFR基因催化域的ATP结合位点边缘C797结合,形成不可逆的共价键,从而抑制癌细胞的增殖。EGFR结合位点包含L858R,19Del和含有T790M的双突变,但对野生型的EGFR基因结合能力较差,奥希替尼对EGFR基因抑制能力大小为T790M>EGFRs>wtEGFR[7]。奥希替尼与EGFR相关基因结合后,可能与通过阻断突变EGFR同源二聚化或诱导EGFR突变细胞降解等途径,从而阻断EGFR下游信号传递有关[8],口服奥希替尼治疗后的病人,其肺部组织活检发现大部分治疗后的肿瘤EGFR通路的蛋白受到抑制,在细胞系及肺癌移植瘤小鼠模型中,也观察到类似的结果[9]。有研究其作用机制示意图如图2所示。
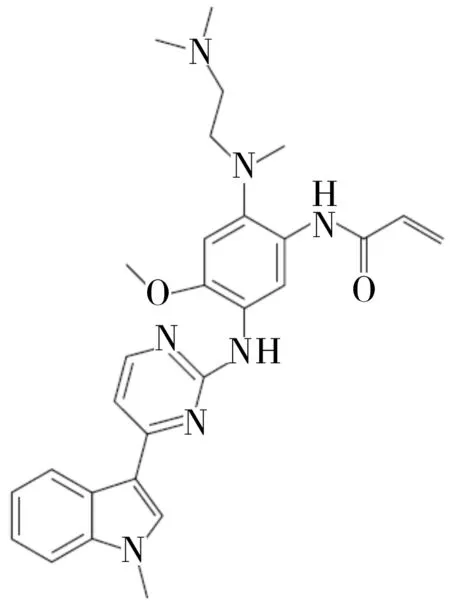
图1 奥希替尼化学结构
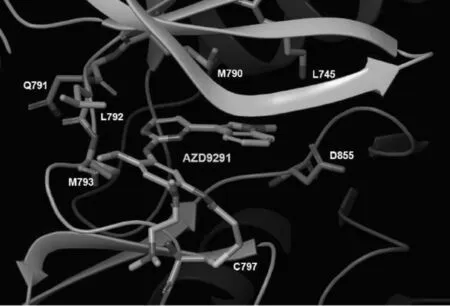
图2 奥希替尼作用机制示意图
2 研究历程
从2013年3月奥希替尼进行I/II临床试验,2015年11月FDA批准奥希替尼加速上市,到2017年3月FDA完全批准奥希替尼上市,其从研发到批准上市花费时间仅4年左右,这得益于奥希替尼在临床试验中显示出的显著效果以及对第一代、第二代EGFR-TKI耐药的局部晚期或转移性NSCLC病人的急迫需求。关于奥希替尼的研究历程中里程碑事件(包含审批时间和临床试验)见图3[2,5,10-11]。
3 药效学
奥希替尼是新型的,不可逆的第三代EGFR-TKI,在体外试验中对EGFR T790M突变的亲和力是野生型的200倍[12]。2015年和2016年,国际顶尖医学杂志《The New England Journal of Medicine》分别发表了奥希替尼Ⅰ期[13]和Ⅲ期[14]临床试验结果,该实验结果进一步证实奥希替尼在EGFR T790M基因突变阳性的局部晚期或转移性NSCLC中的疗效。

图3 奥希替尼研发历程
3.1Ⅰ期临床试验Jänne等[13]进行了奥希替尼Ⅰ期临床试验,该实验总共纳入了来自世界各地的253例NSCLC病人,该病人为已接受EGFR-TKI治疗,且通过射线检查表明,疾病有进展。每次给药剂量范围为20~240 mg/d,试验分为两组,一组为剂量递增组(31例),以确定最大中毒剂量;一组为扩大组(222例,5小组),以评估奥希替尼的治疗效果。扩大组中病人进行肿瘤组织活检,以确定EGFR T790M 的状态。实验结果表明在每次最高240 mg/d的给药剂量下,没有观察到中毒表现,最大中毒剂量没有确定。试验中最常见的不良反应是腹泻、皮疹、恶心、食欲下降。总体目标肿瘤反应率为51%(95%CI,45~58),在127名被确定为EGFR T790M阳性的病人中,总体目标肿瘤反应率为61% (95%CI,52~70)。相反,在61名被确定为EGFR T790M阴性的病人中,总体目标肿瘤反应率为21% (95%CI,12~34)。在EGFR T790M阳性的病人中,中位无进展生存期(PFS)为9.6个月(95%CI,8.3~未知),EGFR T790M阴性的病人中,中位无进展生存期(PFS)为2.8个月(95%CI,2.1~4.3)。该实验结果证明,奥希替尼对已接受其它EGFR-TKI治疗,且疾病进展并伴有EGFR T790M突变阳性的病人具有显著的活性。正是凭借这一实验结果,2014年4月FDA授予奥希替尼突破性治疗药物[15]。
3.2Ⅱ期临床试验在Ⅰ期临床试验的基础上,Ⅱ期试验的给药剂量为80 mg/d,旨在对奥希替尼治疗过往接受EGFR-TKI治疗后,疾病进展的EGFR T790M 突变阳性的NSCLC 病人,的治疗效果进行进一步评估。结果表明:平均治疗4.9个月后,客观缓解率(ORR)为58%,疾病控制率为92%[15]。
另一项随机、开放、多中心、3-组Ⅱ期临床试验中,比较奥希替尼和吉非替尼治疗策略。试验分为三组:①给予奥希替尼,直至疾病发生进展;②首先给予吉非替尼治疗直到检测到EGFR T790M 突变阳性后立即转为奥希替尼治疗,直至疾病发生进展;③首先给予吉非替尼治疗直到疾病进展后立即转为奥希替尼治疗,直至疾病发生进展。统计结果证实,经过吉非替尼治疗后,出现EGFR T790M 突变阳性后立即转为奥希替尼治疗,治疗效果最佳[16]。
3.3Ⅲ期临床试验Mok等[17]进行了随机、国际化、非盲、Ⅲ期临床试验,试验共纳入了419位接受EGFR-TKI治疗后,疾病发生进展的晚期NSCLC病人,以2∶1的比例分为两组,分别接受口服奥希替尼(80 mg/d)或培美曲塞(500 mg/m2)加卡铂或顺铂(75 mg/m2)为期三周期一疗程,最多不超过六疗程。以无进展生存期(PFS)为首要的评价终点。结果表明:口服奥希替尼组的无进展生存期(PFS)为10.1个月,明显高于培美曲塞(500 mg/m2)加卡铂或顺铂(75 mg/m2)组的4.4个月。客观缓解率(ORR)方面,奥希替尼组71%(95%CI,65~76)明显高于培美曲塞(500 mg/m2)加卡铂或顺铂(75 mg/m2)组的31%(95%CI,24~40)。在144例中枢神经系统转移性病人中,奥希替尼组和培美曲塞加卡铂或顺铂组的无进展生存期(PFS)分别为8.5个月和4.2个月。不良反应3级及以上的发生率,奥希替尼组为23%,低于培美曲塞加卡铂或顺铂组的47%。在中枢神经系统转移和不良反应方面,奥希替尼的效果同样更好。
4 药动学
健康志愿者单次口服奥希替尼20 mg片剂或胶囊剂,生物利用度方面几乎没有差别[17]。与空腹相比,高脂肪饮食会减少奥希替尼的血药浓度,病人口服80 mg时,与食物同服和禁食状态下对血药浓度无显著影响[15,18]。奥希替尼口服吸收缓慢,达Cmax时间约为6 h,持续给药22 d血药浓度逐渐平稳,最高血药浓度与最低血药浓度比为1.6,表观分布容积为986 L。奥希替尼的血浆蛋白结合率较高,在Ⅱ期临床试验中,两例脑转移病人的脑脊液浓度分别为3.44 nmol/L和 0.77 nmol/L,相当于其稳态血药浓度的1%和0.2%。这可以进一步解释奥希替尼对中枢神经系统转移病人中能产生效果。奥希替尼口服清除率为14.2 L/h,主要通过CYP3A氧化代谢和脱烷基化途径代谢,半衰期约为55 h,血浆中可检测到两种具有药理活性的代谢物(AZ7550 和AZ5104) ,稳态下其代谢物的浓度 约为奥希替尼的10%。奥希替尼约68%经粪便排泄,14%经尿液清除,其中以原形排除体外的极少,约占2%。适用于肾功能不全的病人[19]。
5 不良反应
在临床试验中,奥希替尼表现了较好的耐受性,其不良反应发生率要明显低于第一、第二代EGFR-TKI。在240 mg/d剂量下,没有观察到中毒反应。最常见的不良反应发生率为腹泻(42%),皮疹(41%),皮肤干燥(31%),神经毒性(25%),4.4%的病人因为耐受性原因,减少给药剂量或终止治疗。导致剂量减少或者治疗中断的主要原因是QT间期延长(2.2%)和嗜中性白血球减少症(1.9%)。严重不良反应的发生率为2%,主要是导致肺炎和肺栓塞[20]。
临床上暂没有奥希替尼与CYP抑制剂或诱导剂相互作用的相关资料。但联合使用强CYP3A抑制剂或诱导剂时,可能导致奥希替尼血药浓度改变,因此应尽可能的避免,如需要一起使用,必须密切监测病人的各项体征,如肺栓塞、心脏抑制以及其他不良反应。奥希替尼应尽可能避免联合使用对CYP3A、BCRP 、CYP1A2抑制剂敏感且治疗指数较低的药物,以防这些药物血药浓度过低或过高,从而发生不良反应。但有临床资料表明[21],连续使用奥希替尼后,再服用奥美拉唑,没有发生药物相互作用的不良事件。
6 耐药机制
虽然奥希替尼对EGFR T790M突变的NSCLC病人有显著的疗效,但长期使用(约10个月)仍会导致耐药性的发生[22]。Niederst等[23]采用新一代测序技术,对15例接受奥希替尼治疗的病人进行基因检测,结果发生C797S 突变的病人约占40%,EGFR C797S是位于EGFR 20号外显子的一个位点,该突变导致奥希替尼作用靶点改变,即797 位半胱氨酸突变为丝氨酸,该改变将阻碍奥希替尼与Cys797 氨基酸残基结合,从而导致耐药的发生。然而,仍有33%病人未检测到C797S突变基因,27%的病人未检测到单纯的EGFR T790M突变。C797S突变是T790M突变NSCLC病人对osimertinib产生获得性耐药的主要机制,分为三种类型:①C797S突变以及EGFR敏感突变和T790M突变;②T790M突变以及EGFR敏感突变,无C797S突变;③EGFR敏感突变,但T790M突变消失以及无C797S突变[24]。这说明针对T790M突变发生耐药的机制具有复杂性,其耐药机制有待进一步研究。
7 展望
我国是一个肺癌大国,到2025年我过肺癌病人将超过一百万,成为全球第一大肺癌国[25]。第三代EGFR-TKI奥希替尼对EGFR T790M基因突变阳性的局部晚期或转移性NSCLC病人显示出显著的活性,尤其是对伴有脑转移或者中枢神经系统转移更有优势,能进一步延长病人的疾病无进展期,改善病人生存质量。但奥希替尼长期使用仍然会导致耐药性的发生。然而,该耐药病人目前却没有相应的治疗药物。以第三代EGFR-TKI耐药为突破口,研制第四代EGFR-TKI将是以后研究的一个热点[26]。随着多学科的交叉渗透和研究的进一步深入,未来在肺癌的治疗领域将会有更大的突破。
