LC-MS/MS法同时测定人血浆中万古霉素和去甲万古霉素的质量浓度
2019-01-15姚鸿萍程晓亮
张 雷,姚鸿萍,程晓亮
(西安交通大学第一附属医院药学部,西安 710061)
万古霉素和去甲万古霉素为糖肽类抗菌药物,用于预防和治疗多种革兰氏阳性菌感染,包括耐甲氧西林金黄色葡萄球菌(MRSA)[1]。二者在结构上除了在去甲万古霉素的N末端缺少1个甲基以外几乎相同,化学结构见图1。万古霉素与去甲万古霉素的抗菌谱和活性相似,治疗窗均较窄,万古霉素和去甲万古霉素的谷质量浓度治疗窗分别为10~20[2-3]和5~10 μg·mL-1[4]。谷质量浓度低于治疗窗时治疗效果不佳,谷质量浓度高于治疗窗时出现肾毒性和耳毒性的风险增加[2-3]。因此,需要进行治疗药物监测以确保药物疗效并防止毒性和不良反应发生[2]。
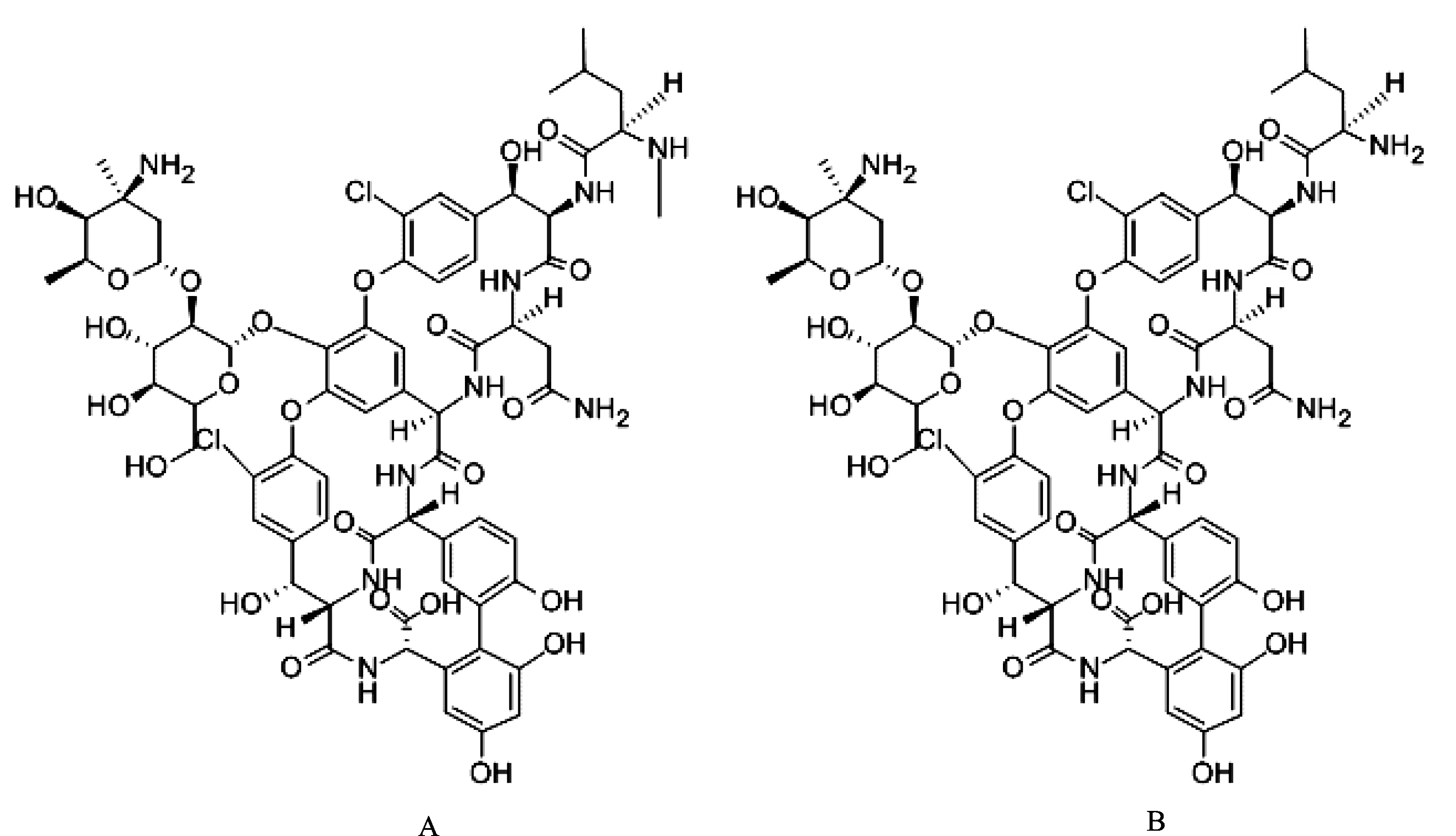
图1万古霉素(A)和去甲万古霉素(B)的化学结构式
Fig.1 Chemical structure of vancomycin (A) and norvancomycin (B)
文献报道的万古霉素药物质量浓度的分析方法有多种,包括免疫分析法[5]、HPLC法[6]和液相色谱-质谱联用法(LC-MS/MS)[7-12]。尽管免疫分析法的速度快、操作方便,但该方法的特异性和灵敏度不高,需要特定的设备[13]。HPLC法的紫外或荧光检测器对分析物的结构选择性不高,且需要将分析物与内源性物质完全分离,因此分析时间较长[14]。LC-MS/MS法是一种灵敏度高、结构选择性强的分析方法。目前文献报道的LC-MS/MS法测定万古霉素质量浓度包括在线样品萃取和柱切换技术[8]、三氟乙酸和甲醇[9]、三氯乙酸[10]或乙腈[11-12]沉淀蛋白。这些方法采用离子对色谱或正相色谱,萃取过程较复杂,在线样品萃取费用较高。只有少数文献报道测定去甲万古霉素质量浓度的方法,包括荧光偏振免疫[15]、HPLC法[16]和LC-MS/MS法[17],但这些方法灵敏度较低。
本研究的目的是建立一种简单的反相色谱测定血浆中万古霉素和去甲万古霉素的LC-MS/MS法,结果表明,该方法灵敏度高、准确和可靠,可用于血药质量浓度的监测。
1 材料与方法
1.1仪器与试药
1.1.1仪器 Thermo TSQ Endura型三重四极杆质谱仪(配有可加热电喷雾离子源),戴安Ultimate 3000型高效液相色谱仪(配有HGP-3200RS型双梯度泵、SRD-3200型真空脱气机和自动进样器)(美国Thermo公司);Basic型电子天平(德国赛多利斯公司);AllegraTM×-22R高速冷冻离心机(美国Beckman Coulter公司);Elix@3纯水仪(美国Millipore公司)。
1.1.2试药 万古霉素(批准文号H20140174)和去甲万古霉素(批准文号H13020286)均购自北京百灵威科技有限公司;甲醇和甲酸均为色谱纯,购自德国默克公司;水为实验室自制超纯水。
1.2方法
1.2.1色谱条件 色谱柱:Thermo Scientific Hypersil GOLD aQ (100 mm×2.1 mm,1.9 μm);流动相:1 mL·L-1甲酸水溶液(A)-甲醇(B);流速:0.3 mL·min-1。梯度洗脱程序:0~1.5 min,90%A;1.5~3 min,90%~40%A,并保持4 min;7~7.5 min,40%~90%A,保持0.5 min。分析时间:8 min;进样量:20 μL。
1.2.2质谱条件离子源 离子源:可加热电喷雾(HESI)离子源;检测方法:正离子模式检测;电喷雾电压:3 500 V,离子源蒸发温度:400 ℃;离子传输管温度:300 ℃。扫描方法为选择反应监测(SRM),万古霉素、去甲万古霉素和内标的检测离子对分别为m/z725.7→144.2,m/z718.3→144.2和m/z338.3→296.0,套管透镜补偿电压分别为164,164和167 V,碰撞能量分别为33,33和17 V。碰撞气氩气的压力为1.5 mTorr,鞘气(N2)和辅助气(N2)压力分别为35和8 Arb。万古霉素、去甲万古霉素和利奈唑胺的驻留时间均为200 ms。
1.3储备液、对照品溶液和对照血浆样品的制备 精密称取万古霉素和去甲万古霉素对照品各10 mg,置于10 mL量瓶中,加纯水溶解并稀释至刻度,分别配制成质量浓度为 1 mg·mL-1的对照品储备液。精密吸取上述万古霉素和去甲万古霉素储备液,分别用纯水稀释成质量浓度为0.2,0.4,1,5,10,100和200 μg·mL-1的系列对照品溶液,置于4 ℃冰箱中保存,备用。
取180 μL空白血浆,分别加入10 μL不同质量浓度的万古霉素和去甲万古霉素对照品溶液,制备万古霉素和去甲万古霉素终质量浓度为0.01,0.02,0.05,0.25,0.5,2.5,5和10 μg·mL-1的对照血浆样品。空白血浆中加入不同质量浓度的对照品溶液,制备万古霉素和去甲万古霉素终质量浓度为0.02,0.25和8 μg·mL-1的质控样品。
1.4血浆样品的前处理 取200 μL空白血浆,置于EP管中,加入10 μL质量浓度为500 ng·mL-1的利奈唑胺内标溶液,再加入40 μL高氯酸沉淀蛋白,涡旋30 s。加入400 μL的纯化水,涡旋30 s,以提高万古霉素和去甲万古霉素的回收率,以11 750 r·min-1离心15 min后加入50 μL二氯甲烷,涡旋30 s。取20 μL上清液进样分析。
1.5方法学验证
1.5.1专属性 通过对比空白血浆、分别加入万古霉素和去甲万古霉素对照品溶液或内标溶液的空白血浆以及给药后患者的血浆样品色谱图,考察该方法的专属性。
1.5.2标准曲线的制作 取空白血浆180 μL,分别加入10 μL万古霉素和去甲万古霉素系列质量浓度的对照品溶液和利奈唑胺内标溶液,血浆中万古霉素和去甲万古霉素的理论质量浓度为0.01,0.02,0.05,0.25,0.5,2.5,5和10 μg·mL-1。按照1.4项下方法处理后进样分析,分别以万古霉素和去甲万古霉素的峰面积与内标利奈唑胺峰面积的比值对其质量浓度作图,用加权最小二乘法进行线性回归计算,得加权标准曲线。
1.5.3定量下限和最低检测限 取空白血浆180 μL,加入10 μL万古霉素和去甲万古霉素对照品溶液,进行样品处理后进样分析,当信噪比(S/N)为10时的检测质量浓度为本方法的定量下限(LLOQ),当信噪比(S/N)为3时的检测质量浓度为本方法的最低检测限(LLOD)。
1.5.4精密度与准确度 平行制备高、中、低质控样品各5份,1 d内进样分析,计算日内精密度RSD值和准确度(以相对误差表示);连续5 d进样分析,计算日间精密度和准确度。要求日间和日内精密度RSD值小于15%,日间和日内的相对误差在±15%之内。
1.5.5提取回收率与基质效应 取180 μL空白血浆,分别加入10 μL万古霉素、去甲万古霉素质控溶液和利奈唑胺溶液,按照1.4项下方法处理后进样分析,得峰面积A。取空白血浆,按照1.4项下方法处理,取620 μL上清液,分别加入10 μL万古霉素、去甲万古霉素质控溶液和利奈唑胺溶液,进样分析得峰面积B。取620 μL水,分别加入10 μL万古霉素和去甲万古霉素质控溶液和利奈唑胺溶液,进样分析得峰面积C。A/B为本方法的提取回收率,B/C为本方法的基质效应。
1.5.6稳定性 将质量浓度为0.02,0.25和8 μg·mL-1万古霉素和去甲万古霉素的血浆样品反复冻融3次,室温下保存24 h(短期稳定性)和-80 ℃保存1个月(长期稳定性)后进行分析,考察万古霉素和去甲万古霉素的稳定性。
1.5.7稀释效应 用空白血浆将质量浓度为50 μg·mL-1的万古霉素和去甲万古霉素血浆样品稀释10倍,经1.4项下方法处理后进样分析,考察稀释对质量浓度测定的影响。
1.6治疗药物监测应用 将LC-MS/MS法应用于万古霉素和去甲万古霉素治疗药物的监测。万古霉素和去甲万古霉素血药质量浓度达到稳态后,在下一次给药前采集谷质量浓度血样,离心后收集血浆样品进行分析。实验方案经西安交通大学第一附属医院医学伦理委员会批准,所有患者均签署知情同意书。
2 结果
2.1LC-MS/MS法的建立 本研究的目的是建立一种测定人血浆中万古霉素和去甲万古霉素质量浓度的LC-MS/MS法,并应用于治疗药物监测。万古霉素和去甲万古霉素母离子和子离子全扫描谱图见图2。m/z1 450.7和m/z1 436.4的万古霉素和去甲万古霉素的[M+H]+峰观测不到,但分子离子峰分别出现在m/z725.7和m/z718.3。说明万古霉素和去甲万古霉素带双电荷,这是因为万古霉素和去甲万古霉素具有多个可离子化的碱性基团。根据万古霉素和去甲万古霉素的子离子谱图,选择万古霉素和去甲万古霉素的子离子m/z144.2作为定量离子。因此,万古霉素和去甲万古霉素的选择反应监测离子对分别为m/z725.7→144.2和m/z718.3→144.2。
万古霉素和去甲万古霉素的亲水性强,文献报道采用离子对色谱[11]和正相色谱[12]分离万古霉素和内源性物质。本研究采用梯度洗脱,用反相色谱柱分离万古霉素、去甲万古霉素和内源性物质。开始时,低甲醇相(10%)保持1.5 min,甲醇相在1.5 min内逐渐增加至60%,并保持4 min,高比例的有机相有利于分析物的电离。见图3。由图3可知,万古霉素、去甲万古霉素和利奈唑胺的保留时间分别为3.67,3.71和4.62 min,说明分析物达到了较好的色谱分离。
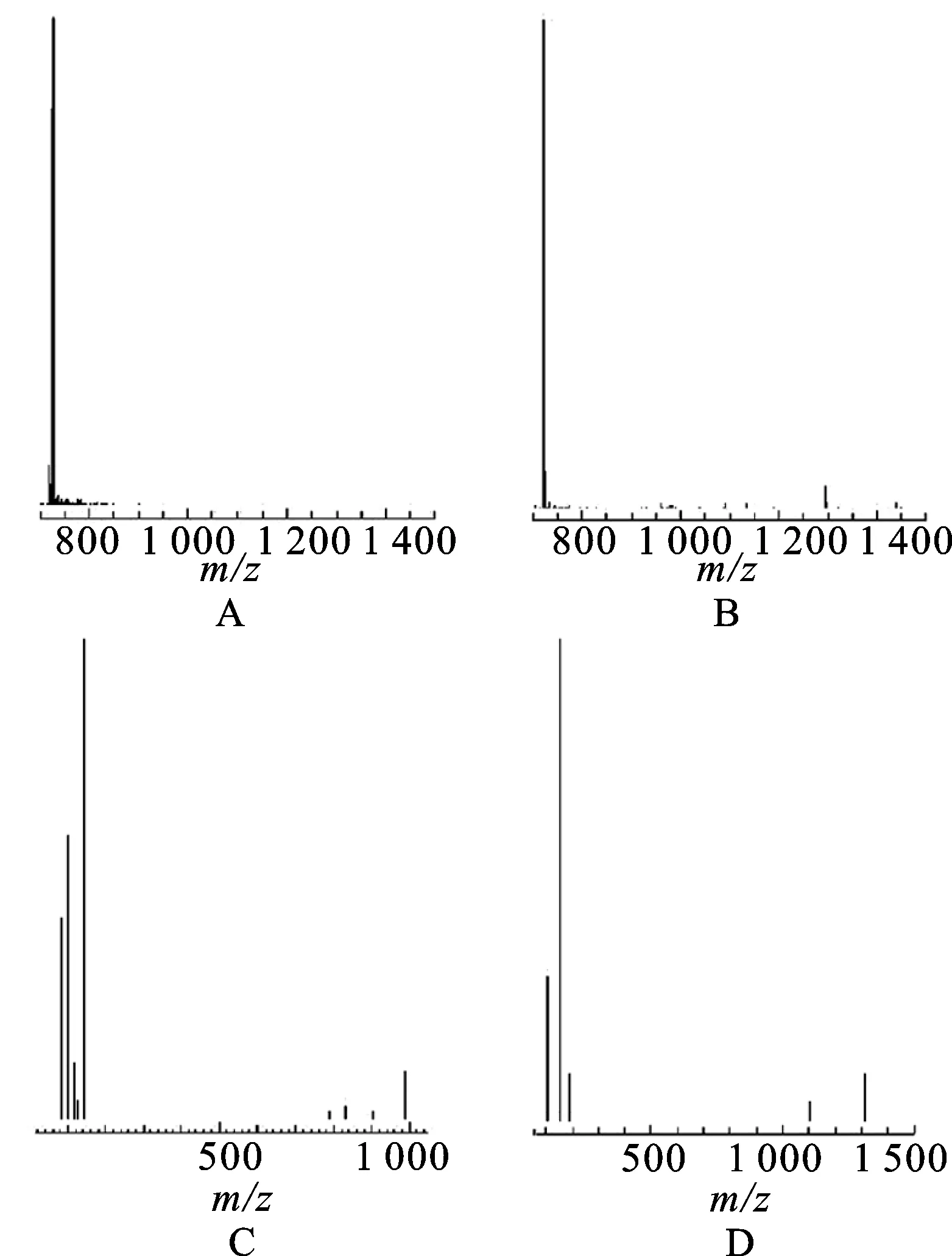
图2万古霉素和去甲万古霉素母离子和子离子全扫描谱图
A.万古霉素母离子;B.去甲万古霉素母离子;C.万古霉素子离子;D.去甲万古霉素子离子。
Fig.2 Full scan mass spectra for the parent and product of vancomycin and norvancomycin
A.parent ion for vancmycin;B.parent ion for norvancmycin;C.product ion for vancmycin;D.product ion for norvancmycin.
蛋白沉淀或有机试剂萃取通常用于提取分析物,但由于万古霉素和去甲万古霉素难溶于有机试剂,因此不能采用有机试剂萃取,用甲醇或乙腈沉淀蛋白导致万古霉素和去甲万古霉素的灵敏度降低。实验选择高氯酸沉淀蛋白,以增加分析物的灵敏度,高氯酸沉淀蛋白后万古霉素和去甲万古霉素的回收率约为50%。为了提高回收率,蛋白沉淀后加入不同体积的水,回收率随水体积的增加而增大。但水稀释了样品,降低了灵敏度,因此选择加入2倍体积的水,万古霉素和去甲万古霉素的回收率大于70%。
生物样品中内源性物质引起的基质效应是LC-MS/MS分析中的一个难点,血浆中极为丰富的磷脂是基质效应的主要来源[17-18]。二氯甲烷是提取脂类的良好溶剂[17],用于减少基质效应。蛋白质沉淀后,用二氯甲烷萃取上清液以降低基质效应,结果显示二氯甲烷萃取后无明显的基质效应。
2.2方法学验证
2.2.1专属性 在空白血浆中分别加入万古霉素、去甲万古霉素或内标溶液(万古霉素和去甲万古霉素终质量浓度为5 μg·mL-1)其与用药后患者血浆的色谱图见图3。万古霉素、去甲万古霉素和利奈唑胺的保留时间分别为3.67,3.71和4.62 min,血浆中内源性物质对万古霉素和去甲万古霉素的检测无干扰。
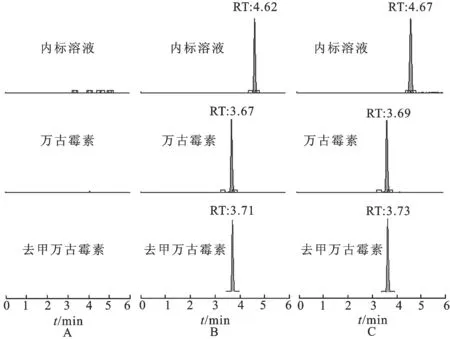
图3万古霉素和去甲万古霉素的典型色谱图
A.空白血浆;B.空白血浆中分别加入万古霉素、去甲万古霉素和内标溶液(万古霉素和去甲万古霉素的终质量浓度为5 μg·mL-1);C.患者使用万古霉素或去甲万古霉素后的血浆。
Fig.3 Typical chromatograms of vancomycin and norvancomycin
A.blank plasma;B.blank plasma spiked with vancomycin,norvancomycin or internal standard (final concentration of vancomycin and norvancomycin was 5 μg·mL-1);C.trough blood samples collected from patients received vancomycin or norvancomycin therapy.
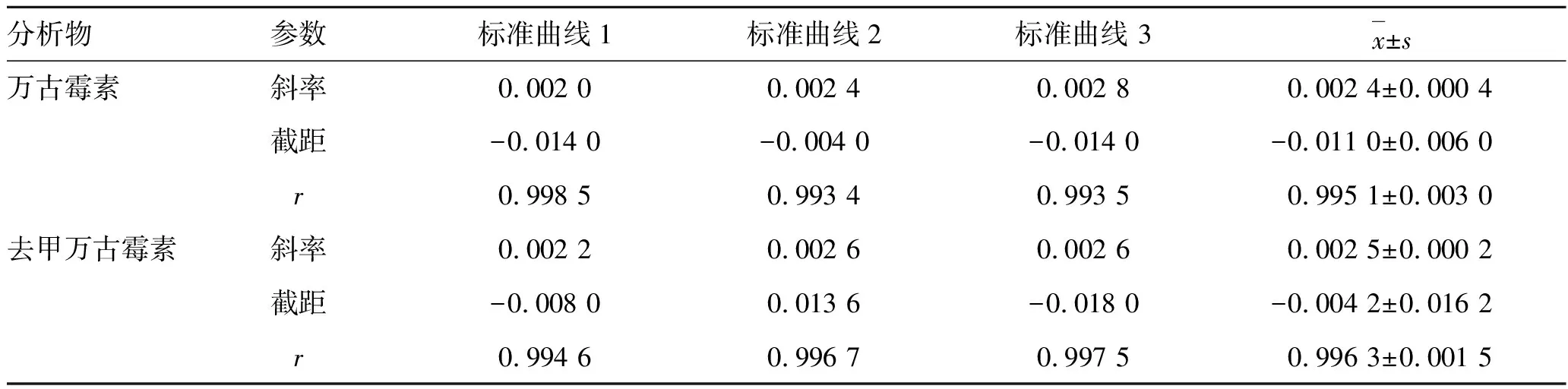
2.2.2标准曲线 分别以血浆中万古霉素或去甲万古霉素的质量浓度为自变量(x),对其峰面积与利奈唑胺峰面积的比值(y)作图,以1/C2为权重,进行最小二乘法线性回归,得血浆样品中万古霉素和去甲万古霉素的标准曲线。连续3 d制备标准曲线,结果见表1。结果表明,万古霉素和去甲万古霉素质量浓度在0.01~10 μg·mL-1范围内线性关系良好,定量下限的实际质量浓度和理论质量浓度的误差在±20%以内,其他质量浓度的误差在±15%以内。
表1万古霉素和去甲万古霉素3条标准曲线
Tab.1 Calibration curves of vancomycin and norvancomycin in 3 runs
分析物参数标准曲线1标准曲线2标准曲线 3x±s万古霉素斜率0.002 00.002 40.002 80.002 4±0.000 4 截距-0.014 0-0.004 0-0.014 0-0.011 0±0.006 0 r0.998 50.993 40.993 50.995 1±0.003 0 去甲万古霉素斜率0.002 20.002 60.002 60.002 5±0.000 2 截距-0.008 00.013 6-0.018 0-0.004 2±0.016 2 r0.994 60.996 70.997 50.996 3±0.001 5
2.2.3最低检测限和定量下限 万古霉素和去甲万古霉素的最低检测限和定量下限分别为3和10 g·mL-1。
2.2.4精密度和准确度 万古霉素和去甲万古霉素质控样品的日内和日间精密度RSD值均小于15%,准确度误差在±15%之内,符合体内生物样品分析的要求。结果见表2和表3。
表2万古霉素和去甲万古霉素日内精密度和准确度
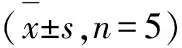
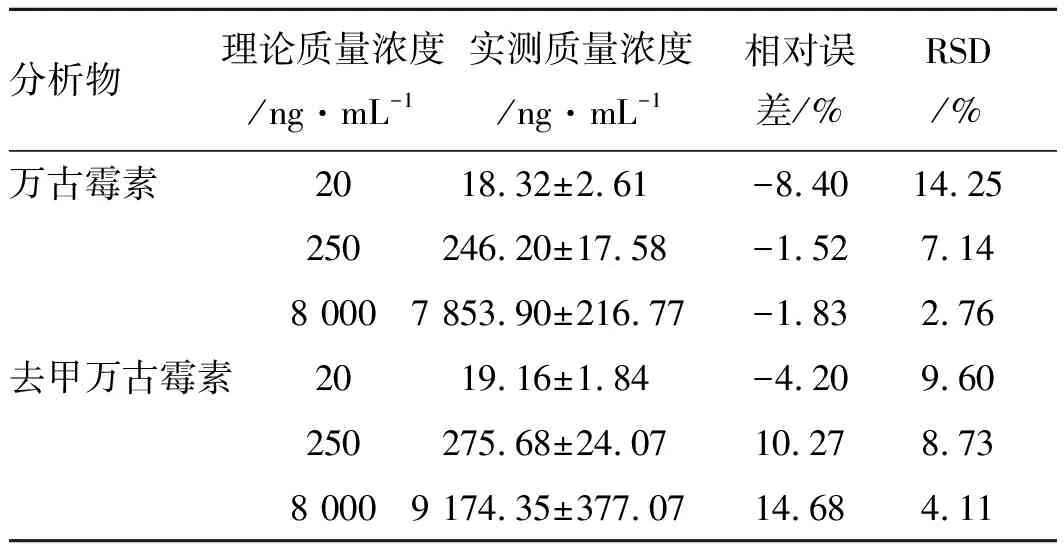
分析物理论质量浓度/ng·mL-1实测质量浓度/ng·mL-1相对误差/%RSD/%万古霉素2018.32±2.61-8.4014.25250246.20±17.58-1.527.148 0007 853.90±216.77-1.832.76去甲万古霉素2019.16±1.84-4.209.60250275.68±24.0710.278.738 0009 174.35±377.0714.684.11
2.2.5基质效应和提取回收率 万古霉素低、中和高质控样品的回收率分别为74.16%±8.13%,76.57%±5.73%和76.79%±7.18%,去甲万古霉素低、中和高质控样品的回收率分别为73.01%±6.23%,77.71%±5.14%和81.11%±6.86%,符合体内生物样品分析的要求。万古霉素和去甲万古霉素的基质效应分别为98.86%~108.69%和95.97%~109.64%,说明无显著的基质效应。结果见表4。内标物的回收率和基质效应分别为74.07%±1.24%和118.17%±6.42%。
2.2.6稳定性 万古霉素和去甲万古霉素血浆样品在反复冻融3次、室温下保存24 h和-80 ℃保存1个月的稳定性结果见表5。结果表明,万古霉素和去甲万古霉素血浆样品在上述条件下稳定。
表3万古霉素和去甲万古霉素日间精度度和准确度
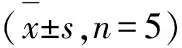
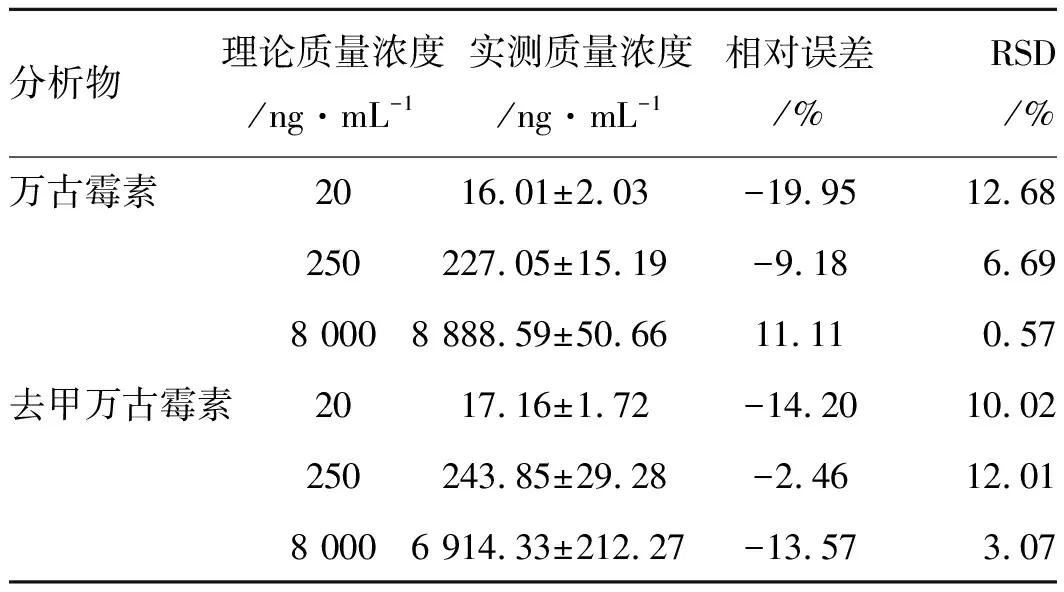
分析物理论质量浓度/ng·mL-1实测质量浓度/ng·mL-1相对误差/%RSD/%万古霉素2016.01±2.03-19.9512.68250227.05±15.19-9.186.698 0008 888.59±50.6611.110.57去甲万古霉素2017.16±1.72-14.2010.02250243.85±29.28-2.4612.018 0006 914.33±212.27-13.573.07
表4万古霉素和去甲万古霉素提取回收率和基质效应
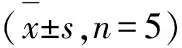
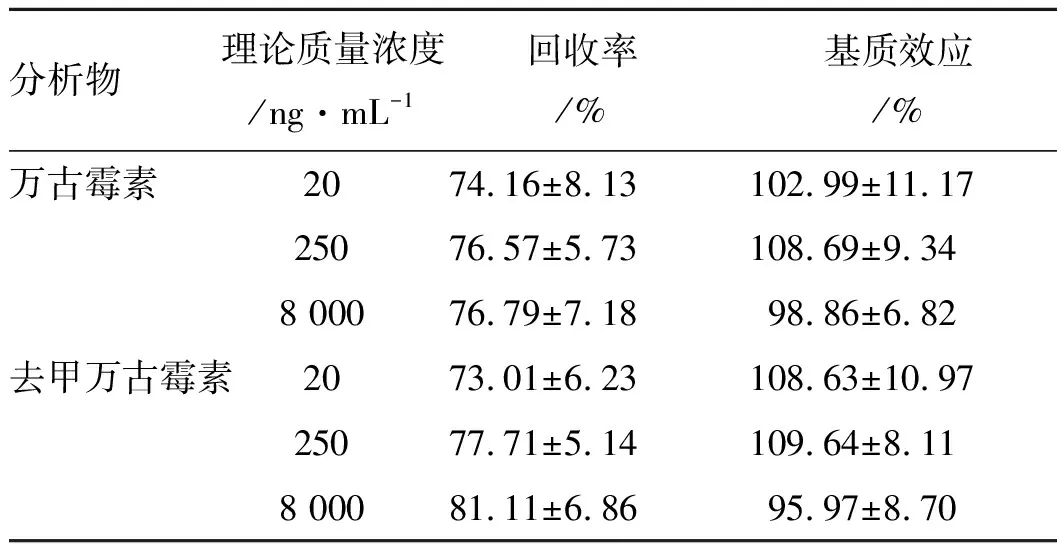
分析物理论质量浓度/ng·mL-1回收率/%基质效应/%万古霉素2074.16±8.13102.99±11.1725076.57±5.73108.69±9.348 00076.79±7.1898.86±6.82去甲万古霉素2073.01±6.23108.63±10.9725077.71±5.14109.64±8.118 00081.11±6.8695.97±8.70
2.2.7稀释效应 血浆稀释后测定值与理论值进行比较,万古霉素的相对误差和RSD值分别为8.41%和8.35%,去甲万古霉素的相对误差和RSD值分别为0.20%和1.48%。二者的相对误差和RSD值均小于15%,结果表明本方法可用于测定质量浓度高于标准曲线上限的样品。
表5万古霉素和去甲万古霉素样品的稳定性结果
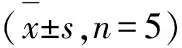
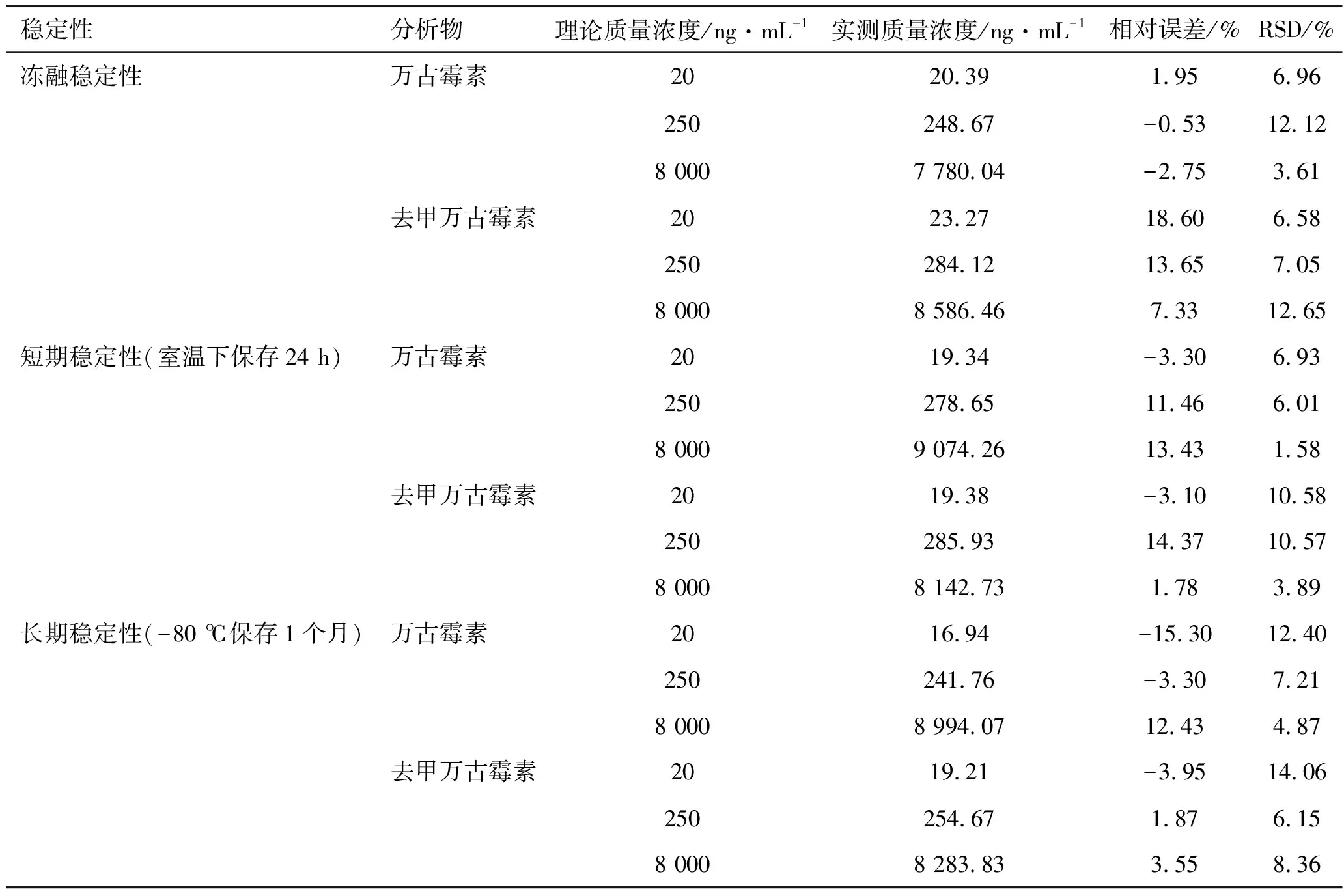
稳定性分析物理论质量浓度/ng·mL-1实测质量浓度/ng·mL-1相对误差/%RSD/%冻融稳定性万古霉素2020.391.956.96250248.67-0.5312.128 0007 780.04-2.753.61去甲万古霉素2023.2718.606.58250284.1213.657.058 0008 586.467.3312.65短期稳定性(室温下保存24 h)万古霉素2019.34-3.306.93250278.6511.466.018 0009 074.2613.431.58去甲万古霉素2019.38-3.1010.58250285.9314.3710.578 0008 142.731.783.89长期稳定性(-80 ℃保存1个月)万古霉素2016.94-15.3012.40250241.76-3.307.218 0008 994.0712.434.87去甲万古霉素2019.21-3.9514.06250254.671.876.158 0008 283.833.558.36
2.2.8治疗药物监测应用 对接受推荐剂量万古霉素和去甲万古霉素治疗的患者进行治疗药物监测,万古霉素和去甲万古霉素的稳态谷质量浓度分别见图4A和4B。52.94%的患者达到万古霉素的治疗窗(10~20 μg·mL-1),33.82%的患者低于治疗窗,而13.24%的患者高于治疗窗。45.45%的患者达到去甲万古霉素的治疗窗(5~10 μg·mL-1),9.09%的患者低于治疗窗,而45.45%的患者高于治疗窗。因此,治疗药物监测对确保万古霉素和去甲万古霉素疗效及降低毒性和不良反应是很有必要的。
图4接受推荐剂量治疗患者的万古霉素(A)去甲万古霉素(B)稳态谷质量浓度
Fig.4 Steady state trough concentration of vancomycin (A) and norvancomycin (B) in patients received recommended dose
3 讨论
LC-MS/MS法与HPLC法相比,具有灵敏度高、专属性强、分析时间短的优点。本研究建立的LC-MS/MS法与已有的方法相比有以下优点:①可同时测定万古霉素和去甲万古霉素的质量浓度,方法适用性强。②血样前处理采用简单的高氯酸沉淀蛋白,与文献报道的在线样品萃取和柱切换[10]、乙腈提取样品后蒸干和复溶后分析[14]等方法相比,样品前处理简单、方便和省时。③高氯酸沉淀蛋白后万古霉素和去甲万古霉素的回收率为50%,由于分析物在水中的高溶解性,当加入2倍体积的水涡旋后,万古霉素和去甲万古霉素的回收率大于70%。④使用梯度洗脱,用反相色谱柱分离万古霉素、去甲万古霉素和内源性物质,万古霉素、去甲万古霉素和内标的保留时间分别为3.67,3.71和4.62 min。未观察到显著的基质效应,说明被测物与内源性基质达到了较好的分离。⑤用利奈唑胺作为内标,相对于用氘代内标,更易获得,且满足分析的需求。⑥本方法的定量下限为10 ng·mL-1,可满足低质量浓度样本的测定需求。
本研究建立了一种简单、快速、可靠以及能同时测定人血浆中万古霉素和去甲万古霉素的LC-MS/MS法,该方法具有高选择性和灵敏度,已应用于万古霉素和去甲万古霉素治疗药物监测,52.94%和45.45%的患者分别达到万古霉素和去甲万古霉素的治疗窗,表明治疗药物监测对确保万古霉素和去甲万古霉素疗效及降低毒性和不良反应很有必要。
