菊糖衍生物的制备、表征、功能 及应用研究进展
2018-10-22黄桂颖何琦怡张炳杰赵肃清曾晓房刘敏荣洪丽冰
黄桂颖,何琦怡,张炳杰,张 焜,*,赵肃清,*,王 佳,曾晓房,刘敏荣,洪丽冰
(1.广东工业大学轻工化工学院,广东广州 510090; 2.仲恺农业工程学院轻工食品学院,广东广州 510225; 3.广东省食品检验所,广东广州 510410)
菊糖是一种果聚糖型多糖,其主链是由(2→1)糖苷键连接β-D-果糖残基聚合而成,末端通常以(1→2)键合的α-D-葡糖残基结束,该结构被命名为GFn,其聚合度(DP)一般在2~60的范围内[1]。菊糖作为一种存储碳水化合物,先后被发现存在于数千种植物中,如洋葱、大蒜、芦笋、小麦、黑麦、大麦和香蕉等。目前,菊糖的商业来源主要是菊科的菊苣(chicorium)根与菊芋块茎(HelianthustuberosusL.)[2]。功能活性丰富是菊糖备受关注的原因之一。由于菊糖对人体无害,静脉注射时,不与血浆蛋白结合,能被肾脏自由过滤,其被用于称为清除方法的肾衰竭测试[3]。菊糖因其β(2-1)糖苷键在上消化道里不被分解,能完整进入肠道并被肠道微生物菌群发酵利用产生短链脂肪酸、丁酸盐和丙酸盐等功能性物质而被称为“益生元”[4]。菊糖能降低机体大肠致病菌数量,缓解便秘,预防及治疗结肠癌[5]。菊糖的摄入有利于控制机体体重,降低低密度脂蛋白胆固醇含量,降低动脉粥样硬化的风险和心血管疾病的发病率。菊糖亦可调节人体免疫功能,控制炎症,改善脂质和葡萄糖代谢,对二型糖尿病有一定的治疗作用[6]。通过增加人体所需矿物质的吸收率,菊糖的摄入能减少机体骨质疏松症风险[7]。除了功能性原因被广泛应用于医药食品行业外,菊糖还因其物理特性被用于改善食品感官性质上。低聚合度菊糖具有一定的甜度,常作为糖尿病人的代糖使用。高聚合度菊糖的流变特性使其作为脂肪替代物被广泛用于食品加工中[3]。作为医药食品的无毒无色无味,生物可降解材料,菊糖降低疫苗在体内的免疫应激反应同时保护了疫苗的稳定性,是疫苗的良好佐剂[8]。菊糖与抗生素一起摄入,降低抗生素对肠道有益菌的不良影响[9]。
作为无毒,可生物降解和具有特殊功能特性的天然生物聚合物,菊糖在医药食品的材料中具有良好的应用前景。然而,有限的溶解度与亲和力限制了菊糖的应用范围。因此,菊糖衍生化技术引起了人们的广泛关注。化学衍生化法通过改变菊糖的结构,从而改善其物理化学性质与生物活性。衍生化既改进了菊糖骨架的特性包括亲水性,疏水性,溶解度,反应性和弹性,也增强了菊糖的抗氧化、抗炎和抗癌等活性。同时,菊糖骨架的引入对于改善某些生物活性分子的热敏性,光稳定性,溶解性和靶向性亦存在积极的作用。科技的发展也促进了菊糖衍生物表征方法从化学法发展到多种仪器法,丰富的表征手段给菊糖衍生物与其生物活性的构效关系提供了更详细的理论依据。近几十年来关于菊糖衍生物的研究颇丰,包括了菊糖衍生物合成方法与表征,菊糖衍生物的活性,以及菊糖衍生物的应用等三大类研究。通过对这三类研究的综合分析,有助于研究菊糖衍生物的衍生方法、结构表征与功能活性或者应用之间的关系,是掌握菊糖衍生物开发利用新方向的重要依据。
1 菊糖的衍生化
1.1 功能基团修饰菊糖
1.1.1 取代反应 酰化。Arvind 等在真空和避水的条件下,以DMF为溶剂,加入菊糖、乙酸钠和乙酸酐40 ℃反应24 h后,得到菊糖乙酸酯[10]。应用类似方法,可将乙酸酐替代成酯酰氯制备菊糖乙酸酯、菊糖琥珀酸酯、菊糖丙酸酯、菊糖月桂酸甲酯、菊糖肉豆蔻酸甲酯、菊糖棕榈酸甲酯、油酸甲酯以及菊糖肉桂酸酯[11-15]。Grandtner和Rusu等将两种酰氯同时加入反应体系,分别制备得到菊糖甲基丙酸酯和月桂酸酯的混合酯,以及菊糖甲基丙烯酸酯和棕榈酸酯的混合酯[16]。Han等分别用烷基链长为C10、C12、C14和C16的脂肪酸酰氯在室温和氢氧化钠的催化下与菊糖反应,生成相应的长链菊糖酯[17]。Mooter和Vervoort等将菊糖溶于DMF中,加入DMAP后按需加入甲基丙烯酸缩水甘油酯,室温反应72 h后异丙醇沉淀反应物得到菊粉甲基丙烯酸酯[18-20]。Castelli等在此基础上制备了菊糖-甲基丙烯酸酯-琥珀酸酯(INU-MA-SA)。上述反应产物菊糖甲基丙烯酸酯、琥珀酸酐和TEA溶于DMF中,25 ℃反应24 h得到INU-MA-SA[21]。Pitarresi等分两步制备了菊糖-琥珀酸酯-半胱氨酸(INU-SA-Cys)。首先,在氩气下将适量的菊粉溶于无水DMF中,加入适量TEA和琥珀酸酐(SA),在25 ℃下反应24 h,乙醚/丙酮沉淀反应物得到INU-SA。然后,在室温和氩气环境下,在INU-SA水溶液里加入1-乙基-3-(3-二甲氨基丙基)碳化二亚胺(EDC),pH调4.75活化1 h,加入半光氨酸,在pH5.3下保持3 h后,调到pH8.0加入DL-二硫苏糖醇反应3 h得到INU-SA-Cys[22]。Janciauskaite等将菊糖琥珀酸酯溶于蒸馏水中,并加入EDC。将该溶液与一定比例的壳聚糖乙酸水溶液合并,在50 ℃反应48 h得到菊糖-壳聚糖共聚物[23]。Morros等在加入十二烷基三甲基溴化铵(DTAB),pH8.5~9.0的水介质中,使菊糖和2-辛烯-1-基琥珀酸酐(OSA)和2-十二碳烯-1-基琥珀酸酐(DDSA)反应1 h,制备了中长链菊糖烯基琥珀酸酯[24]。Sardo等两步合成了菊糖-咪唑-二亚乙基三胺(INU-IMI-DETA)。首先把菊糖、4-咪唑乙酸盐、DCC和DMAP置于DMF中,25 ℃反应6 h得到INU-IMI。然后,把溶于DMSO的INU-IMI与双(4-硝基苯基)碳酸酯(4-BNPC)混合物置于微波反应堆里25 W照射1 h。接着在60 ℃以下,把DETA的DMSO溶液缓慢滴入混合物中反应4 h,丙酮沉淀得到INU-IMI-DETA[25]。Hartzell等将甲酰基水杨酸溶于DMF中,缓慢加入羰基二咪唑,以及溶于DMSO的菊糖和TEA,反应4 h后得到菊糖甲酰基氨基水杨酸酯[26]。胡云霞等分两步把氨基吡啶基嫁接到菊糖。首先,在菊糖水溶液中加入氯乙酰氯,室温搅拌12 h,丙酮沉淀得到氯乙酰菊糖。然后,把氯乙酰菊糖和吡啶或者氨基吡啶溶于DMF里,60 ℃下搅拌24 h,用丙酮沉淀得到氨基吡啶基菊糖[27]。
醚化。Öner等先将菊糖溶于去离子水中,加入氢氧化钠和氯乙酸,混合物在60 ℃加热1 h,降到室温后加入乙醇沉淀得到羧甲基菊糖(CMI)[28]。CMI进一步衍生为含有酰胺键的菊糖化合物Schoener等将CMI、N-羟基磺基琥珀酰亚胺(sulfo-NHS)和EDC制备了CMI-阿霉素缀合物。首先CMI、sulfo-NHS和EDC一起置于水中混合1 h,再加入阿霉素混合2 h得到菊糖-阿霉素缀合物[29]。Joshi等将CMI溶在一定比例的EDC和sulfo-NHS溶液中孵育1.5 h后,将银-石墨烯量子点纳米复合物中性悬浮缓冲液加入预备溶液中并放置过夜得银-石墨烯量子点核心和羧甲基菊糖壳的核-壳结构[30]。Sun等通过两步制备了CMI-4-氨基苯硫酚聚合物(ATP-CMI)。适量的CMI溶于蒸馏水中,先用HCl转化为其游离酸。然后加入一定比例的NHS和EDC。混合3 h后,加入4-ATP乙醇溶液,并在4 ℃在黑暗中搅拌过夜。用硼氢化钠将pH再次调节至7。反应混合物在乙醇中沉淀后得到CMI-ATP缀合物[31]。Rahul等在室温下将菊糖分散在异丙醇中,将适量的氢氧化钠和(3-氯-2-羟丙基)三甲基氯化铵加入到上述溶液中,并将混合物在50 ℃反应6 h,然后把pH调节到7,经丙酮沉淀得到2-羟丙基三甲基氯化铵菊糖[32]。Morros等将菊糖溶于水中,加入氢氧化钾和硼氢化钠,在25 ℃剧烈搅拌,80 ℃搅拌1 h,继续加入溶于异丙醇的1,2-环氧十二烷反应1 h后,冷却到室温,用5% HCl中和至pH6.00,经透析,丙酮结晶处理后得到β-羟烷基醚化菊糖[33]。Ren等在25 ℃下,将一定量的NaOH加入菊糖水溶液。在室温下搅拌后4 h,混合物在-20 ℃下结霜8 h,温度升高到75 ℃,加入乙烯亚胺,在75 ℃下反应16 h。混合物经甲醇沉淀得到O-(氨基乙基)菊糖[34]。
1.1.2 加成反应 Exerowa等在碱性催化剂叔胺作用下,异氰酸酯和菊糖反应得到菊糖氨基甲酸酯[35]。同样方法可制备菊糖月桂基氨基甲酸酯和菊糖氨基甲酯[36-37]。Rahul等以硝酸铈铵为自由基引发剂,用微波辐射冷却循环技术辅助菊糖与丙烯酰胺反应得到菊糖聚丙烯酰胺共聚物[38]。Fares等在氮气环境下,使菊粉完全溶解在40 ℃的双蒸水中,加入适量硝酸铈铵,再逐滴加入丙烯酸单体,30 ℃下缀合4 h得到菊糖聚丙烯酸共聚物[39]。Pitarresi等把菊糖在氩气下溶于DMF,3 h后加入二乙烯基砜,3 h后加入TEA,60 ℃反应24 h得到乙烯基砜基菊糖[40]。
1.2 生物活性分子修饰菊糖
刘俊等将菊糖溶于蒸馏水中,加入适当的抗坏血酸和儿茶素,无氧硝基气流中混合半小时,加入适量的过氧化氢在氮气的环境下反应12 h,制备儿茶素-g-菊糖共聚物[41-42]。Arizmendi-Cotero等将菊糖溶于去离子水中,随后加入相应量的没食子酸和过氧化氢/抗坏血酸引发剂。混合物在25 ℃恒温搅拌24 h得到没食子酸-菊糖共聚物[43-44]。张鲁中等将适当比例的布洛芬、N,N′-羰基二咪唑和菊糖置于DMSO中80 ℃下反应24 h,制备了菊糖-布洛芬共聚物[45]。Mandracchia等在氮气环境下,将生育酚琥珀酸酯溶于DMF溶液中,加入N,N′-二环己基碳化二亚胺(DCC)和N-羟基磺基琥珀酰亚胺钠盐(NHSS)使其活化3 h,形成生育酚琥珀酸酯NHSS溶液。然后将含有催化剂TEA的菊糖DMF溶液滴加到生育酚琥珀酸酯NHSS溶液中,在25 ℃或40 ℃,氮气下反应12 h,经过丙酮沉淀得到不同取代度的菊糖生育酚琥珀酸酯[46-48]。
1.3 生物大分子修饰菊糖
美拉德反应。美拉德反应又称羰氨反应,一般发生在还原糖或者还原糖基的羟基和氨基酸的氨基之间。Jing等通过美拉德反应制备了酪蛋白菊糖、卵类粘蛋白菊糖、白蛋白菊糖、溶菌酶菊糖缀合物[49]。吴慧伦等将一定比例的菊糖和精氨酸溶解于二次蒸馏水中,在100 ℃下进行回流反应。然后,用乙醇或丙酮提取菊糖美拉德反应产物菊糖-精氨酸缀合物[50]。
与氨基酸的偶联。与美拉德反应不同,菊糖氨基酸的偶联是菊糖的羟基与氨基酸的羧基发生缩合反应。Stevens等介绍了以DMF为溶剂,DMAP为催化剂,DCC为缩合剂,菊糖与氨基被封闭的甘氨酸或者赖氨酸的羧基反应得到甘氨酸偶联菊糖和赖氨酸偶联菊糖[51]。菊糖与氨基酸的偶联化合物可用于荧光标记菊糖。菊糖首先与酪氨酸(Tyr)偶联,产物在碱性水溶液中与荧光物质异硫氰酸荧光素(FITC)反应12 h,再用终浓度为80%乙醇沉淀得到亮黄绿色异硫氰酸荧光素菊糖(FITC-inulin)[52]。
2 菊糖衍生物的结构表征方法
傅里叶红外光谱仪(FT-IR)、核磁共振仪(1H-MNR和13C-NMR)、X射线衍射仪(XRD)等技术常用于确认分子与基团在菊糖骨架上的成功嫁接。基于嫁接到菊糖上的基团分子的性质不同,还可以选用薄层色谱(TLC)、高效液相色谱-示差检测器-紫外检测器(HPLC-RID-UV)、扫描电镜(SEM)、透射电镜(TEM)、聚丙烯酰胺凝胶电泳(SDS-PAGE)等设备进一步表征菊糖衍生物的结构[53]。
基于菊糖的衍生化多为呋喃果糖上羟基的氢离子被取代,通过FT-IR图像,可以清晰地观察到衍生前后,菊糖的羟基以及嫁接基团或化合物的特征峰振动情况,从而判断菊糖衍生化的程度,以及菊糖骨架的保留状况[34,42,54-55]。1HMNR既能观察到相应化合物修饰菊糖的情况,也能反映衍生化的取代度。含碳氢氧的基团取代菊糖上的羟基时会引起该区域的峰数、峰型和面积的改变来判断嫁接情况[40,43,56-57]。XRD常用于对比菊糖衍生前后的结晶度的改变,以及菊糖与嫁接上的基团分子之间的相互作用力。一般情况下,峰高的降低,峰数量的增加,以及峰位的变化,均表明衍生物具有新的物理结构[35,58]。
TLC可用于确认酚类化合物在菊糖骨架上的成功嫁接。通常,游离酚在TLC硅胶平板上迁移一段距离,而菊糖-酚类缀合物则保持在基线[58]。由于嫁接了酚类化合物的菊糖含有紫外吸收基团,紫外分光光度计(UV)亦可用于判断菊糖-酚类缀合物的情况。HPLC结合反相C18色谱柱和紫外检测器适用于菊糖-酚类缀合物与游离酚酸的分离分析。此外,基于菊糖-酚类缀合物的分子量显示了酚类物质的接枝率,HPLC亦用于测定菊糖-酚类缀合物的分子量。通常采用尺寸排阻色谱(SEC)或凝胶渗透色谱(GPC)与折射率检测器(RID)结合使用[25,45,59-62]。
3 菊糖衍生物的活性与应用
表1可见,菊糖衍生物的应用与其结构、活性密切相关,而这些结构与活性主要由菊糖本身以及其嫁接的化合物决定。
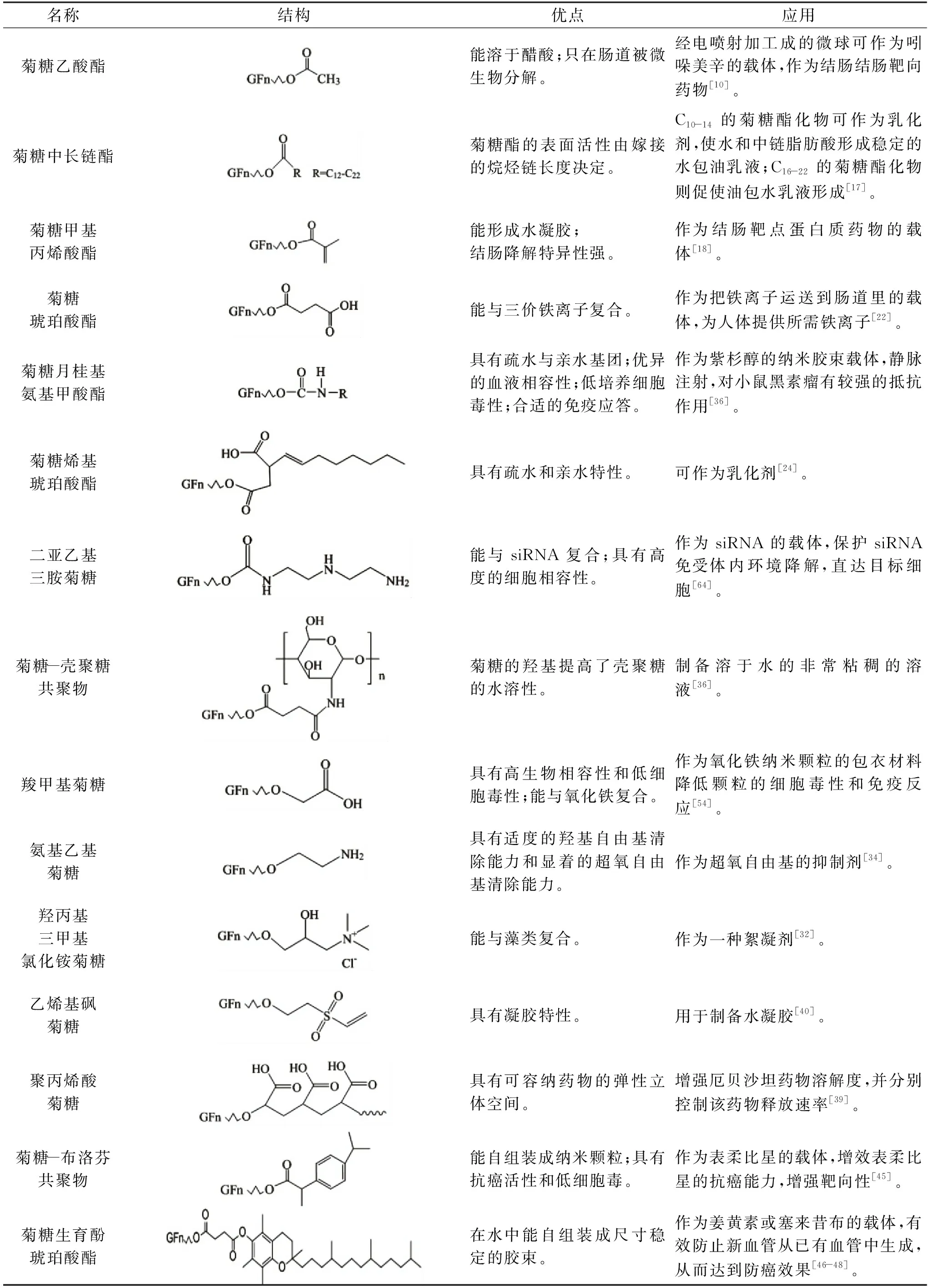
表1 菊糖衍生物的名称、结构、优点与应用Table 1 Name,stucture,synthesis and advantage of inulin derivative
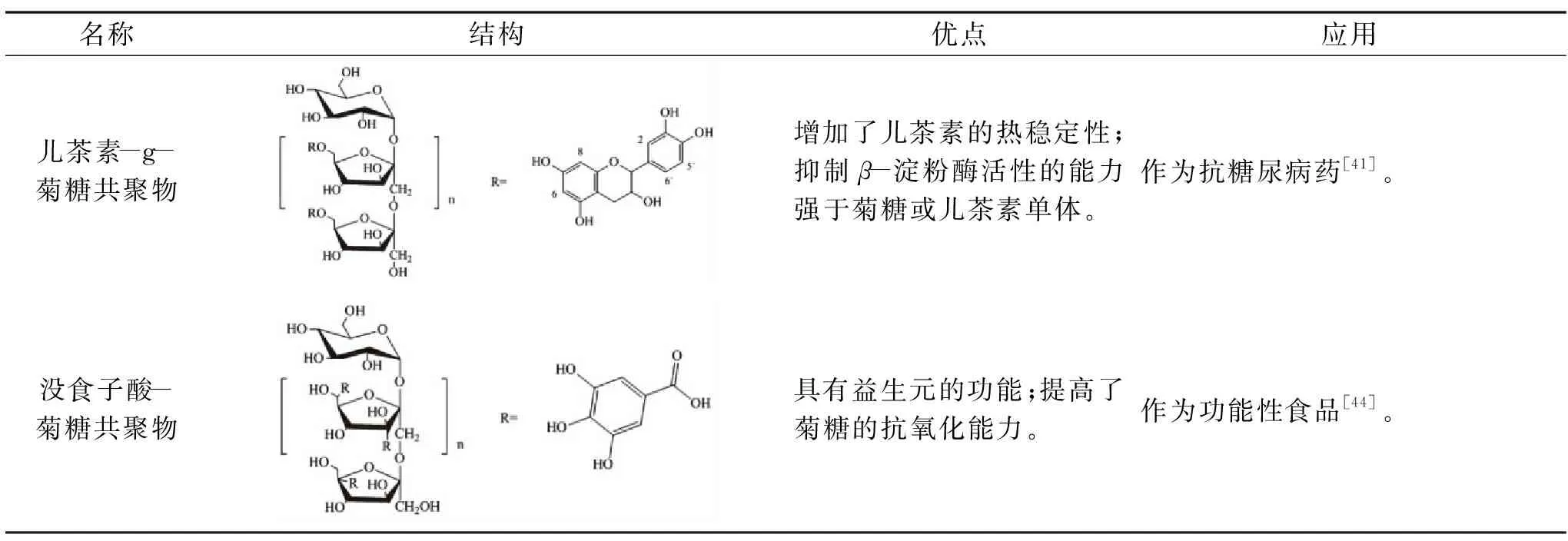
续表
3.1 菊糖衍生物的活性
一般情况下,生物活性分子的嫁接有利于提高菊糖的抗氧化活性[63]。多酚黄酮等生物活性分子嫁接到菊糖上,既增加了菊糖相应的生物活性同时,亦有利于体内对多酚黄酮的消化吸收以及调整靶向性。多种氨基吡啶基乙酰基菊糖不同程度地提高了菊糖清除羟基自由基、超氧自由基及DPPH自由基的能力。儿茶素-g-菊粉除了对超氧自由基,羟自由基和H2O2有清除作用,以及对脂质过氧化有抑制作用外,对糖尿病和急性肝损伤也有潜在的治疗和保护作用。嫁接了没食子酸的菊糖衍生物保留了其益生元的作用,能刺激嗜酸乳杆菌的生长,同时也显示了清除DPPH和O2等自由基的能力并且可以降低脂质过氧化。美拉德反应产物酪蛋白菊糖、卵类粘蛋白菊糖、白蛋白菊糖、溶菌酶菊糖、精氨酸菊糖缀合物都具有较菊糖好的DPPH自由基的清除能力。
菊糖是一种能够在静脉注射后达到尿路高浓度的聚合物,其与具有降低尿路氧化应激能力的生育酚缀合后,形成的菊糖生育酚琥珀酸酯纳米颗粒,可作为注射型尿路细菌感染的靶向抗炎症和感染药物。菊糖甲酰基氨基水杨酸酯除了保留了5-氨基水杨酸治疗溃疡性结肠炎等功效外,菊糖在肠道中发酵产生的短链脂肪酸有协同增效作用。药物嫁接到菊糖上可以增加其对光,温度,水解和化学试剂的稳定性,同时增加药物效果,减少药物用量。研究显示菊糖阿霉素缀合物被用于改善阿霉素单体的癌症治疗药物。菊糖阿霉素缀合物较阿霉素本身更稳定,也更容易与循环肿瘤DNA结合。在Caco-2和HT29-MTX结肠癌细胞模型中,基于菊糖本身能降低和抑制结肠肿瘤细胞的转移活性和生长,缀合物的使用减少了阿霉素的用量从而降低药物对心脏的毒性。
3.2 菊糖衍生物的应用
3.2.1 乳化剂 烷基菊糖酯多作为乳化剂应用于乳液的制备。烷基菊糖酯相对于纤维素酯更易于溶解和加工,其亲水和疏水的性质与应用范围也可通过调整菊糖和酯化组分的链长,以及取代度进行改变。基于烷基链长与取代度的影响,烷基链较短的菊糖酯化物可作为水包油乳液的乳化剂,而烷基链较长的菊糖酯化物则可促油包水乳液的形成。菊粉氨基甲酸酯具有张力活性,可用作化妆品或制药应用中的乳化剂。除了菊糖酯化物,美拉德反应是提高菊糖的乳化性的另外一种方式,如菊糖与酪蛋白的美拉德反应的产物可作乳化剂。
3.2.2 包埋材料 基于菊糖结构和活性特点,菊糖衍生物亦常作为包埋材料,被用于靶向性药物载体。经电喷射进行处理的菊糖乙酸酯微球,在缺乏菊糖酶和肠道微生物低pH的肠胃模拟液中较稳定,提高了药物在结肠中的生物利用度,是微生物触发的药物递送系统。菊糖生育酚琥珀酸酯作为载体,很好地提高了抗癌药物姜黄素和塞来昔布的生物活性以及水溶性。月桂基氨基甲酸酯菊糖可作为紫杉醇的载体,形成粒径大约为260 nm的胶束,除了提高紫杉醇的水溶性以外,还增加抗癌靶向性,相同功效情况下,被包埋的紫杉醇剂量可减半。作为载体,二亚乙基三胺菊糖有效地与短干扰核糖核酸(siRNA)复合成具有高度细胞相容性,平均尺寸为600 nm的颗粒。在肝细胞癌衍生细胞JHH6中,二亚乙基三胺菊糖可以有效递送功能性siRNA[64]。菊糖布洛芬药物载体与RGD肽聚合的纳米颗粒对于盐酸表阿霉素具有高效的载药性和靶向性。菊糖肉桂酸酯作为甲氨蝶呤的载体,对结肠癌具有良好的靶向性。负载铁离子的INU-SA-Cys在模拟肠道中较好地释放铁离子,是潜在的缺铁性贫血的口服治疗方式。除了靶向性好,菊糖衍生物的包埋率和缓释率都比较理想。菊糖乙酸酯微胶囊对于吲哚美辛的包埋率达到100%。包埋了右旋花椒酚的菊糖乙酸酯和丙酸酯,在喷雾干燥后形成10~700 μm的光滑球型颗粒,均具有缓释作用。24 h后,菊糖乙酸酯微球中的右旋花椒酚释放率为60%,菊糖丙酸酯微球的释放率是10%。另外,菊糖衍生物亦能形成稳定的水凝胶载体。在硫酸铵和N,N,N′,N′-四甲基乙二胺存在的情况下,菊糖甲基丙烯酸酯的双键转化成共价交联的方式从而形成载药的水凝胶。基于INU-MA-SA的药物释放水凝胶与由二肉豆蔻酰磷脂酰胆碱的单层囊泡制成的生物膜模型,在pH7.4下具有良好的释放能力。
3.2.3 包衣材料 菊糖衍生物亦可用作药物载体的包衣材料。CMI包封3-氨基丙基三乙氧基硅烷接枝的氧化铁纳米颗粒提高了生物相容性。CMI缀合银-石墨烯量子点纳米复合材料显着降低银-石墨烯量子点制剂的细胞毒性,CMI的缀合使负载5-氟尿嘧啶的银-石墨烯量子点纳米复合物提高了对胰腺癌细胞靶向治疗的效率。
3.2.4 荧光标记物载体 菊糖衍生物可用于了解目标化合物在体内的行为特征。菊糖短链脂肪酸酯可用于探测食物、肠道微生物与体内代谢之间的关系。参加实验的男性在摄入适量的13C标记菊糖丙酸酯7 d后,减少了食物摄入量。结果显示结肠中一定量的丙酸盐能产生食欲调节作用。荧光标记菊糖(FITC-inulin)和改进的灌注系统可实时监控小鼠小肠的液体和/或电解质的运动[65]。安全的FITC-inulin可代替放射性同位素用于肾功能微穿孔等方式评估单肾过滤率[66-68]。
4 结论
通过取代、加成、氧化还原、美拉德等反应,可把特定功能基团、生物活性分子以及生物大分子嫁接到菊糖上。FT-IR、1HNMR、13CNMR、XRD、TLC、HPLC、UV和SEM等多种化学及仪器方法可用于菊糖衍生物的结构分析。一般情况下,菊糖衍生化后的抗氧化活性较衍生前好,尤其以嫁接了黄酮多酚等生物活性分子的菊糖在清除羟基自由基、超氧自由基及DPPH自由基的能力上都有明显的提高。嫁接了抗炎抗癌药物的菊糖衍生物,除了具备了相应的抗炎抗癌功效外,还兼有菊糖的生物相容性好、毒性低、免疫反应小和靶向性好等功能。菊糖衍生物多用于食品、药品及化妆品的递送系统中。在递送系统中,菊糖衍生物的应用灵活和多样化,可作为乳化剂、包埋材料和包衣材料,改善了被包埋成分的毒副作用大、透膜性差和稳定性差等问题。同时,菊糖衍生物也可作为荧光标记物的载体,对体内如肠道运作的监控有重要作用。
5 展望
尽管在菊糖衍生物的开发利用方面已有大量的工作基础,但仍有三个研究领域需要探讨:a.对用于衍生化的菊糖来源、结构和分子量分布进行分析。分子量分布的差异赋予了菊糖特殊的物化性质和生物活性。相对于短链菊糖,不溶于37 ℃水的半结晶体长链菊糖(δ inulin),氢键结合成的反平行螺旋形状更多,其免疫应答更强,在肾脏的排出更缓慢,能被作为免疫佐剂使用[69-70]。这些特性对菊糖衍生物活性的影响仍有待研究。b.基于抗氧化机理的多样性,单一的评价方法存在不足,多种体内外抗氧化评价方法的使用有利于全面了解菊糖及其衍生物的抗氧化活性。研究表明虽然化学法评价结果显示菊糖不具备显著的抗氧化性,但生物法评价结果却证明菊糖具有较好的抗氧化效果,该活性通过保护机体结肠粘膜和粘膜下层避免蛋白质氧化实现[71]。然而,目前菊糖与其衍生物的抗氧化活性评价方法主要为化学法,可见,建立一套系统合理的评价方法有利于更准确地表征菊糖及其衍生物的抗氧化活性。c.进一步拓展菊糖衍生物的应用。近年菊糖衍生物的应用集中在生物医学和制药学领域中,在食品方面的应用有待开发。功能和风味是现在食品的重要因素。菊糖衍生物可作为功能性食品使用,或用于延长食品风味的释放时间和改善食品感官状况,如风味物质的包埋,不良风味的掩盖等。
