果胶和热处理对蛋白质乳液凝胶结构特性和复合维生素稳定性的影响
2018-10-08高彦祥毛立科
穆 硕,鹿 瑶,高彦祥,毛立科*
(北京食品营养与人类健康高精尖创新中心,教育部北京市共建功能乳品重点实验室,中国农业大学食品科学与营养工程学院,北京 100083)
蛋白质乳液凝胶又称乳化颗粒填充蛋白质凝胶,其特点是蛋白质凝胶中含有乳化的油滴。乳化油滴表面积较大,可以和凝胶网络中的分子有更多的接触,成为网络结构中的支撑物。通过改变油滴结构,包括粒径大小与分布、油相结晶度等可以调节凝胶的形成过程,并影响凝胶的质构特性[1]。许多食品,如豆腐、香肠、奶酪、酸奶都可以归类为蛋白质乳液凝胶。另一方面,蛋白质乳液凝胶可以作为食品功能因子的传递体系:脂溶性功能因子可以分散在油滴中,水溶性功能因子则可以分散到凝胶结构当中[2]。功能因子一方面受到凝胶的保护,另一方面被凝胶结构固化,因此具有较高的化学稳定性[3]。以往针对食品功能因子传递体系的研究主要集中于单一功能因子或者相似极性功能因子,而对于能够同时包埋不同极性功能因子的传递体系研究较少[4-5]。
许多食品体系中同时含有蛋白质和多糖。荷电能力不同的多糖与蛋白质相互作用各不相同,两者共存时可以形成单连续相凝胶体系、双连续相凝胶体系、均匀连续凝胶体系、非均匀链状凝胶体系等不同微观结构[6-7]。但是,已有的研究主要针对体系组分和结构相对简单的蛋白质凝胶体系[8],而对含有油相和油水界面的蛋白质乳液凝胶的研究非常有限。乳液凝胶中,多糖的存在不仅影响水相结构和蛋白质的凝胶过程,还影响油滴分布、界面组分和结构[9-10],因此多糖对乳液凝胶性能的影响机制更加复杂,需要更深入的研究。
本课题研究果胶对大豆分离蛋白乳液凝胶理化性质及复合维生素稳定性的影响机制。通过控制大豆分离蛋白乳状液油滴粒径大小、调节油滴界面组成,研究不同果胶添加量及热处理温度对乳状液稳定性、蛋白质凝胶过程(凝胶时间)及凝胶结构(质构、持水性)特性的影响;通过追踪蛋白质乳液凝胶在贮藏过程中复合维生素含量的变化,阐释凝胶结构对不同维生素稳定性的影响机理。
1 材料与方法
1.1 材料与试剂
大豆分离蛋白(930E) 山东万德福公司;玉米油山东三星玉米产业科技有限公司;葡萄糖酸-δ-内酯(glucono delta-lactone,GDL) 上海新洛洛食品有限公司;果胶(食品级) 北京宝得瑞公司;VE(食品级) 浙江新和成股份有限公司;D-异抗坏血酸钠(食品级) 诸城华源生物工程有限公司;无水乙醇、碘、淀粉指示剂(均为分析纯) 北京化工厂。
1.2 仪器与设备
JY 92-IIN超声波细胞粉碎机 宁波新芝生物科技公司;T25高速剪切机 德国IKA公司;NS1001L2K高压均质机 意大利GEA NiroSoavi公司;Zeta-sizer Nano-ZS90马尔文激光粒度仪 英国Malvern公司;LF111 LUMiSizer稳定性分析仪 德国LUM公司;AR1500流变仪 美国TA公司;TNS-Pro质构仪 美国FTC公司;3k15离心机 德国Sigma公司;UV-1800紫外-可见分光光度计 日本岛津公司。
1.3 方法
1.3.1 大豆分离蛋白乳状液的制备
将定量大豆分离蛋白与去离子水混合,磁力搅拌实现初步分散;分散液在室温条件下通过超声波细胞粉碎机进行超声处理(400 W、5 min),促进大豆分离蛋白的溶解;加入0.01%的叠氮化钠防止蛋白质腐败;向蛋白质水溶液中分别加入质量分数0%、0.05%、0.1%、0.2%的果胶,磁力搅拌过夜使果胶充分水合并分散在溶液当中;大豆分离蛋白-果胶混合溶液在70 ℃或80 ℃水浴中加热30 min,利用冰浴迅速冷却;此溶液作为乳状液制备的水相。
水相中添加玉米油(油水相质量比1∶4),使用高速剪切仪以10 000 r/min的转速剪切1 min制成粗乳液;再通过高压均质机(50 MPa均质3 次)获得乳液;所得乳液通过冰水迅速冷却至室温。
1.3.2 蛋白质乳液凝胶的制备[11]
向制备的乳液中添加质量分数0.5%的GDL并混匀,室温条件下静置12 h以获得蛋白质乳液凝胶。当利用乳液凝胶作为复合维生素传递体系时,在乳液的水相和油相中分别加入D-异抗坏血酸钠(0.5%)和VE(1%)。预实验表明,2 种维生素的添加对乳液粒径、稳定性及凝胶的质构特性无显著影响。
1.3.3 乳液粒径和Zeta电位的测定
采用激光粒度仪测定乳液的粒径与电位。取100 μL样品于试管中,加入20 mL去离子水稀释200 倍。测量时设定折光系数为1.450,25 ℃保温平衡2 min。为了减少多重散射所造成的测量误差,每个样品重复测定3 次,取平均值。
1.3.4 乳液稳定性的测定[12]
应用LUMiSizer稳定性分析仪,通过加速分层和量化沉淀、悬浮的方法快速测定乳液的稳定性。测量过程中,取乳液约1.8 mL注射到光径为2 mm的样品试管底部,平放至仪器中,使用近红外或蓝色光从侧面照射样品试管,并通过另一面的探测器接收样品不同位置透过的光,从而得到样品透射率分布的变化。通过测量不同时间条件下样品的透射曲线,从而分析样品物理稳定性和粒子迁移过程。
实验条件设定为温度25 ℃,离心转数4 000 r/min,样品透射率的特征线每10 s记录一次,共800 次。每次测定做一组平行。
1.3.5 凝胶时间的测定[11]
采用1.3.2节方法在流变仪平行面板上实现乳液向凝胶转变,利用流变仪动态监测凝胶形成过程中储能模量和损耗模量(G’和G”)的演变过程。流变仪参数:60 mm平行面板(探头),平板间隙1 mm,实验温度25 ℃。振荡实验:0.5%应变,1 Hz振荡频率,每10 s进行一次测定,共测定12 h。样品周边涂一薄层硅油以减少测量过程中水分的蒸发。定义凝胶时间为G’-时间曲线和G”-时间曲线的交点。
1.3.6 蛋白质乳液凝胶质构分析
采用1.3.2节方法使乳液在50 mL离心管中成胶,使用质构仪测定凝胶的硬度和弹性。质构仪参数:圆柱型柱塞探头(直径20 mm),在25 ℃条件下以1 mm/s的速率压缩(形变10 mm)2 次,做3 组平行并记录压力-时间曲线。定义硬度为第1次压缩时的最大峰值压力,定义弹性为第2次压缩中所测到的样品恢复高度与第1次压缩型变量之比,即样品经过第1次压缩后能够再恢复的程度。
1.3.7 贮藏过程中蛋白质乳液凝胶中维生素稳定性分析
含有复合维生素的乳液凝胶在室温条件下贮藏12 d,每3 d测定凝胶中维生素的含量,计算维生素的包埋率,公式如下:

1.3.7.1 VE含量的测定[13]
参考GB 1886.233—2016《食品添加剂维生素E》。准确称取含VE的乳液凝胶3.0 g,加无水乙醇25 mL,搅拌,促进VE的溶出,冷却过滤,提取3 次合并滤液;采用分光光度计法测定在284 nm波长处的滤液吸收峰;利用标准曲线(y=0.005 2x-0.033 5)计算滤液中VE的含量。
1.3.7.2 D-异抗坏血酸钠含量的测定[14]
参考GB 8273—2016《食品添加剂D-异抗坏血酸钠》的方法测定。准确称取凝胶样品5 g,加30 mL蒸馏水捣碎后水浴加热溶解;3 600 r/min离心30 min。用注射器吸取下层清液,采用碘滴定法测定清液中D-异抗坏血酸钠含量。
1.4 数据处理
每组实验至少重复2 次,每个样品至少检测3 组数据,结果用表示。运用Origin 8.0软件,采用Duncan法对数据进行单因素方差分析,显著水平为5%。
2 结果与分析
2.1 果胶对乳状液性质的影响
乳状液液滴大小及其分布对乳状液的稳定性有很大的影响[15]。根据斯托克斯规律,颗粒粒径越小,沉淀速度越慢,乳状液也就越稳定。如表1所示,随着果胶质量分数的增加乳液的粒径都呈上升趋势,这可能是由于加热过程中蛋白质与果胶形成了分子质量更大的共价复合物,无法在均质过程中快速吸附[16],使得部分油滴未能被乳化剂充分覆盖而发生聚集。而温度越高,则越可能促进该共价反应的进行。所以,复合物溶液制备的乳状液粒径越大。乳液Zeta电位的测定结果进一步验证了此推论:果胶质量分数越高,乳液界面电势强度(Zeta电位的绝对值)越低;温度升高,界面电势强度减弱(表1)。尽管有研究表明,蛋白质和多糖在带相同电荷的情况下也可能通过静电吸引形成非共价复合物(如通过蛋白质的正电基团与果胶的负电基团)[17],但在本体系中无法确定其影响。
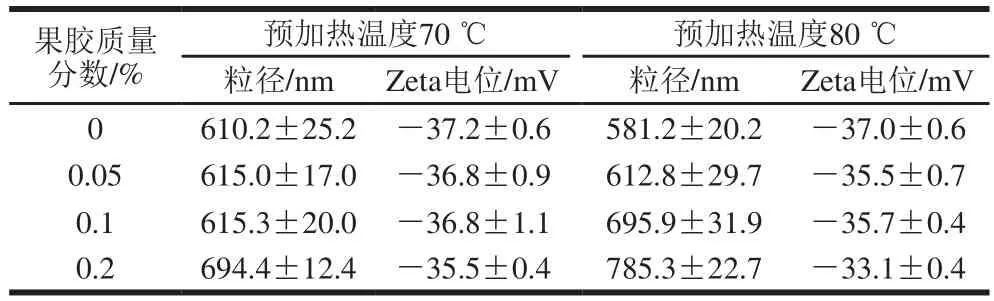
表1 果胶质量分数和预加热温度对乳液粒径和Zeta电位的影响Table 1 Effects of pectin concentration and preheating temperature on particle size and zeta potential of emulsions
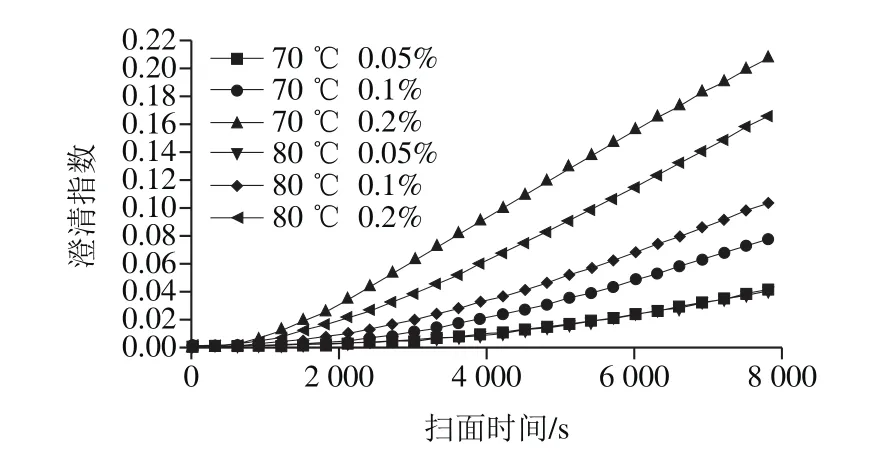
图1 果胶质量分数和预加热温度对乳液稳定性的影响Fig. 1 Effects of pectin concentration and preheating temperatures on the stability of emulsions
本实验应用LUMiSizer稳定性分析仪研究不同乳液的物理稳定性,实验时通过加速离心的方法快速测定乳液的油-水分层情况,并记录乳液各部位随时间的透光率变化(通过澄清指数表示),变化越慢则说明乳液的物理稳定性越好[18]。如图1所示,乳液体系澄清指数处于较低的水平(<0.25),表明乳液在贮藏过程中具有良好的乳析稳定性,不易出现分层现象。这一方面是由于体系较高的界面电势(|Zeta电位|≥30 mV),分散相液滴间存在较大的静电斥力;另一方面,果胶的存在使得体系黏度进一步增大,减少了液滴碰撞形成较大液滴的几率。但是果胶质量分数越高,澄清指数越高,说明蛋白质-果胶复合物的存在使得乳液体系稳定性有下降的趋势[19]。
2.2 果胶对蛋白质乳液凝胶性质的影响
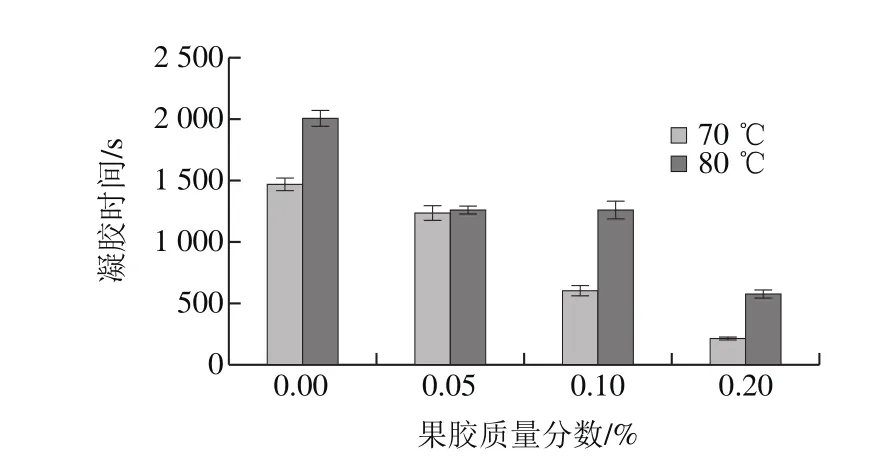
图2 果胶质量分数和预加热温度对乳液凝胶时间的影响Fig. 2 Effects of pectin concentration and preheating temperature on the gelation time of emulsions
加热过程中,蛋白质三级结构展开,更多的疏水基团暴露。添加GDL后,乳液体系pH值不断降低,蛋白质分子荷电量减弱,使得蛋白质分子互相交联形成聚合物并最终形成三维网状结构的凝胶[20-21]。但是,果胶的存在对凝胶过程及凝胶结构均产生重要影响。如图2所示,乳液体系中果胶质量分数越高,乳液凝胶时间越短。这可能由于果胶质量分数的增加使得体系黏度提高,可以加速凝胶网络结构的形成。通常条件下,高温处理可以促进蛋白质三级结构的展开,进而加速蛋白质凝胶的形成[22]。但是,高温处理过程中蛋白质与果胶形成共价复合物,疏水基团暴露量降低,减缓了蛋白质凝胶的形成。
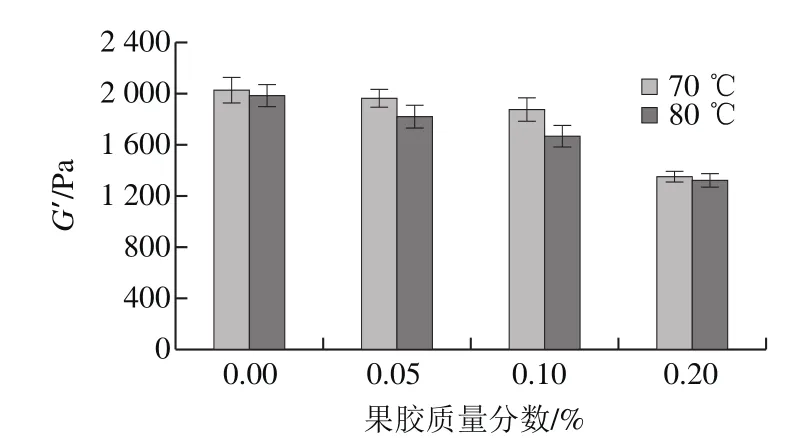
图3 果胶质量分数和预加热温度对乳液凝胶储能模量的影响Fig. 3 Effect of pectin concentration and preheating temperature on the storage modulus of emulsion gels
如图3所示,由于蛋白质-果胶复合物的形成,使得参与蛋白质凝胶形成的有效蛋白质含量降低。因此,果胶质量分数增加,乳液凝胶的强度(储能模量G’)呈减弱趋势。同时,因温度升高(80 ℃)而产生的更多暴露的疏水基团并未完全参与蛋白质交联,反而是由于复合物生成量增加导致最终凝胶强度较70 ℃处理体系呈变小的趋势,但差异不显著。众多研究表明,在中性pH值附近,微小的pH值变化都可能对乳清蛋白-果胶复合物结构及理化性质产生重要影响。在pH 7条件下,乳清蛋白-果胶复合物经85 ℃加热30 min后形成的凝胶(由GDL诱导)其强度高于乳清蛋白单独加热处理后添加果胶形成的凝胶。但是在pH 6.5和pH 6.2条件下,两类凝胶的强度无显著性差异[23-24]。

图4 果胶含量和预加热温度对乳状液胶硬度(A)和弹性(B)的影响Fig. 4 Effect of pectin concentration and preheating temperature on firmness (A) and springiness (B) of emulsions
如图4A所示,无论是果胶质量分数,还是蛋白质-果胶溶液加热温度,均未对凝胶的硬度产生显著性影响(P>0.05)。这可能是由于本研究中所形成的凝胶强度较低(G’<2 000 Pa),在质构仪分析条件下凝胶结构被迅速破坏,无法区分出不同组分和处理条件下的凝胶的硬度差异。如图4B所示,不同组分的乳液凝胶其弹性存在较大差异。一方面,经过80 ℃热处理的蛋白质-果胶复合溶液其最终形成的乳液凝胶弹性较70 ℃热处理后形成的乳液凝胶弹性更高;另一方面,凝胶弹性随果胶质量分数的增加出现先上升后下降的趋势。这些结果表明,蛋白质-果胶复合物对最终凝胶的弹性有重要影响。尽管果胶的存在使得凝胶强度降低,但可以使凝胶弹性增强。
2.3 蛋白质乳液凝胶中复合维生素稳定性测定
传递体系具有改善功能因子的水(或油)分散性,增强功能因子稳定性,提高生物利用率等优点,是功能配料与功能食品领域研究的一个重要方向。近20年来,科学家针对多种功能因子传递体系,如乳状液、脂质体、生物大分子颗粒,开展了较为系统的研究[25-29]。但是,现有的食品传递体系主要针对脂溶性功能因子,适用于水溶性功能因子的传递体系并未得到深入研究,能够同时包埋脂溶性和水溶性功能因子的传递体系则鲜有报道[4,30]。乳液凝胶同时包含适用于传递脂溶性功能因子的乳化油滴,又包含适用于传递水溶性功能因子的蛋白质凝胶,因此可以被用来同时传递不同极性食品功能因子。本研究中利用脂溶性的VE和水溶性的D-异抗坏血酸钠作为模式功能因子,分析乳液凝胶对复合维生素稳定性的影响规律。
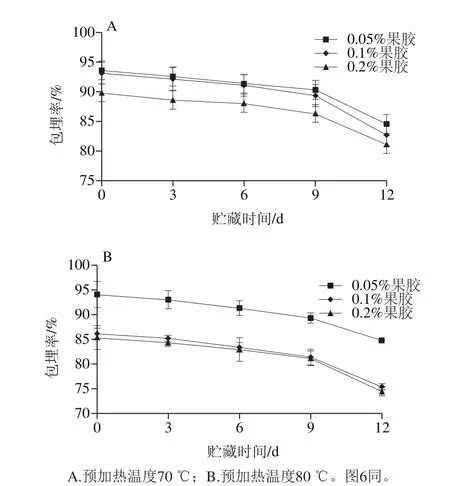
图5 果胶质量分数对贮藏过程VE稳定性的影响Fig. 5 Effect of pectin concentration on the stability of vitamin E in emulsion gels during storage
由图5可知,乳液凝胶中的VE含量在贮藏过程缓慢下降,其下降程度受体系组分的影响。首先,果胶质量分数越高的体系VE初始包埋率较低,降解速度也更快;其次,相比于经过70 ℃加热处理后形成的凝胶,经过80 ℃加热处理后形成的凝胶中VE初始包埋率和贮藏实验末期VE包埋率都较低。这是由于含有蛋白质-果胶复合物的凝胶强度较弱,对VE的保护作用较低,容易受外界环境影响而发生氧化降解。
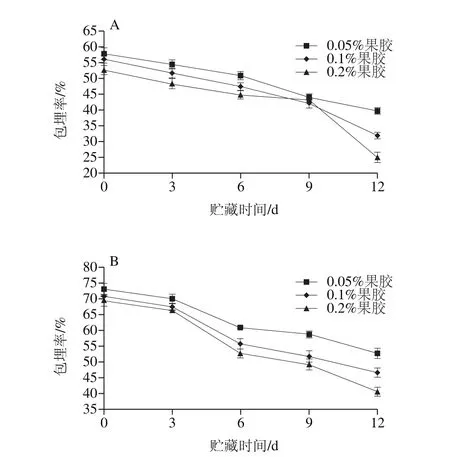
图6 果胶质量分数对贮藏过程D-异抗坏血酸钠稳定性的影响Fig. 6 Effect of pectin concentration on the stability of sodium erythorbate in emulsion gels during storage
如图6所示,乳液凝胶中的D-异抗坏血酸钠的降解规律与VE有一定的相似性,即果胶质量分数高的体系D-异抗坏血酸钠包埋率越低。但是,相比于VE,D-异抗坏血酸钠的降解速率更高。例如,在含有0.2%果胶的乳液凝胶(80 ℃处理条件下)中,经过12 d贮藏后,VE包埋率约从85%下降到75%,而D-异抗坏血酸钠的包埋率则从70%下降到40%。造成此差异的主要原因是:1)异抗坏血酸钠主要分布在水相,与外界环境直接基础,更容易受到光、热、氧的影响;2)含有果胶的乳液凝胶强度较弱,持水率低,在贮藏过程中出现较明显失水现象,导致部分D-异抗坏血酸钠随水分迁移到凝胶表面,失去凝胶的保护;3)D-异抗坏血酸钠作为抗氧化剂,在一定程度上保护了VE。
3 结 论
果胶与大豆分离蛋白在加热过程中形成复合物,进而影响蛋白质乳液凝胶的结构特性。果胶质量分数越高,凝胶中油滴粒径越大,凝胶时间越短,凝胶强度下降。此外,蛋白质-果胶的预加热温度也对凝胶结构产生影响。因此,通过改变果胶添加量和预加热温度可以有效调控乳液凝胶的结构特性。
蛋白质乳液凝胶可以作为复合维生素的传递体系,其稳定性受凝胶结构影响明显。含有果胶的凝胶强度较低,复合维生素稳定性随果胶含量增加而下降,D-异抗坏血酸钠降解速率显著高于VE,表明水相中D-异抗坏血酸钠作为抗氧化剂保护了油相中的VE。此外,复合维生素的稳定性变化可能还存在一定的协同机制,需要进一步研究。
