计算氢分子离子键能的一种新方法
2018-09-12高晓明
何 帅,高晓明
(1.延安大学西安创新学院,陕西 西安 710000;2.延安大学化学与化工学院, 陕西省化学反应工程重点实验室,陕西 延安 716000)
1 引言
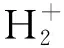
笔者受启发于热传导、可逆反应、渗透平衡等随时间变化最终达到动态平衡。例如气体在某一密闭容器内扩散随着时间变化密度保持不变;将蔗糖溶液加入水中稀释,随着时间的变化浓度保持不变;在孤立系统中,将等体积的一杯80℃的水和20℃的水均匀混合,最终水的温度为50℃,最终都达到一种动态平衡。提出了一种简单的氢分子离子成键模型,假定氢原子结合成氢分子,氢分子转变为氢分子离子后,其平均电势能密度是守恒的。得到了氢分子离子键能与结构之间的方程式,用一种新颖的宏观方法计算氢分子离子键能[7-9]。
2 氢分子离子成键模型
氢分子离子是用电子束轰击放电管中的氢气时得到的三质点体系,它的性质活泼,寿命很短,一旦与其他物质接触立即会被夺取电子而形成氢分子[1]。氢分子离子可以认为是氢原子偶然失去一个电子,整个体系的吸引作用突然减小,两核间的距离逐渐增大以减小其排斥作用,最终达到一种吸引和排斥平衡[5-6]。
笔者认为两个氢原子结合为氢分子的微观机理为:假定两个氢原子形成氢分子之后,氢分子的电势能与体积的比值和氢原子的电势能与体积的比值相等,氢分子的电势能与体积的比值和重叠部分电势能与体积的比值相等,也和未重叠部分电势能与体积的比值相等,之后氢分子失去一个电子转化为氢分子离子,仍然与氢分子离子的电势能和体积的比值相等。
当氢原子处于平衡态时,我们定义氢原子平均电势能密度与基态氢原子电势能成正比,与氢原子体积成反比。
用方程式可表示为:
(1)
式中:φ为平均电势能密度,Ep为氢原子势能,eV;V为氢原子体积,m3。使用标准国际单位制时,K=1。
由于氢原子总的电势能为:
(2)
式中,k为静电引力常数,k=8.99×109N·m2/C2;R0为氢原子半径;z为质子的电荷量,e为电子的电荷量,其值均为Q=1.60×10-19C;R0=0.529Å。
则氢原子平均电势能密度为:
(3)
根据假设,氢分子离子的平均电势能密度与氢原子电势能密度相等。依据这一假设,我们可以得到氢分子离子电势能与其结构之间的方程式。即:
(4)
式中,Ep1为氢分子离子的电势能,V1为氢分子离子的体积。氢分子离子的电子运行轨道为椭球,我们可以用椭球体积公式计算其体积。即:
(5)
式中,a和b是赤道半径,c是极半径。
很明显,这个方程式通过量子引力场很可能存在流体特性这一假定,可以将氢分子离子键能与其结构联系到一起。
接下来计算椭球的赤道半径和极半径。如图1所示,是某时刻氢分子离子的结构图。图中a为氢分子离子的半长轴,b为氢分子离子的半短轴。氢分子离子的轨道指数ζ=1.24,即有效核电荷数为1.24。假定氢分子转变为氢分子离子后仍然是静电引力提供向心力[5,10]。则氢分子半短轴可以用下面的方程式计算:
(6)
经计算,氢分子离子的半短轴和半长轴分别为:
b=c=0.589Å

3 氢分子离子键能计算
根据假定:氢分子的平均电势能密度与氢分子离子平均电势能密度相等,根据这一原理可以计算氢分子离子的键能。
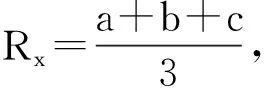
(7)
将(3)、(4)、(5)式与(7)式联立 :
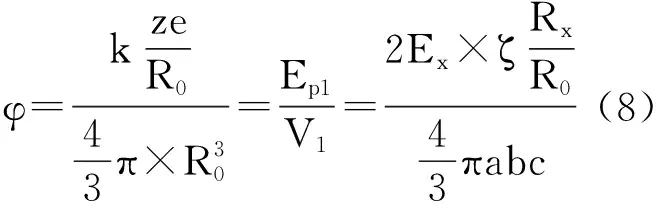
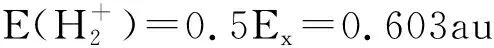
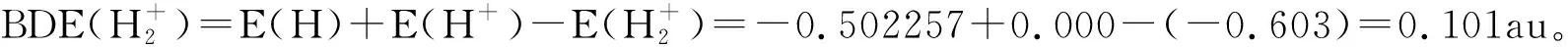
即氢分子离子键能为0.101au。
实验值为De=0.102 375 331 au,相对误差为1.5%,理论值与实验值较好的吻合。
4 讨论
目前认为经典力学不能解决原子的激发态、光谱、各种轨道(s、p、d、f)的差异、轨道杂化、π键与共轭键等物质结构中的各种问题。笔者提出静电场很可能有流体特性这一假设,以此为基础,建立氢分子离子成键模型。假定氢分子离子键能和结构之间存在联系,即氢原子结合成氢分子,氢分子转变为氢分子离子后,其平均电势能密度是守恒的。得到了氢分子离子键能与结构之间的方程式,用一种新颖的宏观方法计算氢分子离子键能De=0.101au,所得的理论计算值与实验值较好的吻合,并且计算过程较为简单。这表明,对于简单分子的键能完全可以用经典力学较好的解决。

图1 氢分子离子结构图
