奥希替尼治疗非小细胞肺癌的成本效果研究
2018-06-23官海静刘国恩盛亚楠王雅楠李洪超
官海静 刘国恩 盛亚楠 王雅楠 李洪超
(1北京大学药学院 北京 100191;2北京大学中国卫生经济研究中心 北京 100080;3北京大学国家发展研究院北京100080;4中国药科大学国际医药商学院 南京 211198)
1 背景
2015年我国约有73.3万例新发肺癌病例,占全部新发癌症病例的17.1%;肺癌死亡病例达到61.0万例,占癌症死亡总数的21.7%[1]。肺癌已成为我国死亡率最高的恶性肿瘤。肺癌中约75%为非小细胞肺癌(nonsmall-cell lung cancer,NSCLC),EGFR(epidermal growth factor receptor)基因突变是NSCLC基因突变患者最常见的类型。对于这部分患者,使用表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKIs)是标准一线治疗方案,如吉非替尼、厄洛替尼、埃克替尼等。但是,一线EGFR-TKIs治疗9-13个月之后,肿瘤会发生进展。在进展患者中,约60%来自T790M突变而导致耐药[2]。因此,NSCLC临床实践指南推荐既往EGFR-TKIs治疗失败后首先进行T790M检测,阳性患者可使用甲磺酸奥希替尼片(以下简称奥希替尼),阴性患者则选择含铂双药化疗[3]。
奥希替尼是一种口服、不可逆、对中枢神经系统有效,同时对EGFR敏感突变和EGFR T790M耐药突变具有高选择性的药物。关于奥希替尼的有效性和安全性:利用两项二期单臂临床研究(NCT01802632和NCT02094261)数据的一项汇总分析发现(N=411),奥希替尼的客观反应率为66%,中位无进展生存期为11.0月;一项奥希替尼和含铂双药化疗的头对头三期临床研究(NCT02151981,N=419),结果显示奥希替尼的中位无进展生存时间显著长于含铂双药化疗(10.1月 vs 4.4月),客观反应率也显著高于对照组(71% vs 31%)[2]。
目前有两项关于奥希替尼成本效果的研究:Bertranou(2017)对英国患者的研究显示,奥希替尼相比含铂双药化疗的增量成本效果比(incremental cost-effectiveness ratio,ICER)是41705英镑/QALY,在支付意愿为50000英镑时具有成本效果的概率为63.4%[4]。吴斌对中国和美国患者的研究显示,奥希替尼相比含铂双药化疗的ICER分别为48081美元/QALY和232895美元/QALY,超过了社会平均意愿支付阈值[5]。两项研究得到了不同结论,这和模型结构、参数来源和各国的卫生服务体系有关。随着奥希替尼有了新的临床证据以及美国NCCN指南的更新,药物经济学评价也需要随之更新,尤其是基于多来源参数的模型法,更需要基于不同模型设定和参数来源探讨结果的稳健性。因此,本研究的目的是评价奥希替尼相比含铂双药化疗治疗中国NSCLC患者的成本效果,根据最新临床指南的建议,搭建模型和形成评价方案,采用最新的临床效果数据,并将评价方法和结果与现有研究进行比较分析,进一步探讨奥希替尼的成本效果,为国家医保目录动态调整和专利药谈判提供参考。
2 方法
2.1 目标人群
模型中的目标人群是既往经EGFR-TKIs治疗时或治疗后出现疾病进展或治疗失败的局部晚期或转移性NSCLC患者。根据是否清楚EGFR T790M的突变情况,分为两种情境:情境一,对于T790M阳性患者,试验组使用奥希替尼,对照组使用含铂双药化疗;情境二,对于进展后尚未进行基因检测T790M突变情况的所有患者,试验组首先进行组织活检,阳性患者使用奥希替尼,阴性患者使用含铂双药化疗,对照组不接受基因检测直接使用含铂双药化疗。
2.2 模型结构
本研究基于卫生服务体系的角度,通过构建动态Markov模型,对奥希替尼和含铂双药化疗这两种治疗方案的临床和经济产出进行分析。Markov模型结构包括三种状态:无进展、进展、死亡。患者入组时均在无进展状态,即NSCLC的IIIB/IV期。在每个周期的模拟中,患者将存在于某一状态中,并接受相关药物治疗。根据临床研究和肺癌化疗方案,将模型的循环周期设为3周。为了充分呈现两种治疗方案的获益,研究时限设为终身,即当模拟队列中活着的人小于1%时,模型停止模拟。两种方案的治疗路径参照2018年美国NCCN指南和2016版中国原发性肺癌诊疗指南的建议。对照组无进展状态使用培美曲塞联合顺铂双药化疗,最多4个周期,若仍无进展,则使用培美曲塞维持治疗直至进展;进展后,26%的患者[6]使用多西他赛继续化疗,余下患者进入最佳支持治疗。随后是终末期姑息治疗,直至死亡。奥希替尼可能改变NSCLC二线治疗方案的临床路径,即延后现有的标准临床路径。试验组无进展状态使用奥希替尼直至疾病进展,进展后26%的患者使用含铂双药或多西他赛单药继续化疗,余下患者进入最佳支持治疗。其后的路径与对照组一致,为终末期姑息治疗,直至死亡。
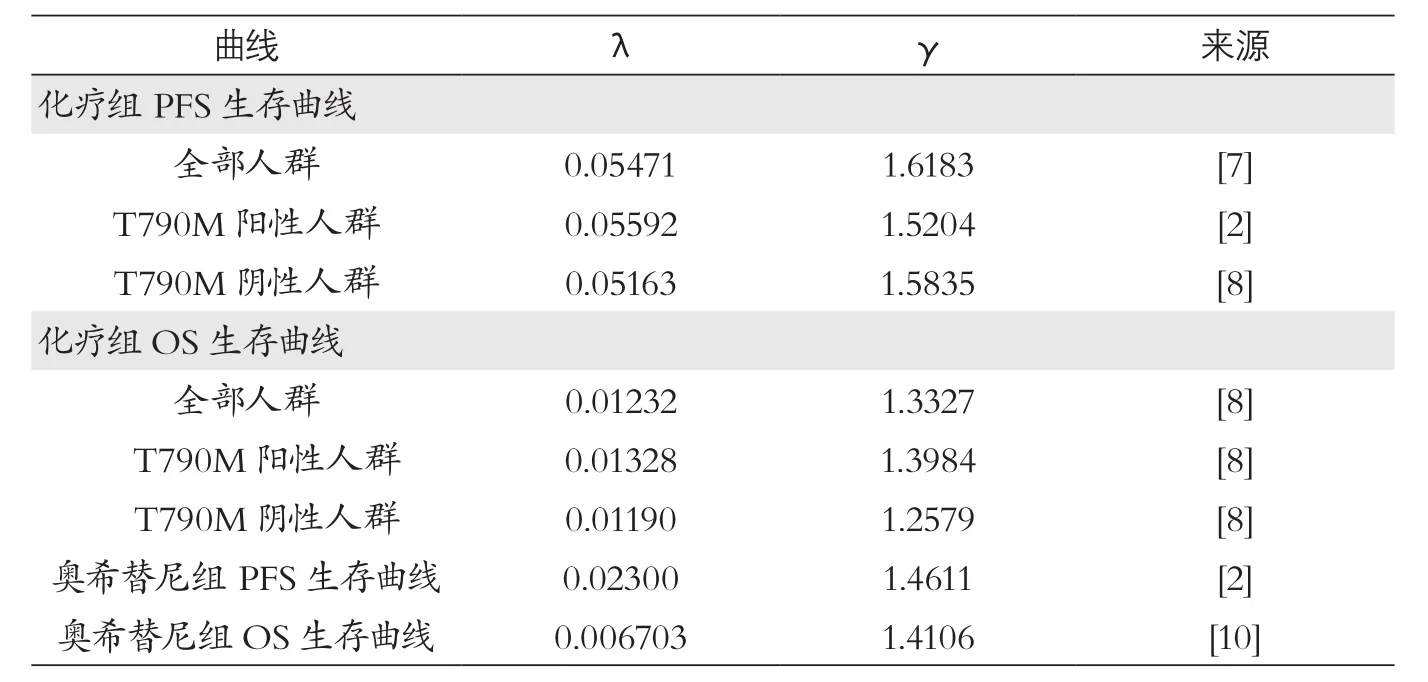
表1 生存曲线参数表
2.3 临床数据
两种治疗方案的临床疗效数据来源于一系列已发表的临床研究。由于本研究基于不同人群考虑了两种不同的用药情境,因而不同情境的参数来源不同。情境一中,试验组和对照组的无进展生存期(Progression Free Survival,PFS)的K-M曲线均来自AURA3研究[2]。AURA3是一项随机、国际多中心、开放的三期临床研究,是第一项奥希替尼和含铂双药化疗治疗T790M阳性NSCLC患者的头对头研究,两组样本量分别为279人、140人。研究结果显示奥希替尼的中位PFS显著长于含铂双药化疗[2]。情境二中,试验组根据基因检测结果分别使用奥希替尼和含铂双药化疗,对于阳性人群使用奥希替尼的PFS曲线仍然来源于AURA3[2],对于阴性人群则来源于IMPRESS研究[8]。IMPRESS研究是一项关于培美曲塞和顺铂联用吉非替尼,与培美曲塞和顺铂联用安慰剂相比的随机对照研究,目标人群是局部晚期或转移性NSCLC的二线患者[7,8]。对于试验组中的T790M阴性患者,使用IMPRRESS研究中T790M阴性患者的PFS数据[8]。情境二中的对照组使用该研究中所有目标人群(包括阴性和阳性人群)的PFS数据[7]。
由于奥希替尼和含铂双药化疗头对头临床研究的总生存期(Overall Survival,OS)尚未发表,因此两组OS数据来自不同研究。目前关于奥希替尼OS数据均来自AURA扩展和AURA2两个II期临床研究的汇总数据,用于评价奥希替尼的有效性和安全性。但是,由于数据截取时间不同,目前关于奥希替尼OS的估计并不一致:根据Bertranou(2017)研究,截至2015年11月,仅有24%患者死亡,其中位OS预测值为40.2月[9];根据Mitsudomi(2017)研究,截至2016年11月数据,有46%患者死亡,其调整后的中位OS值为26.8月[10]。这两项研究关于OS的数据都不成熟,但后者根据临床试验的最新进展调低了中位OS值,对OS进行了更准确的估计。因此,本研究使用Mitsudomi研究中关于OS的数据。含铂双药化疗的OS K-M曲线依据不同基因型选择相应的IMPRESS研究中的OS曲线[8]。
模型中,无进展状态到死亡的概率假设为自然死亡率。EGFR T790M在人群的突变率为66%[11]。根据Guyot P(2012)的方法重新构建各条K-M曲线的个体水平数据,并利用生存分析进行拟合[12]。奥希替尼组无法获得OS K-M曲线,因而根据Mitsudomi(2017)时间点及对应生存率,推算其生存函数[10]。基于现有文献,由于Weibull分布对生存数据能进行更好的拟合,因此利用其对K-M曲线进行拟合和外推,估计患者终生每个时点t的无进展概率和生存概率。基于Weibull分布,在t时间的生存概率S(t)=exp(-λtγ),在模型周期为t时的转移概率P(t)=1-exp[λ(t-1)γ-λtγ]。见表1。
2.4 成本和效用值
由于本研究基于卫生服务体系的角度,因此只考虑直接医疗成本。模型中的直接医疗成本包括:T790M的基因检测费用(采用组织活检的方式)、奥希替尼和化疗方案的药品费用、支持治疗费用、随访费用(包括医生访视、其他检查及药物费用)、严重不良事件治疗费用、终末期姑息治疗费用。
奥希替尼采用中国公立医院的零售价,推荐剂量为每日80 mg,直至疾病进展或出现无法耐受的毒性。培美曲塞和顺铂价格为全国各省份药品中标价格平均值。培美曲塞(500mg/m2,d1,q21)联合顺铂(75mg/m2,d1)双药化疗、培美曲塞维持治疗的费用通过用法用量计算得到。为了预防和减缓皮肤反应和细胞毒性,地塞米松、叶酸和维生素B12均按照临床研究设计,与化疗药物共同使用[2],其费用来源于全国各省份药品中标价格平均值。多西他赛单药化疗方案、随访费用、终末期姑息治疗费用、严重不良事件相关的管理费用等均来自现有文献[13-18]。奥希替尼和含铂双药化疗的不良反应发生率来自AURA3研究[2]和IMPRESS研究[7]。
为了提高我国NSCLC患者对靶向药物的可及性,中国慈善总会对靶向药物通常制定相应的慈善援助方案(Patient Assistance Program, PAP)。针对奥希替尼的援助模式也已经颁布:对于非低保人群而言,全额自费连续服药满4个月,经项目审批后第一阶段最多可以获得8个月的援助药品,第一阶段援助结束。患者一期退出项目后,如经项目医生评估,患者仍可从药品治疗中获益,患者全额自费连续服药满3个月后申请再次入组,项目再次审批后,第二阶段可以获得药品援助直至病情进展。本研究PAP情景下的奥希替尼费用根据该援助方案分别在不同阶段设置不同的数值。两种方案在无进展状态的效用值来自Bertranou E (2017) 的研究,奥希替尼组和含铂双药化疗组分别是0.805、0.778,该效用值已经考虑了两组不良事件的影响;两组在进展状态的效用值均为0.715[9]。
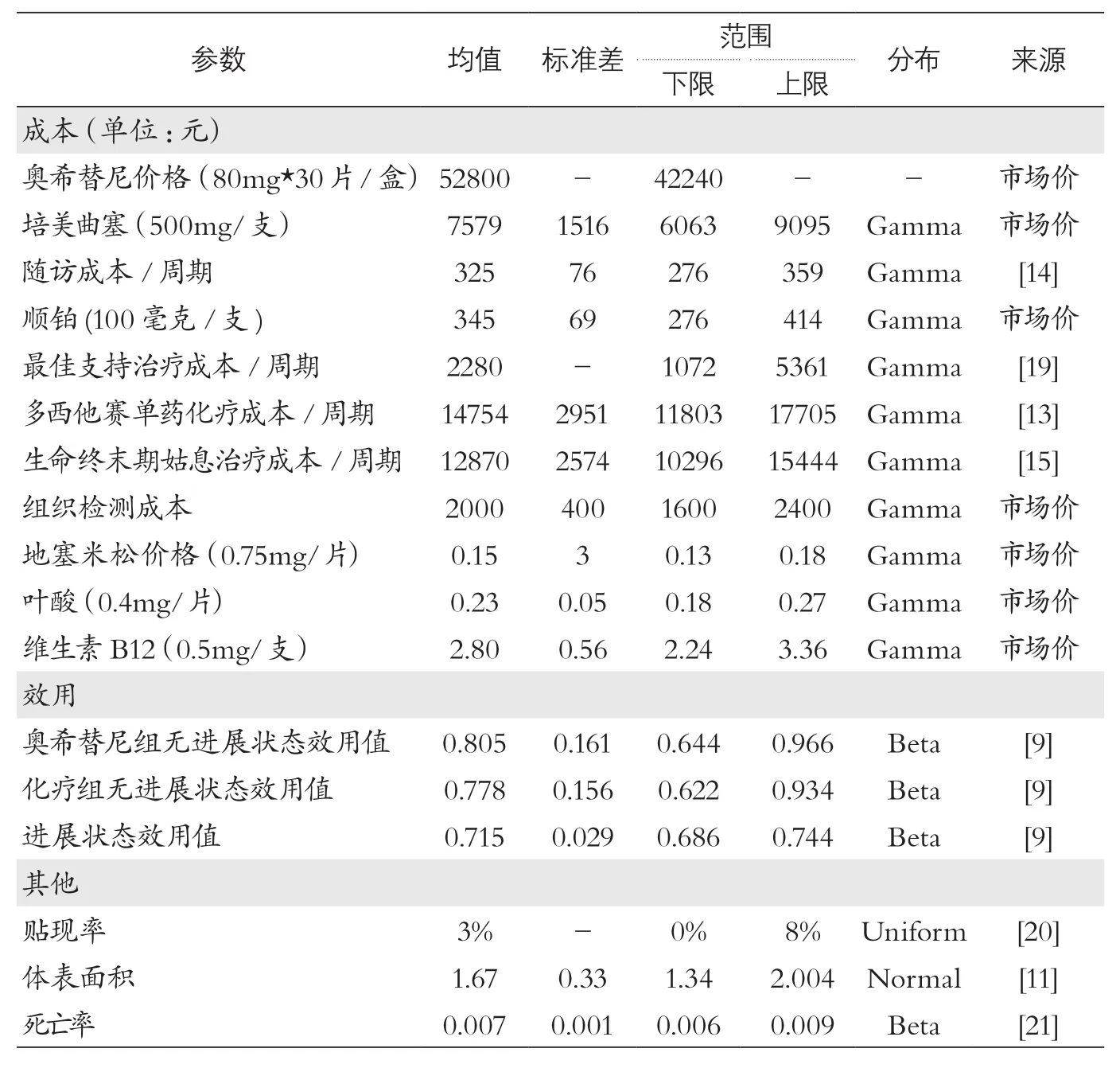
表2 模型输入参数和分布
2.5 基础分析和敏感性分析
在两种情境下分别计算了考虑援助方案和不考虑援助方案的结果。模型主要产出指标包括两种治疗方案的生命年、质量调整生命年、直接医疗费用。通过计算ICER,将其与意愿支付值比较,进行成本效果分析。根据WHO三倍人均GDP的判断标准,本研究将2017年中国3倍人均GDP(17.90万元)作为阈值[21]。考虑到中国各地经济发展差异明显,本研究还探讨了在不同地区阈值下奥希替尼具有的成本效果比较优势的概率。
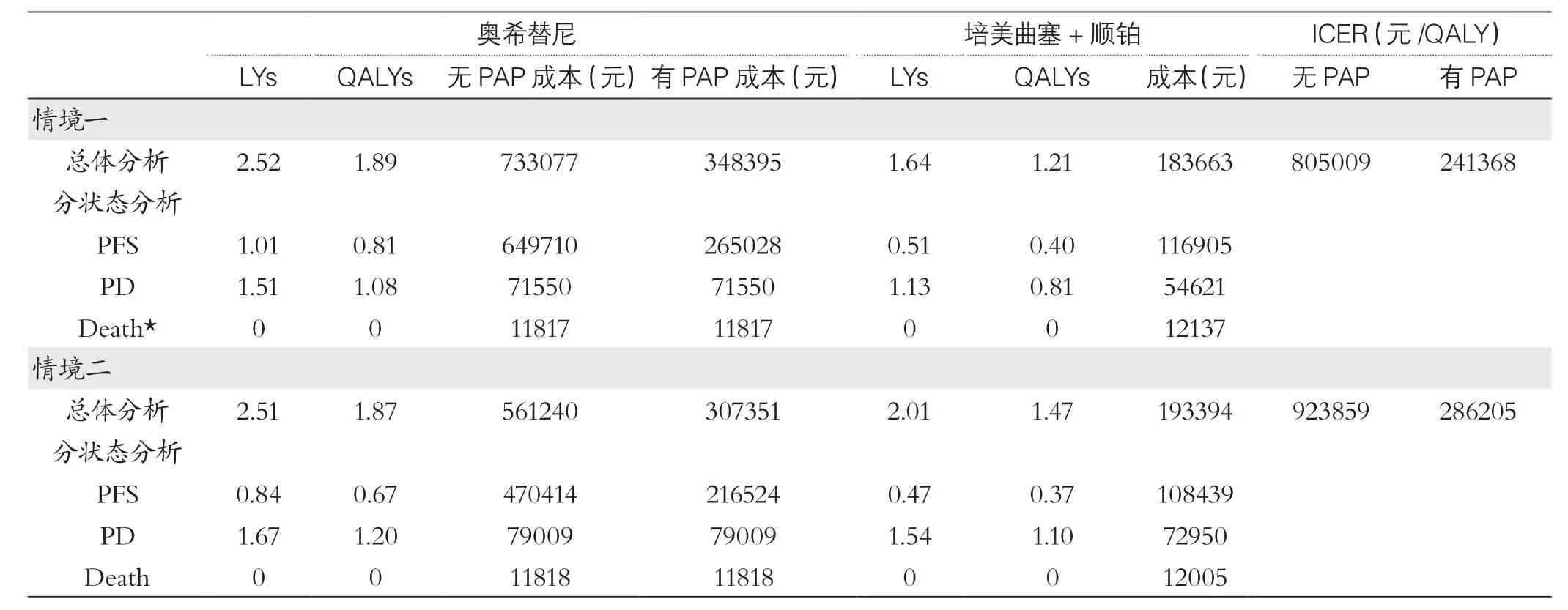
表3 基础分析结果
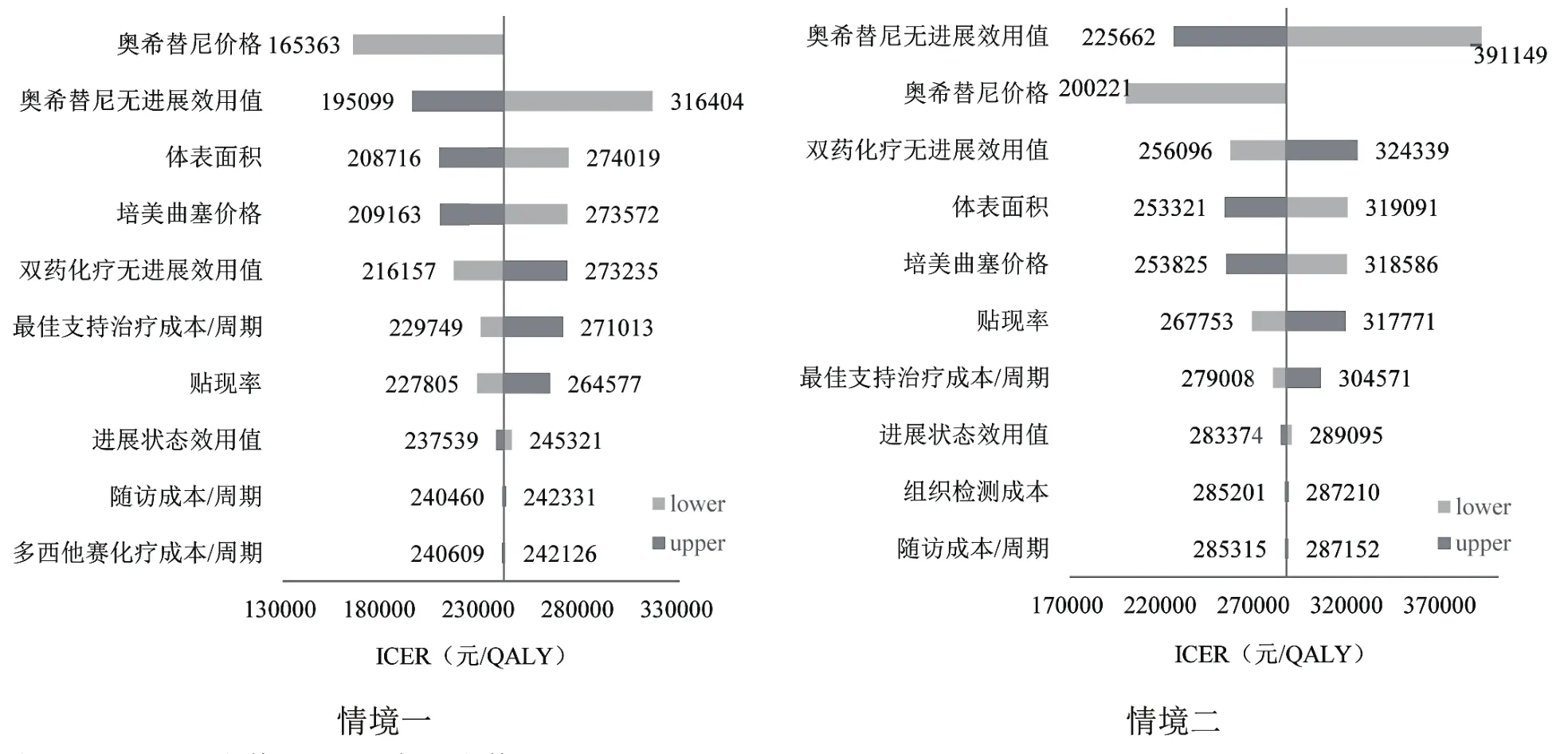
图1 单因素敏感性分析旋风图
通过单因素敏感性分析,分析每个参数的变化对结果的影响,并用旋风图呈现结果。参数在无法获得取值范围时,以±20%为变动范围,各参数变化的最小值和最大值见表2。此外,采用二价蒙特卡洛模拟(second order Monte Carlo simulation)进行敏感性分析。基于各个参数不同的分布假设,重复抽样1000次,计算两种治疗方案基于每次抽样的ICER值,并以散点图的形式呈现在成本效果象限中。概率敏感性分析的结果通过成本效果可接受曲线呈现。
3 结果
3.1 基础分析
由表3的基础分析结果可知:在情境一中,奥希替尼组的生命年(Life Years,LYs)(2.52年)比含铂双药化疗组(1.64年)高0.88年,质量调整生命年(1.89QALYs)比含铂双药化疗组(1.21QALYs)高0.68 QALYs。其中,两组在无进展状态的质量调整生命年之差为0.41QALYs,在进展状态之差为0.27QALYs。不考虑援助方案时,奥希替尼组的终身医疗费用为73.3万元,比化疗组高54.9万元;考虑援助方案时,奥希替尼组的终身医疗费用为34.8万元,比化疗组高16.5万元。两种情况下ICER值分别为80.5万/QALY和24.1/QALY。
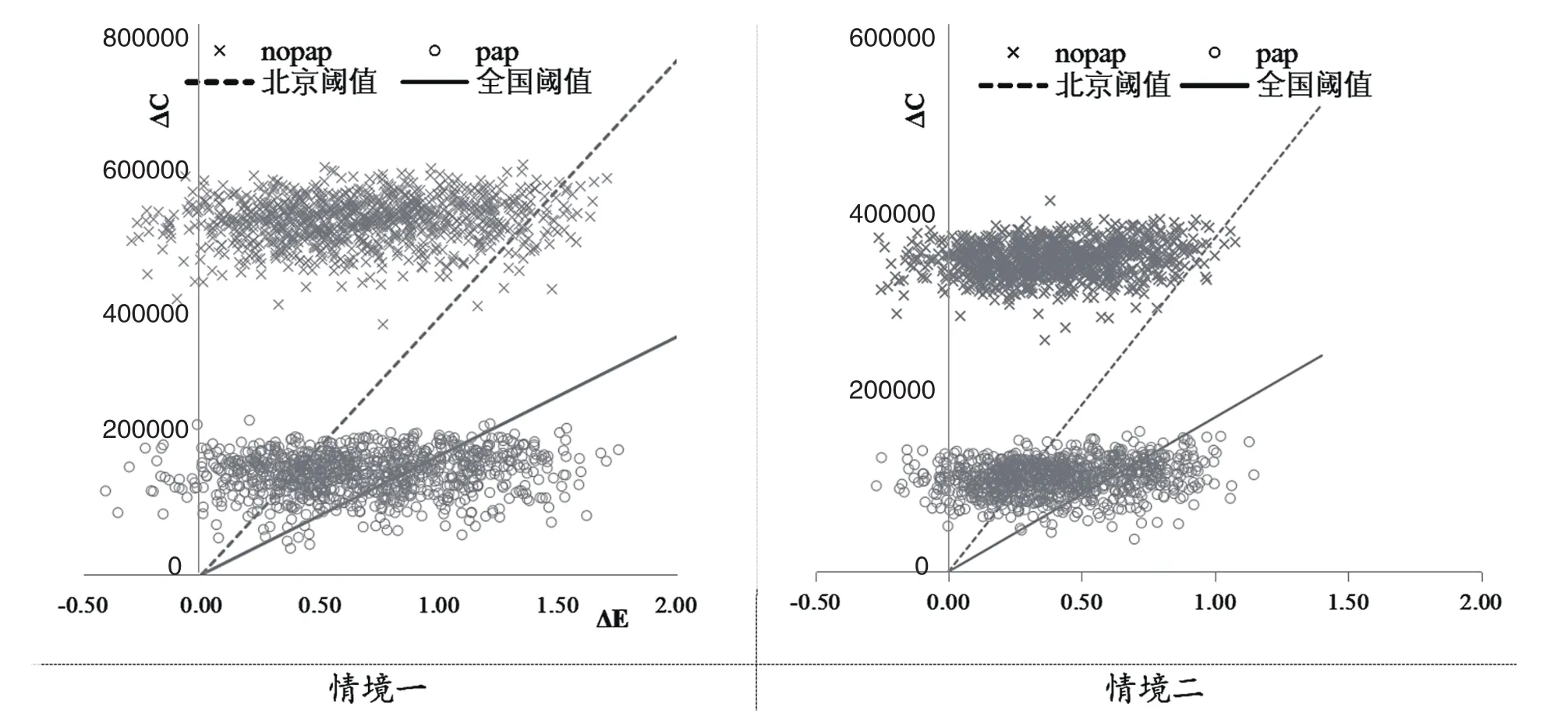
图2 蒙特卡洛散点图
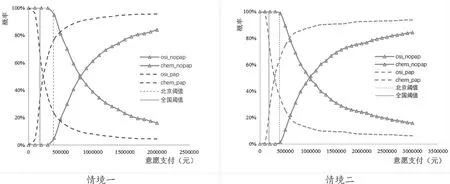
图3 成本效果可接受曲线
在情境二中,奥希替尼组的LYs(2.51年)比含铂双药化疗组(2.01年)高0.50年,质量调整生命年(1.87 QALYs)比含铂双药化疗组(1.47 QALYs)高0.40QALYs。其中,两组在无进展状态的质量调整生命年之差为0.30QALYs,在进展状态之差为0.10QALYs。不考虑援助方案时,奥希替尼组的终身医疗费用为56.1万元,比化疗组高36.8万元;考虑援助方案时,奥希替尼组的终身医疗费用为30.7元,比化疗组高11.4万元。此时,两种情况下ICER值分别为92.4万元/QALY和28.6万元/QALY。
两种情境下赠药和不赠药的ICER值均高于2017年中国3倍人均GDP阈值(17.90万元),但赠药情况下两种情境的ICER值均低于2017年北京、天津、上海、江苏地区的三倍人均GDP。
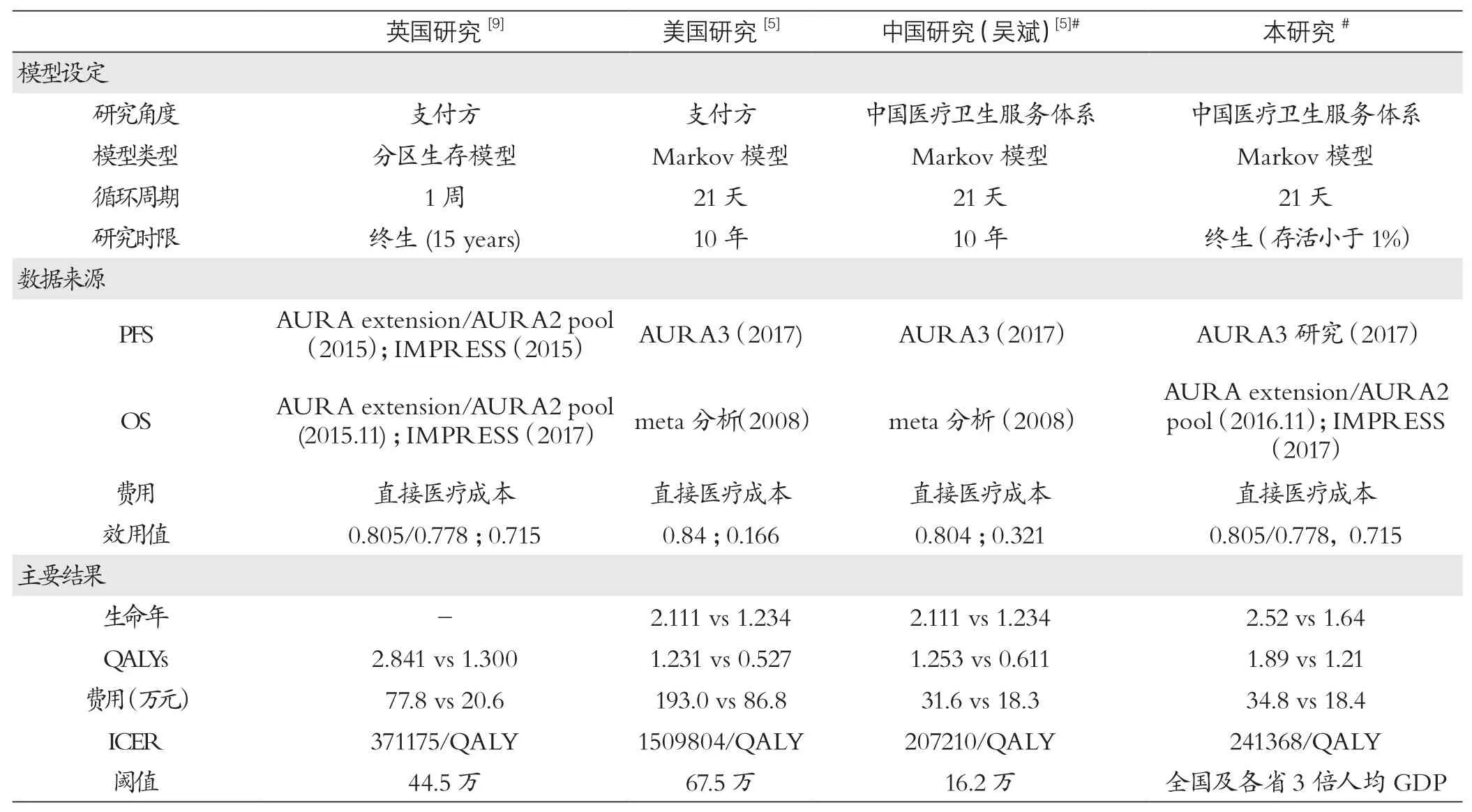
表4 现有关于奥希替尼成本效果研究的比较①②
3.2 敏感性分析
对于赠药情况的单因素敏感性分析发现,情境一中奥希替尼价格、奥希替尼无进展状态生命质量、体表面积是对结果影响的主要因素。情境二中奥希替尼无进展状态生命质量、奥希替尼价格、含铂双药无进展状态生命质量是主要影响因素。单因素敏感性分析的旋风图见图1。由于篇幅限制,在此未呈现非赠药情况的旋风图。
概率敏感性分析如图2。情境一中,考虑慈善赠药时,分别有33.1%和75.9%的散点在全国和北京的意愿支付曲线之下,说明根据全国或北京阈值,奥希替尼具有成本效果的概率分别为33.1%和75.9%。情境二中,考虑慈善赠药时,分别有22.6%、64.2%散点低于全国和北京的意愿支付曲线,说明奥希替尼具有成本效果的概率分别为22.6%和64.2%。
图3成本效果可支付曲线显示,社会平均支付意愿越高,奥希替尼具有成本效果的概率也会更高。情境一中不考虑援助方案时,当支付意愿为85万元时,奥希替尼治疗方案的具有成本效果的概率高于化疗方案;考虑援助方案时,若支付意愿为25万元,奥希替尼方案具有成本效果的概率高于化疗方案。情境二中不考虑援助方案时,支付意愿为100万元时,奥希替尼治疗方案的具有成本效果的概率高于化疗方案;考虑援助方案时,若支付意愿为30万元,奥希替尼方案具有成本效果的概率高于化疗方案。
4 讨论
本研究基于现有多项临床研究中的最新数据,采用动态Markov模型,对奥希替尼和含铂双药化疗治疗中国NSCLC患者的成本效果进行了分析。情境一中,奥希替尼组患者的生命年比含铂双药化疗组患者提高0.88年,质量调整生命年提高0.68 QALYs,不赠药和赠药情况下终身费用分别高54.9万元和16.5万元,其ICER值分别为80.5万元/QALY和24.1万元/QALY。情境二中,奥希替尼组患者的生命年比含铂双药化疗组患者提高0.50年,质量调整生命年提高0.40QALYs,不赠药和赠药情况下的终身费用分别高36.8万元和11.4万元,其ICER值分别为92.4万元/QALY和28.6万元/QALY。研究发现,奥希替尼能延长NSCLC患者的生命年,提高生命质量,同时也增加医疗费用。根据WHO三倍人均GDP的判断标准,在赠药前提下,对于人均GDP达到9.6万元以上的中国经济发达地区,使用奥希替尼具有成本效果的比较优势。
目前已有2篇关于奥希替尼对照培美曲塞联合顺铂化疗的经济性研究,分别为英国、美国及中国环境下的评估[5,9]。各个研究在角度、模型和数据来源方面存在差异,因而结果也存在不同。Bertranou对英国NSCLC患者使用奥希替尼的成本效果研究采用分区生存模型,本研究及其他两个均采用Markov模型。英国的研究中试验组的PFS和OS均来自于AURA扩展和AURA2的混合分析,对照组PFS和OS来源于IMPRESS研究。随着关于奥希替尼和双药化疗头对头临床研究的开展,因而吴斌以及本研究均使用了最新的AURA3的PFS数据。但关于奥希替尼的OS数据目前均尚未成熟,英国的研究中OS数据截至2015年11月,有24%患者死亡,本研究OS数据截至2016年11月,有46%患者死亡。吴斌则未考虑奥希替尼对OS数据的影响,选择了进展状态的OS数据,该OS数据为一系列化疗方案的综合结果[22]。英国研究中效用值来源于与临床试验同步的效用值测量,吴斌研究中,美国和中国的效用值来源于一项国际性的NSCLC患者效用值测量结果,但由于该研究样本人群为NSCLC一线用药人群[23],本研究则至少为二线用药,因而本研究最终选择与临床试验同步的效用值测量结果。在结果方面,由于本研究与英国对照组数据均来源于IMPRESS研究,因而对照组效用值较为接近(1.30QALYs,1.21QALYs),但试验组由于OS数据截至日期不同效用值相差较大(2.841QALYs vs 1.89QALYs)。吴斌研究由于效用值的选取、OS数据的选取与本研究存在较大差异,因而结果也不尽相同。目前这三项研究均从不同方面展现了奥希替尼的成本效果,为决策者提供更全面的信息和参考,其他相关比较情况详见表4。
关于晚期癌症的药物进行药物经济学评价时,对阈值的探讨很重要。生命末期患者的时间价值不同于整个生命周期其他阶段的价值,当死亡临近时,时间的价值随之增加,对全社会而言也是如此[24]。英国NICE针对生命终末期患者制定了特别政策,如果满足相关条件,药物进行卫生技术评估时可以超过3万英镑的意愿支付阈值。在2009-2011年间通过该特别政策批准的8个药物中,意愿支付阈值提高了6%-79%,其中,两个治疗非小细胞肺癌的药品托帕替康、培美曲塞分别的阈值分别提高了13%、57%[25]。美国常用5万-10万美元作为通用意愿支付阈值,但是,对于癌症药品的判断阈值也可能提高:一项研究将治疗卵巢癌的贝伐单抗的意愿支付阈值提升到20万美元[26],还有研究对肿瘤科专家的意愿支付阈值进行了调查,发现30万美元是一个平均可接受值[27]。由此可见,对于生命终末期患者的治疗药物,是否应当提高社会平均支付意愿,以及提高的程度,都有待进一步探讨和形成共识。
为了进一步提高患者对药物的可及性,中国医保部门将对医保目录进行动态调整,其中对于具有创新性的靶向药物将通过国家谈判,判断是否报销,以及确定支付标准。通过医保和药企的平等谈判协商,制定一个相对合理的支付标准。2017年首次医保谈判纳入目录的36种药物的价格平均降幅约44%,这大大减轻了中国患者的医疗费用负担,提高了药物可及性;同时,也充分体现了创新药物的临床价值和经济价值。本研究中,有援助方案下两种情境的ICER值分别为24.1万元/QALY和28.6万元/QALY,高于2017年中国3倍人均GDP,但低于北京、天津、上海、江苏等省市的3倍人均GDP。随着社会经济的发展和人均GDP的提高,这些地区会越来越多。因此,结合中国经济发展水平和社会平均支付意愿,探索奥希替尼的合理医保支付标准,将有助于进一步提高靶向药的可及性和依从性,延长肺癌患者存活时间,提高生命质量,同时保证医保基金可承受。
本研究也存在一些局限,主要体现在:第一,模型中使用的临床研究,目标人群不单纯是中国NSCLC患者。目前,仅有AURA17(NCT02442349)这一II期临床研究的目标人群为亚太患者,由于其是一个奥希替尼的单臂研究,并且中位PFS和AURA3比较接近(9.7mon vs 10.1mon),因此本研究未采用AURA17研究的数据。尽管效果数据不来源于本国患者是被《中国药物经济学评价指南》允许的,但是,缺乏中国NSCLC患者使用奥希替尼和含铂双药化疗的头对头临床研究证据,增加了研究的不确定性。第二,无进展状态和进展状态的效用值也不是源于中国NSCLC患者。单因素敏感性分析显示,奥希替尼组在无进展状态的效用值在两种情境中均是主要的影响因素,化疗组在无进展状态的效用值也位于前五。对于中国肺癌患者特定治疗方案的效用值仍未检索到公开发表的文献,仅有的中国肺癌患者的效用值测量结果也主要针对一线用药人群[23]。第三,由于目前没有一条关于奥希替尼的完整、成熟的OS曲线,只能基于现有最新临床数据进行模拟和外推。本研究和英国研究奥希替尼OS K-M曲线的截取时间间隔了1年,死亡人数由24%增加到46%,拟合的中位OS相差了13.2个月。尽管本研究比英国研究作出了更加保守的估计,并且在概率敏感性分析中探讨了奥希替尼OS曲线不确定性对分析结果的影响,在该数据完全成熟之际,用以验证本研究的结果将是非常必要的。第四,奥希替尼的使用,很可能将改变现有NSCLC的IIIB/IV期患者二线用药的临床路径,即将现有的标准路径含铂双药化疗和单药化疗整体后移。但是,奥希替尼对后续治疗方案的用药选择以及疾病病程会产生影响,尚无临床研究或真实世界证据。因此,需要进一步开展奥希替尼基于真实世界的研究,探讨奥希替尼对临床路径、对效果和费用的影响,为卫生和医保决策者提供更加全面的证据。
[1]Chen W, Zheng R, Baade P D, et al. Cancer statistics in China, 2015[J]. CA: a cancer journal for clinicians, 2016, 66(2): 115-132.
[2]Mok T S, Wu Y L, M-J A, et al. Osimertinib or Platinum-Pemetrexed in EGFR T790MPositive Lung Cancer[J]. New England Journal of Medicine, 2017, 376(7):629.
[3]NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines), Nonsmall Cell Lung Cancer, Version 2. 2018
[4]NICE. Osimertinib for treating locally advanced or metastatic EGFR T790M mutationpositive non-small-cell lung cancer[EB/OL].2016[2016.10.26]. https://www.nice.org.uk/guidance/ta416/chapter/4-Committee-discussion
[5]Wu B, Gu X, Zhang Q. Cost-effectiveness of osimertinib for EGFR-mutation-positive nonsmall-cell lung cancer after progression of firstline EGFR TKI therapy[J]. Journal of Thoracic Oncology Official Publication of the International Association for the Study of Lung Cancer, 2017.
[6]Jr M J, Koeller J. Chemotherapy given near the end of life by community oncologists for advanced non-small cell lung cancer[J]. Oncologist, 2006,11(10):1095.
[7]Soria J C, Wu Y L, Nakagawa K, et al.Gefitinib plus chemotherapy versus placebo plus chemotherapy in EGFR-mutation-positive nonsmall-cell lung cancer after progression on firstline gefitinib (IMPRESS): a phase 3 randomised trial.[J]. Lancet Oncology, 2015, 16(8):990.
[8]Mok T, Kim S W, Wu Y L, et al. Gefitinib Plus Chemotherapy Versus Chemotherapy in Epidermal Growth Factor Receptor Mutation-Positive Non-Small-Cell Lung Cancer Resistant to First-Line Gefitinib (IMPRESS):Overall Survival and Biomarker Analyses.[J].Journal of Clinical Oncology Official Journal of the American Society of Clinical Oncology,2017:JCO2017739250.
[9]Bertranou E, Bodnar C, Dansk V, et al. Costeffectiveness of osimertinib in the UK for advanced EGFR-T790M non-small cell lung cancer[J].Journal of Medical Economics, 2017:1.
[10]T. Mitsudomi, M-J. Ahn, et al. Overall survival (OS) in patients (pts) with EGFR T790M-positive advanced non-small cell lung cancer (NSCLC) treated with osimertinib: Results from two phase II studies[J], Annals of Oncology,2017, 28:482
[11]Wu Y L, Tong R Z, Zhang Y, et al.Conventional real-time PCR-based detection of T790M using tumor tissue or blood in patients with EGFR TKI-resistant NSCLC[J]. Oncotargets& Therapy, 2017, 10:3307-3312.
[12]Guyot P, Ades A E, Ouwens M J, et al.Enhanced secondary analysis of survival data:reconstructing the data from published Kaplan-Meier survival curves.[J]. Bmc Medical Research Methodology, 2012, 12(1):9.
[13]Li X, Wang Y, Yan W, et al. Supportive Care Costs Associated with Second-Line Chemotherapy in Chinese Patients with Advanced Non-Squamous Non-Small Cell Lung Cancer:A Retrospective Cohort Study[J]. Drugs - Real World Outcomes, 2015, 2(1):87-97.
[14]Wu B, Ye M, Chen H, et al. Costs of Trastuzumab in Combination With Chemotherapy for HER2-Positive Advanced Gastric or Gastroesophageal Junction Cancer: An Economic Evaluation in the Chinese Context[J].Clinical Therapeutics, 2012, 34(2):468-479.
[15]曹海涛, 王俊琪, 施永兴. 五省市注册临终关怀机构晚期恶性肿瘤患者的医疗费用调查[J].中国全科医学, 2010, 13(31):3544-3546.
[16]Zhang C, Zhang H, Shi J, et al. Trial-Based Cost-Utility Analysis of Icotinib versus Gefitinib as Second-Line Therapy for Advanced Non-Small Cell Lung Cancer in China[J]. Plos One,2016, 11(3):e0151846.
[17]Zheng H, Xie L, Zhan M, et al. Costeffectiveness analysis of the addition of bevacizumab to chemotherapy as induction and maintenance therapy for metastatic nonsquamous non-small-cell lung cancer[J]. Clinical& Translational Oncology, 2017:1-8.
[18]陈斌斌, 范长生. 注射用紫杉醇(白蛋白结合型)治疗晚期乳腺癌的预算影响分析[J]. 中国医疗保险, 2016(12):60-63.
[19]Lu Y, Cheng J, Lin Z, et al.Pharmacoeconomic analysis for pemetrexed as a maintenance therapy for NSCLC patients with patient assistance program in China.[J]. Journal of Medical Economics, 2017:1.
[20]刘国恩. 中国药物经济学评价指南及导读:2015 版[M]. 科学出版社 , 2015.
[21]国家统计局.中华人民共和国2017年国民经济和社会发展统计公报[EB/OL]. (2018-02-28) http://www.stats.gov.cn/tjsj/zxfb/201802/t20180228_1585631.html.
[22]Nafees B, Lloyd AJ, Dewilde S, Rajan N,Lorenzo M. Health state utilities in non-small cell lung cancer: an international study. Asia Pac J Clin Oncol. March 2016.
[23]Nafees B, Lloyd A J, Dewilde S, et al. Health state utilities in non-small cell lung cancer: An international study.[J]. Asia Pac J Clin Oncol,2017, 13(5): e195-e203.
[24]Round J. Is a QALY still a QALY at the end of life?[J]. Journal of health economics, 2012, 31(3):521-527.
[25]National Institute for Health and Clinical Excellence. Appraising life-extending end of life treatments.2009
[26]Barnett J C, Alvarez Secord A, Cohn D E,et al. Cost effectiveness of alternative strategies for incorporating bevacizumab into the primary treatment of ovarian cancer[J]. Cancer, 2013,119(20): 3653-3661.
[27]Nadler E, Eckert B, Neumann P J. Do oncologists believe new cancer drugs offer good value?[J]. The oncologist, 2006, 11(2): 90-95.
