甲壳素清洁生产过程中柠檬酸钙回收工艺研究
2018-04-12方旭波陈小娥胡道亨
刘 峰,李 丽,方旭波,陈小娥,*,胡道亨
(1.浙江海洋大学食品与医药学院,浙江舟山 316022; 2.浙江国际海运职业技术学院,浙江舟山 316104; 3.舟山市海圣生物有限公司,浙江舟山 316105)
甲壳素,广泛存在于甲壳类动物壳内,是当前自然界中除纤维素外含量最丰富的生物聚合物,被广泛应用于食品、医药等诸多领域[12]。酸碱法作为甲壳素的传统生产方法,工艺简单,操作方便,但生产过程中伴随着大量含有蛋白质和无机盐的酸碱废水产生,处理难度较大,尤其是酸性废水中氯离子含量高,废水往往不能达标排放,成为困扰行业的共性问题[34]。
鉴于此,近年来有专家开始致力于应用柠檬酸替代盐酸清洁生产甲壳素的新工艺研究,以减少高氯离子污染废水排放。陈利梅等[5]用柠檬酸和氢氧化钠从南美白对虾中提取甲壳素,避免了氯含量高的酸性废水产生,但由于碱煮脱蛋白对环境污染仍然较大,其生产工艺尚有待改进。许庆陵等[6]利用Alcalase酶脱蛋白、柠檬酸脱钙从虾壳中提取甲壳素,柏韵等[7]通过柠檬酸和碱性蛋白酶的作用从中国对虾虾壳中制备甲壳素,并通过响应面设计优化了柠檬酸脱钙工艺,但这些研究均未涉及到柠檬酸钙副产物的回收利用,且工艺时间较长,不利于产业化应用。研究表明,超声波具有强烈的空化和机械效应[8],能破坏原料的组织结构,有利于促进有效物质的释放、溶解[9],既能提高生产效率,又能大大缩减生产时间,达到减少能耗的目的。
因此,本实验以红虾虾壳为原料,选用柠檬酸代替传统工艺的盐酸,在碱性蛋白酶脱除蛋白质、柠檬酸脱除钙盐制备甲壳素工艺基础上,结合超声波辅助法,以柠檬酸钙得率为指标,通过响应面优化实验对其副产物柠檬酸钙回收工艺条件进行优化。在制备甲壳素的同时回收了柠檬酸钙,副产物柠檬酸钙品质良好,可作为鏊合剂、组织稳定剂等,具有广阔的应用前景[10]。本研究旨在为甲壳素清洁生产过程中柠檬酸钙的回收利用提供科学的理论参考依据。
1 材料和方法
1.1 材料与仪器
红虾虾壳 舟山市海圣生物有限公司提供;碱性蛋白酶(20万 U/g) 南宁庞博生物工程有限公司;柠檬酸(食品级) 河南兴源化工产品有限公司;氢氧化钙(食品级) 上海缘钛化工产品有限公司;乙二胺四乙酸二钠、钙指示剂、高氯酸、硝酸、氯化铵等 均为国产分析纯。
GZX9240MBE型电热恒温鼓风干燥箱 上海博迅实业有限公司医疗设备厂;JR22 实验室用绞肉机 诸城市汇丰食品机械有限公司;THYP1004型消化炉 上海纤检仪器有限公司;KSW4011 型灰化炉 上海博迅实业有限公司;Nicolet 6700 型傅立叶变换红外光谱仪 美国Thermo Nicolet 公司;EL303电子天平 梅特勒托利多仪器(上海)有限公司;JJ1A 精密增力电动搅拌器 上海凌托仪器设备有限公司;DL180B 型超声清洗仪 上海之信仪器有限公司;DFT250 高速万能粉碎机 温岭市林大机械有限公司;HH4 数显恒温水浴锅 国华电器有限公司。
1.2 实验方法
1.2.1 红虾虾壳预处理 虾壳原料经挤压破碎后,碱性蛋白酶酶解,酶添加量为5000 U/g,在反应温度60 ℃、液料比10∶1 mL/g、pH8.5下反应6 h后,过滤、清洗、得到脱蛋白的虾壳,干燥、粉碎,备用[4]。
1.2.2 甲壳素清洁生产过程中柠檬酸钙的回收 准确称取脱蛋白后红虾虾壳25 g,在本次研究设定的条件(超声时间、超声温度、液料比、柠檬酸浓度)下进行超声处理,并搅拌,超声工作频率60 kHz,额定功率240 W。经过滤后,取酸滤液,测酸滤液钙含量,计算柠檬酸钙得率。滤渣经去离子水洗涤至中性后,干燥得甲壳素成品,计算得率并测定其主要质量指标。
取酸滤液,水浴加热至70 ℃,边搅拌边加入氢氧化钙调节滤液体系pH至6.5左右,室温静置24 h,待沉淀完全后过滤得白色柠檬酸钙,去离子水洗涤以除去其表面附着的残留物后,120 ℃烘干2~3 h,研细、过筛得白色粉状柠檬酸钙成品[11]。
1.2.3 单因素实验 依据1.2.2中方法,综合考察柠檬酸浓度、超声时间、超声温度、液料比四个因素对柠檬酸钙得率的影响。柠檬酸钙回收的实验条件为:固定液料比8∶1 mL/g、柠檬酸浓度为10%、超声温度50 ℃,考察不同超声时间(20、30、40、50、60 min)对柠檬酸钙得率影响;固定超声时间30 min、液料比8∶1 mL/g、超声温度50 ℃,考察不同浓度柠檬酸(8%、10%、12%、14%、16%)对柠檬酸钙得率影响;固定超声时间30 min、柠檬酸浓度为10%、超声温度50 ℃,考察不同液料比(6∶1、8∶1、10∶1、12∶1、14∶1 mL/g)对柠檬酸钙得率影响;固定柠檬酸浓度为10%、液料比8∶1、超声时间30 min,考察不同超声温度(40、50、60、70、80 ℃)对柠檬酸钙得率影响。
1.2.4 柠檬酸钙回收响应曲面优化实验设计 依据单因素实验结果,选取柠檬酸浓度、超声时间、液料比为实验因子,以柠檬酸钙得率为指标,利用DesignExpert V 8.0.6软件对所得结果进行分析与优化[12],以得到甲壳素清洁生产过程中柠檬酸钙回收的最佳工艺条件。实验因素水平设计见表1。
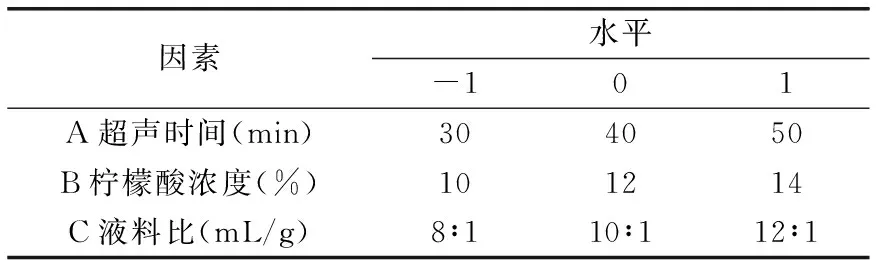
表1 响应面分析实验设计因素与水平Table 1 Independent variables and their levels used in the response surface design
1.2.5 虾壳中钙含量测定
1.2.5.1 虾壳消化方法 称取虾壳2.5 g放入盛有50 mL消化液(硝酸∶高氯酸=4∶1)烧瓶内,放入电热套内加热消化,溶液透明后停止加热,冷却、定容备用[13]。
1.2.5.2 钙含量测定 采用EDTA络合滴定法测定虾壳中钙含量[14]。钙含量由式1得到。
式(1)
式中:C为待测酸滤液中的钙离子含量,mol/L;C1为EDTA物质的量浓度,mol/L;V1为EDTA消耗体积,L;V2为待测酸滤液体积,L。
1.2.6 柠檬酸钙得率的计算 取酸滤液,按照上述1.2.5.2中的方法测其钙含量,由式2和式3计算柠檬酸钙得率[15]。
m(g)=M×19.8%
式(2)
式(3)
式中:m为虾壳中钙离子含量,g;M为脱蛋白后虾壳质量,g;y为柠檬酸钙得率,%;M0为钙离子的摩尔质量,g/mol;V为酸滤液总体积,L。
1.2.7 甲壳素得率的计算 甲壳素得率由式4得出[16]。
式(4)
式中:R为甲壳素得率,%;m1为甲壳素成品质量(以干重计),g;m2为红虾虾壳质量(以干重计),g。
1.2.8 甲壳素成品灰分含量测定 参照GB 5009.4-2016《食品中灰分的测定》,采用灼烧法测定甲壳素中灰分含量[17]。
1.2.9 甲壳素水分含量测定 参照GB 5009.32016《食品中水分的测定》,采用直接干燥法测定甲壳素中水分含量[18]。
1.2.10 蛋白质含量测定 参照GB 5009.52016《食品中蛋白质的测定》,采用凯氏定氮法测甲壳素中蛋白含量[19]。
1.2.11 柠檬酸钙的红外光谱定性分析 取少量柠檬酸钙成品粉末与KBr混合后,经过研磨处理,由压片模具进行压片,通过傅立叶变换红外光谱仪在400~4000 cm-1扫描范围内测定红外光谱[20]。
1.2.12 柠檬酸钙主要质量指标检测 柠檬酸钙成品,外观、含量(以干基计)、铅(Pb)含量、干燥减量、氟化物、砷(As)的检测,均参照GB 1903.142016《食品安全国家标准 食品营养强化剂 柠檬酸钙》[21]。
1.3 数据处理
本实验中,采用Origin 8.5作图,应用SPSS 17.0进行数据分析,用DesignExpert V 8.0.6软件优化实验结果。
2 结果与分析
2.1 虾壳中钙含量
脱蛋白后的红虾虾壳经消化后,通过EDTA络合滴定法测得钙含量为19.8%,钙含量较高,因此,本次实验在制备甲壳素工艺基础上对柠檬酸钙回收,有利于充分挖掘虾壳中的钙资源,变废为宝,为甲壳素清洁生产过程中副产物综合利用提供一条有效途径。
2.2 柠檬酸钙回收单因素实验
2.2.1 超声时间对柠檬酸钙得率的影响 由图1可知,柠檬酸钙得率随超声时间的增加而提高。当超声时间为40 min时,柠檬酸钙得率达78.24%,之后随着超声时间的增加,柠檬酸钙得率几乎不再提高。这表明增加超声时间,能提高柠檬酸分子与虾壳中钙离子碰撞几率,生成的柠檬酸钙越来越多,柠檬酸钙得率相应提高,但超过一定时间,底物钙浓度降低,柠檬酸钙的生成速率有所降低,最终趋于平衡,柠檬酸钙得率几乎没有变化[14]。故实验中超声时间约40 min比较适宜。
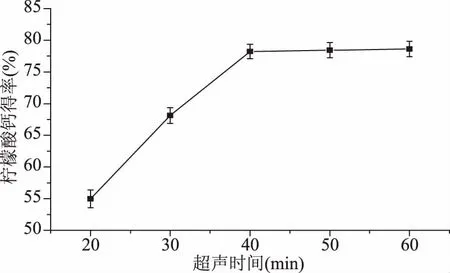
图1 超声时间对柠檬酸钙得率的影响Fig.1 Effect of ultrasound time on the yield of calcium citrate
2.2.2 柠檬酸浓度对柠檬酸钙得率的影响 由图2可以看出,随着柠檬酸浓度增加,柠檬酸钙得率随之提高。当柠檬酸浓度达12%时,柠檬酸钙得率达最高值76.44%,后随柠檬酸浓度增加,柠檬酸钙得率有小幅度下降,但总体趋于平稳。分析原因,在8%~12%的柠檬酸浓度范围内,底物浓度的增加,有利于柠檬酸钙的生成,柠檬酸钙得率提高。超过12%,反应趋于平衡,可能由于柠檬酸中的氢离子不能完全游离出来与碳酸钙进行反应,柠檬钙得率反而略有下降。因此,本实验柠檬酸浓度12%左右较为适合。
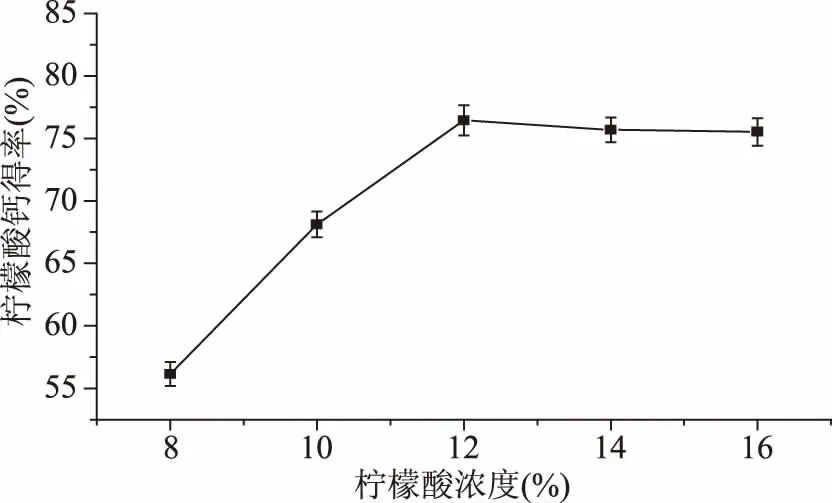
图2 柠檬酸浓度对柠檬酸钙得率的影响Fig.2 Effect of citric acid concentration on the yield of calcium citrate
2.2.3 液料比对柠檬酸钙得率的影响 图3表明,当液料比小于10∶1 mL/g时,柠檬酸钙得率随液料比增加而明显提高。液料比的增加有利于柠檬酸与虾壳中的钙盐充分接触,加速钙盐的析出,滤液中钙含量随之变大,柠檬酸钙得率也随之提高。当液料比达10∶1 mL/g后,柠檬酸钙得率上升趋势减缓,几乎不再提高,因此实验中选液料比10∶1 mL/g较佳。
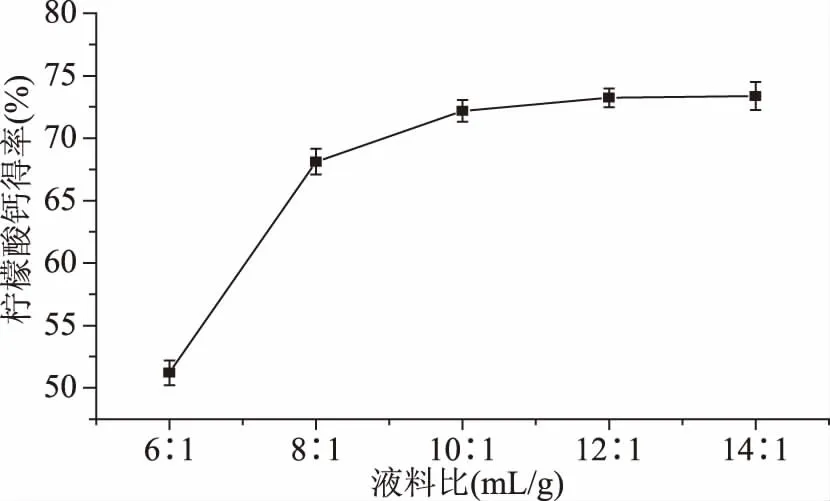
图3 液料比对柠檬酸钙得率的影响Fig.3 Effect of solidliquid on the yield of calcium citrate
2.2.4 超声温度对柠檬酸钙得率的影响 从图4可以看出,随着超声温度的增加,柠檬酸钙得率随之提高,当超声温度为50 ℃时,柠檬酸钙得率达68.12%,超过50 ℃,柠檬酸钙得率变化趋势不明显,且超声温度对柠檬酸钙得率影响相对较小。综合考虑能耗和柠檬酸钙得率,后续响应面实验中选择最佳超声温度为50 ℃。
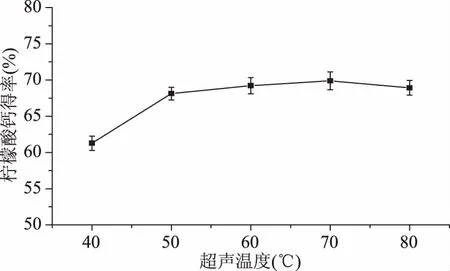
图4 超声温度对柠檬酸钙得率影响Fig.4 Effect of ultrasound temperature on the yield of calcium citrate
2.3 响应面优化柠檬酸钙回收回收工艺参数
2.3.1 BoxBehnken 实验设计与结果 依据单因素实验结果,固定超声处理温度为50 ℃,柠檬酸浓度、超声时间、液料比为实验因子,以柠檬酸钙得率为指标,通过响应面法优化柠檬酸钙回收工艺,响应面实验设计与结果见表2。
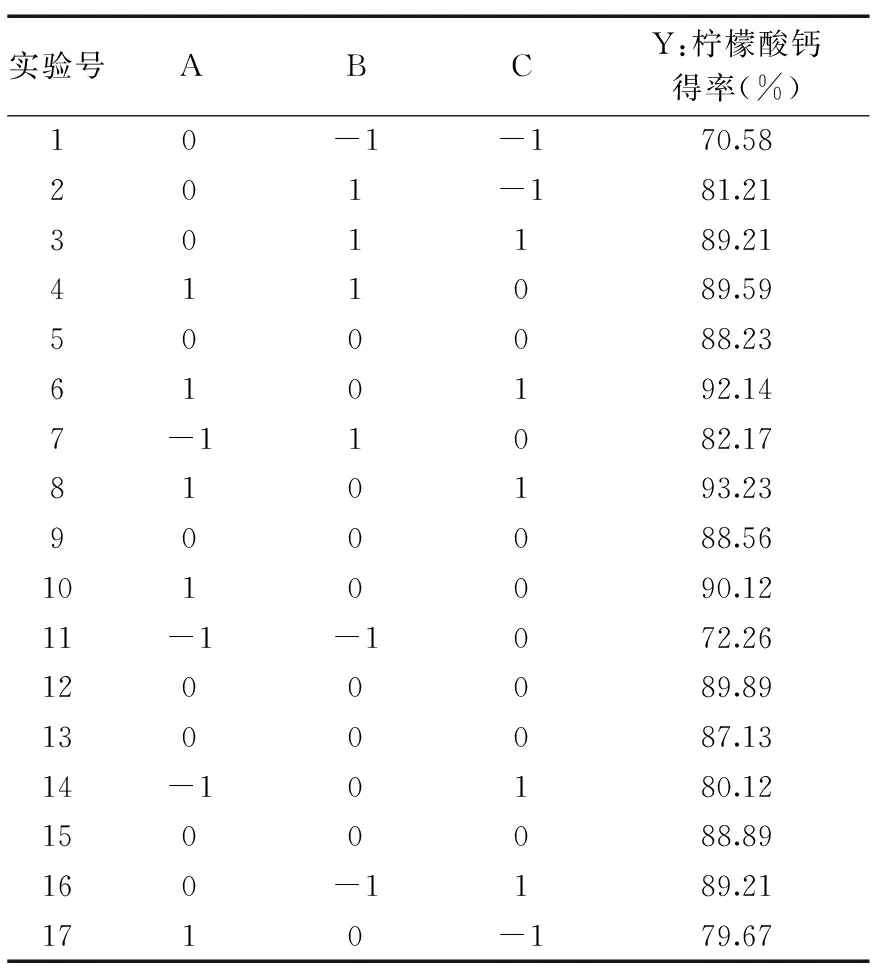
表2 响应面实验设计与结果Table 2 Response surface experimental design and results
2.3.2 回归方程拟合与方差分析 通过回归拟合分析,得到柠檬酸钙得率对超声时间、柠檬酸浓度、液料比3个因素的二次多项式回归模型为:Y=86.50+6.06A+2.66B+6.55C2.30AB+0.091AC2.66BC-4.00A21.33B24.56C2。
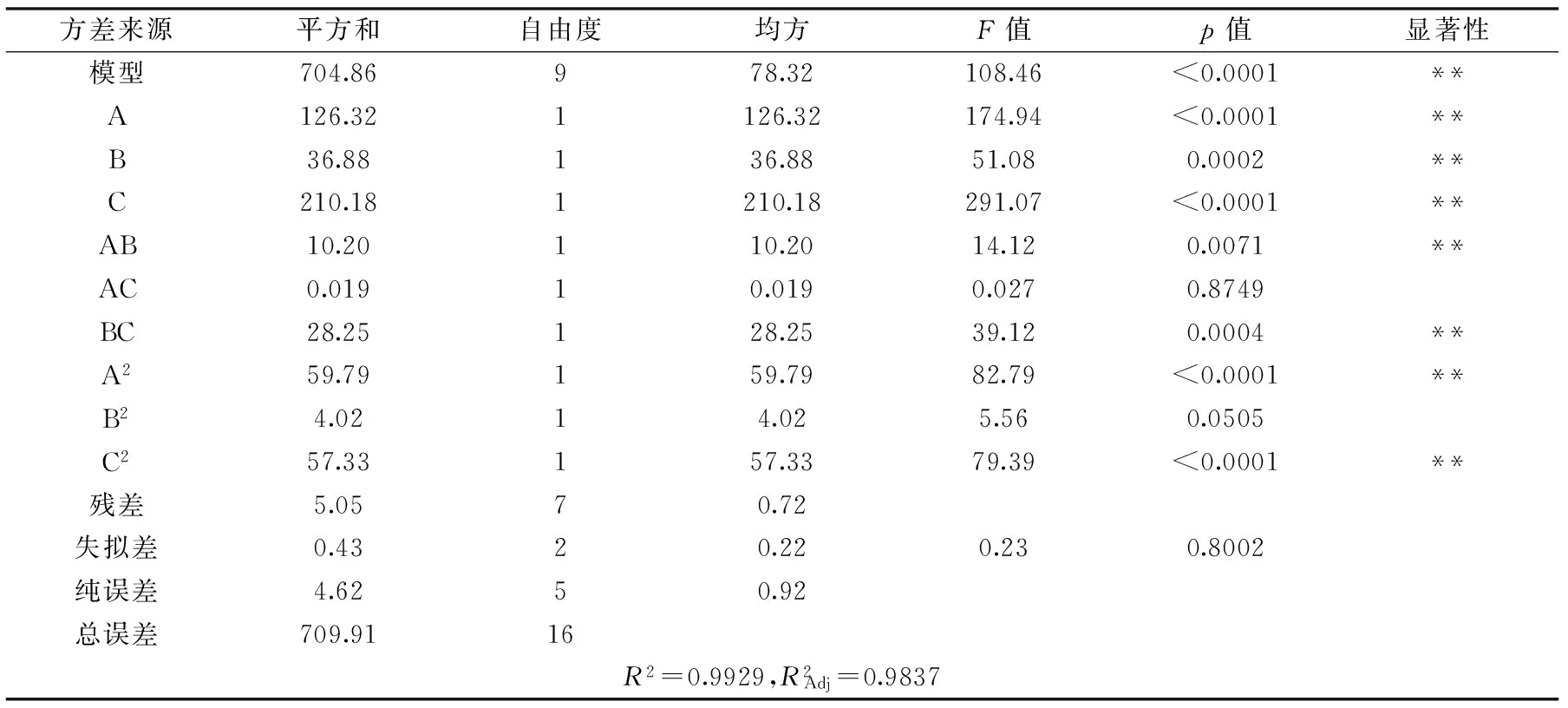
表3 回归模型的方差分析Table 3 Analysis of variance of the regression model
2.3.3 响应面图分析 利用软件DesignExpert获得各响应曲面图和等高线图,如图5~图7所示。观察图中等高线图,如果其形状呈现出椭圆形状且排列越密集,说明该因素对实验结果影响较大,呈现出圆形且排列稀疏,说明该因素对实验结果影响较小[22];观察图中响应曲面,如果其所在坡度越陡,说明相对应的工艺参数对实验结果影响较大,其所在坡度越平缓,说明其相对应的工艺参数对实验结果影响越小[23]。从图5~7可以看出,图5中柠檬酸浓度和超声时间所对应的响应曲面坡度较陡,图7中柠檬酸浓度和液料比所对应的响应曲面坡度也较陡,表明超声时间和柠檬酸浓度、柠檬酸浓度和液料比的交互作用较显著,此分析得出的结论对比于二次回归方程分析所得的结论,两者相一致。
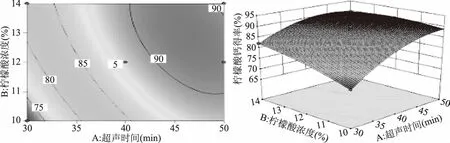
图5 柠檬酸浓度和超声时间对柠檬酸钙得率影响的响应面与等高图Fig.5 Response surface and contour plots for citric acid concentration and acid leaching time on the yield of calcium citrate
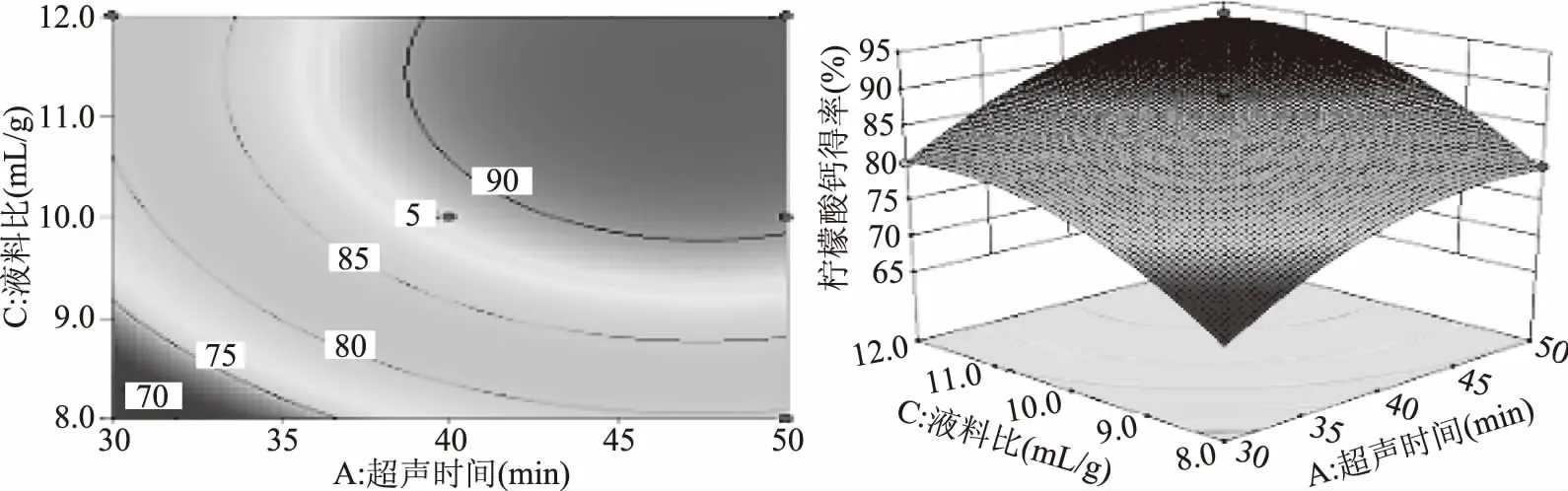
图6 超声时间和液料比对柠檬酸钙得率影响的响应面与等高线图Fig.6 Response surface and contour plots for ultrasonic time and ratio of liquid to solid on the yield of calcium citrate
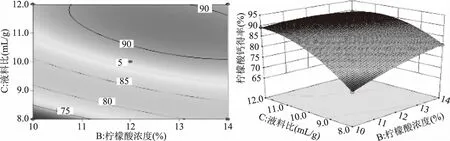
图7 柠檬酸浓度和液料比对柠檬酸钙得率影响的响应面与等高线图Fig.7 Response surface and contour plots for citric acid concentration and ratio of liquid to solid on the yield of calcium citrate
从图5可知,柠檬酸浓度处于较低水平时,增加超声时间,柠檬酸钙得率逐渐提高后趋于平稳。增加柠檬酸浓度,柠檬酸钙得率随着超声时间的增加先提高,后略有降低。随着柠檬酸浓度的增加,红虾虾壳中的钙盐同柠檬酸反应逐渐趋于完全,反应体系呈酸性,柠檬酸钙沉淀溶解,测得酸滤液中钙含量变大,柠檬酸钙得率随时间的增加而提高,后趋于稳定。
由图6可见,增加液料比,柠檬酸钙得率也相应提高;超声时间增加,随着液料比的增加,柠檬酸钙得率先提高后略有降低。可以看出,当液料比较低时,由于柠檬酸随反应的进行而被消耗,导致溶液pH变大,柠檬酸钙析出吸附于甲壳素上,测得酸滤液中钙含量变少,柠檬酸钙得率较低;增加液料比,反应溶液体系呈酸性,柠檬酸钙沉淀溶解,测得酸滤液中钙含量变大,柠檬酸钙得率也相应提高,超声时间和液料比存在相互作用。
由图7可以看出,当增加柠檬酸浓度和液料比时,柠檬酸钙得率呈现出先提高后略有下降的趋势,响应面坡度较陡,柠檬酸浓度和液料比交互作用较显著,对柠檬酸钙得率的影响较大。
2.3.4 验证实验 通过模型并结合响应面曲线图分析,得出甲壳素清洁生产过程中柠檬酸钙回收最佳工艺条件为:柠檬酸浓度10.33%,液料比11.94∶1 mL/g,超声时间50 min,预测的柠檬酸钙得率93.62%,为了简化实际操作,选取柠檬酸浓度10%,液料比12∶1 mL/g,超声时间50 min,在该条件下,进行重复验证实验,得到柠檬酸钙得率为93.49%±0.07%,与回归方程预测所得的柠檬酸钙得率相对误差仅为0.14%,说明响应面法可以有效地优化甲壳素清洁生产过程中柠檬酸钙回收工艺。在此条件下,甲壳素得率达18.93%±0.06%。
2.4 柠檬酸钙成品红外光谱分析
柠檬酸钙成品红外光谱图,如图8所示。柠檬酸的特征吸收峰有νCH3297.7 cm-1,νOH3496.4 cm-1,νC=O1700.9 cm-1,νCC1178.3 cm-1,δOH775.3 cm-1[24],图中柠檬酸钙的峰形与之对比,较为吻合,只是稍有偏移。其中OH伸缩振动减少56.01 cm-1,出现在3440.39 cm-1处;羰基峰吸收峰减少了161.98 cm-1,出现在1538.92 cm-1处,表明羧酸与钙离子形成了配位键,柠檬酸同虾壳中钙反应生成了柠檬酸钙。
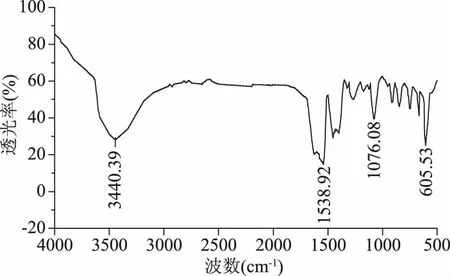
图8 柠檬酸钙成品红外光谱图Fig.8 Infrared spectra of calcium citrate production in chitin clean production
2.5 柠檬酸钙成品主要质量指标分析
参照GB 1903.142016对柠檬酸钙成品进行质量指标分析,结果见表4。可以看出,柠檬酸钙成品主要质量指标符合GB 1903.142016要求,可作为生物活性螯合剂、缓冲剂等广泛应用于食品行业,具有广阔的应用发展前景。
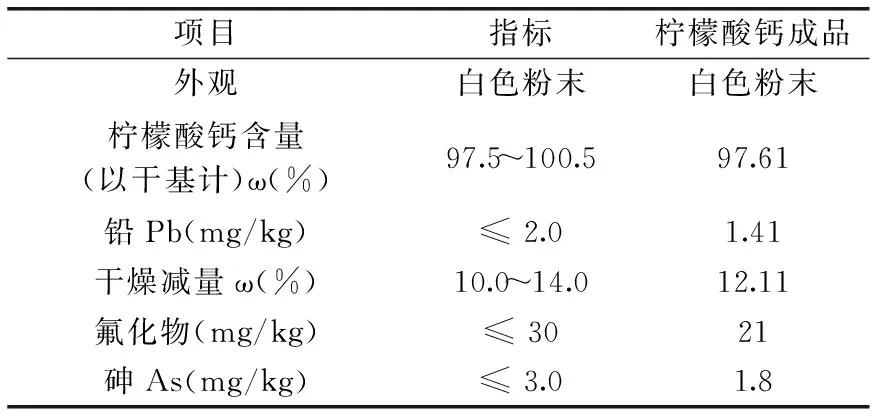
表4 柠檬酸钙成品的主要质量指标Table 4 The main quality indicators of calcium citrate products
2.6 甲壳素成品质量分析
甲壳素成品主要质量指标,如表5所示。可以看出,甲壳素成品质量指标达到食品级标准[25]。在保证甲壳素成品质量的条件下,实现副产物柠檬酸钙最大回收利用,既降低了环保压力,又能合理利用资源。

表5 甲壳素成品质量分析Table 5 Quality analysis of chitin prepared by the optimum parameter
3 结论
本实验在碱性蛋白酶脱蛋白、柠檬酸脱钙制备甲壳素的工艺基础上,结合超声辅助法,采用响应面实验设计对副产物柠檬酸钙回收工艺条件进行优化,得到最优工艺条件:柠檬酸浓度10%,液料比12∶1 mL/g,超声时间50 min,此时柠檬酸钙得率达93.49%±0.07%,在此条件下,甲壳素的得率达18.93%±0.06%。柠檬酸钙成品经傅立叶变换红外光谱仪定性分析,并参照GB 1903.142016主要质量指标进行定量检测,其柠檬酸钙含量达97.61%,符合我国柠檬酸钙食品添加剂要求,在食品行业中应用范围广。甲壳素成品主要质量指标经检测,达到食品级标准。
本次研究在兼顾甲壳素质量的前提下,首次对甲壳素清洁生产过程中柠檬酸钙回收工艺进行优化,有利于充分挖掘虾壳的利用价值,提高生产厂家的利润,因而具有较好的市场推广应用价值。
[1]姜山,史源,朱启忠. 壳聚糖文献分析[J]. 大学化学,2011,26(4):4548.
[2]Ashish D,Jithin C,Sreeja V,et al. Novel carboxymethyl chitin nanopaonal apprrticles for drug delivery applications[J]. Carbohydrate Polymers,2010,79(4):10731079.
[3]黄湛媛,李丽,陈小娥,等. 甲壳素生产工艺中虾蛋白回收工艺研究[J]. 食品工业,2016,37(11):1519.
[4]刘锡红,赵灵希,张成杰,等. 酶法从虾壳中提取甲壳素工艺优化的研究[J]. 食品工业科技,2013,34(22):209-212,216.
[5]陈利梅,戴桂芝,李德茂. 南美白对虾甲壳素提取工艺的优化[J]. 中国调味品,2009(2):8385.
[6]许庆陵,曾庆祝. 虾壳甲壳素及壳聚糖提取工艺的研究[J]. 中国食品添加剂,2013(6):104109.
[7]柏韵,李然,张振,等. 中国对虾虾壳制备几丁质工艺研究[J]. 食品工业科技,2017,38(9):174180.
[8]彭元怀,黄川,赵泽洁. 超声波辅助提取虾壳甲壳素的工艺研究[J]. 食品工业科技,2012,33(9):304308.
[9]张昌军,原方圆,邵红兵. 超声波法在提取多糖类化合物中的应用研究[J]. 化工时刊,2007(2):5456.
[10]段元斐,何忠诚,庄桂东,等. 甲壳素提取新工艺的研究[J]. 食品工业,2007(3):78,10.
[11]李逢振,马美湖,张雯亭,等. 鸡蛋壳中碳酸钙转化制备柠檬酸钙的研究[J]. 食品工业科技,2013,34(5):192-194,199.
[12]Li M,Wang Z C,Dai H J,et al. Response surface optimization of polysaccharides extraction from Liriope Roots and its modulatory effect on sjogren syndrome[J]. Carbohydrate Polymers,2009,45(3):284288.
[13]韩凯宁,王盼盼,林海,等. 有机酸中虾壳中钙的溶出特性研究[J]. 广州化工,2013,41(8):7172,159.
[14]李明华,孟秀梅. 超声波辅助柠檬酸法龙虾壳脱钙工艺研究[J]. 食品工业,2017(5):810.
[15]张勇,周建群,高丽红,等. 饲料添加剂柠檬酸钙质量剖析及质量指标的设定[J]. 粮食与饲料工业,2014(8):4042.
[16]谢宇,胡金刚,魏娅,等. 基尾虾虾壳中提取甲壳素工艺研究[J]. 河南工业大学学报:自然科学版,2009,30(1):3741.
[17]GB 5009. 42016. 食品中灰分的测定[S]. 北京:中国标准出版社,2016.
[18]GB 5009. 32016. 食品中水分的测定[S]. 北京:中国标准出版社,2016.
[19]GB 5009.52016. 食品中蛋白质的测定[S]. 北京:中国标准出版社,2016.
[20]陈士勇. 四角蛤蜊贝壳钙制剂及肽螯合钙制剂的工艺研究[D]. 南京:南京中医药大学,2012.
[21]GB 1903.142016. 食品安全国家标准食品营养强化剂柠檬酸钙[S]. 北京:中国标准出版社,2016.
[22]张辉. 黑曲霉HQ1产羧甲基纤维素酶的发酵条件优化[J]. 酿酒科技,2011(5):2731.
[23]杨杰,谷新晰,李晨,等. 响应面法优化植物乳杆菌绿豆乳增值培养基[J]. 中国食品学报,2015,15(12):8390.
[24]林丽丽,文健,潘荣楷,等. 以贝壳制备柠檬酸钙的研究[J]. 湛江师范学院学报,2010,31(6):9598.
[25]唐义宝,谢晶. 柠檬酸用于虾头、虾壳的脱钙处理[J]. 食品科学,2012,33(10):69.
