三种典型重金属污染物对电镀生化处理单元污泥脱氢酶活性的抑制效应
2018-04-03熊亚波黄东伟关永年刘洪波
熊亚波,黄东伟,关永年,刘洪波
(1.上海理工大学环境与建筑学院,上海 200093;2.苏州工业园区清源华衍水务有限公司,江苏苏州 215021)
电镀废水是我国每年排放量最大的工业废水之一,废水中除含有不同种类与浓度的Cu、Cr、Ni等重金属污染物,还有氰化物、氨氮、磷酸盐、有机物等污染物[1]。电镀废水处理一般有重金属捕集法、化学沉淀法、活性污泥法等[2],这些方法具有明显的针对性,但在实际过程中,考虑物化处理药剂和污泥处置成本昂贵、活性污泥方法可操作性强等因素,电镀废水处理往往采取物化-生化联用的方式,物化处理工艺出水中重金属种类与含量对后续生化工艺中活性污泥活性的影响,是合理耦合物化-生化工艺的重要参考[3]。重金属离子对活性污泥微生物的毒性作用的机理十分复杂[4]。通常来说,重金属对活性污泥的毒性取决于两个因素,重金属的种类(价态)和浓度。其中,重金属浓度是破坏活性污泥系统的主要因素之一[5]。重金属对微生物的影响可导致生化处理过程中微生物种群结构发生变化,影响污水处理效果[6];微生物不能降解重金属,但微生物可以对重金属进行吸附和转化,具有一定的拮抗作用和毒害作用[7-8]。因此,协调微生物与污水中基质之间的关系,也是环境可持续发展的重要方向[9]。
生物处理废水的过程是在多种酶的催化作用下进行的一系列氧化和还原反应,本质上是一种酶促反应[10]。依据微生物酶系统受抑制机理的相关研究,脱氢酶的活性在很大程度上可以反映污泥微生物的活性状态,并且可以直接表示生物对某些基质降解能力的大小[11-12]。因此,本研究利用脱氢酶活性作为指示指标,表征重金属对污泥微生物的毒害作用。
相关报道表明,无论是单一重金属还是复合重金属,当进水的总浓度到10 mg/L时,会对连续流模式的活性污泥处理系统的处理效果产生50%以上的影响。荣宏伟等[13]研究出当加入1~10 mg/L Cu2+时,受到影响的微生物系统和活性污泥可在后期的培养驯化中恢复其相关功能,指标可恢复至未投加Cu2+时的水平。另外,王越等[6]在Cr6+对活性污泥硝化活性的抑制及在污泥中的分布特点研究中发现,Cr6+对活性污泥硝化活性的抑制程度随着Cr6+浓度的增大而提高,且对微生物的抑制作用大小是:氨氧化菌>亚硝酸盐氧化菌>异氧菌。王伟等[14]在研究Ni2+对活性污泥活性及群落多样性的影响中指出,当Ni2+的浓度低于5 mg/L时,其对序批式反应器内活性污泥TTC-ETS的活性未产生显著的影响。当浓度超过10 mg/L时,其显著抑制了活性污泥微生物对碳源的利用。
本研究主要通过试验配置电镀废水常见的三种不同重金属溶液,对活性污泥进行暴露试验,通过脱氢酶活性指示重金属对污泥微生物活性的影响,探索在不同的条件下电镀废水重金属污染物对其生化单元污泥脱氢酶活性的抑制效应,为电镀废水物化处理和生化处理的衔接提供参考。
1 试验材料和方法
1.1 试验材料
试验选取电镀废水三种重金属的四种典型形态Cu2+、Ni2+、Cr6+、Cr3+为研究对象,分别用Cu(NO3)2·3H2O、Ni(NO3)2·6H2O、Cr(NO3)2·9H2O、K2Cr2O7分析纯药品配成浓度为1 g/L的Cu2+、Ni2+、Cr3+、Cr6+储备溶液,试验过程中取一定量的储备液稀释,配制成不同浓度的重金属污水,然后对活性污泥进行暴露试验。试验所用的接种污泥来自上海市杨浦区东区污水处理厂曝气池内的活性污泥,其活性良好,镜检可见大量菌胶团,用其作为种泥进行驯化培养,在反应器中以人工配置的营养液对其进行培养,参考文献中的配方[15],反应器所用人工配水组成成分如表1所示。
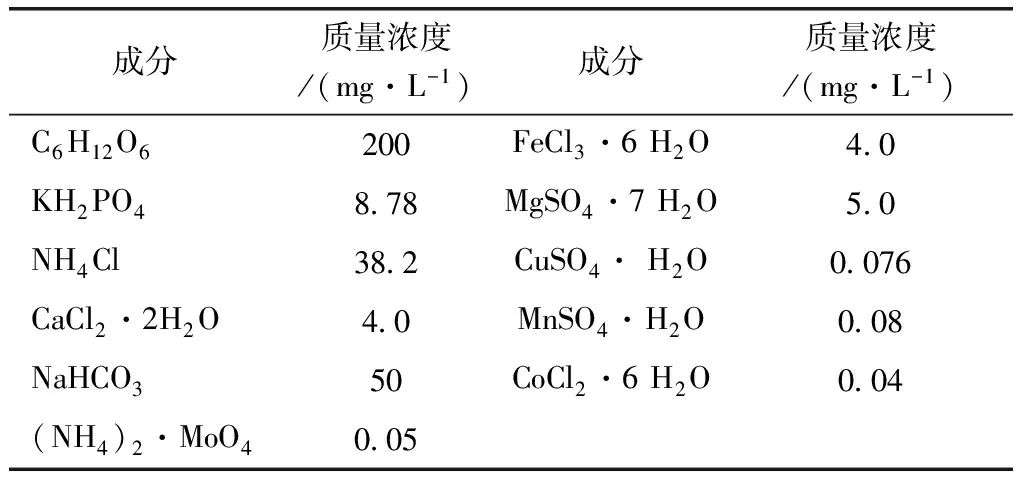
表1 活性污泥培养期人工配水组分
1.2 试验方法
1.2.1活性污泥的驯化
从上海市杨浦区东区污水处理厂好氧池内取的活性污泥放入有效容积为10 L的反应器中,反应器内设置曝气装置,空气经空压机压缩后通过反应器底部的曝气头扩散至整个反应器。该反应器每天运行4个周期,每个周期为6 h,控制时间为: 4 h曝气,2 h静置换水,换水时按表1 添加营养液。调节反应器pH值为7.5~8.0,控制污泥浓度为4 000±500 mg/L,设置溶解氧DO为6±1 mg/L,水力停留时间HRT为6 h,污泥龄SRT为10 d。
1.2.2活性污泥重金属染毒过程
取反应器内驯化好的活性污泥200 mL放入烧杯中,在试验设置的不同浓度重金属溶液、培养时间及pH条件下进行染毒,相同试验条件下进行曝气,曝气结束后取样进行后续重金属浓度测定及后续污泥活性的测定试验。
1.2.3不同影响因素下重金属对污泥脱氢酶活性的抑制试验
关于不同浓度的重金属对污泥脱氢酶活性的影响试验中,分别配置0、1、2、5、25、50、100、150、200、250、300 mg/L浓度的Cu2+、Cr3+、Cr6+、Ni2+溶液,取反应器内的活性污泥200 mL放入烧杯中,再加入不同浓度100 mL的重金属溶液,在一定条件下进行4 h的曝气,曝气结束后取混合液进行后续重金属浓度测定及污泥脱氢酶活性测定试验。
关于不同培养时间下重金属对污泥脱氢酶活性的影响试验中,取反应器内的活性污泥200 mL放入烧杯中,再加入100 mL 5 mg/L的重金属溶液,在一定条件下进行0、0.5、1、2、4、8、12、24、36 h曝气试验,曝气结束后取混合液进行后续重金属浓度测定及污泥脱氢酶活性测定试验。
关于不同pH下重金属对污泥脱氢酶活性的影响试验中,取反应器内的活性污泥200 mL放入烧杯中,分别加入100 mL pH值=5.4浓度为100 mg/L硝酸铜溶液、pH值=4.0浓度为350 mg/L 硝酸铬溶液、pH值=6.4浓度为150 mg/L的硝酸镍溶液、三种重金属的混合溶液,在一定条件下通过碱或酸调节pH,在不同的值下曝气进行试验,曝气结束后取混合液进行后续重金属浓度测定及污泥脱氢酶活性测定试验。
1.3 分析方法
1.3.1活性污泥脱氢酶测定
活性污泥中微生物的活性用脱氢酶活性进行指示。脱氢酶活性采用定量分析法[16],选用无色的2,3,5-氯化三苯基四氮唑(TTC)作为受氢体,水中的有机质在脱氢酶的作用下,发生脱氢反应,人工受氢体(即TTC)接受氢原子被还原而显色,溶液反应前后颜色深度发生变化。利用分光光度计测出相应的光密度(OD值),计算产物三苯基甲酯(TF)含量,求出脱氢酶活性。通常TF值越大,脱氢酶活性也越大,其还原方式如式(1)和式(2)。

(1)
[TTC]Cl(无色)+2H→TF(红色)+HCl
(2)
取2 mL混合均匀的活性污泥混合液于10 mL的离心管中,再加入2 mL Tris-HCl缓冲溶液、0.5 mL 0.36%的Na2SO3溶液,以及1 mL 0.4%的TTC溶液。随后立即将离心管放入(35±1)℃的恒温水域锅中反应20 min左右,结束后向离心管中加入1滴浓硫酸以终止反应。接着向离心管中加入5 mL的二氯甲烷溶剂,振荡以提取TF,过滤后在485 mm波长下比色,读取OD值,再在标准曲线上查出相应的TF值。
1.3.2重金属测定
试验主要考察重金属Cu2+、Ni2+、Cr3+及Cr6+,重金属浓度采用火焰原子分光光度法,仪器型号为TAS-990,Cu、Ni、Cr的标准曲线分别为0~3.0、0~3.0 mg/L和0~5.0 mg/L。
2 结果和讨论
2.1 不同浓度重金属离子对活性污泥微生物脱氢酶活性的影响
重金属离子在不同浓度下与TTC -DHA(脱氢酶活性)的抑制试验结果及灵敏度分析如图1所示,表示TF含量及活性污泥抑制百分比与重金属浓度之间的关系。
由图1(a)可知,在Cu2+胁迫下,随着Cu2+浓度的增大,活性污泥脱氢酶活性急剧下降,TTC抑制百分比上升。当Cu2+浓度达到25 mg/L时,微生物胞内的TF含量几乎为0,TTC抑制率高达90%,说明此时活性污泥脱氢酶基本上处于失活状态。在此状态下,Cu2+与微生物体内酶分子上的-SH基团发生可逆结合[17-18],从而导致脱氢酶活性的下降,抑制微生物的生长。
Cr3+和Cr6+对脱氢酶活性的影响及TTC反应毒性的灵敏度如图1(b)和图1(c)所示。废水中铬离子一般以三价或者六价的形式存在,利用活性污泥法处理含铬废水时,活体微生物不但对铬离子有吸附作用,同时还存在酶的催化转化作用,及细胞内代谢产物的还原作用、絮凝作用和沉淀作用等[8]。但当铬离子浓度超过一定活性污泥微生物的承受能力时,就会对生物体造成极大的伤害,直至导致微生物的死亡,废水处理系统最终的失败。由图1可知,微生物细胞中的TF含量随着铬离子浓度的增大不断呈下降趋势,相应地脱氢酶活性的抑制百分比不断增大,这表明无论是Cr6+还是Cr3+均对活性污泥脱氢酶的活性产生了很强的抑制作用。对于Cr3+而言,即使是1 mg/L的Cr3+也会对活性污泥的脱氢酶活性产生强烈的抑制作用,使微生物体内的TF从原来的64.97 mg/L下降到16.36 mg/L,抑制率达到74.82%。当Cr3+浓度增大到5 mg/L时,TF持续下降到8.16 mg/L,此时抑制率逐渐上升到87.46%。说明在低浓度条件下,Cr3+同样会对活性污泥脱氢酶活性产生强烈的抑制作用,并且重金属离子浓度越大,抑制效果也越明显。对于Cr6+而言,如图1(c)所示,在无Cr6+投加的情况下,活性污泥脱氢酶活性为64.91 mg/L,说明此时活性污泥微生物具有较好的活性。随着Cr6+浓度的增加,活性污泥的活性逐渐下降。当Cr6+浓度达到1 mg/L时,Cr6+对活性污泥脱氢酶活性的抑制率达到57.79%。当Cr6+浓度增大到5 mg/L时,污泥细胞内TF的含量为14.45 mg/L,与原空白对照相比,Cr6+对污泥脱氢酶活性的抑制增大到77.74%。进一步研究可以发现,当Cr6+的投加量在1~30 mg/L时,重金属对活性污泥脱氢酶活性抑制率在50%~80%。因此,当Cr6+在0~5 mg/L的低浓度投加段,生物体内TF含量随重金属浓度的增加下降非常明显,脱氢酶活性受到的抑制十分强烈。当Cr6+浓度增加到5 mg/L以上时,脱氢酶活性受到的抑制相对趋于平缓。
图1(d)表示不同浓度Ni2+对应的活性污泥TF含量及其抑制率。由图1(d)可知,在未投加Ni2+的活性污泥中,微生物体内的TF含量为64.97 mg/L,此时微生物具有较好的脱氢酶活性。与空白试验相比,投加1 mg/L的Ni2+时,微生物体内的TF含量下降到了23.53 mg/L,Ni2+对污泥脱氢酶活性的抑制率达到了63.78%。继续增大Ni2+的浓度至5 mg/L时,TF含量继续下降至31.45 mg/L,抑制率增大至51.59%。当Ni2+浓度大于5 mg/L时,活性污泥的抑制率可以达到80%以上,说明Ni2+对活性污泥微生物具有较强的生物毒性。当Ni2+的投加量在1~50 mg/L时,重金属对活性污泥脱氢酶活性的抑制率均在50%~80%,在0~5 mg/L的低浓度投加段,生物体内TF含量随重金属浓度的增加下降趋势明显,脱氢酶活性受到的抑制较大。
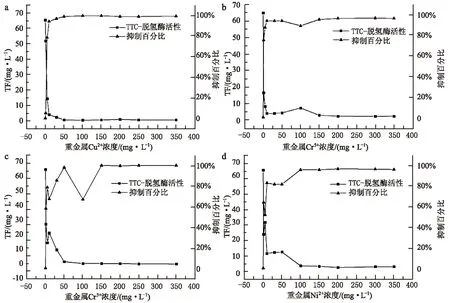
图1 不同浓度重金属对脱氢酶活性的影响
对比分析Cu2+、Cr6+、Cr3+、Ni2+四种重金属离子对活性污泥中微生物脱氢酶活性的影响程度可以发现,用TTC表征Cu2+、Cr6+、Cr3+、Ni2+对活性污泥微生物的毒性大小均具有比较高的灵敏度。通过TF含量及活性污泥抑制百分比与重金属浓度之间的关系分析可以发现,以活性污泥微生物脱氢酶活性表征的重金属毒性大小的顺序为:Cu2+>Cr6+>Ni2+>Cr3+[19], TTC可以很好地反映出活性污泥微生物的活性,并且表征灵敏度也相对较高。
2.2 培养时间对活性污泥微生物脱氢酶活性的影响
重金属离子在不同暴露时间下对活性污泥脱氢酶活性的影响如图2(a)和图2(b)所示。由图2(a)可知,随着暴露时间的增加,活性污泥微生物细胞内的TF含量逐渐下降,TTC抑制百分比急剧上升,表明培养时间越长,活性污泥脱氢酶活性越低。以Cu2+为例,当活性污泥在金属溶液中暴露2 h后,细胞内TF含量从原来的13.14 mg/L下降到5.36 mg/L,脱氢酶活性的抑制率达到59.2%;对于Cr6+而言,TF含量从原来的31.05 mg/L下降到18.32 mg/L,脱氢酶活性的抑制率达到了40.05%;对Cr3+而言,细胞内的TF含量从原来的41.31 mg/L下降到了17.59 mg/L,脱氢酶活性的抑制率达到了57.42%;对Ni2+而言,细胞内的TF含量从原来的20.99 mg/L下降到14.35 mg/L,脱氢酶活性的抑制率达到了31.68%。随着暴露时间继续延长到5 h, Cu2+的抑制率继续上升到92%, Cr6+的抑制率增大到73.95%,Cr3+的抑制率上升到62.87%,Ni2+的抑制率上升到74.32%。在0~5 h时,5 mg/L的重金属浓度即可让脱氢酶活性达到60%~90%的抑制率。当暴露时间继续延长后,脱氢酶活性虽会继续增加,但趋势逐渐缓慢。对于活性污泥微生物脱氢酶活性而言,随着暴露时间的延长,Cu2+的抑制率最高,其次为Cr6+和Cr3+,Ni2+最低。与不同浓度重金属对脱氢酶活性毒害作用顺序相似。
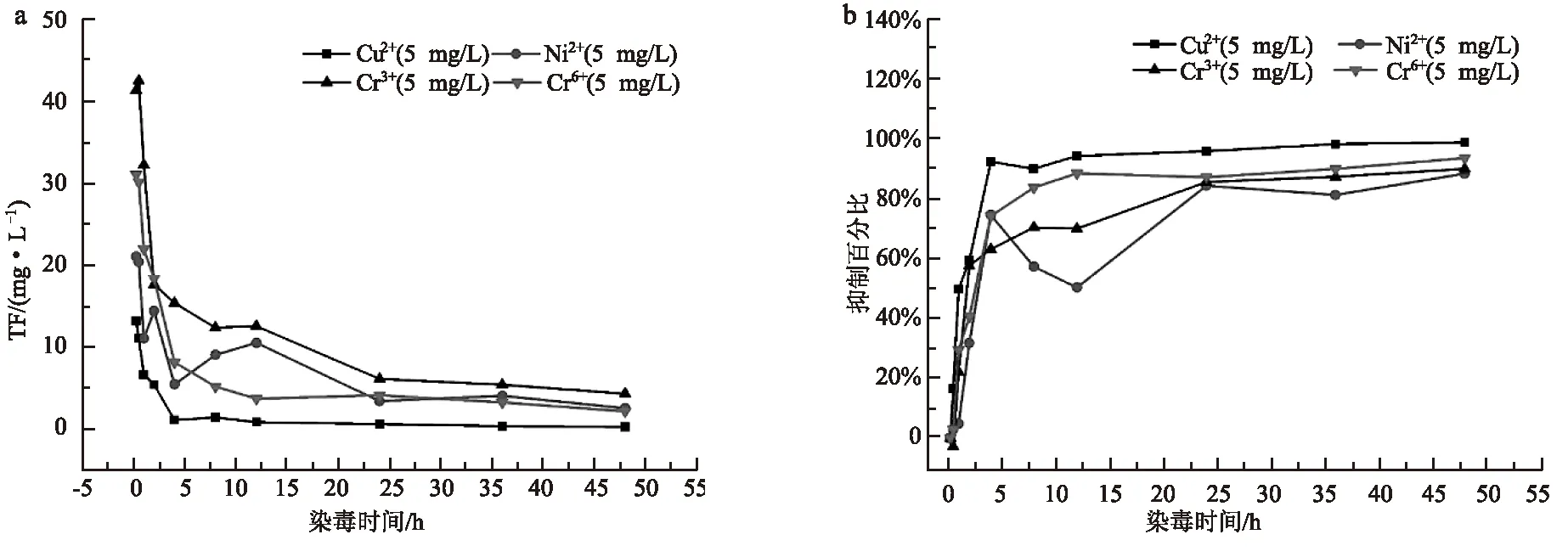
图2 不同培养时间下重金属对活性污泥活性的影响以及抑制率
2.3 pH对活性污泥微生物脱氢酶活性的影响
由图3(a)可知,随着pH的增大,溶液中总铬的离子浓度越来越小,直至pH值升到7.0左右,Cr3+浓度几乎下降为0。当溶液pH值在4.0时,Cr3+处于完全水解的离子态,溶液中的离子浓度很大,此时对活性污泥脱氢酶的抑制率高达96.1%,当pH值在4.0~7.0时,溶液中的铬离子大部分以胶体氢氧化铬的形式存在,分子量逐渐增大,溶解度逐渐降低,此时溶液中的铬离子浓度逐渐降低,对活性污泥微生物体内脱氢酶活性的抑制率逐渐降低,并且随着反应的进行,抑制率迅速下降。当溶液pH值继续上升到8.0及以上时,溶液中铬离子均以氢氧化铬的形式存在,溶解度降至最低,溶液中的Cr3+浓度为0.06 mg/L,此时对活性污泥脱氢酶活性的抑制也最小,仅为20.98%。当溶液pH值继续上升至12.0~13.0时,出水总铬浓度会微微上升,这是由于过量的氢氧根会与氢氧化铬发生反应生成亚铬酸钠所致。
如图3(b)所示,随着pH值的增大,溶液中铜离子浓度逐渐降低,在pH值升到7.0~8.0时,出水总铜浓度降至最低。当pH值=5.0时,铜处于完全水解的离子态,此时图3(b)显示活性污泥脱氢酶的抑制率达到了94.1%,微生物几乎处于完全失活状态。当pH值在5.0~7.0时,溶液中的铜大部分以胶体氢氧化铜的形式存在,分子量逐渐增大,溶解度逐渐降低,对活性污泥微生物体内脱氢酶活性的抑制率也在逐渐减小。当溶液pH值继续上升到8.0时,已经大于Cu2+的沉淀pH值,氢氧化铜的溶解度降至最低,大量的氢氧化铜沉淀开始析出,此时对活性污泥脱氢酶活性的抑制也最小。随着溶液pH值的继续增大,溶液中Cu2+浓度变化不大,但对活性污泥脱氢酶的活性抑制率却出现逐渐上升的趋势。出现这种现象主要是由于加入了过量的NaOH调节pH,pH值越大,加入的NaOH溶液越多,对活性污泥毒害越大。在利用沉淀法处理实际废水时,需要注意碱的投加量,最好控制在能够使金属离子刚好完全沉淀时即可,投加过多导致出水pH过高时,则需用酸回调pH至中性附近,否则会对后续的生物处理造成伤害。
由图3(c)可知,随着pH的增大,溶液中总镍的离子浓度越来越小。当pH值升到10.0左右时,Ni2+浓度几乎下降为0。当溶液pH值在6.0时,Ni2+处于完全水解的离子态,溶液中的离子浓度很大,此时对活性污泥脱氢酶的抑制非常强,抑制率高达93.5%,当pH值在6.0~10.0时,溶液中的镍离子大部分以胶体氢氧化镍的形式存在,分子量逐渐增大,溶解度逐渐降低,此时溶液中的镍离子浓度逐渐降低,对活性污泥微生物体内脱氢酶活性的抑制率逐渐降低。当溶液pH值继续上升到10.0以上时,溶液中的铬镍均以氢氧化镍的形式存在,溶解度降至最低,溶液中的镍浓度几乎为0,此时对活性污泥脱氢酶活性的抑制也最小,抑制率仅为30.7%。
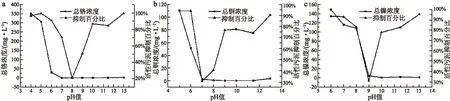
图3 不同pH条件下各重金属对活性污泥活性的影响
实际电镀废水组分比较复杂,在废水中只存在单一重金属离子的情况很少,往往同时存在多种重金属离子,除与其他污染组分形成许多复合污染物之外,金属离子之间还会存在协同作用、拮抗作用和非相关性等三种行为[20-21]。
混和重金属去除结果如图4(a)所示,与单独重金属溶液相比,混和溶液初始pH值有所下降,为3.0,溶液更显酸性。由沉淀规律上可知,混和溶液中的重金属离子到达完全沉淀的pH阈值有所提前,Cu2+与Cr3+在pH值=6.0时即到达沉淀终点,而Ni2+在pH值=7.0时到达沉淀终点。在单独重金属溶液中,Cu2+、Cr3+、Ni2+到达各自的沉淀终点时的pH值分别为7.0、7.0、9.0。因此,当Cu、Cr、Ni三者重金属离子混合在一起时具有协同效应,有助于各自沉淀的进行[20]。另一方面,在单一含Cr3+溶液中,pH值大于11.0时,铬离子浓度又会大幅上升,这是因为氢氧化铬与过量的氢氧根反应,生成了水溶性的亚铬酸钠,增加了溶液中总铬的浓度。而当混入铜离子与镍离子后,铜离子与镍离子消耗了大量氢氧根,抑制了氢氧化铬与氢氧根的反应,有利于出水铬离子浓度的达标。
混合溶液重金属离子对活性污泥脱氢酶活性的影响如图4(b)所示。随着溶液中金属离子沉淀的进行,活性污泥细胞内的TF含量经历了由低到高的过程,活性污泥脱氢酶活性的抑制率则呈现相反的趋势。当三种重金属处于强酸状态下,各自以离子态的形式存在于溶液中时,此时检测出的重金属离子浓度极高,对活性污泥的抑制率高达94%,TF含量仅为1.2 mg/L。随着溶液pH值的增大,各离子会剧烈地抢夺水中的氢氧根离子,形成水溶氢氧化态和胶状氢氧化态,由于离子间的协同作用,分子量增大很快,溶解度迅速降低,此时,溶液中的离子浓度也逐渐降低,对活性污泥的毒害也逐渐减少。当pH值到达8.0左右,絮状氢氧化物迅速形成,形成大量的沉淀,各自的浓度降到最低值,对活性污泥的抑制率也达到最低,为41.0%。随着碱量的继续投加,活性抑制率又持续上升。
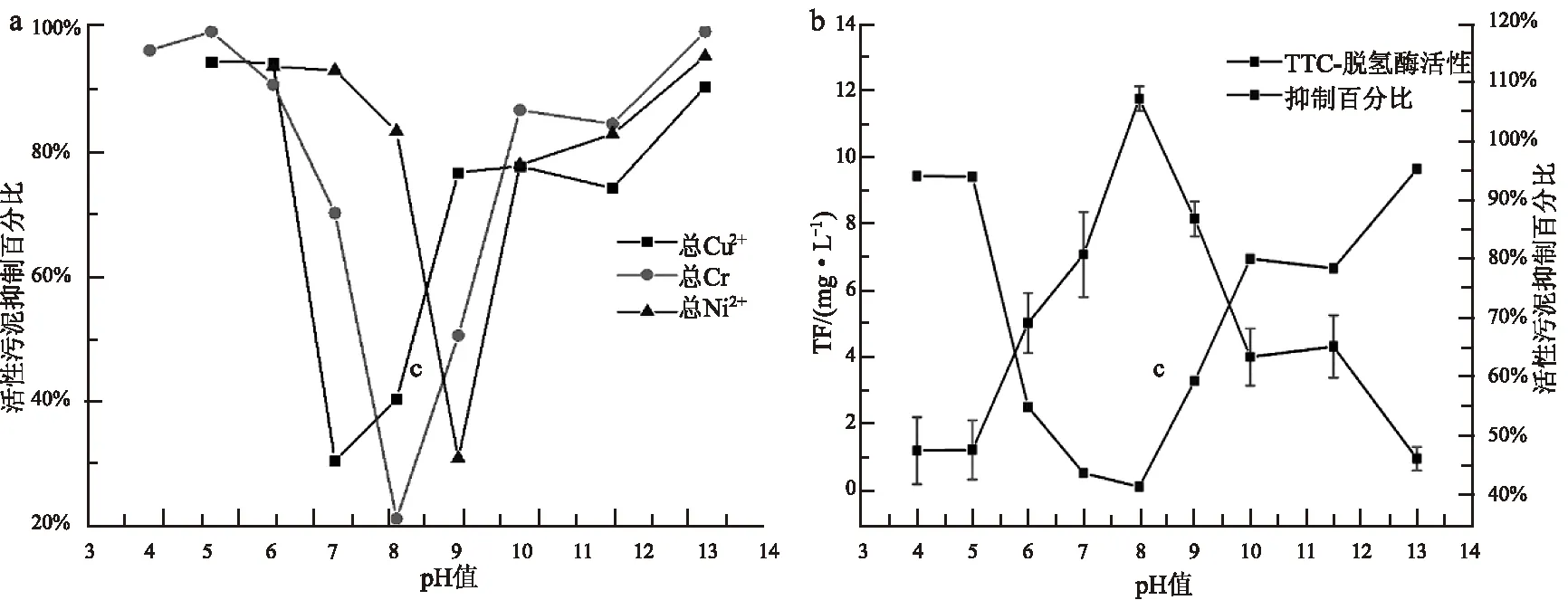
图4 不同pH条件下混合重金属对活性污泥活性的影响
3 结论
重金属的浓度、形态、存在方式、暴露时间等均对活性污泥微生物的活性产生影响,以活性污泥微生物脱氢酶活性表征的重金属对污泥微生物毒性大小的顺序为:Cu2+>Cr6+>Ni2+>Cr3+。当溶液为酸性时,重金属处于离子态,对活性污泥脱氢酶活性的抑制较大,当Cu2+溶液pH值=8.0、Cr3+溶液pH值=7.0、Ni2+溶液pH值=10.0时,三种重金属离子几乎处于完全沉淀状态,此时对活性污泥脱氢酶活性的抑制最低。在三种重金属混合状态下,pH值为8.0时,对活性污泥微生物活性的抑制率最低。不同价态的重金属对活性污泥脱氢酶活性存在着明显的低浓度抑制效应,即在0~5 mg/L的低浓度投加段,生物体内TF含量随重金属浓度的增加下降非常明显,抑制率即达到50%~80%。而当浓度增加到5 mg/L以上时,脱氢酶活性受到的抑制相对趋于平缓与稳定。对于活性污泥微生物脱氢酶活性而言,随着暴露时间的延长,Cu2+对其的抑制率最高,其次为Cr6+和Cr3+,Ni2+最低。
[1]王卓然,王广智,耿钰萱,等.电镀废水中重金属处理的研究进展[J].电镀与环保,2017,37(1):1-3.
[2]Kumar R,Bhatia D,Singh R,etal.Metal tolerance and sequestration of Ni(II),Zn(II) and Cr(VI) ions from simulated and electroplating wastewater in batch process:Kinetics and equilibrium study[J].International Biodeterioration & Biodegradation,2012,66(1):82-90.
[3]王天行,刘晓东,喻学敏.电镀废水处理技术研究现状及评述[J].电镀与涂饰,2017(9):493-500.
[4]Yu D,Lu B,Zhai J,etal.Toxicity detection in water containing heavy metal ions with a self-powered microbial fuel cell-based biosensor[J].Talanta,2017,60(3):210-216.
[5]姚诚纯,张寒,张利华,等.金属离子对好氧活性污泥活性影响的研究现状[J].四川环境,2015,34(3):131-135.
[6]王越,翟洪艳,季民,等.Cr(Ⅵ)对活性污泥硝化活性的抑制及在污泥中的分布特点[J].环境科学学报,2015,35(5):1435-1443.
[7]张道方,魏宇,史雪飞,等.微型生物在污水回用处理中的指导作用[J].能源研究与信息,2004(3):151-155.
[8]朴永哲,黄玮,崔玉波.细菌对重金属的抗性及解毒机理研究进展[J].安全与环境学报,2015,15(6):250-254.
[9]肖巍.“环境文化”与可持续发展[J].上海理工大学学报(社会科学版),2012(4):295-298.
[10]Wang L,Liu J,Zhao Q,etal.Comparative study of wastewater treatment and nutrient recycle via activated sludge,microalgae and combination systems[J].Bioresource Technology,2016,26(13):1-5.
[11]王帆,任庆凯,田曦,等.低温城市污水活性污泥脱氢酶活性变化的试验研究[J].长春工程学院学报(自然科学版),2014(3):58-61.
[12]李迷,王素英,董世瑞,等.TTC-脱氢酶还原法测定螺旋藻细胞活性的条件优化[J].微生物学杂志,2015,35(6):33-37.
[13]荣宏伟,李权斌,张朝升,等.Cu2+对污泥微生物活性影响的恢复性研究[J].工业水处理,2016,36(7):34-38.
[14]王伟,徐艳,侯昭牧,等.Ni2+对活性污泥活性及群落多样性的影响[J].环境工程学报,2014,8(1):138-143.
[15]魏伟,李迪武,李杰,等.二价铁耦合有机碳源强化低碳源污水脱氮除磷处理[J].净水技术,2017(2):45-50.
[16]宋殿军.TTC-脱氢酶活性法测定污水厂污泥活性[J].黑龙江科技信息,2010(4):7.
[17]Liu S H,Zeng G M,Niu Q Y,etal.Bioremediation mechanisms of combined pollution of PAHs and heavy metals by bacteria and fungi:A mini review[J].Bioresource Technology,2017,27(22):25-33.
[18]Jeremic S,Beškoski V P,Djokic L,etal.Interactions of the metal tolerant heterotrophic microorganisms and iron oxidizing autotrophic bacteria from sulphidic mine environment during bioleaching experiments[J].Journal of Environmental Management,2016,44(9):151-161.
[19]Vaiopoulou E,Gikas P.Effects of chromium on activated sludge and on the performance of wastewater treatment plants:A review[J].Water Research,2012,46(3):549-570.
[20]Liu H,Zhu M,Gao S.Application of three tailing-based composites in treating comprehensive electroplating wastewater[J].Water Science & Technology,2014,70(1):47-54.
[21]Kumar R,Bhatia D,Singh R,etal.Metal tolerance and sequestration of Ni(II),Zn(II) and Cr(VI) ions from simulated and electroplating wastewater in batch process:Kinetics and equilibrium study[J].International Biodeterioration & Biodegradation,2012,66(1):82-90.
【专家点评】 废水中的重金属是影响污水生化处理效能的关键因素,论文通过试验配置电镀废水常见的三种不同重金属溶液,对活性污泥进行暴露试验,通过脱氢酶活性指示重金属对污泥微生物活性的影响,研究了不同条件下电镀废水重金属污染物对其生化单元污泥脱氢酶活性的抑制效应。论文撰写规范,试验数据分析合理,较好地表达了研究内容和结果。选题具有理论和实际意义,研究成果为电镀废水物化处理和生化处理的衔接提供参考。
