经桡动脉入径行经皮冠状动脉介入术后桡动脉慢性闭塞危险因素分析
2017-11-15毕希乐樊延明汪雁博肖宇杨王庆胜刘丽傅向华
毕希乐 樊延明 汪雁博 肖宇杨 王庆胜 刘丽 傅向华
经桡动脉入径行经皮冠状动脉介入术后桡动脉慢性闭塞危险因素分析
毕希乐 樊延明 汪雁博 肖宇杨 王庆胜 刘丽 傅向华
目的 通过分析桡动脉闭塞的原因,指导临床釆取有效的预防措施。方法 2013年11月至2014年11月共入选河北医科大学第二医院669例患者,排除63例患者(24例不符合入选标准、31例经桡动脉穿刺失败交叉到其他路径、6例失访、2例死亡)。根据术后有无桡动脉闭塞分为桡动脉闭塞组和桡动脉未闭塞组。主要终点事件为术后1年桡动脉闭塞和术后出血。建立多因素Logistic回归分析模型评价性别、体重指数、糖尿病、高血压病、高脂血症、吸烟、桡动脉直径/鞘管外径比值、桡动脉痉挛、桡动脉穿刺点距桡骨茎突距离等危险因素对桡动脉闭塞的影响。结果 最终纳入606例患者行冠状动脉造影及经皮冠状动脉介入治疗。1年随访中共发现56例桡动脉闭塞(桡动脉闭塞组),均为无症状桡动脉闭塞;未见桡动脉闭塞550例(桡动脉未闭塞组)。两组患者性别、年龄、体重指数、病变程度、危险因素、桡动脉痉挛、药物治疗、肝素剂量、术后出血及手术时间比较,差异均无统计学意义(均P>0.05)。但桡动脉闭塞组桡动脉直径/鞘管外径≤1患者的比例显著高于桡动脉未闭塞组(41.1% 比23.6%,P=0.041),差异有统计学意义。桡动脉闭塞组在穿刺点距桡骨茎突 0 cm处[28.6% (16/56)比 9.3%(51/550),P=0.002],1 cm处[25.0%(14/56)比 8.7%(48/550),P=0.001)]桡动脉闭塞发生率均显著高于桡动脉未闭塞组,但4 cm处[1.8%(1/56)比 22.7%(125/550),P=0.001)]桡动脉闭塞发生率显著低于桡动脉未闭塞组,差异均有统计学意义。建立Logistic回归分析模型评估各危险因素对桡动脉闭塞的影响,对包括性别、体重指数、吸烟、高血压病、糖尿病、高脂血症、桡动脉穿刺点距桡骨茎突距离、桡动脉痉挛、桡动脉直径/鞘管外径比值≤1等因素进行初步筛选,结果显示桡动脉穿刺点在距桡骨茎突0 cm(OR 3.08 95%CI 1.65~5.76,P=0.002)、1cm(OR 2.86 95%CI 1.49~5.52,P=0.001)和桡动脉直径 /鞘管外径比值≤ 1(OR 1.74 95%CI 1.03~2.93,P=0.036)分别是发生桡动脉闭塞的危险因素,而桡动脉穿刺点在距桡骨茎突4 cm(OR 0.08 95%CI 0.01~0.57,P=0.001)为桡动脉闭塞的保护性因素。多因素Logistic回归分析结果显示桡动脉穿刺点距桡骨茎突0 cm(OR 9.65,95%CI 1.20~77.50,P=0.033)和 1 cm(OR 8.90,95%CI 1.10~72.40,P=0.040)及桡动脉直径/鞘管外径比值≤1(OR 2.45,95%CI 1.30~4.51,P=0.004)是桡动脉闭塞发生的独立危险因素。结论 穿刺点选择在距桡骨茎突0~1 cm时发生桡动脉闭塞风险增高。
经皮冠状动脉介入治疗;桡动脉;穿刺点;危险因素
经桡动脉入径已成为我国经皮冠状动脉介入治疗(percutaneous coronary intervention, PCI)首选途径,其优势在于创伤小、出血并发症少、不影响抗栓抗凝治疗、术后无需长时间卧床、明显减轻术者及患者的心理负担等诸多优点[1-2]。但经桡动脉入径PCI术后的桡动脉闭塞发生率5%~12%[3-7],已引起介入医师的关注。避免或减少桡动脉闭塞的发生具有临床意义。桡动脉闭塞的危险因素可能与穿刺鞘直径大小、穿刺点距桡骨茎突距离、置管和压迫时间、重复手术、导管使用数量、肝素剂量等有关[8-10]。 本研究通过穿刺点位置和闭塞的关系,分析桡动脉闭塞的原因,旨在指导临床釆取有效的预防方法,降低介入操作对桡动脉结构和功能的损伤。
1 对象与方法
1.1 研究对象
连续入选2013年11月至2014年11月于河北医科大学第二医院行冠状动脉造影及PCI患者。入选标准:(1)首次经右桡动脉入径行PCI患者;(2)Allen试验正常;(3)愿意接受试验。 排除标准:(1)既往接受过经桡动脉入径行PCI患者;(2)急性ST段抬高型心肌梗死(STEMI)行直接PCI患者;(3)美国纽约心脏病学会(NYHA)分级Ⅲ~Ⅳ级;(4)外周血管疾病史;(5)右桡动脉穿刺失败者;(6)患者拒绝参加试验。
1.2 研究方法
1.2.1 分组方法
符合入选标准的患者根据术后1年随访有无桡动脉闭塞分为桡动脉闭塞组和桡动脉未闭塞组。
1.2.2 穿刺点位置和桡动脉长度测量
穿刺点位置记录为穿刺点距桡骨茎突的距离。前臂长度记录为从肘窝下2 cm到桡骨茎突间的距离,用皮尺测量并记录。前臂动脉造影后通过冠状动脉定量测量系统(quantitative coronary analysis,QCA)测定桡动脉长度。桡动脉长度定义为从肱动脉分叉处到桡骨茎突间的距离。
1.2.3 超声心动图术前和随访检查
采用美国产Terason T3000彩色超声影像系统(频率范围5~12 MHz,12L5A型探头),患者在术前行前臂桡动脉多普勒超声检查。术前并用超声心动图测量桡动脉(距桡骨茎突距离0~5 cm各点处)的直径和深度。在患者术后1年行前臂动脉多普勒超声检查评估桡动脉闭塞情况。
1.2.4 经桡动脉入径行PCI治疗
常规选取右侧桡动脉作为PCI的首选入径血管。桡动脉穿刺点选取距桡骨茎突0~5 cm,穿刺点选取搏动最强点,用2%利多卡因局麻,以20 G穿刺针采用Seldinger技术进行桡动脉血管穿刺,应用日本泰尔茂公司桡动脉穿刺套装(Terumo,Japan)。穿刺成功见回血后沿穿刺针送入0.025 in(1 in=2.54 cm)导丝,刀片切片后沿导丝置入动脉鞘管,经鞘管侧孔给予硝酸甘油200 μg,普通肝素3000 U。若行PCI,普通肝素剂量至100 U/kg,维持活化凝血时间(activated clotting time, ACT )250~300 s。冠状动脉造影常规应用4 F或5 F造影导管(Terumo,Japan)。冠状动脉血管成形术应用6 F指引导管,术后立即拔除桡动脉鞘管,用三层纱布卷叠层并用三条胶带固定压迫穿刺点处6 h,每隔2 h松开一条胶带放松压迫[11]。如无禁忌PCI术后常规给予阿司匹林和氯吡格雷双联抗血小板治疗。
1.2.5 研究终点事件
主要终点事件为术后1年桡动脉闭塞和术后出血。出血定义为穿刺点处的皮下出血或血肿。
1.3 统计学分析
所有数据采用SPSS13.0统计软件进行处理。连续变量的正态分布计量资料以均数±标准差表示,非正态分布者以四分位数表示。计数资料以百分率表示。两组间数据资料比较时,正态分布的计量资料比较采用student t检验,不符合正态分布的计量资料使用Mann-Whitney U检验。计数资料的比较使用卡方检验。以p<0.05为差异有统计学意义。建立Logistic回归分析模型评估各危险因素对桡动脉闭塞的影响,首先性别、体重指数、吸烟、高血压病、糖尿病、高脂血症、桡动脉穿刺点距桡骨茎突距离、桡动脉痉挛、桡动脉直径/鞘管外径比值等因素进行初步筛选,应用单因素Logistic回归分析采用Enter法计算没有校正的OR值,初步筛选桡动脉闭塞危险因素。然后将单因素分析中有意义的变量和临床上认为对桡动脉闭塞有影响的变量纳入多因素Logistic回归分析模型,应用向后逐步法(Backward LR,Entry 0.05,Removal 0.10)确定桡动脉闭塞的危险因素。变量设置如下:桡动脉直径/鞘管外径比值(0表示桡动脉直径/鞘管外径比值>1,1表示桡动脉直径/鞘管外径比值≤1),穿刺点位置进行再分类(桡动脉穿刺点距桡骨茎突距离,0代表5 cm,1代表4 cm,2代表3 cm,3代表2 cm,4代表1 cm,5代表0 cm,选用Indicator first对比模式)。
2 结果
2.1 两组基线临床资料特征比较(表1)
2013年11月至2014年11月共入选669例患者,排除63例患者(24例不符合入选标准、31例经桡动脉穿刺失败交叉到其他路径、6例失访、2例死亡),最终纳入606例患者。1年随访中共发现56例桡动脉闭塞(桡动脉闭塞组),均为无症状桡动脉闭塞;未见桡动脉闭塞550例(桡动脉未闭塞组)。两组患者性别、年龄、体重指数、病变程度、危险因素、桡动脉痉挛、药物治疗、肝素剂量、术后出血及手术时间比较,差异均无统计学意义(均P >0.05)。但桡动脉闭塞组桡动脉直径/鞘管外径≤1患者的比例显著高于桡动脉未闭塞组(41.1% 比23.6%,P=0.041)显著高于桡动脉未闭塞组,差异有统计学意义。
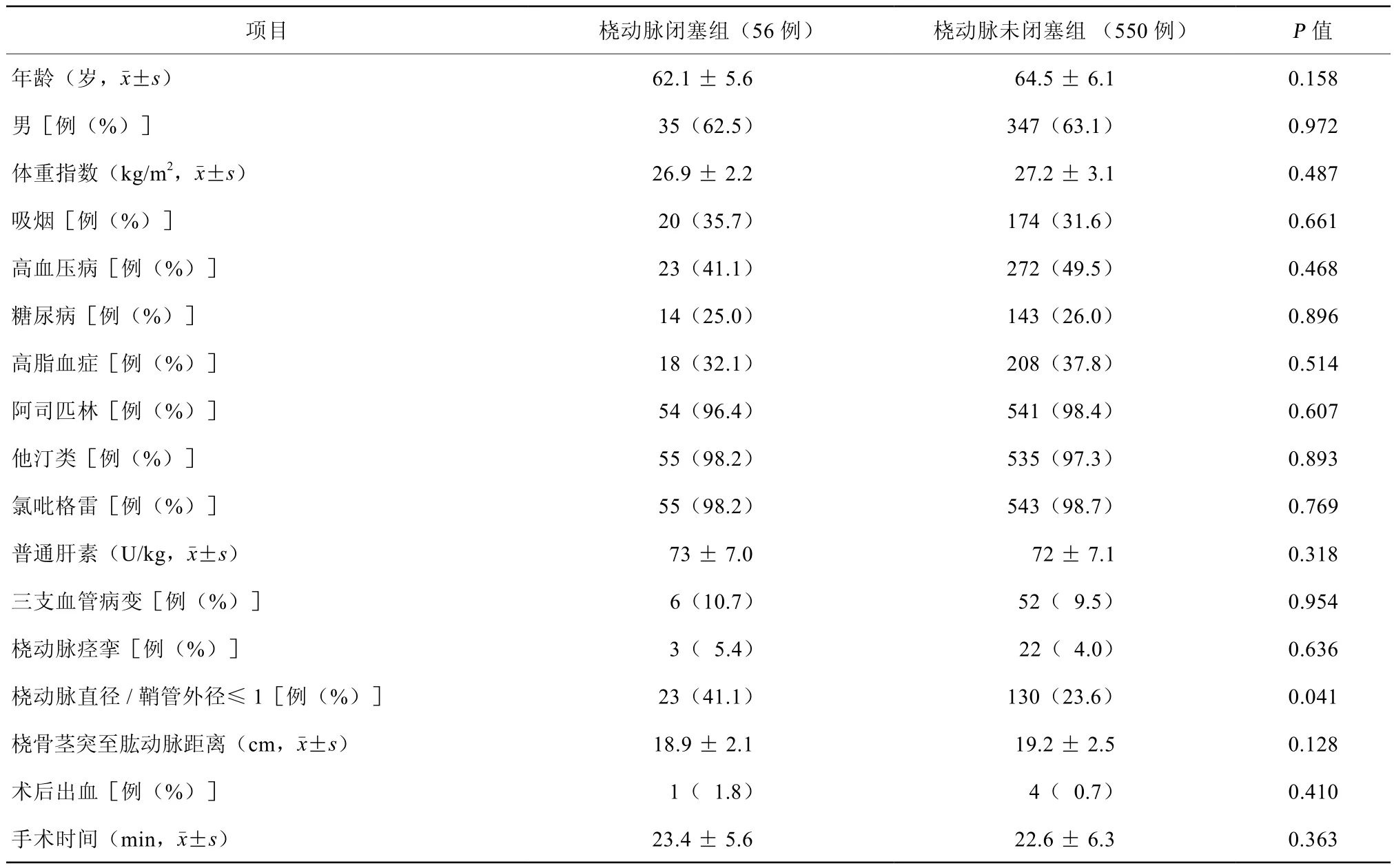
表1 两组基线临床资料特征比较
2.2 两组患者穿刺点发生桡动脉闭塞情况比较
桡动脉闭塞组在穿刺点距桡骨茎突 0 cm处[28.6% (16/56)比 9.3%(51/550),P =0.002],穿刺点距桡骨茎突1 cm处[25.0%(14/56)比 8.7%(48/550),P=0.001)]桡动脉闭塞发生率均显著高于桡动脉未闭塞组,但穿刺点距桡骨茎突4 cm处桡动脉闭塞发生率显著低于桡动脉未闭塞组[1.8%(1/56)比 22.7%(125/550),P=0.001)],差异均有统计学意义(表2)。
2.3 桡动脉闭塞Logistic回归分析
建立Logistic回归分析模型评估各危险因素对桡动脉闭塞的影响,对性别、体重指数、吸烟、高血压、糖尿病、高脂血症、桡动脉穿刺点距桡骨茎突距离、桡动脉痉挛、桡动脉直径/鞘管外径比值≤1等因素进行初步筛选,结果显示桡动脉穿刺点在距桡骨茎突 0 cm(OR 3.08 95%CI 1.65~5.76,P=0.002)、1 cm(OR 2.86 95%CI 1.49~5.52,P =0.001)和桡动脉直径/鞘管外径比值≤1(OR 1.74 95%CI 1.03~2.93,P =0.036)分别是发生桡动脉闭塞的危险因素,而桡动脉穿刺点在距桡骨茎突4 cm(OR 0.08 95%CI 0.01~0.57,P=0.001)为桡动脉闭塞的保护性因素(表3)。
多因素Logistic回归分析结果显示桡动脉穿刺点距桡骨茎突 0 cm(OR 9.65,95%CI 1.20~77.50,P=0.033) 和 1 cm(OR 8.90,95%CI 1.10~72.40,P=0.040)及桡动脉直径/鞘管外径比值≤1(OR 2.45,95%CI 1.30~4.51,P=0.004)是桡动脉闭塞发生的独立危险因素。

表2 两组患者穿刺点发生桡动脉闭塞情况比较[例(%)]

表3 桡动脉闭塞单因素Logistic回归分析
3 讨 论
经桡动脉入径具有微创不需卧床和出血并发症少等优点,已经成为我国PCI治疗首选入径。但桡动脉细小,易因鞘管和导管摩擦发生动脉内皮功能损伤甚至闭塞。本研究旨在重点分析经桡动脉入径术后穿刺点位置对桡动脉闭塞的影响。
本研究通过对经桡动脉入径术后1年随访发现桡动脉闭塞发生率在穿刺点距桡骨茎突0~1 cm明显高于穿刺点距桡骨茎突≥2 cm的患者,超声心动图发现桡动脉闭塞均是在桡动脉近端和接近肱动脉分叉处发生血流中断,与Lanspa等[12]研究中前臂动脉造影显示桡动脉闭塞发生在近端一致,但研究目的是在桡动脉闭塞时尝试尺动脉的可能性,并未进一步探讨桡动脉闭塞位置的原因。本研究试图通过闭塞位置角度出发进行分析桡动脉闭塞的原因和影响因素。本研究通过超声心动图测得右侧桡动脉直径在距桡骨茎突0~5 cm范围内相似(2.78~2.88 mm),桡动脉深度从远端到近端是不断增加(2.50~4.52 mm),随着桡动脉深度的增加并未增加前臂出血并发症发生率。本研究定义为从肱动脉分叉处至桡骨茎突(19.0±2.2)cm,应用6 F桡动脉鞘长度为16 cm,可见鞘长度小于桡动脉长度,即在桡动脉内置入鞘管后,桡动脉近段必然存在一个无鞘保护的区域。所以,随着穿刺点位置的选择不同,会导致桡动脉近段的无鞘保护区域发生变化,即穿刺点越靠近桡动脉远端,则桡动脉无鞘保护区域越增加;反之,穿刺点越靠近桡动脉近端,桡动脉无鞘保护区域会相应减少。本研究通过超声心动图发现桡动脉闭塞均是在桡动脉近端和接近肱动脉分叉处发生血流中断,桡动脉闭塞的直接原因是桡动脉内血栓形成,所以闭塞起始部位会存在血栓形成。Lanspa等[12]和 Kedev等[13]均经过前臂造影显示桡动脉闭塞发生在桡动脉近段和接近肱动脉分叉处,但两位学者研究目的并不是观察桡动脉闭塞位置问题,但通过前臂造影和超声心动图共同发现桡动脉闭塞段位于桡动脉近端和接近肱动脉分叉处,进一步证据表明桡动脉近段无鞘保护区域的血管内皮是易受损伤的。
Yonetsu等[14]研究发现桡动脉内膜撕裂超过50%发生在桡动脉中段区域(即距穿刺点9~16 cm)和鞘管外至桡肱动脉分叉处区域(即距穿刺点16 cm至肱动脉分叉处区间),说明桡动脉内膜损伤并不局限在穿刺点周围,而是桡动脉全程包括有鞘保护区域和无鞘保护区域都存在很高的内膜损伤发生率。桡动脉远端中膜损伤可能与穿刺和桡动脉鞘的置入过程有关,桡动脉近端无鞘保护区域中膜损伤发生率高可能与导管的前送和后撤损伤有关。Heiss等[15]研究认为经桡动脉入径PCI术中导管数量增加会引起肱动脉远端内皮功能损伤,内皮功能受损不再仅仅局限在桡动脉置入鞘管处,而是全程包括肱动脉远端,并与导管使用数量有关。因桡动脉鞘的长度短而不能完全覆盖桡动脉全程,所以在桡动脉近端无鞘保护区域可能由于内皮广泛摩擦受损而发生血栓聚集。可以推测桡动脉远端的穿刺和鞘管置入损伤是一次性的,而桡动脉近段的损伤是导管反复摩擦刺激造成的,损伤的形式不同可能会对血管内皮造成的后果不一样。有些血栓聚集在早期经过抗凝治疗是可以恢复的。Uhlemann等[16]研究报道445例经桡动脉入径PCI治疗患者在术后1~2 d超声心动图检查显示共113例桡动脉闭塞,其中54例接受抗凝药物治疗者中17例(31.5%)再通,37例未接受抗凝治疗者中2例(5.4%)再通,桡动脉闭塞总再通率为20.9%。
Uhlemann等[16]研究发现应用 6 F桡动脉鞘组比5 F桡动脉鞘组明显增加闭塞率(30.5% 比13.7%,p<0.001)。该研究中使用的是欧洲版泰尔茂穿刺套装,较我国常规用的鞘管外径小。该研究6 F鞘管外径2.10mm,5 F鞘管外径1.92mm,鞘管外径大显然会增加血管内皮的损伤,但该研究未测量桡动脉置鞘前的基础血管直径,因此无法解释是否血管直径与鞘管直径不匹配是导致桡动脉闭塞的原因。在临床实践中也发现当基础桡动脉直径大于鞘管外径时仍会有闭塞发生,也不能完全用鞘管外径与血管直径不匹配解释桡动脉闭塞发生的原因。
此外,桡动脉痉挛时血管狭窄会加重鞘管置入或导管通过时对桡动脉内皮的摩擦损伤。桡动脉直径小时容易诱发痉挛,也可能导致血管闭塞[17]。桡动脉闭塞是一个多因素作用的结果。本研究在术前并未排除桡动脉直径小于鞘管外径的人群,有可能影响到桡动脉闭塞结果。本研究冠状动脉造影常规给予3000 U肝素,相比国外5000 U肝素剂量偏小,也有可能对桡动脉闭塞结果造成偏倚。考虑到临床手术主要由4名术者完成,不同术者间可能会产生结果偏倚。本研究为回顾性单中心研究,样本量偏小,在统计效力上会存在一定的偏差,仍有待扩大样本量,延长随访时间进一步证实。
[1] Valgimigli M, Saia F, Guastaroba P, et al. Transradial versus transfemoral intervention for acute myocardial infarction: a propensity score-adjusted and-matched analysis from the REAL (REgistro regionale AngiopLastiche dell'Emilia-Romagna) multicenter registry. JACC Cardiovasc Interv, 2012 ,5(1):23-35.
[2] Jolly SS, Niemelä K, Xavier D, et al. Design and rationale of the radial versus femoral access for coronary intervention (RIVAL)trial: a randomized comparison of radial versus femoral access for coronary angiography or intervention in patients with acute coronary syndromes. Am Heart J, 2011,161(2):254-260.
[3] Sławin J, Kubler P, Szczepański A, et al. Radial artery occlusion after percutaneous coronary interventions-an underestimated issue.Postepy Kardiol Interwencyjnej, 2013,9(4):353-361.
[4] Lisowska A, Knapp M, Tycińska A, et al. Radial access during percutaneous interventions in patients with acute coronary syndromes: should we routinely monitor radial artery patency by ultrasonography promptly after the procedure and in long-term observation? Int J Cardiovasc Imaging, 2015,31(1):31-36.
[5] Sanmartin M, Gomez M, Rumoroso JR, et al. Interruption of blood fl ow during compression and radial artery occlusion after transradial catheterization. Catheter Cardiovasc Interv, 2007,70(2):185-189.
[6] Bertrand OF, Rao SV, Pancholy S, et al. Transradial approach for coronary angiography and interventions: results of the fi rst international transradial practice survey. JACC Cardiovasc Interv,2010,3(10):1022-1031.
[7] Shen H, Zhou YJ, Liu YY, et al. Assessment of early radial injury after transradial coronary intervention by high-resolution ultrasound biomicroscopy: innovative technology application. Chin Med J (Engl),2012,125(19):3388-3392.
[8] Plante S, Cantor WJ, Goldman L, et al. Comparison of bivalirudin versus heparin on radial artery occlusion after transradial catheterization. Catheter Cardiovasc Interv, 2010,76(5):654-658.
[9 ] Tuncali BE, Kuvaki B, Tuncali B, et al. A comparison of the eff i cacy of heparinized and nonheparinized solutions for maintenance of perioperative radial arterial catheter patency and subsequent occlusion.Anesth Analg, 2005,100(4):1117-1121.
[10] Kindel M1, Rüppel R. Hydrophilic-coated sheaths increase the success rate of transradial coronary procedures and reduce patient discomfort but do not reduce the occlusion rate: randomized single-blind comparison of coated vs. non-coated sheaths. Clin Res Cardiol, 2008,97(9):609-614.
[11] Pancholy S, Coppola J, Patel T, et al. Prevention of radial artery occlusion-patent hemostasis evaluation trial (PROPHET study): a randomized comparison of traditional versus patency documented hemostasis after transradial catheterization. Catheter Cardiovasc Interv, 2008,72(3):335-340.
[12] Lanspa TJ, Reyes AP, Oldemeyer JB, et al. Ulnar artery catheterization with occlusion of corresponding radial artery.Catheter Cardiovasc Interv, 2004,61(2):211-213.
[13] Kedev S, Zaf i rovska B, Dharma S, et al. Safety and feasibility of transulnar catheterization when ipsilateral radial access is not available. Catheter Cardiovasc Interv, 2014,83(1):E51-60.
[14] Yonetsu T, Kakuta T, Lee T, et al. Assessment of acute injuries and chronic intimal thickening of the radial artery after transradial coronary intervention by optical coherence tomography.Eur Heart J, 2010,31(13):1608-1615.
[15] Heiss C, Balzer J, Hauffe T, et al. Vascular dysfunction of brachial artery after transradial access for coronary catheterization: impact of smoking and catheter changes. JACC Cardiovasc Interv, 2009 ,2(11):1067-1073.
[16] Uhlemann M, Möbius-Winkler S, Mende M, et al. The Leipzig prospective vascular ultrasound registry in radial artery catheterization:impact of sheath size on vascular complications. JACC Cardiovasc Interv, 2012,5(1):36-43.
[17] Fukuda N, Iwahara S, Harada A, et al. Vasospasms of the radial artery after the transradial approach for coronary angiography and angioplasty. Jpn Heart J, 2004,45(5):723-731.
Predictors of chronic radial artery occlusion after transradial catheterization
BI Xi-le,FAN Yanming,WANG Yan-bo,XIAO Yu-yang,WANG Qing-sheng, LIU li,FU Xiang-hua.
Department of Cardiology, the Second Hospital of Hebei Medical University,Shijiazhuang 050000,China
BI Xi-le,Email:bixile@163.com
Percutaneous Coronary Intervention; Radial Artery; Puncture Site; Risk Factors
R541.4
10. 3969/j. issn. 1004-8812. 2017. 10. 006
河北省医学科学研究重点课题计划(20170223)
050000 河北石家庄,河北医科大学第二医院心内科(毕希乐,樊延明, 汪雁博,肖宇杨,傅向华);秦皇岛市第一医院心内科(毕希乐,王庆胜,刘丽)
毕希乐,Email:bixile@163.com
本研究为第一作者在研究生期间所完成
【Abstrsct】 Objective To investingate the possible predictory of radial artery occlusion(RAO)after transradial approach and its preventive measures. Methods We prospectively assessed the occurrence of RAO in 669 consecutive patients undergoing transradial approach and 63 patients were excluded from the fi nal study(24of them did not meet the inclusion criterium, 31 patients converted to other artery approaches,6 patients lost clinical follow-up and 2 patients died). Artery occlusion was evaluated with Doppler ultrasound in 2 days and 1 year after the intervention. The risk factors of RAO including sex, body mass index(BMI), smoking, hypertension, diabetes, dyslipidemia, puncture site, vessel spasm, and artery diameter/sheath ratio were evaluated using a multivariate model analysis. Results Among the 606 patients, RAO occurred in 56 patients. There were no differences in sex ,age ,BMI ,coronary lesions,rates of vessel spasm,vessel length ,medication given and operation time between the 2 group of patients with vs without ROA(all P>0.05).Univariate logistic analysis showed puncture site at 0 cm away from radial styloid and artery diameter/sheath ratio ≤1 were possible risk factory and puncture site > 4 cm from radial styloid was possible protective factor. Further multivariate analysis showed the odds ratio(OR)for occlusion risk at 0 cm and 1 cm were 9.65(P=0.033)and 8.90(P=0.040), respectively. The RAO occurred in the ratio of the arterial diameter to the sheath diameter ≤1 (OR=2.45,P=0.004). Conclusions Distal puncture sites(0–1 cm away from the radius styloid process)can lead to a higher rate of RAO.
2017-02-08)
