探讨医用胶细胞毒性试验方法的选择
2017-08-10田小俊田胜慧郑保婷徐红蕾广东省医疗器械质量监督检验所广东广州510663
田小俊 田胜慧 郑保婷 徐红蕾 广东省医疗器械质量监督检验所 (广东 广州 510663)
探讨医用胶细胞毒性试验方法的选择
田小俊 田胜慧 郑保婷 徐红蕾 广东省医疗器械质量监督检验所 (广东 广州 510663)
目的:分析不同细胞毒性试验方法对医用胶细胞毒性评价的影响。方法:用浸提液法、直接接触法、间接接触法对α-氰基丙烯酸酯类粘合剂和多糖纤维素医用胶液进行细胞毒性试验,比较不同试验方法对其细胞毒性评价的影响。结果:同种样品采用不同试验方法得出的细胞毒性结果不同。结论:细胞毒性试验方法的选择应根据样品的物理性质和用途,尽量模拟临床使用情况进行选择。
医用胶 细胞毒性 试验方法
细胞毒性试验具有简便、快速、敏感性高的特点,是医疗器械进行临床安全性评价前的首选和必选试验项目。GB/ T 16886.5-2003规定了三类体外细胞毒性试验:浸提液试验、直接接触试验、间接接触试验[1]。GB/T 16886.12-2005也规定了细胞毒性试验所要遵循的样品制备和参照样品的选择要求,指出不同物理形态的医疗器械应按照以上两份标准要求选择合适的样品制备方法和细胞毒性试验方法[2]。
对于以α-氰基丙烯酸酯类粘合剂为代表的原位聚合类产品,和以多糖纤维素医用胶液为代表的液态产品,如何按照标准要求,选择合适的试验方法才能科学合理地评价其细胞毒性?本文做了一系列对比实验,并对如何选择这两类产品的细胞毒性试验方法进行了探讨。
1.材料与方法
1.1 材料
试验样品:α-氰基丙烯酸酯快速医用胶(1号);α-氰基丙烯酸酯医用粘合剂(2号);多糖纤维素医用胶液(3号)。
细胞:ATCC CCL1小鼠成纤维细胞(中科院上海细胞与生物化学研究所)。
主要试剂:RPMI-1640培养基(美国Hyclone公司),小牛血清(Gibco),琼脂培养基,中性红染色液。
1.2 方法
1.2.1 浸提液法:①样品浸提液制备:成膜后浸提法。将样品均匀的滴在直径9 cm平板上,按6 cm2/mL的比例充入不含血清的RPMI-1640培养基,(37±1)˚C下浸提(24±2)h备用。直接浸提法。将样品分别按0.2g/mL或0.1g/mL的比例滴入不含血清的RPMI-1640培养基,静置10 min后,(37±1)˚C下浸提(24±2)h备用;②空白对照液:RPMI-1640培养基;③阴性对照液:高密度聚乙烯;④阳性对照:5g/L苯酚溶液。⑤试验方法:按照GB/ T 14233.2-2005规定的MTT试验方法进行。将1×104/mL细胞悬液接种于96孔板,每孔100 μL[3]。置CO2培养箱37˚C培养24h后,弃去原培养液。加入样品浸提液,每孔100 μL,置CO2培养箱37˚C培养72h。⑥细胞毒性分级:每孔加入20 μL 5 g/L的MTT溶液,培养4 h后弃去孔内液体,加入150 μL DMSO,在酶标仪570 nm和630 nm双波长下测定吸光度(OD值)。按下式计算细胞相对增殖率(RGR):

注:RGR:相对增殖率,%;A:供试品组(阴性组、阳性组)吸光度;A0:空白对照组吸光度。
根据GRG按表1分级标准判定。阴性对照组的反应不大于1级,阳性对照组的反应至少为3级时,判定结果可靠。

表1. MTT法细胞毒性反应分级
1.2.2 直接接触法:①样品制备:按照GB/T 16886.5-2003规定,将滤纸片裁剪成表面积约100mm2的片状,沾取适量液体样品作为试验样品;②阴性对照:将滤纸片裁剪成表面积约100mm2的片状,沾取适量RPMI-1640培养基作为阴性对照;③阳性对照:将表面积约100mm2的滤纸片浸透20%苯酚溶液作为阳性对照。④试验方法:将细胞按1.5×105/mL的密度接种于直径35mm的培养皿,置5%的CO2培养箱37˚C培养至近汇合单层细胞形成。弃去原培养液,加入2mL新鲜培养基,在培养皿中央部位的细胞层上放置一片试验样品,继续培养24h、48h。⑤细胞毒性分级/计分:根据GB/T 16886.5-2003给出的细胞毒性定性评价计分方法分级(见表2)。

表2. 间接接触法和直接接触法试验细胞毒性反应分级
1.2.3 间接接触法:样品制备、阴性对照、阳性对照及细胞毒性分级/计分同直接接触法。试验方法:将细胞按1.5×105/mL的密度接种于六孔板,每孔2 mL。置5%的CO2培养箱37˚C培养至近汇合单层细胞形成。弃去培养基,取琼脂培养基注入培养皿。每皿加入1 mL中性红染色液,置培养箱中避光保持20 min。弃去多余染色液,将试验样品放在琼脂表面。每孔放1个样品,每组3孔,置培养箱继续培养24h、48h。培养结束后,在培养皿底部标出试验样品轮廓,除去琼脂表面试样。将培养皿置显微镜下观察细胞区域褪色现象。
2.结果
浸提液法细胞相对增值率及细胞毒性评级见表3,直接接触法和间接接触法细胞毒性评级见表4。
3.讨论
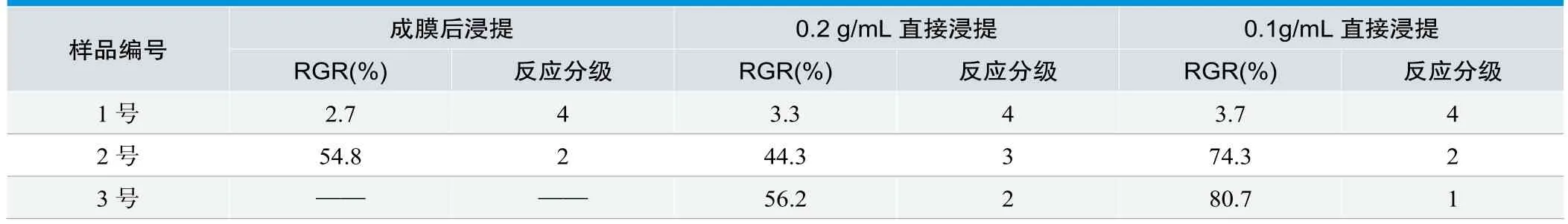
表3. 浸提液法细胞相对增值率及细胞毒性评级

表4. 直接接触法和间接接触法细胞毒性评级
3.1 同种方法不同样品细胞毒性结果分析
从表3可以看出,1号、2号、3号样品无论是成膜后浸提,还是直接浸提,1号样品的细胞相对增值率RGR均低于4%,反应分级为4级,表现出重度细胞毒性。这可能是由于1号样品含有较多的小分子添加剂、单体或低聚物,浸提液中含有较多的此类物质,细胞培养过程中,严重破坏细胞膜,导致细胞凋亡或影响细胞增殖。
从表3也可以看出,无论是哪种浸提方式,1号、2号、3号样品的细胞毒性依次减小。这说明,医用胶液的组成成分会直接影响细胞毒性结果,后续需对产品组成成分做进一步分析,证实不同成分物质对产品细胞毒性的影响。另外,表3结果还表明,同为α-氰基丙烯酸酯类医用胶的1号和2号样品比多糖纤维素医用胶液的3号样品细胞毒性大,这与多糖类高分子材料比聚丙烯酸酯类高分子材料具有更好的生物相容性有关。同时,两类产品的主要用途也有所差别,多糖生物医用胶液主要用于创面的冲洗,起到润滑隔离及生物屏障作用,从而利于创面组织的修复,而氰基丙烯酸酯类医用胶主要利用其快速粘结特点,封闭创面,促进创面修复。
从表3还可以看出,2号、3号样品的细胞毒性随浸提液浓度的降低而降低。这说明浸提时样品比例的选择对试验结果产生直接影响,实验时务必按照标准要求,或经验证的合理的浸提比例进行浸提,科学合理有效的评价产品的细胞毒性。
3.2 不同方法同种样品细胞毒性结果分析
对比分析表3和表4可以看出,同种样品不同细胞毒性试验方法的结果中,采用浸提液法试验测得的细胞毒性最大,采用间接接触法测得的细胞毒性最小。这表明,细胞毒性试验方法的选择对产品细胞毒性评价起决定性作用,也间接表明科学合理有效的评价医用胶细胞毒性的关键在于采用合适的试验方法。
在评价原位聚合的医疗器械产品(如医用粘合剂)时,应尽量模拟材料的使用条件对样品进行试验,以提供治疗过程中聚合物的反应组分的潜在毒性信息。试验方法中使用浸提液来评价原位固化的材料,浸提过程应从材料被置于原位固化点开始[4]。但是,这种方法所得的试验液含有比临床应用更高浓度的α氰基丙烯酸辛酯单体、低聚物,以及添加剂医用级聚甲基丙烯酸甲酯,这些物质是产生细胞毒性的主要物质,虽然能最大限度地提供治疗过程中医用胶的潜在细胞毒性信息,但所得的细胞毒性试验结果不能完全代表产品在临床使用过程中产生的细胞毒性。
3.3 细胞毒性试验方法的选择
GB/T 16886.5-2003医疗器械生物学评价 第5部分:体外细胞毒性试验 规定的体外细胞毒性试验分为三类:浸提液试验、直接接触试验、间接接触试验。三种方法对样品的制备方法要求不同,具体操作也有所差别,但基本都是对材料中存在的可溶出的毒性物质进行试验,一般包括原料单体、低分子聚合物、塑化剂、催化剂、稳定剂、乳化剂等。试验方法直接决定了样品制备、细胞制备、样品/细胞/浸提液之间的接触方法等。三类方法各具特点,也有各自的局限性[5,6]。试验方法的选择需要尽量模拟样品实际使用情况或严于样品实际使用情况,达到有效评价样品细胞毒性的目的。对于医用胶类原位聚合产品而言,直接接触法为模拟临床使用的最佳细胞毒性评价方法,但任何单项试验结果都不宜作为推断样品是否安全的唯一依据。
细胞毒性试验方法的选择对产品细胞毒性评价起决定性作用,科学合理有效的评价医用胶细胞毒性的关键在于采用合适的试验方法。在评价医用粘合剂这类原位聚合产品时,应尽量模拟材料的使用条件对样品进行试验。
[1] 国家药品监督管理局. GB/T 16886.5-2003 医疗器械生物学评价 第5部分:体外细胞毒性试验[S]. 北京:中国标准出版社, 2003.
[2] 国家食品药品监督管理局. GB/T 16886.12-2005 医疗器械生物学评价 第12部分:样品制备与参照样品[S]. 北京:中国标准出版社, 2005.
[3] 国家食品药品监督管理局. GB/T 14233.2-2005医用输液、输血、注射器具检验方法 第2部分:生物学试验方法[S]. 北京:中国标准出版社, 2006.
[4] 奚廷斐. 医疗器械生物学评价[M]. 北京:中国质检出版社, 中国标准出版社, 2012:94.
[5] 李瑞, 王青山. 生物材料生物相容性的评价方法和发展趋势[J]. 中国组织工程研究与临床康复, 2011,15(29):5471-5474.
[6] 贾文英, 史弘道. 细胞毒性试验评价医用装置生物相容性的研究概况[J]. 实用美容整形外科杂志, 2001,12(5):253-255.
The Research of Cytotoxicity Test Methods Selection of Medical Adhesive
TIAN Xiao-jun TIAN Sheng-hui ZHENG Bao-ting XU Hong-lei Guangdong Medical Devices Quality Surveillance and Test Institute (Guangdong Guangzhou 510663)
Objective: to analyze the impact of different cell toxicity test methods on the cytotoxicity of medical adhesive. Methods: in vitro cytotoxicity of cyanoacrylate adhesive and polysaccharide cellulose medical solution were tested by the extract liquid method , the direct contact method and the indirect contact method, then comparing the results of different testing methods. Results: the cytotoxicity results of same sample were different by using different test methods. Conclusion: the in vitro cytotoxicity test methods should be selected according to the physical properties of the sample and usage, to simulate the clinical usage as far as possible.
medical adhesive, cytotoxicity, test method
1006-6586(2017)11-0058-03
R197.39
A
2017-02-23
快速医用胶生物安全耐受性检测方法研究(广东省科技计划项目,项目编号:2012B061700112)。
