β—榄香烯纳米聚合物胶束包封率、载药量及释药性测定
2017-03-04王静李学涛袁子民
王静 李学涛 袁子民

摘要:目的 建立β-榄香烯纳米聚合物胶束包封率和载药量的RP-HPLC测定方法,并对其释药性进行考察。方法 以二硬脂酰磷脂酰乙醇胺-聚乙二醇2000(DSPE-PEG2000)为载体材料制备载药胶束,采用石油醚萃取法测定包封率和载药量,采用透析法对其释药性进行研究。结果 所制备的β-榄香烯纳米聚合物胶束平均包封率为89.47%,平均载药量为8.33%,体外释药缓慢。结论 包封率和载药量的测定简便、准确,所制得的胶束具有缓释作用。
关键词:β-榄香烯纳米聚合物胶束;包封率;载药量;释药性
DOI:10.3969/j.issn.1005-5304.2017.02.023
中图分类号:R284.1 文献标识码:A 文章编号:1005-5304(2017)02-0091-03
榄香烯是临床常用的中药广谱抗肿瘤药物,该药及其脂质体注射液和口服乳制剂通过抗增殖和诱导凋亡作用,在体外及临床用于脑胶质瘤治疗方面取得了较好治疗效果,但也存在一定不良反应[1-3]。β-榄香烯是由榄香烯经精馏后去除γ、δ-榄香烯异构体,得到的抗癌单体有效成分[4]。为增加β-榄香烯对血脑屏障的透过性及其载药制剂在肿瘤组织的通透和滞留增强效应,本课题组以二硬脂酰磷脂酰乙醇胺-聚乙二醇(DSPE-PEG2000)为载体材料,将其制成抗脑胶质瘤的新型脑靶向制剂,本研究对其包封率、载药量进行测定,并考察其体外释药性,为进一步控制本品质量、优化制备工艺及其应用提供依据。
1 仪器与试药
Agilent 1100高效液相色谱仪(美国安捷伦公
司),CENCO型涡旋仪(荷兰Breda公司),RCZ-6B3型药物溶出度仪(改装为释放溶出仪,上海黄海药检仪器有限公司),85-1型集热式恒温加热磁力搅拌器(江苏省金坛市友联仪器研究所),透析袋(截留分子量8000~15 000,上海华蓝生物科技有限公司),旋转蒸发器RE-52A(上海亚荣生化仪器厂)。
β-榄香烯原料药(含量>98%,自制),β-榄香烯对照品(中国食品药品检定研究院,批号100268- 200401,供含量测定用),DSPE-PEG2000(上海艾韦特医药科技有限公司,批号20150922),甲醇为色谱纯,其余均为分析纯。
2 方法与结果
2.1 β-榄香烯纳米聚合物胶束及空白胶束的制备
采用薄膜水化法制备。精密称取处方量的DSPE-PEG2000载体材料100 mg、β-榄香烯原料药10 mg,置于茄形瓶中,加10 mL甲醇溶解,摇匀,于35 ℃旋转蒸发真空干燥除去甲醇,在茄形瓶底部及内壁形成一层均匀的脂膜,加入pH 7.4磷酸盐缓冲液5 mL,在40 ℃水浴中水化30 min,冷却至室温,经0.2 ?m聚碳酸酯膜过滤,即得透明的β-榄香烯纳米聚合物胶束(β-ELE-DSPE-PEG2000-PMs)[5-6]。同法制备不加β-榄香烯原料药的空白胶束。
2.2 包封率和载药量的测定
2.2.1 色谱条件 色谱柱为DiamonsilTM C18(5 μm, 200 mm×4.6 mm),流动相为甲醇-水(95∶5),流速1.0 mL/min,柱温35 ℃,检测波长210 nm。
2.2.2 对照品溶液的制备 精密称取β-榄香烯对照品8.30 mg置于10 mL量瓶中,加入甲醇溶解并稀释至刻度,摇匀,即得。
2.2.3 供试品溶液制备及包封率、载药量测定 精密量取β-ELE-DSPE-PEG2000-PMs 1 mL置25 mL量瓶中,加入适量甲醇溶解并稀释至刻度,摇匀,过0.45 μm微孔滤膜,即得载药胶束供试品溶液,测定胶束中总的药物量(W1)。同法制成空白膠束对照溶液。另精密量取β-ELE-DSPE-PEG2000-PMs 1 mL于5 mL离心管中,加入石油醚(30~60 ℃)3 mL,摇匀,涡旋3 min,静置,待分层后,弃去石油醚层,同法重复萃取1次,除去未包封的游离β-榄香烯。将下层胶束加入适量甲醇溶解,转移至25 mL量瓶中并稀释至刻度,摇匀,过0.45 μm微孔滤膜,测定石油醚萃取后包封的β-榄香烯药物量(W2),计算包封率(EE),EE(%)=W2/W1×100%[5-6]。载药量(DL)即胶束中单位质量的DSPE-PEG2000可以包封的药物,DL(%)=W2/W×100%,W为DSPE-PEG2000加入量。
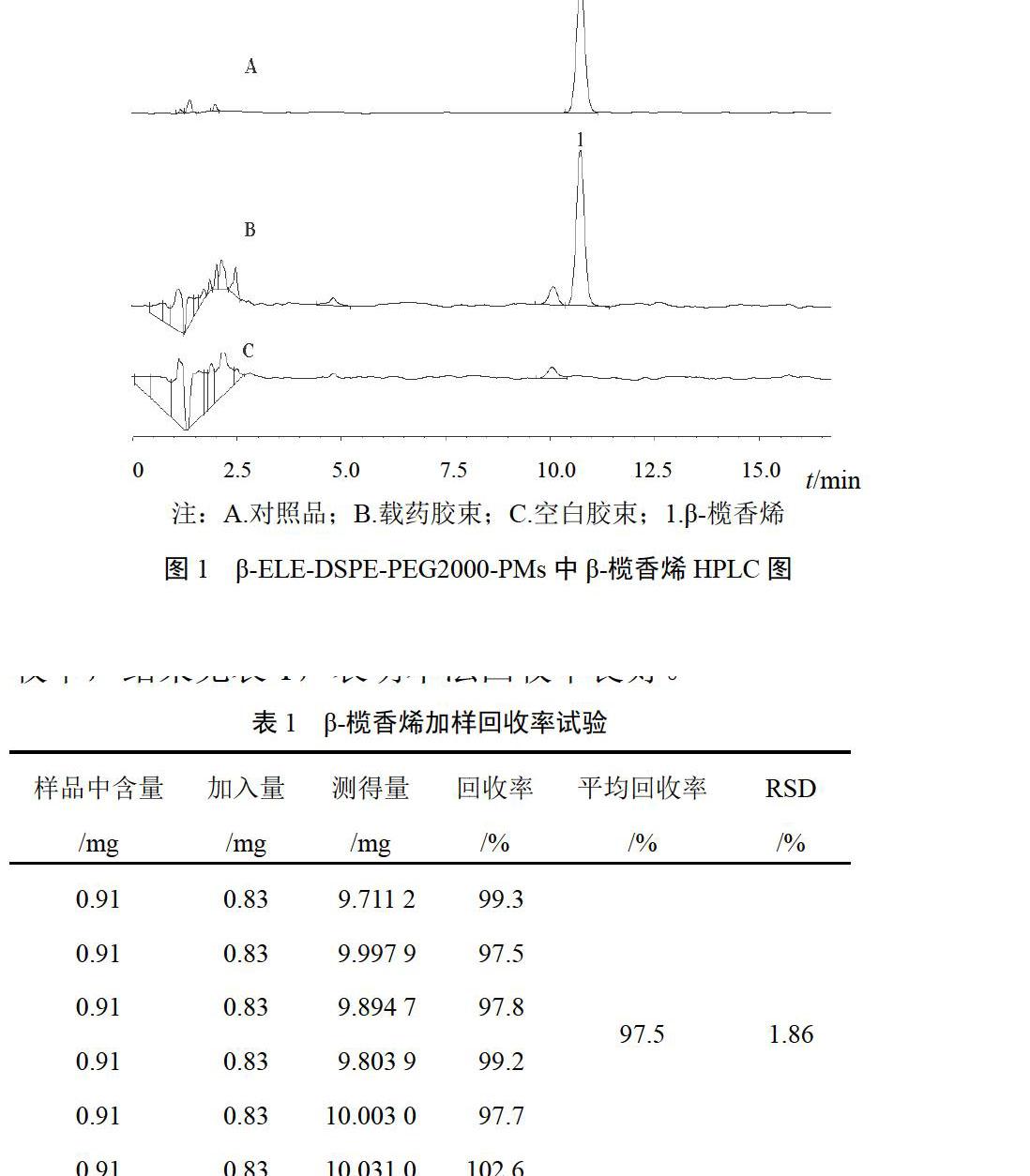
2.2.4 空白干扰试验 精密吸取上述对照品溶液、载药胶束供试品溶液、空白胶束溶液各10 μL,按上述色谱条件测定,结果空白胶束对本品含量测定无干扰。色图谱见图1。
2.2.5 线性关系考察 分别精密量取“2.2.2”项下对照品溶液0.1、0.25、0.5、1.0、1.5、2.5 mL于10 mL量瓶中,分别加甲醇稀释至刻度,摇匀,分别精密吸取10 μL,注入液相色谱仪,记录峰面积。以对照品浓度为横坐标,峰面积为纵坐标,绘制标准曲线,得回归方程Y=4.129 9X+6.902 1,r=0.999 8。结果β-榄香烯浓度在8.3~207.5 μg/mL范围内与峰面积呈良好线性关系。
2.2.6 精密度试验 精密吸取同一载药胶束供试品溶液10 μL,注入高效液相色谱仪,连续进样6次,记录峰面积,结果表明,精密度良好,RSD=1.62%。
2.2.7 稳定性试验 精密吸取同一载药胶束供试品溶液,分别于0、2、4、6、8、10 h进样,记录峰面积,结果β-榄香烯在10 h内保持稳定,RSD=1.72%。
2.2.8 重复性试验 取同一载药胶束样品各6份,分别按载药胶束供试品溶液制备方法操作,精密吸取各供试品溶液10 μL,分别注入液相色谱仪,测定。结果β-榄香烯平均含量为1.82 mg/mL,RSD=2.02%,表明重复性良好。
2.2.9 加样回收率试验 分别精密量取已知含量β-ELE-DSPE-PEG2000-PMs溶液(1.82 mg/mL)0.5 mL共6份,置25 mL容量瓶中,分别精密加入β-榄香烯对照品溶液(0.83 mg/mL)1.0 mL,其余按载药胶束供试品溶液制备方法及上述色谱条件测定并计算回收率,结果见表1,表明本法回收率良好。
2.3 体外释药研究
采用透析法考察载药胶束的体外释药性。分别取载药胶束溶液(1.82 mg/mL)及β-榄香烯原料药溶液(1.80 mg/ mL)各2 mL,置预先处理好的透析袋中,两端扎紧,固定于桨式搅拌器上,并将透析袋置于含pH 7.4磷酸盐缓冲液(含0.5%十二烷基硫酸钠)释放介质50 mL的烧杯中,于(37.0±0.5)℃恒温水浴中振荡(100 r/min),分别于0.5、1、2、4、6、8、10、12、24 h 取样1 mL,过0.45 μm微孔滤膜,并补充同温等量释放介质。平行操作3份。样品用0.45 μm 微孔滤膜过滤,按“2.2.1”项下色谱条件,取滤液进样20 μL测定,计算累积释放率及3份样品各点的平均值,并绘制释药曲线,结果见图2。从图2中可知,在pH 7.4磷酸盐缓冲液释放介质中,β-榄香烯原料药溶液24 h内几乎完全释放,而载药胶束仅释放70%左右,且0~2 h属于突释,之后释放缓慢,表明该胶束具有缓释性能,利于使药物到达病灶部位的靶组织[7-10]。
3 讨论
胶束包封率测定方法主要有高速离心法、透析法、葡聚糖凝胶柱层析法等,但透析法、葡聚糖凝胶柱层析法时间较长、操作繁琐,且β-榄香烯为挥发油,不溶于水,因此洗脱剂及透析介质很难选择。另外,高速离心法对难溶于水的固体药物较为适合,不适合相对密度小于水的β-榄香烯。因此,本试验采用石油醚萃取法,除去未包封的游离药物,方法简便、快速、重复性好;同时对石油醚的萃取次数进行了考察,结果萃取2次基本提取完全。
体外释药研究多采用生物膜扩散、透析袋法等技术。本试验采用透析法,该法简单、易行。释放介质选用与人体血浆pH值相近pH 7.4磷酸盐缓冲液,为增加β-榄香烯在水中的溶解度及达到漏槽条件,在释放介质中加入十二烷基硫酸钠作为增溶剂。
为验证β-ELE-DSPE-PEG2000-PMs抗脑胶质瘤作用的靶向性,后续研究还需通过与原料药注射液对照,结合细胞毒试验、细胞凋亡试验、细胞摄取试验、动物体内的组织分布或活体成像技术验证其抗脑胶质瘤的作用及靶向性。
参考文献:
[1] 黄朝刚,蔡翔.榄香烯注射液联合放化疗治疗脑胶质瘤的疗效分析[J].中国医药指南,2013,11(11):281.
[2] 汪维佳,方东升,华育晖.榄香烯注射液所致新的不良反应临床分析[J].实用肿瘤杂志,2013,28(4):388-390.
[3] 谢恬李,铖璐,王淑玲,等.榄香烯脂质体系列靶向抗癌天然药物基础研究进展[J].中國中西医结合杂志,2014,34(4):507-509.
[4] 花文峰,蔡绍晖.β-榄香烯抗肿瘤作用的基础与临床研究[J].中药材, 2006,29(1):93-97.
[5] 胡一晨,孔维军,杨美华.姜黄挥发油脂质体制备及其抗黄曲霉菌评价研究[J].世界中医药,2015,10(8):1157-1162.
[6] 禹玉洪,李雪春,吴涛,等.注射用柴胡挥发油脂质体制备工艺研究[J].中国中药杂志,2004,29(6):521-525.
[7] MUSACCHIO T, LAQUINTANA V, LATROFA A, et al. PEG-PE micelles loaded with paclitaxel and surface-modified by a PBR-ligand: synergistic anticancer effect[J]. Mol Pharm,2009,6(2):468-479.
[8] 马文转,王金铃,屠鹏飞.黄芩苷纳米胶束的制备、表征及其对MCF-7细胞抑制作用的研究[J].中草药,2015,46(4):507-512.
[9] 毛骁丽,张翮,俞媛,等.穿膜肽修饰盐霉素胶束的制备与表征[J].中国新药杂志,2014,23(23):2812-2816.
[10] 胡凯莉,贾娜,刘梅,等.多烯紫杉醇脂质核胶束的制备及性质考察[J].中成药,2014,36(6):1181-1186.
(收稿日期:2016-04-08)
(修回日期:2016-04-28;编辑:陈静
