连续性肾脏替代治疗对重症急性胰腺炎诱导的肠黏膜屏障功能的影响*
2016-11-01李正荣李曼丽杜晓刚
沈 清,甘 华,李正荣,李曼丽,杜晓刚
(重庆医科大学附属第一医院肾内科,重庆 400016)
论著·临床研究doi:10.3969/j.issn.1671-8348.2016.26.013
连续性肾脏替代治疗对重症急性胰腺炎诱导的肠黏膜屏障功能的影响*
沈清,甘华,李正荣△,李曼丽,杜晓刚
(重庆医科大学附属第一医院肾内科,重庆 400016)
目的探讨连续性肾脏替代治疗(CRRT)对重症急性胰腺炎(SAP)诱导的肠黏膜屏障功能障碍的影响。方法选取SAP患者78例,根据治疗方案的不同,分为CRRT组43例,非CRRT组35例,监测SAP患者治疗前后APACHEⅡ评分变化,比较两组间的病死率。分别在CRRT治疗0、12、24、48、72 h等不同时间点检测血清肿瘤坏死因子(TNF-α)、C-反应蛋白(CRP)、血浆二胺氧化酶(DAO)和D-乳酸的变化。结果治疗后24、72 h CRRT组APACHⅡ评分分别为10.2±3.8、6.4±2.6,较非CRRT组明显改善(P<0.05),病死率(18.6%)也明显下降。CRRT组治疗后血清TNF-α、CRP、DAO、D-乳酸水平下降,与治疗前比较差异有统计学意义(P<0.05)。而非CRRT组患者经常规治疗后,血清TNF-α、CRP、DAO、D-乳酸水平与治疗前比较无明显变化(P>0.05)。结论CRRT治疗对SAP诱导的肠黏膜屏障功能障碍具有改善作用。
胰腺炎;肾替代治疗;乳酸;肠黏膜屏障功能;血清DAO
重症急性胰腺炎(severe acute pancreatitis,SAP)是一种常见的危重急腹症,常因全身炎症反应综合征(systemic inflammatory response syndrome,SIRS),多器官功能衰竭死亡[1]。最近研究发现肠黏膜屏障功能障碍与SAP的不良预后密切相关[2];SAP患者早期就可出现肠黏膜屏障功能障碍,从而促使肠道内细菌和毒素发生移位,炎性介质经通透性增高的肠黏膜进入血液循环,使机体出现SIRS,最终引起多器官功能衰竭的发生[3]。连续性肾脏替代治疗(continuous replacement therapy,CRRT)已成为SAP综合治疗的有效手段之一[4]。但CRRT能否改善肠黏膜屏障功能障碍,减轻SIRS的发生,目前少见报道。本研究观察了CRRT治疗对SAP患者肠黏膜屏障功能的影响,现报道如下。
1 资料与方法
1.1一般资料选取2011年1月至2012年6月在本院确诊为SAP的患者78例,其中男47例,女31例;年龄23~76岁,平均(47.3±14.8)岁;病因包括胆源性23例、饮酒18例、高脂饮食15例、暴饮暴食13例、不明原因9例。SAP的诊断参照1992年Atlanta International Conference on Pancreatic Diseases制订的标准,所有患者全部符合SAP诊断标准,除了有急性胰腺炎的临床和生化改变,还具备下列条件之一者:局部并发症(胰腺坏死、假性囊肿或胰腺脓肿);发生器官衰竭;且APACHEⅡ评分大于或等于8分。SAP患者按入院时间先后分为CRRT组43例(常规治疗+CRRT),非CRRT组35例(常规治疗)。CRRT组在内科综合治疗基础上增加连续性肾脏替代治疗;非CRRT组仅接受内科综合治疗。两组患者在性别、年龄、APACHEⅡ评分、CT评分等方面差异无统计学意义(P>0.05),具有可比性。健康对照组20例,其中男12例,女8例,平均年龄(41.2±10.8)岁。研究计划经本院伦理委员会通过,所有患者或家属签署知情同意书。
1.2治疗方法
1.2.1常规治疗方法根据患者病情给予个体化治疗措施,如禁食,胃肠减压,抑制胃酸分泌,生长抑素抑制胰腺分泌及抗感染,营养支持等综合治疗;根据呼吸状况和血气分析结果,予以高流量面罩吸氧或机械通气,部分患者使用血管活性物质维持血压的稳定。
1.2.2连续性肾脏替代治疗采用中心静脉置管建立血管通路,采用连续性血液滤过模式(continues hemofiltration,CHF),使用德国贝朗CRRT机,GambroAN69聚砜膜血液滤器,血流量为200~300 mL/min,置换液流量为4 000~6 000 mL/h,超滤量根据病情需要调整,采用普通肝素或低分子肝素抗凝,严重出血倾向者不使用肝素。治疗时间24~72 h,根据病情重复3~5次。
1.3患者的病情观察在CRRT治疗前、后每1小时记录患者生命体征、神志、腹部体征等的变化;每天检测血常规、肾功能、淀粉酶(AMS)、脂肪酶、血气分析、电解质等的变化;动态进行APACHEⅡ评分,观察病情的变化。
1.4血清细胞因子的检测按实验设计分别在CRRT治疗0、12、24、48、72 h等不同时间点采集患者和健康志愿者静脉血10 mL,离心后留取血清,-80 ℃冰箱编号冷冻保存。检测包括:肿瘤坏死因子(TNF-α,ELISA法,购自Sigma公司)、C-反应蛋白(CRP,ELISA法,购自南京凯基公司)、血浆二胺氧化酶(DAO,ELISA法,购自南京建成公司)、D-乳酸(ELISA法,购自南京建成公司)。操作步骤和方法参照产品说明书。
2 结 果
2.1两组患者治疗前后APACHⅡ评分、血生化指标的变化两组患者治疗前APACHEⅡ评分分别为(13.8±4.5)、(14.1±3.7)分,比较差异无统计学意义(P>0.05)。CRRT组经治疗后,患者APACHⅡ评分、血AMS逐渐下降,与治疗前比较差异均有显著意义(P<0.05);而非CRRT组患者经常规治疗后,APACHⅡ评分,血淀粉酶虽较治疗前有所下降,但差异无统计学意义(P>0.05)。见表1。
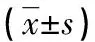
表1 2组患者治疗前后APACHⅡ评分、AMS的变化
a:P<0.05,与治疗前比较。
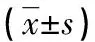
表2 CRRT治疗前后SAP患者血清DAO、D-乳酸、TNF-α和CRP水平的变化
a:P<0.01,与对照组比较;b:P<0.05,与治疗前比较。
2.2两组患者治疗效果及预后比较CRRT治疗组43例,治愈好转35例(81.4%),死亡8例(18.6%);非CRRT组35例,治愈好转22例(62.9%),死亡13例(37.1%),两组比较差异具有统计学意义(P<0.05)。
2.3SAP患者治疗前后血清细胞因子的变化两组SAP患者血清DAO、D-乳酸、TNF-α和CRP均明显高于健康对照组,与治疗前相比,CRRT组血清DAO、D-乳酸、TNF-α和CRP水平在24 h下降(P<0.05),并一直持续到治疗48 h(P<0.05),其中72 h下降最明显。而非CRRT组患者经常规治疗后,血清TNF-α有所下降,但与治疗前比较差异无统计学意义(P>0.05),而DAO、D-乳酸水平和CRP水平与治疗前比较无明显下降,部分指标甚至有所上升,表2。
3 讨 论
SAP是一种病情凶险、并发症多、病死率较高的危重急腹症,其病程早期即可出现SIRS、多器官功能障碍,甚至多器官功能衰竭导致死亡,其病死率高达30%[1],临床治疗相当棘手。近来研究发现,直接威胁SAP患者的不是胰腺坏死,而是肠道细菌移位,肠源性内毒素血症及胰腺的继发感染[5]。SAP早期就可出现肠黏膜上皮细胞通透性增高,促使肠道内细菌和毒素发生移位,炎性介质经通透性增高的肠黏膜进入血液循环,使机体出现内源性、自我破坏的全身炎症反应,导致组织和器官的损害,最终引起多器官功能障碍综合征的发生[3]。因此肠道被称为SIRS和多器官功能障碍的“枢纽器官”和炎症介质的扩增器[6],减轻肠黏膜屏障功能障碍对阻止疾病的发展,改善SAP患者的预后显得至关重要。
CRRT是近年来发展起来的新型血液净化治疗方式,已成为SAP综合治疗的有效手段之一[4]。一般认为这种作用与其去除炎症介质,减轻全身炎症反应,恢复免疫调节和改善内皮细胞功能有关[7]。虽然最近研究发现肠黏膜屏障功能障碍与SAP的预后不良密切相关[2];但CRRT能否改善肠黏膜屏障功能障碍,从而减轻了SIRS的发生,改善了SAP的预后,目前少见报道。
本研究中分别给予两组患者常规治疗联合CRRT治疗和单独常规治疗,观察其病情变化。结果表明,与非CRRT组比较,治疗72 h后,CRRT组病情改善明显,APACHEⅡ评分降低和血AMS明显下降、而对照组经72 h常规治疗后病情改善不明显,并且CRRT组病死率较非CRRT组明显下降,从而证实CRRT治疗与传统常规治疗相比较,能有效地减轻胰腺炎症,降低APACHEⅡ评分,降低病死率,从而改善SAP患者的临床转归。
DAO是一种与核酸和蛋白合成密切相关的细胞内酶,95%以上存在于小肠的黏膜上皮细胞中,肠黏膜屏障功能受损,DAO进入肠细胞间隙淋巴管和血流增加,导致血DAO水平升高。D-乳酸是细菌发酵的代谢产物,在正常情况下很少被吸收,肠黏膜上皮细胞受损时,肠道中细菌所产生的大量D-乳酸经过受损的肠黏膜进入血液循环。因此认为血中DAO和D-乳酸水平能灵敏地反映肠黏膜通透性,可作为急性肠黏膜损害早期诊断的标志物[8-9]。通过检测血清DAO、D-乳酸水平的变化来判断SAP患者是否存在肠黏膜屏障功能障碍,以及CRRT对其的影响。研究结果显示,两组SAP患者血清DAO、D-乳酸水平均较健康对照组增高,提示SAP存在肠黏膜屏障功能的损害。与非CRRT组比较,CRRT组患者经CRRT治疗后,血清DAO、D-乳酸水平逐渐下降,24 h后与治疗前比较有明显差异,一直持续到治疗48 h(P<0.05),其中72 h下降最明显;而非CRRT组经常规治疗后,血清DAO、D-乳酸水平与治疗前比较无明显变化。由于DAO相对分子质量为25×104,不能直接通过弥散和对流被CCRT清除,故其水平下降反映了肠黏膜屏障功能改善。
TNF-α是一种重要的促炎介质,它可以增加血管内皮细胞及肠上皮细胞的通透性,降低上皮的屏障功能,在SAP病程中起着重要作用[10]。在SAP的早期阶段,由于全身炎症反应,大量的炎性介质包括TNF-α的释放,导致肠黏膜上皮通透性增高,促使肠源性内毒素血症的发生[11]。本研究发现SAP患者在CRRT治疗前TNF-α、CRP明显增高,但CRRT治疗后TNF-α和CRP明显下降,24 h已显著低于治疗前,72 h更加明显。而非CRRT组经72 h常规治疗后TNF-α和CRP无明显变化,提示CRRT能清除TNF-α等炎症因子,减轻SAP患者体内炎症反应的作用,由于CRP的相对分子质量较大,CRRT不能直接清除,故其浓度的降低与炎症反应的减轻有关。
本研究发现CRRT治疗后SAP患者血清DAO、D-乳酸水平明显下降,同时TNF-α和CRP水平明显下降,APACHEⅡ评分改善,提示CRRT治疗可能通过清除某些致肠上皮细胞通透性增加的因子(TNF-α等),降低肠黏膜上皮细胞的通透性,从而改善肠黏膜上皮的屏障功能,并有效阻止了肠源性内毒素血症的发生有关,减轻了全身炎症反应,降低SAP患者APACHEⅡ评分和病死率。
[1]Carnovale A,Rabitti PG,Manes G,et al.Mortality in acute pancreatitis:is it an early or a late event?[J].JOP,2005,6(5):438-444.
[2]Liu H,Li W,Wang X,et al.Early gut mucosal dysfunction in patients with acute pancreatitis[J].Pancreas,2008,36(2):192-196.
[3]Banan A,Choudhary S,Zhang Y,et al.Oxidant-induced intestinal barrier disruption and its prevention by growth factors in a human colonic cell line:role of the microtubule cytoskeleton[J].Free Radic Biol Med,2000,28(5):727-738.
[4]Mayumi T,Ura H,Arata S,et al.Evidence-based clinical practice guidelines for acute pancreatitis:proposals[J].J Hepatobiliary Pancreat Surg,2002,9(4):413-422.
[5]Rahman SH,Ammori BJ,Holmfield J,et al.Intestinal hypoperfusion contributes to gut barrier failure in severe acute pancreatitis[J].J Gastrointest Surg,2003,7(1):26-35.
[6]Leaphart CL,Tepas JJ.The gut is a motor of organ system dysfunction[J].Surgery,2007,141(5):563-569.
[7]季大玺,龚德华,徐斌.连续性血液净化在重症监护病房中的应用[J].中华医学杂志,2002,82(18):1292-1294.
[8]Li JY,Sun D,Lu Y,et al.Change in intestinal function in sepsis in rat[J].Zhongguo Wei Zhong Bing Ji Jiu Yi Xue,2004,16(6):352-354.
[10]Mao EQ,Tang YQ,Zhang SD.Effects of time interval for hemofiltration on the prognosis of severe acute pancreatitis[J].World J Gastroenterol,2003,9(2):373-376.
[11]Zhang JB,Du XG,Zhang H,et al.Breakdown of the gut barrier in patients with multiple organ dysfunction syndrome is attenuated by continuous blood purification:effects on tight junction structural proteins[J].Int J Artif Organs,2010,33(1):5-14.
Effects of continuous renal replacement therapy on intestinal mucosal barrier dysfunction induced by severe acute pancreatitis*
Shen Qing,Gan Hua,Li Zhengrong△,Li Manli,Du Xiaogang
(DepartmentofNephrology,theFirstAffiliatedHospitalofChongqingMedicalUniversity,Chongqing400016,China)
ObjectiveTo investigate the effects of continuous renal replacement therapy (CRRT) on intestinal mucosal barrier dysfunction induced by severe acute pancreatitis (SAP).Methods78 patients with SAP were enrolled and randomized to receive two different study therapeutic regimens:CRRT plus routine therapy (CRRT group,n=43) and routine therapy alone (non-CRRT group,n=35).Changes in APACHEII score and mortality between the two groups were compared.Serum levels of tumor necrosis factor-alpha (TNF-α),C-reactive protein (CRP),diamine oxidase (DAO) and D-lactic acid were determined at 0,12,24,48,72 hours during CRRT therapy.ResultsThe APACHⅡscore in the CRRT group decreased significantly along with a lower mortality when compared with those in the non-CRRT group (P<0.05).The serum TNF-α,CRP,DAO and D- lactic acid levels with CRRT decreased significantly(P<0.05),while no change in these substances was found with non-CRRT therapy(P>0.05).ConclusionIntestinal mucosal barrier dysfunction is an established condition in SAP.CRRT is not only shows a protective effect on the intestinal mucosal barrier dysfunction induced by SAP.
pancreatitis;renal replacement therapy;lactic acid;intestinal mucosal barrier;DAO
中国医院协会基金项目(CHABP2016-04);重庆市卫生局科研基金资组课题(2010-2-075)。作者简介:沈清(1971-),副教授,博士,主要从事血液净化治疗在危重症患者中治疗的研究。△
,E-mail:893233187@qq.com。
R495.5
A
1671-8348(2016)26-3640-03
2016-02-18
2016-05-22)
