加工工艺对浑浊型银耳饮料稳定性的影响
2016-09-28旭朱新鹏吕远平
杨 旭朱新鹏吕远平
(1. 安康学院现代农业与生物科技学院,陕西 安康 725000;2. 陕西省富硒食品工程实验室,陕西 安康 725000;3. 四川大学食品工程系,四川 成都 610065)
加工工艺对浑浊型银耳饮料稳定性的影响
杨旭1,2朱新鹏1,2吕远平3
(1. 安康学院现代农业与生物科技学院,陕西 安康725000;2. 陕西省富硒食品工程实验室,陕西 安康725000;3. 四川大学食品工程系,四川 成都610065)
以含水率为指标,确定银耳的适宜复水条件;以熬煮液中总糖、还原糖和多糖的含量考查熬煮时间对其影响,并结合DPPH和羟自由基清除活性,分析不同熬煮时间下产品的抗氧化稳定性;以黏度值和悬浮稳定性为指标,通过单因素和均匀试验选择适宜稳定剂及复配方案。结果表明:50 ℃复水15 min,银耳含水率可达92.91%;熬煮时间为5 h熬煮液中多糖含量最高,达1 741.00 g/L,且DPPH和羟自由基清除活性也最强,分别为17.84%和12.38%;瓜尔胶、CMC、阿拉伯胶最适复配添加量分别为0.10%,0.05%,0.05%时,饮料黏度值为23.4 mPa·s,悬浮稳定性为94.69%,加权稳定性为91.72%。该工艺下得到的银耳饮料均一稳定,并保留较高的抗氧化活性,为其工业化生产提供了理论依据。
银耳;浑浊型饮料;多糖;抗氧化;稳定性
银耳又名白木耳,是一种营养丰富且药用价值极高的食用菌[1],含有蛋白质、粗纤维、碳水化合物、脂肪、无机盐、维生素B类等多种营养成分[2]。其中,银耳多糖由于具有免疫调节、抗肿瘤、降血糖血脂、促进神经细胞生长等生物活性而被广泛关注[3-4]。特别是其能够清除自由基以减少对机体内大分子活性物质及细胞的有害攻击,从而赋予了银耳制品抗氧化的保健功能特性[5-6]。
在食品生产以及实际生活中,一般是通过熬煮工艺实现对银耳中多糖等有效成分的溶出利用。已报道的文献[7-9]表明,银耳制品多是通过熬煮、酶法浸提等技术,选择多糖浸出率为指标制备银耳提取液,并以此为原料经不同加工工艺制成饮料、罐头、酸豆奶等保健食品。然而,关于熬煮工艺对银耳饮料制品中多糖含量及其生物活性的影响,浑浊型银耳饮料中稳定剂复配及稳定性研究等却鲜有报道。因此,本试验从复水条件、熬煮工艺、浆渣混合比例、稳定剂选择及其稳定性4个方面考查加工工艺对浑浊型银耳饮料稳定性的影响,其中熬煮工艺结合了对不同熬煮时间下熬煮液中多糖含量的变化和其DPPH、羟基自由基清除活性的变化进行优化,稳定性研究则是结合了制品的黏度和悬浮稳定性进行衡量。从成本、过程、功效等多方面来看,本研究具有良好的应用价值和市场前景,为生产、生活中银耳的熬煮、加工提供理论依据和工艺参数,并提高浑浊型银耳饮料在生产和储存中的稳定性。
1 材料与方法
1.1材料与仪器
1.1.1材料与试剂
干银耳:市售;
羧甲基纤维素钠、阿拉伯胶、瓜尔胶:食品级,河南天润生物科技有限公司;
黄原胶、果胶、海藻酸钠、卡拉胶:食品级,河南百福食品添加剂有限公司;
苯酚、浓硫酸、氢氧化钠、酒石酸钠、亚硫酸钠、三羟甲基氨基甲烷、浓盐酸、乙醇、水杨酸:分析纯,成都科龙试剂厂;
1,1-二苯基-2-苦肼基(DPPH):分析纯,日本TCI公司;
3,5-二硝基水杨酸:分析纯,美国Sigma公司;
D-无水葡萄糖标品:分析纯,上海江莱生物科技有限公司。
1.1.2主要仪器设备
紫外可见分光光度计:TU-1901型,北京普析通用仪器有限责任公司;
低速离心机:LD4-2A型,北京医用离心机厂;
电热恒温水浴锅:HWS-26型,上海齐欣科学仪器有限公司;
电热恒温鼓风干燥箱:GZX-GF101-2-BS型,上海跃进医疗器械有限公司;
榨汁机:HR1848型,珠海飞利浦家庭电器有限公司;
快速混匀器:XK96-A型,江苏新康医疗器械有限公司;
黏度计:DV-2+PRO型,上海精密仪器仪表有限公司。
1.2试验方法
1.2.1工艺流程

1.2.2银耳的复水试验
(1) 复水时间的确定:准确称取8份银耳样品,加入水置于常温下,分别复水5,10,15,20,25,30,35,40 min后,沥干20 min,并用吸水纸吸干其表面水分,准确称量至质量基本不变为止,根据复水前后的质量变化计算得到银耳的含水率。
(2) 复水温度的确定:准确称取5份银耳样品,加水后分别置于30,40,50,60,70 ℃水浴中复水15 min,后续操作同1.2.2(1)。
(3) 复水液多糖含量的测定:将不同条件下得到的复水液在3 000 r/min离心5 min,准确吸取上层清液15 mL,加入无水乙醇60 mL,混匀5 min。再置于3 000 r/min离心10 min,弃去上层清液,残渣用80%的乙醇洗涤3次,低温烘干后在60 mL热水中溶解,抽滤后移入100 mL容量瓶中进行测定[10]。
1.2.3银耳熬煮时间的确定准确称取3.0 g银耳,按1.2.2确定的条件复水后加入500 mL蒸馏水,超声处理15 min,分别回流熬煮1,2,3,4,5,6,7,8 h,液渣分离,并将熬煮液定容至500 mL待测。
(1) 熬煮时间对熬煮液中总糖含量的影响:采用苯酚—硫酸法[11][12]13-14测定银耳熬煮液中总糖的含量,以D-无水葡萄糖溶液浓度为横坐标,吸光度为纵坐标,绘制葡萄糖标准曲线。在相同的反应条件下,取各熬煮液0.1 mL,根据标准曲线确定各熬煮液中总糖的含量。
(2) 熬煮时间对熬煮液中还原糖含量的影响:采用DNS法[12]14-15测定银耳熬煮液中还原糖的含量,同样以D-无水葡萄糖为标准品。在相同反应条件下,取各熬煮液1 mL,根据标准曲线确定各熬煮液中还原糖的含量。
(3) 熬煮时间对熬煮液DPPH自由基清除活性的影响:准确吸取不同熬煮时间的样品液各2 mL于10 mL比色管中,分别加入2 mL 0.08 mg/mL DPPH乙醇溶液和1 mL Tris—HCl缓冲液(pH 7.4)。反应在闭光条件下进行30 min后,于517 nm下测定吸光度[13]。相同条件下,不添加DPPH作为本底组,不添加样品液作为空白组。DPPH自由基清除率按式(1)计算:

(1)
式中:
S——清除率,%;
As——样品组的吸光度值;
Ab——本底组的吸光度值;
Ac——空白组的吸光度值。
(4) 熬煮时间对熬煮液羟基自由基清除活性的影响:将9 mmol/L硫酸亚铁溶液1 mL,9 mmol/L水杨酸—乙醇溶液1 mL,8.8 mmol/L H2O21 mL,和不同熬煮时间下得到的各样品液1 mL混合,在37 ℃下反应30 min,于510 nm下测定其吸光度[14]。在相同条件下,不添加H2O2作为本底组,不添加样品作为空白组。羟自由基清除率按式(1)计算。
1.2.4熬煮滤液与浆液混合比例的确定准确称取6份3.0 g的银耳样品,按1.2.3所述方法回流熬煮5 h,液渣分离。将滤渣打浆后得到浆液,分别按1/1,1/2,1/3,1/4,1/5,1/6的比例与滤液混合,测定其黏度。
1.2.5浑浊型银耳饮料中稳定剂的选择
(1) 稳定剂的单因素试验:准确称取7份银耳样品,均为3.0 g,按1.2.3所述方法回流熬煮5 h后液渣分离,取浆液与滤液1/4混合,得到银耳浑浊汁。分别加入0.2%的黄原胶、卡拉胶、瓜尔胶、果胶、羧甲基纤维素钠(CMC)、海藻酸钠和阿拉伯胶,以黏度和悬浮稳定性为测定指标,选择稳定效果好的稳定剂进行下一步的均匀试验。
(2) 稳定剂的均匀设计试验:采用DPS软件数据处理系统进行均匀试验设计,以确定出最佳的稳定剂配方[15]。根据稳定剂的单因素试验结果,选择出对银耳饮料稳定性影响较大的黄原胶、瓜尔胶、CMC和阿拉伯胶四因素,再根据每种稳定剂的用量范围,确定8个水平。选取黏度和悬浮稳定性两个测定因素,分别按照25%和75%的权重加成,得到表征饮料稳定性的综合指标,并进行试验组的测定。
1.2.6浑浊型银耳饮料稳定性的测定
(1) 黏度测定:采用DV-2+PRO数字式黏度计在室温下测定液体的黏度。
(2) 悬浮稳定性测定:采用紫外分光光度计法[16-17],以蒸馏水为空白对照,于660 nm下测定银耳饮料的吸光度值A1,再取银耳饮料50 mL,4 200 r/min离心15 min,上层清液于660 nm下测定吸光度值A2,A1/A2即为浑浊型银耳饮料的悬浮稳定性。
1.2.7数据分析所有数据以均值±标准差表示,每次样品的测定均重复3次。采用SPSS 19.0进行方差分析和最小显著性差异分析(P<0.05即为差异显著)。其中,均匀设计试验数据以均值表示,采用DPS对数据进行多元线性回归分析。
2 结果与分析
2.1银耳复水试验
由图1(a)可知,复水时间为15 min时银耳已经充分吸水,含水率达到(89.91±0.12)%,再延长复水时间,含水率基本不变。从保证产品质量并缩短生产时间的方面考虑,适宜的复水时间为15 min。
由图1(b)可知,复水温度从30 ℃升至50 ℃,含水率的变化趋势逐渐增加,而后,温度的升高对含水率的影响不大,变化趋于平缓。形成这种趋势的原因可能是刚开始水温升高,使得水分子的运动加剧,水向银耳细胞内部扩散的速率随之增大。当外界环境中的水分渗透压与银耳细胞内的胞液压相等时,吸水停止,含水率的增加也趋于稳定。因此,适宜的复水温度为50 ℃,此时含水率可达(92.91±0.03)%。

不同字母表示相互之间差异显著(P<0.05)
Figure 1Effects of rehydration time and temperature on the moisture content of Tremella fuciformis
采用F检验的方法对复水时间、复水温度进行单因素方差分析,结果表明两个因素对银耳含水率的影响均显著。对此复水条件下银耳复水液中多糖含量进行测定,醇沉处理后未得到沉淀,说明经复水处理,银耳多糖并无损失,此复水工艺合理可行。
2.2银耳熬煮时间的试验结果
2.2.1熬煮时间对熬煮液中总糖、还原糖及多糖含量的影响
以D-无水葡萄糖为标准品,根据葡萄糖溶液不同浓度(x)所对应的吸光度值(y)绘制总糖含量测定标准曲线,见图2。所得标准曲线的回归方程为y=0.016 68+0.050 5x,R2=0.996 01。根据此回归方程,计算得到银耳熬煮液中总糖的含量。

图2 总糖含量测定标准曲线
同样以D-无水葡萄糖为标准品,根据葡萄糖溶液不同浓度(x)所对应的吸光度值(y)绘制还原糖含量测定标准曲线,见图3。所得标准曲线的回归方程为y=-0.010 52+0.016 75x,R2=0.999 04。根据此回归方程,计算得到银耳熬煮液中还原糖的含量。
由表1可知,随着熬煮时间的延长,总糖和还原糖含量均不断增加。就总糖含量的变化趋势而言,熬煮时间为1~4 h,总糖含量的增长速率不断增加,随后,熬煮时间继续增加,总糖含量的增长趋于平缓。出现此变化趋势的原因可能是熬煮开始时,在适宜的固液比和熬煮温度下,随着时间的增长,银耳与熬煮液充分接触,加速了银耳细胞内总糖的传质,更有利于总糖的溶出。而后,熬煮时间继续延长,此作用效应减弱,表现出总糖含量的变化速率逐渐平缓。

图3 还原糖含量测定标准曲线
还原糖由于其分子质量小于多糖,在相同条件下更易溶出。然而从还原糖含量的变化来看,熬煮1 h的熬煮液中并未检测出还原糖,而随着熬煮时间的增长,还原糖的含量随之增加,这说明还原糖含量的增加是来自于高温长时间熬煮而导致多糖降解的,变化速率仍然呈现出先增加后降低的趋势。
多糖含量则是随着熬煮时间的延长先增加后降低,出现此变化的原因可能是熬煮刚开始时,熬煮液中多糖的含量低,在较大浓度梯度的推动作用下,熬煮液中多糖的溶出量增加。当熬煮时间为5 h,多糖含量最高,达到(1 741.00±1.34) mg/L。随后熬煮时间继续延长,由于长时间的高温熬煮,使得多糖部分降解,导致测得的熬煮液中多糖含量降低。
对试验结果进行方差分析,计算所得F值均大于F0.05(7,16),表明熬煮时间对总糖、还原糖、多糖含量的影响均显著。
表1不同熬煮时间下熬煮液中总糖、还原糖及多糖的含量†
Table 1Total saccharides, reducing saccharides and polysaccharides content of Tremella fuciformis boiled drink at different boiling time

熬煮时间/h总糖含量/(mg·L-1)还原糖含量/(mg·L-1)多糖含量/(mg·L-1)1380.95±0.79f0.00±0.00h380.95±0.79h2758.78±1.37e10.40±0.15g748.38±1.28g31188.88±1.64d11.13±0.09f1177.75±1.58f41655.38±2.05c22.58±0.24e1632.80±1.99e51772.20±1.30b31.18±0.31d1741.00±1.34a61774.20±0.75b45.50±0.15c1728.68±1.06b71774.48±0.86b60.23±0.23b1714.25±0.87c81776.88±1.23a69.15±0.58a1707.73±0.92d
†同列不同字母表示相互之间差异显著(P<0.05)。
2.2.2熬煮时间对熬煮液清除DPPH自由基和羟基自由基活性的影响由图4可知,熬煮时间在1~5 h时,DPPH自由基和羟基自由基清除活性均是随着熬煮时间的延长而增强,并在5 h时达到最高清除活性,分别为(17.84±0.45)%和(12.38±0.17)%。这是由于在1~5 h时,银耳熬煮液中多糖的溶出不断增加,而多糖又是发挥DPPH和羟基自由基清除活性的主要生物活性物质。因此,熬煮液中多糖浓度的增加使其DPPH和羟基自由基清除活性增强。熬煮时间在
5~8 h时,DPPH自由基和羟基自由基清除活性反而随着熬煮时间的延长而明显下降。这可能是熬煮液中溶出的多糖在长时间的高温作用下,具有强自由基清除活性的多糖降解为弱自由基清除活性的小分子多糖,甚至是无自由基清除活性的单糖导致的[18]。
同样采用方差分析来考察熬煮时间对DPPH和羟基自由基清除活性的影响,统计结果满足P<0.05,证实了此因素对测定指标的显著影响。
根据不同熬煮时间下熬煮液中总糖、还原糖和多糖含量的测定结果,以及其DPPH和羟基自由基清除活性的测定结果,确定熬煮时间为5 h。此熬煮时间下,熬煮液中多糖含量最高,即功能性成分的含量最高,且熬煮液的DPPH和羟基自由基的清除活性也为最高。在提高工业化生产效率的同时,最大限度地保证产品的质量,维持此银耳产品的保健功能。

不同字母表示相互之间差异显著(P<0.05)
Figure 4DPPH and hydroxyl radical scavenging activity of Tremella fuciformis boiled drink at different boiling time
2.3熬煮滤液与浆液混合比例的试验结果
由表2可知,浆液的添加量从1/1 降至1/6时,黏度值的下降速率也一直随之减慢,而当添加量在1/4~1/6时,下降速率趋于平缓。为了保证稳定剂添加后黏度不至于过高而影响口感,故选择1/4的添加量最为合适。
2.4稳定剂的选择结果
2.4.1单一稳定剂对饮料稳定效果的影响从表3中黏度值大小来看,对浑浊银耳饮料稳定效果较好的稳定剂依次是:瓜尔胶、CMC、阿拉伯胶、黄原胶、果胶、卡拉胶、海藻酸钠;从悬浮稳定性来看,对浑浊银耳饮料稳定效果较好的稳定剂依次是:瓜尔胶、黄原胶、阿拉伯胶、CMC、果胶、卡拉胶、海藻酸钠。根据对黏度值和悬浮稳定性测定结果的比较,选用瓜尔胶、黄原胶、CMC和阿拉伯胶这4种稳定剂进行复配试验。

表2 熬煮滤液与浆液不同混合比例下黏度的测定结果†
†同行不同字母表示差异显著(P<0.05)。

表3 单一稳定剂对饮料稳定效果的影响†
†同列不同字母表示差异显著(P<0.05)。
2.4.2复配稳定剂对饮料稳定效果的影响在单因素试验结果的基础上,进行了四因素八水平的均匀试验设计(表4)。按照因素水平表添加不同比例的稳定剂,同样以黏度值和悬浮稳定性为测定指标,试验结果见表5。
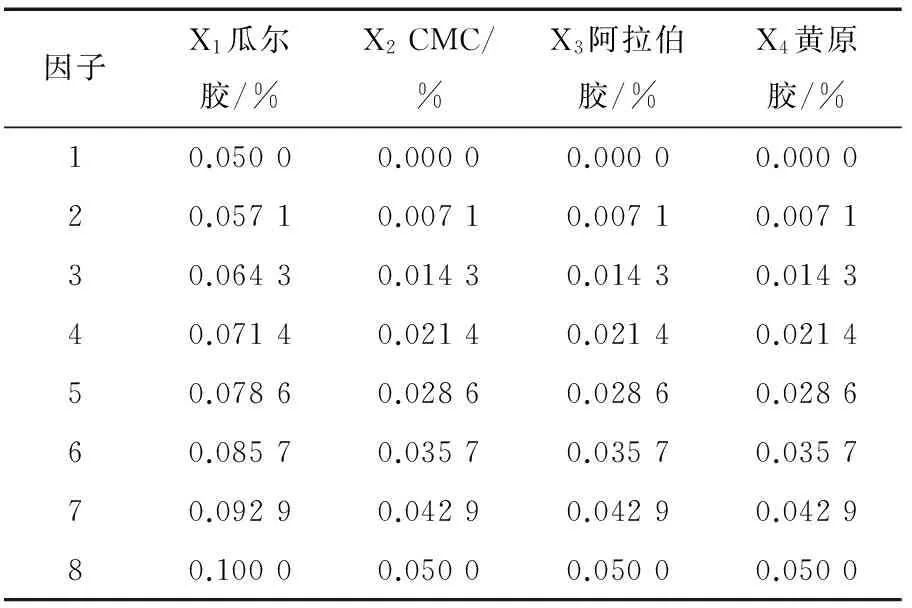
表4 均匀试验设计的因素和水平

表5 U8(84) 均匀试验结果与分析
采用DPS对试验数据进行多元线性回归分析,得到瓜尔胶、CMC、阿拉伯胶、黄原胶与加权稳定性的回归方程为:
(2)
回归方程显著性检验F值为223.185 2,P值为0.051 2,剩余标准差为0.386 6,复相关系数为0.997 4,调整后相关系数Ra为0.999 6,由此说明建立的回归方程具有统计学意义。
从所得的回归方程来看,加权稳定性与瓜尔胶、CMC、阿拉伯胶、黄原胶均有关系,且瓜尔胶与浑浊银耳饮料的加权稳定性呈正相关,因此,在试验范围内应取因素X1的最大水平。同时,因素X1X3和X2X3之间有明显的正交互作用,而因素X1X4则有明显的负交互作用。最终计算分析得到的最优组合为:X1=8,X2=7.999 5,X3=8,X4=1,即瓜尔胶、CMC、阿拉伯胶、黄原胶的添加量分别为0.10%,0.05%,0.05%,0.00%,此时最佳的加权稳定性值为91.78%。为了确定所得到的复配方案对浑浊型银耳饮料的稳定效果,进行了验证实验。此条件下,测得饮料黏度为23.4 mPa·s,悬浮稳定性为94.69%,计算得加权稳定性为91.72%。与理论最佳值基本一致,且高于均匀试验中所有组合,说明此复配方案合理可行。

表6 试验数据的二次多项式逐步回归分析结果
3 结论
浑浊型银耳饮料的加工工艺对其稳定性影响的研究结果表明,银耳在50 ℃复水15 min,含水率可达(92.91±0.03)%;在适宜熬煮时间5 h下,熬煮液中多糖的含量最高,为(1 741.00±1.34) mg/L,且DPPH和羟基自由基清除活性分别为(17.84±0.45)%和(12.38±0.17)%,同样达到最高。根据浑浊银耳饮料的黏度值,确定熬煮浆液添加量为1/4。再通过单因素和均匀设计试验结果,确定稳定剂复配方案为:瓜尔胶0.10%,CMC 0.05%,阿拉伯胶0.05%。此时,饮料的黏度值为23.4 mPa·s,悬浮稳定性为94.69%,加权稳定性达到最高,为91.72%。与以往的研究相比,本研究在银耳熬煮加工环节中对总糖、还原糖、多糖的变化均进行了考察,强调多糖得率的同时,关注了多糖活性的变化;饮料的研制中,并未以多糖浸提液为单一原料或引入其他复合原料,而是将熬煮后子实体浆液按一定比例添加,保证了银耳饮料独特、纯正的风味;多种稳定剂通过单因素初筛、均匀试验复配以及加权稳定性指标的引入,使结果合理、过程可控。如果能够对其贮藏稳定性进行后续研究,则更有利于加工过程的控制与产品质量的提升。
[1] DE BAETSS, VANDAMME E J. ExtracellularTremellapolysaccharides: structure, properties and applications [J]. Biotechnology Letters, 2001, 23(17): 1 361-1 366.
[2] 马素云. 银耳多糖提取纯化、结构特征及溶液性质研究[D]. 杭州: 浙江大学, 2012: 1-3.
[3] 王斌, 连宾. 食药用真菌多糖的研究与应用[J]. 食品与机械, 2005, 21(6): 96-100.
[4] CHEN Bin. Optimization of extraction ofTremellaFuciformispolysaccharides and its antioxidant and antitumour activities in vitro [J]. Carbohydrate polymers, 2010, 81(2): 420-424.
[5] WU Qiong, ZHENG Cheng, NING Zheng-xiang, et al. Modification of low molecular weight polysaccharides fromTremellaFuciformisand their antioxidant activity in vitro [J]. International Journal of Molecular Sciences, 2007, 8(7): 670-679.
[6] WANG Xiao-mei, ZHANG Zhong-shan, ZHAO Ming-xing. Carboxymethylation of polysaccharides fromTremellaFuciformisfor antioxidant and moisture-preserving activities [J]. International Journal of Biological Macromolecules, 2015, 72: 526-530.
[7] 刘健影. 银耳多糖提取工艺优化及其在饮料中的应用[D]. 长春: 吉林农业大学, 2009: 5-12.
[8] GHORAI S, BANIK S P, VERMA D, et al. Fungal biotechnology in food and feed processing [J]. Food Research International, 2009, 42(5/6): 577-587.
[9] 崔蕊静, 张梅申, 刘绍军, 等. 无腥大豆中加入银耳浸提液生产酸豆奶的工艺研究[J]. 农业工程学报, 2005, 21(7): 158-161.
[10] 惠秋沙. 玉米须保健饮料中多糖含量的测定[J]. 食品研究与开发, 2011, 32(8): 103-105.
[11] 周国海, 张泳, 赵力超, 等. 蛹虫草多糖提取纯化工艺研究[J]. 食品与机械, 2014, 30(5): 220-224.
[12] 王玢. 银耳制品的制备及其生理功效研究[D]. 北京: 首都师范大学, 2009.
[14] ZHANG Min, CHEN Hai-xia, LI Jin-lei, et al. Antioxidant properties of Tartary buckwheat wheat extracts as affected by different thermal processing methods [J]. Food Science and Technology, 2010, 43(1): 181-185.
[15] 樊振江, 詹现璞, 栗亚琼, 等. 复合稳定剂对豇豆饮料稳定性的影响[J]. 食品与机械, 2014, 30(1): 232-247.
[16] 李小鑫, 罗昱, 梁芳, 等. 浑浊型刺梨果汁饮料配方及其稳定性研究[J]. 食品与发酵工业, 2013, 39(7): 216-222.
[17] ZHANG Hui, WANG Zhang, XU Shi-ying. Optimization of processing parameters for cloudy ginkgo (GinkgobilobaLinn.) juice [J]. Journal of Food Engineering, 2007, 80(4): 1 226-1 232.[18] 常秀莲. 两种芦荟活性成分及其热稳定性比较研究[D]. 大连: 大连理工大学, 2006: 85-99.
Influence of processing technology on stability of Tremella fuciformis cloudy drink
YANG Xu1,2ZHUXin-Peng1,2LVYuan-Ping3
(1.CollegeofModernAgricultureandBiotechnology,AnkangUniversity,Ankang,Shangxi725000,China;2.ShangxiEngineeringLabsofSe-enrichedFood,Ankang,Shangxi725000,China;3.DepartmentofFoodEngineering,SichuanUniversity,Chengdu,Sichuan610065,China)
The processing technology and its effect on stability ofTremellafuciformiscloudy drink was investigated in this study. The appropriate rehydration conditions were determined by the moisture content ofT.fuciformis. The total saccharides, reducing saccharides and polysaccharides content ofT.fuciformisboiled drink were examined to study the effects on of boiling time. Combining with DPPH and hydroxyl radical scavenging activity, we analyzed the oxidation stability of boiled drink at different boiling time. The appropriate choice for stabilizers and complex program were determined by single factor and uniform design with indicators, including viscosity and suspension stability. Our results indicated that the moisture content ofT.fuciformiswas up to 92.91% at 50 ℃ for rehydration 15 min. When boiled for 5 h, the polysaccharide content ofT.fuciformisboiled drink was the highest (1 741.00 mg/L), and the DPPH and hydroxyl radical scavenging activity were also the strongest (17.84% and 12.38%). Moreover, the guar gum, CMC and gum acacia were selected as a compound stabilizer. When the optimal dosage of guar gum, CMC and gum acacia were 0.10%, 0.05% and 0.05% respectively, the viscosity and suspension stability were 23.4 mPa·s and 94.69%, and the weighted stability was 91.72%. By this processing, the cloudy drink was uniform, stable and with good antioxidant activity. Therefore, our work provides a theoretical basis for industrial production.
Tremella fuciformis; cloudy drink; polysaccharides; antioxidant; stability
杨旭(1989—),女,安康学院助教,硕士。
E-mail:yangxuq@hotmail.com
2016-05-09
10.13652/j.issn.1003-5788.2016.08.047
