不同运行方式对微生物燃料电池处理氨氮废水的影响
2016-07-14赵慧敏赵剑强长安大学环境科学与工程学院陕西西安70054菏泽学院化学化工系山东菏泽7405
赵慧敏,赵剑强(长安大学环境科学与工程学院,陕西 西安 70054;菏泽学院化学化工系,山东 菏泽 7405)
研究开发
不同运行方式对微生物燃料电池处理氨氮废水的影响
赵慧敏1,2,赵剑强1
(1长安大学环境科学与工程学院,陕西 西安 710054;2菏泽学院化学化工系,山东 菏泽 274015)
摘要:微生物燃料电池(MFC)是一种既能去除污染物又能产电的新型污水处理技术,由于其具有利用生物转化能量的节能优势,MFC废水脱氮处理技术引起了更多的关注。本实验在启动MFC的同步硝化与反硝化(SND)后,首先研究了通路与断路条件对MFC产电脱氮的影响,结果表明:断路时有利于硝化反应的发生,氨氮去除率有最大值95.17%;而通路更有利于COD和总氮的去除,表明氮的去除主要依靠阴极接受电子进行。随后分析了曝气阶段+停曝阶段运行方式对MFC产电和脱氮的影响,结果显示:曝气8.5h(DO为4.0mg/L)后停止曝气,停曝阶段为11.5h,DO逐渐降低到2.0mg/L,输出电压由无曝气运行的31mV提高到120mV左右,氨氮去除率最高达到86.42%、总氮去除负荷由无曝气运行的0.064g/(L·d)升高到0.46g/(L·d)。说明曝气阶段+停曝阶段运行方式既能有效提高MFC脱氮产电性能又可以减少维持高浓度DO的能量输入。
关键词:微生物燃料电池;同步硝化与反硝化;溶解氧;总氮去除;曝气
第一作者:赵慧敏(1978—),女,博士研究生,讲师,主要从事水污染控制工程研究。E-mail zhmthreesister@163.com。联系人:赵剑强,教授,博士生导师,从事水污染控制工程研究。
微生物燃料电池(MFC)将电化学和生物学结合,利用微生物作催化剂将化学能转化为电能,并在降解有机物进行脱氮时回收了能量,相对于传统的污水处理方法有诸多优势[1-4]。MFC与生物硝化反硝化工艺结合实现同时产电和脱氮的研究近年引起更多学者的关注[5-7]。
同步硝化和反硝化(SND)工艺在处理氨氮废水时能减少分离硝化阶段,从而节省了反应器的体积和处理时间[8-9]。但传统的 SND工艺中溶解氧(DO)和碳源决定着好氧菌和厌氧菌的比例,这会对总氮去除造成影响。MFC中的反硝化是以电极作为电子供体,不需要额外添加碳源就能进行反硝化反应,还能减少能量输入[10]。VIRDIS等[10-11]对MFC阴极进行曝气发现硝化和反硝化同时发生,在 DO 为5.73mg/L时总氮去除率达到86.9%,对阴极生物膜层分析发现硝化菌位于生物膜的外层,反硝化菌处于内层。而YU等[12]研究表明当MFC中在DO 为0.5mg/L时,总氮去除率达到52%。为了简化反应器的结构,降低离子交换膜费用,SAYESS等[13]发现在MFC反应器中依靠氧气梯度产生好氧和缺氧区可以实现无膜 SND。在上述系统中,高浓度DO会增加曝气能耗,低浓度DO又会影响总氮去除,因此寻找使SND效果良好且节能的脱氮方法将会大大推动MFC技术的发展。
为了进一步明确MFC在处理氨氮废水过程中不同运行方式对其脱氮产电的影响,本实验研究了MFC的启动过程以及通路和断路时对MFC脱氮产电性能的影响,然后重点探讨了曝气阶段+停曝阶段等运行方式对MFC脱氮产电性能的影响,以期既能减少曝气和能源消耗又能取得较好总氮去除效果。
1 材料与方法
1.1 试验装置
MFC阴极室和阳极室为聚乙烯有机玻璃制成,几何尺寸均是15cm × 5cm × 2.5cm。如图1所示,两室由Nafion117质子交换膜(上海河森电气有限公司)隔开,膜面积是 75cm2,贴近膜处放置同等面积的碳布;阴、阳极电极材料为直径5mm碳棒,用钛丝将碳棒与14块面积为11.7cm2碳毡串联并固定,两室净容积均为160cm3;两室内放入饱和甘汞参比电极(SCE 0.242V vs.标准氢电极,212型,上海仪电科学仪器股份有限公司)与阴、阳极室电极和PCI1713型数据采集卡(研华深圳分公司)相连,外电路用钛丝连接可变电阻箱,硅橡胶密封联接处。人工模拟氨氮废水(成分组成见1.2节)经蠕动泵(YZ1515X型,保定兰格恒流泵有限公司)由反应器下部进水口分别以流量20mL/h(阳极室和阴极室的水力停留时间HRT均为8h)进入阴、阳极室,并从阴、阳极室上部出水口分别流出,阴极室反应液用蠕动泵进行回流。
1.2 反应溶液
基本反应溶液包括 8.57g/L Na2HPO4、2.88g/L KH2PO4、0.1g/L MgSO4·7H2O、0.015g/L CaCl2、1mL/L微量元素等[14]。另阳极室添加3.84g/L乙酸钠;阴极室添加氯化铵溶液,启动阶段NH4+-N浓度设为20 mg/L,后续试验中将NH4+-N浓度调整为81 mg/L进行实验。

图1 双室微生物燃料电池装置
1.3 分析方法
输出电压、阳极和阴极电势由数据采集系统实时在线监测和记录,每10 min取平均值;溶解氧浓度(DO)采用Hach-HQ30d型溶解氧仪(美国 HACH公司)测定;化学需氧量浓度(COD)用5B-3A型COD快速测定仪(兰州连华环保科技有限公司)测定;氨氮(NH4+-N)浓度用纳氏试剂分光光度法测定,亚硝态氮(NO2--N)浓度用N-(1-萘基)-乙二胺分光光度法测定,硝态氮(NO3--N)浓度用紫外分光光度法测定[15]。
2 结果与分析
2.1 MFC的启动
MFC接种污泥取自西安汉斯啤酒厂厌氧污泥,将两室电极材料在接种污泥和各自配水中直接浸泡48h,然后装入反应室内开始连续进出水运行。实验温度保持在25℃±1℃,进水溶液pH值为7.5±0.2,外电阻设置为1000Ω。阴极室初始进水NH4+-N浓度设为20mg/L,通过回流装置控制阴极室DO浓度。MFC启动期间的输出电压和阳极电势随运行时间的变化情况如图2所示,MFC输出电压随着时间的延长上升,第10天后逐渐趋于稳定;而阳极电势在第1~8天时快速下降至-493mV左右后,保持基本稳定,表明MFC中产电菌已初步驯化成功。
在MFC启动运行过程中,阴极室中NH4+-N在微生物作用下发生硝化反应生成 NO2--N继而到NO3--N,随后硝态氮在反硝化菌的作用下在阴极作为电子受体被还原成氮气。每天测定阴极出水中各含氮化合物浓度,结果如图3所示。在连续运行的第1~6天中,阴极出水中氨氮浓度、NOx-N浓度(硝态氮和亚硝态氮浓度之和)分别保持在18.2mg/L和 0.4mg/L左右,总氮去除量维持在1.8mg/L左右,表明此阶段阴极室内硝化和反硝化很弱;从第6天起,阴极出水中氨氮浓度下降较快,而总氮去除量、NOx-N浓度开始上升,在第11~13天中,出水氨氮、NOx-N浓度维持在4 mg/L和8mg/L左右,总氮去除量在7mg/L左右,表明MFC中同步硝化与反硝化反应(SND)初步启动成功。
2.2 MFC性能的测定
对初步启动成功的MFC进行极化曲线的测定,结果见图4,得出MFC的内阻约为100Ω。通常情况下,电阻越小,电流则越大,更有利于总氮去除负荷的增加;但因为MFC刚启动,微生物的活性有限,如果电流过大,将会抑制产电菌的生长。故设置外阻和内阻相等进行后续实验来考察MFC产电脱氮性能。
2.3 通路和断路对MFC脱氮产电的影响
从反应器运行第 14天起,保持阴极反应室内DO为1.68mg/L,改变阴极进水氨氮浓度为81mg/L,连续运行35天。阴极出水稳定后,开始后续试验:先连续3天监测MFC产电和阴极出水各特征值;再断开电路7天,然后再接通电路运行3天,以此来探究通路和断路时对MFC脱氮产电的影响。通路时MFC阳极室内产生的电子通过外电路传输到阴极参与还原反应,阴极电子受体除硝态氮和亚硝态氮之外,还有同时参与阴极室中硝化反应和电极还原反应的氧气[16],硝化菌与阴极产电菌竞争使用溶解氧,溶解氧可能优先参与了硝化反应[10]。在通路运行的第1~3天,MFC产电性能和阴极出水浓度的各个指标都处于稳定状态(如图5~图7所示)。

图2 MFC启动阶段电压和阳极电势随时间变化曲线

图3 MFC启动阶段阴极出水氨氮、NOx-N浓度变化曲线

图4 输出电压和功率密度随电流密度的变化曲线
在第4~10天,MFC断路条件下,开路电压迅速上升到450mV,在以后的几天内维持缓慢上升趋势,阳极电势持续下降(图5);断路时阳极无电子向阴极传输,阴极室内主要发生的是硝化反应,氨氮出水浓度从16.4mg/L下降到5mg/L左右,氨氮去除率达到95.17%,这与VIRDIS等[11]得到94%总氮去除率的试验结果相接近。而NOx-N浓度持续上升到达 72.04mg/L,主要是由于此时阴极缺少电子致使反硝化反应被抑制,造成氮氧化物的积累,总氮去除负荷由通路时 0.064g/(L·d)显著下降到0.014g/(L·d)(图6、图7)。断路运行中总氮去除负荷没有下降到 0,可能是由于阴极反应室内为连续进水,水体置换需要一定的时间。除此之外,在最初的断电时间里还有部分氨氮得到去除是因为断路时电极上可形成持续放电的双电层电容,电子仍可以通过微生物的呼吸作用从电极传输给电子受体进行还原反应[12,17]。VIRDIS等[10]在断路20h内也观测到一定量的总氮去除。另外还有部分氮的去除或是由于阴极存在着非电极反硝化[18]。阳极COD去除负荷从1.5g/(L·d)下降到1g/(L·d)左右,表明断路会抑制阳极产电菌氧化有机物的能力,此时大部分的 COD去除是由阳极室内其他非产电菌降解发酵有机物完成[19]。
在第10天接通电路后,MFC从断路时的高电势快速放电形成高电流,反硝化率迅速增加。两天内总氮去除负荷从断路时 0.014g/(L·d)基本恢复为断路前0.064g/(L·d),表明MFC对氨氮废水的总氮去除主要还是依靠阴极接受电子进行,电压也恢复到31mV(图5~图7)。从整个过程来看,接通电路后MFC脱氮产电性能快速恢复到断路前状况,断路7天对MFC性能的影响较小。
2.4 DO对MFC脱氮产电的影响
对阴极室进行间歇进水,NH4+-N 浓度为81mg/L,先曝气8.5h,停止曝气后阴极室内的氧气主要是回流装置引入,分别在反应进行到4个时间点(3.5h、6h、8.5h、15h和20h)后取阴极水样进行测定,连续20h监测阴极室内DO。
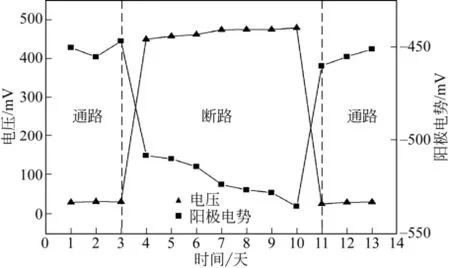
图5 通路和断路时电压和阳极电势随时间变化曲线

图6 通路和断路时阴极出水氨氮浓度、NOx-N浓度变化曲线
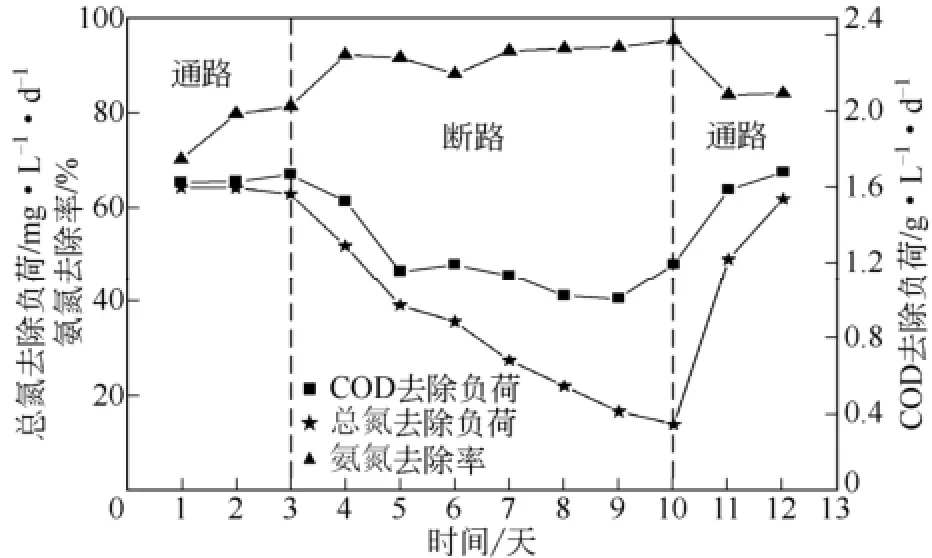
图7 通路和断路时氨氮去除率、总氮去除负荷、COD去除负荷变化曲线

图8 曝气阶段+停曝阶段运行过程中阳、阴极电势、电压和DO随时间变化曲线
从图8中可以看出,曝气时由于提供了更多的氧气,阴极还原反应由硝酸盐较低还原电(+0.74V)的还原反应偏移为氧气在高还原电势下(+0.82V)的反应。因此,电压和阴极电势都处于快速上升阶段,而电子在阴极被快速接受,阳极电势也呈上升趋势。在曝气第100min~120min时段中电压从130mV降到56mV,阳极电势从-417mV升到-250mV,阴极电势也从-286mV升到-193mV,这可能是曝气过程中阴极的部分氧气扩散到阳极,氧气不但能抑制阳极产电菌的活性,在阳极室内还能直接结合电子反应,从而造成电压的下降。随着进入阳极室内的氧气消耗,电压逐渐上升,阳极电势逐渐下降。阴极室硝化菌逐渐适应高浓度DO,硝化反应加快,同时硝化作用能释放质子用来弥补阴极还原中的质子消耗[20],即阴极电极上的还原反应增强,阴极电势随之下降。在曝气150min后,DO从1.68mg/L上升到4.01mg/L,随后的曝气时间内维持在4.15 mg/L左右,阴极室反应逐渐趋于稳定。在曝气第440~470min,由于阳极室内受氧气抑制的产电菌其活性逐渐恢复,分解有机物产生的电子增多,供电能力增强,阳极电势从-333mV降到-390mV,电压从103mV升至136mV。

图9 曝气阶段+停曝阶段运行过程中阴极出水特征值和DO随时间变化曲线
有研究表明,对MFC阴极进行曝气可以保证MFC电压的稳定输出[15]。停止曝气后,DO在30min内从4.05mg/L下降到2.75mg/L,参与阴极电极的氧气还原反应也随之减弱,电压从138 mV下降到114mV,阴极还原反应偏移于较低还原电势的硝酸盐,阴极电势从-258mV下降到-290mV,而阳极电势变化较缓,说明阳极产电菌群的活性逐渐稳定。此时有利于阴极电极反硝化反应的进行,故在第800min时电压出现上升和阴极电势下降趋势。当反应室中硝态氮和DO浓度持续降低时,电压和阴极电势也随之降低。
由于硝化反应是好氧反应,曝气有利于 MFC硝化反应的进行。从图9可知,曝气阶段8.5h内,氨氮出水浓度从进水的81mg/L下降到27.76mg/L,氨氮去除率达到65.82%,总氮去除率达到48.99%。吴伟杰等[21]研究得出曝气时间对MFC处理污水效果影响明显,随着曝气时间的延长,MFC系统中氨氮去除率明显升高。另外,在MFC曝气过程中有部分氨氮变成了易挥发的氨态氮(NH3)进行去除[22]。
停止曝气后,由于阴极室内DO迅速下降,氨氮硝化速率减缓,NOx-N浓度降低,表明有更多的NOx-N参与了阴极的反硝化反应。MFC同步硝化和反硝化反应中,DO是一个关键性的因素。一般认为DO浓度越低时反硝化菌的活性越强,即维持较低的DO浓度有助于提高MFC污水处理脱氮的潜力[12]。刘松山[23]深入考察溶解氧对MFC去除氨氮的影响,结果显示溶解氧浓度增加到4mg/L时,运行72h内氨氮降解速率基本相同,其产电性能逐渐提高。谢珊等[24]试验证明溶解氧浓度控制在3.5~5.0mg/L时,硝化过程未对MFC产电产生明显不利影响。在本实验中,先曝气8.5h,DO保持在4.1mg/L左右,停止曝气后,DO降到2.0mg/L左右,输出电压维持在120mV左右,比曝气前31mV有大幅度提高;总氮去除负荷达到0.46g/(L·d),远高于曝气前的去除负荷0.064g/(L·d)。因此,曝气阶段+停曝阶段运行方式对MFC产电和脱氮都比较有利。
3 结 论
在双室 MFC处理氨氮废水时,阴极室内能发生同步硝化和反硝化现象。断路利于 MFC中氨氮硝化反应的进行,氨氮去除率最大值为95.17%;通路有利于COD和总氮的去除,表明氮的去除主要依靠阴极接受电子进行。在 MFC系统采取曝气阶段+停曝阶段运行方式:在20h内先曝气8.5h后停止曝气,DO由4.1mg/L逐渐降低到2.0mg/L,此时输出电压比无曝气运行的31mV提高到120mV左右;氨氮去除率最高达到86.42%;总氮去除负荷由无曝气运行的0.064g/(L·d)升高到0.46g/(L·d)。说明曝气阶段+停曝阶段运行方式既能有效提高MFC脱氮产电性能又可以减少维持高浓度DO的能量输入。
参 考 文 献
[1] CAMARGO JA,ALONSO A. Ecological and toxicological effects of inorganic nitrogen pollution in aquatic ecosystems:a global assessment[J]. Environment International,2006,32(6):831-849.
[2] KIM Y M,KIM S J,KIM Y S,et al. Overview of systems engineering approaches for a large-scale seawater desalination plant with a reverse osmosis network[J]. Desalination,2009,238(1/2/3): 312-332.
[3] HILAL N,AL-ZOUBI H,DARWISH NA,et al. A comprehensive review of nanofiltration membranes:treatment,pretreatment,modelling,and atomic force microscopy[J]. Desalination,2004,170(3):281-308.
[4] LI X Z,ZHAO Q L. Efficiency of biological treatment affected byhigh strength of ammonium-nitrogen in leachate and chemical precipitation of ammonium-nitrogen as pretreatment[J]. Chemosphere,2001,44(1):37-43. [5] LOGAN B E. Microbial fuel cells[M]. New York:John Wiley & Sons,2007. [6] 王维大,李浩然,冯雅丽,等. 微生物燃料电池的研究应用进展[J]. 化工进展,2014,33(5):1067-1076.
[7] 陈立香,肖勇,赵峰. 微生物燃料电池生物阴极[J]. 化学进展,2012,24(1):157-162.
[8] SCHMIDT I,SLIEKERS O,SCHMID M,et al. New concepts of microbial treatment processes for the nitrogen removal in wastewater[J]. FEMS Microbiology Reviews,2003,27(4):481-492.
[9] YOO H,AHN K H,LEE H J,et al. Nitrogen removal from synthetic wastewater by simultaneous nitrification and denitrification (SND)via nitrite in an intermittently aerated reactor[J]. Water Research,1999,33(1):145-154.
[10] VIRDIS B,READ S T,RABAEY K,et al. Biofilm stratification during simultaneous nitrification and denitrification (SND) at a biocathode Bernardino[J]. Bioresource Technology,2011,102(1): 334-341.
[11] VIRDIS B,RABAEY K,ROZENDAL R A,et al. Simultaneous nitrification,denitrification and carbon removal in microbial fuel cells[J]. Water Research,2010,44(9):2970-2980.
[12] YU C P,LIANG Z H,DAS A,et al. Nitrogen removal from wastewater using membrane aerated microbial fuel cell techniques[J]. Water Research,2011,45(3):1157-1164.
[13] SAYESS R R,SAIKALY P E,MUTASEM E F,et al. Reactor performance in terms of COD and nitrogen removal and bacterial community structure of a three-stage rotating bioelectrochemical contactor[J]. Water Research,2013,47(2):881-894.
[14] LOVLEY D R,PHILLIPS E J. Novel mode of microbial energy metabolism:organic carbon oxidation coupled to dissimilatory reduction of iron or manganese[J]. Applied and Environmental Microbiology,1988,54(6):1472-1480.
[15] 国家环境保护总局. 水和废水监测分析方法[M]. 4版. 北京:中国环境科学出版社,2002.
[16] KELLY P T,ZHEN H. Nutrients removal and recovery in bioelectrochemical systems:a review[J]. Bioresource Technology,2014,153(2):351-360.
[17] 张永娟,李永峰,刘春研,等. 利用双室微生物燃料电池处理模拟废水的产电特性研究[J]. 环境科学,2012,33(7): 2427-2431.
[18] PUIG S,SERRA M,VILAR-SANZ A,et al. Autotrophic nitrite removal in the cathode of microbial fuel cells[J]. Bioresource Technology,2011,102(6):4462-4467.
[19] HUANG B C,FENG H J,WANG M Z,et al. The effect of C/N ratio on nitrogen removal in a bioelectrochemical system[J]. Bioresource Technology,2013,132(3):91-98.
[20] ZHANG F,HE Z. Simultaneous nitrification and denitrification with electricity generation in dual-cathode microbial fuel cells[J]. Chemical Technology Biotechnology,2011,87(1):153-159.
[21] 吴伟杰,王混,姜裙秋,等. 无膜生物阴极微生物燃料电池处理生活污水[J]. 哈尔滨商业大学学报(自然科学版),2013,29(2): 160-163.
[22] 薛腾,张建民,孟立刚. 厌氧阳极铵根离子透过质子交换膜的特性[J]. 净水技术,2014,33(6):62-65.
[23] 刘松山. 生物阴极双室微生物燃料电池同步除碳脱氮与产电特性研究[D]. 上海:东华大学,2014.
[24] 谢珊,陈阳,梁鹏,等. 好氧生物阴极型微生物燃料电池的同时硝化和产电的研究[J]. 环境科学,2010,31(7):1601-1606.
Influence of different operation modes on ammonia nitrogen wastewater treatment of microbial fuel cell
ZHAO Huimin1,2,ZHAO Jianqiang1
(1School of Environmental Science and Engineering,Chang'an University,Xi'an 710054,Shaanxi,China;2Department of Chemistry and Chemical Engineering,Heze University,Heze 274015,Shandong,China)
Abstract:Microbial fuel cell(MFC)is an innovative wastewater treatment technique for pollution remove and energy generation. Nitrogen removal using MFC is of great interest owing to the potential benefits of bioenergy production. In this study,simultaneous nitrification and denitrification in the cathode of MFC was investigated. The performance of MFC was influenced by operating methods. The experimental results demonstrated that maximum ammonia nitrogen removal rate was 95.17% under the condition of open circuit,which indicated that the open circuit is beneficial to nitrification while the closed circuit is more advantageous to COD and nitrogen removal,which showed that nitrogen removal depended mainly on accepting electron at cathode. The influence and mechanism of dissolved oxygen (DO) on the performance of nitrogen removal and electricity generation were investigated. The aeration-unaeration process was operated. The aeration lasted 8.5h at the beginning of the whole 20h experiment. The DO was gradually reduced from 4.0mg/L(aeration) to 2.0mg/L(unaeration). The results demonstrated that compared with the operation without aeration,the output voltage significantly increased from 31mV to 120mV and total nitrogen removal rate increased from 0.064g/(L·d) to 0.46g/(L·d). The ammonia nitrogen removal rate was 86.42%. This suggested that theaeration-unaeration process was an effective way to remove nitrogen,produce electricity and reduce the energy input to maintain high DO concentration.
Key words:microbial fuel cell;simultaneous nitrification and denitrification;dissolved oxygen;total nitrogen removal;aeration
中图分类号:X 703
文献标志码:A
文章编号:1000-6613(2016)05-1549-06
DOI:10.16085/j.issn.1000-6613.2016.05.043
收稿日期:2015-12-01;修改稿日期:2015-12-25。
基金项目:陕西省科技发展计划项目(2014K15-03-02)。
