盐酸埃克替尼治疗体力状况较差EGFR基因状态不明肺腺癌的临床疗效
2016-06-14冀晓辉黄露迷王春梅邵江河王东林李代蓉
冀晓辉,黄露迷,王春梅,邵江河,王东林,李代蓉
(重庆市肿瘤研究所肿瘤内科 400030)
盐酸埃克替尼治疗体力状况较差EGFR基因状态不明肺腺癌的临床疗效
冀晓辉,黄露迷,王春梅,邵江河,王东林,李代蓉△
(重庆市肿瘤研究所肿瘤内科400030)
[摘要]目的评价埃克替尼治疗EGFR基因状态不明体力状况较差晚期肺腺癌患者的疗效及安全性。方法分析2012年8月至2014年8月在重庆市肿瘤研究所就诊的27例美国东部肿瘤协作组-体力状况(ECOG-PS)评分大于或等于2分的晚期EGFR基因状态不明肺腺癌患者,口服盐酸埃克替尼125 mg,3次/d,评价近期疗效和不良反应,计算生存率。结果27例患者,客观缓解率(ORR)为29.6%,疾病控制率(DCR)为81.5%,中位无进展生存期(PFS)6个月。ECOG-PS评分得到改善的比例为70.4%,治疗前、后比较差异有统计学意义(Z=-2.157,P=0.031)。毒性反应主要为Ⅰ~Ⅱ度的皮疹、乏力、纳差及腹泻。结论埃克替尼治疗ECOG-PS≥2分、EGFR基因状态不明的晚期肺腺癌患者,不良反应未明显增加,耐受性良好,患者可以从埃克替尼的治疗中明显获益。
[关键词]肺肿瘤;体力状况;EGFR基因;埃克替尼;治疗结果
目前世界范围内,非小细胞肺癌(non-small cell lung cancer,NSCLC)在恶性肿瘤中发病率和病死率均居第一位[1]。其中约2/3的NSCLC患者在最初诊断时已处于中晚期,化学治疗成为治疗的主要选择。化学治疗相比最佳支持治疗,可以将晚期NSCLC患者的1年生存率从20%提高至29%[2]。但因为不良反应,特别是对于体力状况差的患者,传统化学治疗的应用受到较大的限制,进而使最佳支持治疗成为这些患者的治疗选择。
相较于传统细胞毒性化学治疗药物,靶向治疗具有更小的不良反应。埃克替尼是我国自主研发的第一个EGFR-TKI药物,也是继吉非替尼和厄洛替尼后第3个EGFR-TKI药物。ICO-GEN研究[3]是一个比较埃克替尼与吉非替尼治疗晚期NSCLC优劣的Ⅲ期临床研究。结果显示两药疗效无差异,但埃克替尼在不良反应方面优于吉非替尼。后续的2个埃克替尼Ⅳ临床研究亦充分证实了其有效性及相比于吉非替尼较好的安全性[4-5]。
对于EGFR基因敏感突变型的NSCLC患者,埃克替尼疗效明确。而针对EGFR基因状态不明的NSCLC患者,在埃克替尼上市后进行的大样本(n=6 087)Ⅳ期临床研究[4]亦取得不错的疗效。本研究总结分析了自2012年8月以来到本所就诊的27例EGFR基因状态不明、且体力状况较差的肺腺癌患者口服埃克替尼治疗的有效性及安全性,现报道如下。
1资料与方法
1.1一般资料2012年8月至2014年8月在重庆市肿瘤研究所口服盐酸埃克替尼治疗的27例EGFR基因状态不明、美国东部肿瘤协作组-体力状况(Eastern Cooperative Oncology Group-performance status,ECOG-PS)评分大于或等于2分,未接受手术、放射治疗及化学治疗的肺腺癌患者。其中男10例,女17例;年龄34~87岁,中位年龄58岁;ECOG-PS评分,2分6例, 3~4分21例;吸烟12例,不吸烟15例;按2002年美国癌症研究联合会癌症分期手册(第6版)NSCLC分期标准,Ⅲ期5例,Ⅳ期22例。见表1。所有患者治疗前均采集完整病史、体格检查及进行ECOG-PS评分。所有患者基线状态检查均于治疗前28 d内。常规检查包括三大常规、血生化,胸部CT,其他转移部位诊断依据多为临床影像学(CT/MRI)。排除标准:(1)无病理诊断;(2)无可测量的临床病灶;(3)服用埃克替尼过程中伴有其他可能影响患者疗效评价的治疗手段,如放射治疗、化学治疗、介入治疗等;(4)ECOG-PS<2分。

表1 患者一般临床特征[n(%)]
1.2方法
1.2.1方法口服盐酸埃克替尼125 mg,3次/d,持续用药直至肿瘤进展或出现不可耐受的不良反应。治疗4周后进行近期疗效及不良反应评价。停用盐酸埃克替尼后,根据患者的ECOG-PS评分和意愿给予化学治疗、放射治疗或最佳支持治疗。
1.2.2评价标准基线状态评价于治疗前4周内。埃克替尼治疗4周后进行第一次近期疗效评价,以后每8周接受一次CT和其他影像学检查进行疗效评价。客观疗效评价依据RECIST 1.1标准[6],分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、疾病稳定(stable disease,SD)、疾病进展(progressive disease,PD)。客观缓解率(objective response rate,ORR)包括CR率和PR率。疾病控制率(disease control rate,DCR)为CR率、SD率之和。按照美国国立癌症研究所制订的不良反应评价标准(NCI-CTC)3.0版对不良反应进行分级。治疗过程中进行ECOG-PS评分与基线状态ECOG-PS评分比较。
1.2.3随访采用住院、门诊及电话随访结合的随访方法,定期了解27例患者的生存情况,包括ECOG-PS评分、不良反应、客观疗效、死亡时间、意外情况及原因。随访时间的计算自治疗的时间开始到疾病进展、死亡或末次随访时间(2015年7月1日)为止。本研究主要观察指标为无疾病进展生存期(progession-free survival,PFS),PFS计算始于开始治疗的时间,止于确认疾病进展或死亡的时间。次要观察指标为近期有效率(RR)、不良反应、ECOG-PS评分。
2结果
2.1生存情况本研究27例患者,随访时间1~21个月,失访1例,另有1例于治疗5个月后死于肺栓塞。截止2015年7月1日,共有16例患者死亡,2例患者仍在口服埃克替尼治疗,中位PFS为6月。见图1。
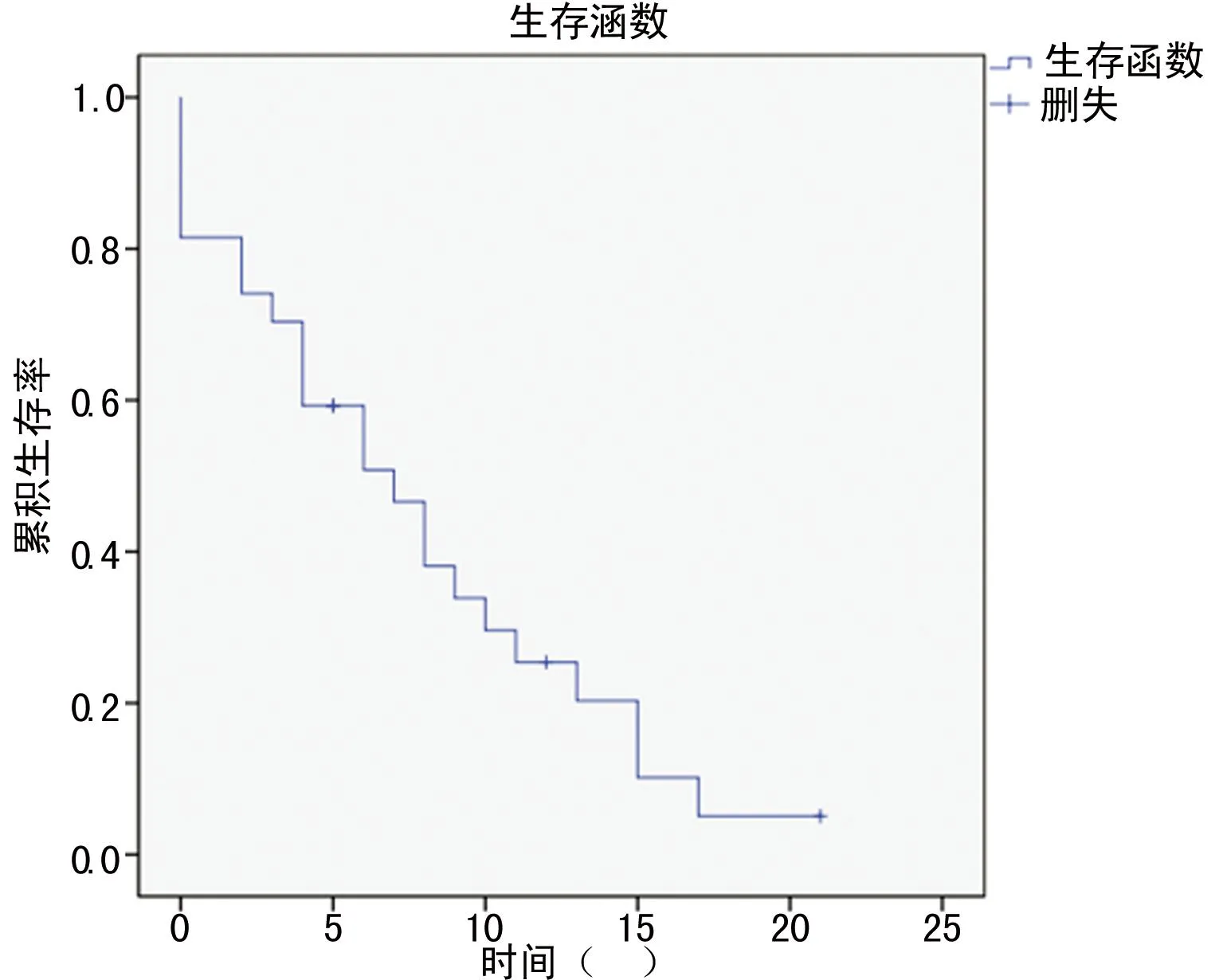
图1 Kaplan-Meier生存曲线
2.2近期疗效评价27例患者中,无CR病例, PR 8例(29.6%),SD 14例(51.9%),PD 5例(18.5%),ORR为29.6%,DCR为81.5%。21例ECOG-PS评分3~4分患者中,无CR病例,PR 5例(23.8%),SD 13例(61.9%),PD 3例(14.3%),ORR为23.8%,DCR为85.7%。
2.3体力状况改善情况27例患者中,在埃克替尼治疗期间,19例(70.4%)患者体力状况得到改善。27例患者治疗前ECOG-PS的评分2~4分,平均(3.04±0.71)分,治疗后ECOG-PS评分1~5分,平均(2.26±1.40)分,治疗前后差异有统计学意义(Z=-2.157,P=0.031)。
2.4不良反应27例患者中,治疗相关不良反应多为轻度,仅有1例患者出现Ⅲ度以上不良反应,无因不可耐受不良反应而退出治疗者。无1例发生间质性肺炎,未发现药物相关性死亡。最常见的不良反应主要为皮疹29.6%(8/27)、乏力18.5%(5/27)、肝功能异常7.4%(2/27)、纳差14.8%(4/27)、腹泻11.1%(3/27),见表2。
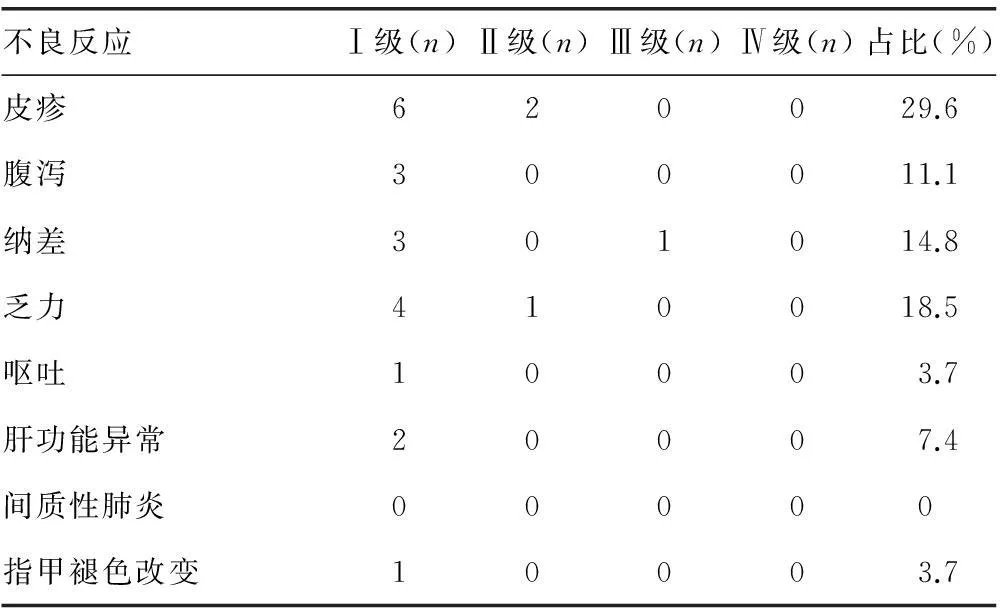
表2 不同级别不良反应发生情况
3讨论
对于PS较差的晚期肺癌患者,目前尚缺乏有效的治疗方案。EGFR-TKI已广泛应用于NSCLC的治疗,特别对于EGFR基因敏感突变型患者,其有效率高、耐受性好等特点,已成为这些患者的主要治疗手段。相对于吉非替尼,ICO-GEN研究[3]显示在晚期NSCLC中。埃克替尼疗效与其相当,但不良反应明显降低,耐受性更好。
尽管埃克替尼对于EGFR基因突变型NSCLC患者疗效确切,耐受性好,其中位PFS为7.8~9.5个月[7-8]。但很多晚期肺癌患者往往由于一般情况差、肿瘤标本取样困难及患者意愿等原因,无法进行EGFR基因检测。埃克替尼在国内上市后,Hu等[4]进行的大样本(n=6 087)Ⅳ期临床研究显示,对于EGFR基因状态不明的NSCLC患者,其ORR为27.3%(1 336/4 884),DCR为78.9%(3 857/4 884),该研究显示对于EGFR基因状态不明的NSCLC患者,埃克替尼仍可取得不错的疗效。
Thatcher等[9]一项随机临床研究显示,在未经选择的NSCLC患者中,相对于最佳支持治疗组,吉非替尼治疗组患者未从治疗中获益。而依据病理类型(腺癌)、吸烟状态(不吸烟)两个临床特征选择后的亚组患者应用吉非替尼治疗,其ORR达到55.6%,已经与EGFR基因突变、ECOG-PS 0~2分的NSCLC患者的ORR相近[10]。本研究显示,通过病理类型筛选,在体力状况较差(ECOG-PS评分大于或等于2分) 的肺腺癌患者中,埃克替尼治疗的中位PFS达到6个月,与最佳支持治疗比较,PFS得到明显延长。本研究中位PFS状况甚至要优于既往报道的EGFR-TKI治疗未经病理类型选择的体力状况较好的NSCLC患者[3]。
在Wheatley-Price等[11]研究中比较分析了厄洛替尼治疗不同ECOG-PS评分组老年NSCLC患者的疗效,显示ECOG-PS 0~1分与2~3分的有效率无差异。其中ECOG-PS≥2分患者的有效率仍可达38.5%,PFS达7.3个月。Zheng等[12]的埃克替尼回顾性研究报道中,42例肺腺癌,其中ECOG-PS>2分者为41例,其中位PFS为7个月,本研究中位PFS低于其研究结果。分析原因,Zheng等研究42例患者中女性为35例,占比83.3%。本研究男女比例则更为均衡。而数项研究均显示女性患者较男性患者对EGFR-TKI治疗具有更好的反应率及更长的生存期[13-14]。对于体力状况较差的EGFR基因状态不明的肺腺癌患者,Zheng等[12]的研究及本研究均证实ECOG-PS评分并不影响埃克替尼的疗效及安全性。但该结果尚需进一步扩大样本的前瞻性随机对照临床研究进一步证实。
本研究观察到对于ECOG-PS评分较差的患者,盐酸埃克替尼不良反应仍较为轻微,与之前大多数报道类似。本研究中主要不良反应为皮疹29.6%(8/27)、乏力18.5%(5/27)、肝功能异常7.4%(2/27)、纳差14.8%(4/27)、腹泻11.1%(3/27),无1例因不良反应减停药物。ICO-GEN研究[3]报道的盐酸埃克替尼药物相关毒副反应发生率为60.5%,皮疹39.5%,腹泻18.5%,本组的不良反应并不高于ICO-GEN试验及埃克替尼Ⅳ期临床结果。间质性肺炎为EGFR-TKI较为严重的并发症,在埃克替尼Ⅰ期临床研究报道中出现1例[15],ICO-GEN研究中未发现[3],而Ⅳ期大样本(n=5 549)研究出现3例间质性肺炎[4]。吉非替尼及厄洛替尼间质性肺炎发生率约为3%~5%[13-14],高于埃克替尼。Zheng等[12]关于ECOG-PS评分较差的晚期肺腺癌患者接受埃克替尼治疗中,1例出现间质性肺炎死亡,而本研究中未发生类似严重不良反应。故ECOG-PS评分差并不影响此类患者的治疗。
综上,本研究显示埃克替尼治疗ECOG-PS≥2分、EGFR基因状态不明的晚期肺腺癌患者,不良反应未明显增加,耐受性良好。该类患者可以从埃克替尼治疗中获益。因样本量小,该结果尚需在后续的研究中进一步完善。
参考文献
[1]Jemal A,Bray F,Center MM,et al.Global cancer statistics[J].CA Cancer J Clin,2011,61(2):69-90.
[2]NSCLC Meta-Analyses Collaborative Group.Chemotherapy in addition to supportive care improves survival in advanced non-small-cell lung cancer:a systematic review and meta-analysis of individual patient data from 16 randomized controlled trials[J].Clin Oncol 2008,26(28):4617-4625.
[3]Shi Y,Zhang L,Liu X,et al.Icotinib versus gefitinib in previously treated advanced non-small-cell lung cancer (ICO-GEN):a randomised,double-blind phase 3 non-inferiority trial[J].Lancet Oncol,2013,14(10):953-961.
[4]Hu X,Han B,Gu A,et al.A single-arm,multicenter,safety-monitoring,phase IV study of icotinib in treating advanced non-small cell lung cancer (NSCLC)[J].Lung Cancer,2014,86(2):207-212.
[5]Tan F,Gu A,Zhang Y,et al.Safety and efficacy results of a phase IV,open-label,multicenter,safety-monitoring study of icotinib intreating advanced non-small cell lung cancer (NSCLC):ISAFE study[J].J Clin Oncol,2013,31:19161.
[6]TherasseP,ArbuckSG,EisenhauerEA,etal.Newguidelinestoevaluatetheresponsetotreatmentinsolidtumors.EuropeanOrganizationforResearchandTreatmentofCancer,NationalCancerInstituteoftheUnited
States,National Cancer Institute of Canada[J].J Natl Cancer Inst,2000,92(3):205-216.
[7]宋正波,余新民,蔡菊芬,等.埃克替尼在晚期非小细胞肺癌EGFR状态明确的患者中的疗效分析[J].中国肺癌杂志,2013,16(3):138-143.
[8]Sun Y,Shi Y,Zhang L,et al.A randomized,double-blind phase Ⅲ study of icotinib versus gefitinib in patients with advanced non-small cell lung cancer (NSCLC) previously treated with chemotherapy (ICOGEN)[J].J Clin Oncol,2011,29(suppl):7522.
[9]Thatcher N,Chang A,Parikh P,et al.Gefitinib plus best supportive care in previously treated patients with refractory advanced non-small-cell lung cancer:results from a randomised,placebo-controlled,multicentre study (Iressa Survival Evaluation in Lung Cancer)[J].Lancet,2005,366(9496):1527-1537.
[10]Lee DH,Han JY,Yu SY,et al.The role of gefitinib treatment for Korean never-smokers with advanced or metastatic adenocarcinoma of the lung:a prospective study[J].J Thorac Oncol,2006,1(9):965-971.
[11]Wheatley-Price P,Ding K,Seymour L,et al.Erlotinib for advanced nonsmall cell lung cancer in the elderly:an analysis of the National Cancer Institute of Canada Clinical Trials Group Study Br.21[J].J Clin Oncol,2008,26(14):2350-2357.
[12]Zheng X,Liu G,Wang S,et al.A new receptor tyrosine kinase inhibitor,icotinib,for patients with lung adenocarcinoma cancer without indication for chemotherapy[J].Oncol Lett,2014,8(4):1563-1566.
[13]O′Connell J,Kris MG,Gralla RJ,et al.Frequency and prognostic importance of pretreatment clinical characteristics in patients with advanced non small cell lung cancer treated with combination chemotherapy[J].J Clin Oncol,1986,4(11):1604-1614.
[14]Radzikowska E,Glaz P,Roszkowski K.Lung cancer in women:age,smoking,histology,performance status,stage,initial treatment,and survival.Population based study of 20 561 cases[J].Ann Oncol,2002,13(7):1087-1093.
[15]ang H,Zhang L,Wang Y,et al.Phase I trial of icotinib,a novel epidermal growth factor receptor tyrosine kinase inhibitor,in Chinese patients with non-small cell lung cancer[J].Chin Med J (Beijing),2011,124(13):1933.
Clinical effects of icotinib on lung denocarcinoma patients with unknown EGFR gene status and poor performance status*
JiXiaohui,HuangLumi,WangChunmei,ShaoJianghe,WangDonglin,LiDairong△
(DepartmentofMedicalOncology,ChongqingCancerInstitute,Chongqing400030,China)
[Abstract]ObjectiveThis research is aimed to investigate the efficacy and toxicity of icotinib for lung adenocarcinoma patients with poor performance status and unknown EGFR gene status.MethodsA total of 27 lung adenocarcinom patients with poor Eastern Cooperative Oncology Group-Performance status(ECOG-PS) and unknown EGFR gene status referred to Chongqing Cancer Institute from August 2012 to August 2014 were analyzed.Icotinib (125 mg) was orally administered three times per day.Asess the efficacy and adverse reaction,calculate survival rates.ResultsAmong the 27 patients,the objective response rate(ORR) and disease control rates(DCR) were 29.6% and 81.5%,respectively.The median progression free survival time was 6.0 months.A total of 70.4% of patients had an significant improvment in ECOG-PS scores,following icotinib treatment (Z=-2.157,P=0.031).Fatigue,anorexia and diarrhea were the most frequent adverse reaction,which defined as grade 1 to 2 rashes.ConclusionLung adenocarcinoma patients with poor performance status and unknown EGFR gene status may benefit from icotinib therapy,and patients were tolerated well.
[Key words]lung neoplasms;performance status;EGFR gene;icotinib;treatment outcome
doi:论著·临床研究10.3969/j.issn.1671-8348.2016.02.014
基金项目:重庆市医学科研计划资助项目[(重点)2015-277]。
作者简介:冀晓辉(1984-),主治医师,硕士,主要从事肺癌综合治疗研究。 △通讯作者,E-mail:lidairong@sohu.com。
[中图分类号]R734.2
[文献标识码]A
[文章编号]1671-8348(2016)02-0189-03
(收稿日期:2015-08-25修回日期:2015-09-20)
