海藻多糖空心胶囊的制备工艺研究
2016-03-24于海宁郭正昭单伟光
于海宁,郭正昭,刘 研,单伟光
(浙江工业大学 药学院,浙江 杭州 310014)
海藻多糖空心胶囊的制备工艺研究
于海宁,郭正昭,刘研,单伟光
(浙江工业大学 药学院,浙江 杭州 310014)
摘要:以天然海藻卡拉胶、羟丙基甲基纤维素和聚乙二醇为原料,研究海藻多糖空心胶囊的制备技术及工艺条件.通过单因素试验和正交试验,研究配方比例和生产条件对海藻空心胶囊制备工艺的影响,通过考察成品率、脆碎率、崩解时限和含水量等指标,获得海藻空心胶囊的最佳配方和工艺条件.实验结果表明:当卡拉胶的质量浓度为35 mg/mL、PEG400质量浓度为15 mg/mL、羟丙基甲基纤维素的质量浓度为20 mg/mL、溶胶温度为85 ℃、溶胶时间为20 min、烘干温度为65 ℃以及烘干时间为0.5 h时,制备出的空心胶囊崩解时限≤10 min,干燥失重符合标准.
关键词:海藻;卡拉胶;植物空心胶囊
硬壳空心胶囊是一种重要的药辅材料[1],它是随制剂一起进入人体消化系统后再被人体所吸收,故食用的安全性与空心胶囊的质量安全标准息息相关.目前,市场上的空心胶囊仍以明胶胶囊为主[2-6],而明胶胶囊的缺陷也日益明显,研发植物空心胶囊在国内外广受关注,植物空心胶囊的应用市场显现出了极大的发展潜力.我国植物空心胶囊制备技术较欧美国家仍较落后,而用于植物空心胶囊制备的材料包括羟甲基纤维素、多糖及淀粉类[7-9].
我国海藻资源丰富,有多种生物活性物质,并且海藻在制药工业、食品工业和日用品工业等领域有广阔的研究与开发前景[10-14].长期以来,海藻多糖的药理及生物活性功能的开发研究受到广泛关注,并取得了诸多成果[15-16].海藻卡拉胶作为辅料制备植物空心胶囊已有报道,但其配方所含卡拉胶等海藻多糖的比例较低,成分多以纤维素类物质为主[17-18].笔者通过实验探索,获得了以海藻卡拉胶为主要成分的植物空心胶囊配方,以期为后续的海藻空心胶囊制备和产品研发奠定基础,也为新型植物空心胶囊研制提供技术参考.同时,利用海藻多糖制备植物空心胶囊可有效利用资源,特别是利用低值海藻为原料将显著提高海藻加工产业的附加值,对海藻种植及加工行业发展均有一定的促进作用.
1材料与方法
1.1 材料和试剂
海藻卡拉胶购自武汉兴众诚生物科技有限公司;聚乙二醇400购自国药集团化学试剂有限公司,文中称为PEG400;蒸馏水购自娃哈哈矿泉水有限公司;羟丙基甲基纤维素购自山东阿胶药业有限公司,粘度规格为5 mPa·s,文中称为HPMC.
1.2 仪器和设备
电子分析天平(BS224S型,北京赛多利斯仪器系统有限公司);电热恒温水浴锅(H-1012398,上海精宏实验设备有限公司);电热恒温鼓风干燥箱(DGG-9053AD,上海森信实验仪器有限公司);中药材粉碎机(FW500,郑州科丰仪器设备有限公司);真空干燥箱(DZF-6020,上海精密实验设备有限公司);磁力搅拌器(85-2型,上海志威电器有限公司).
1.3 实验方法
1.3.1海藻空心胶囊制备方法
1) 溶胶:加热纯净水至80~90 ℃,缓慢加入海藻卡拉胶,搅拌,加热至形成透明溶液.加入羟丙基甲基纤维素和聚乙二醇,恒温处理,使之融化为均匀的胶液,除去液面上的泡沫,备用.
2) 蘸胶成型:胶囊模具上油,蘸胶,翻转数次,冷却成型.
3) 干燥:电热恒温鼓风干燥机干燥.
4) 拔壳与剪切:拔下囊胚,剪切至规定长度[19].
1.3.2工艺最优参数的确定
1) 单因素试验:依次改变卡拉胶质量浓度、聚乙二醇质量浓度、羟丙基甲基纤维素质量浓度、溶胶温度、溶胶时间、烘干温度和烘干时间等,以海藻空心胶囊成品率、脆碎率、外观评分、崩解时限、重量差异和含水量等为指标,评价各因素最佳工艺条件.
2) 在单因素试验基础上确定各因素水平,并进行正交试验设计[20].
1.3.3测定指标及方法
1) 成品率
按比例称取各成分混合溶胶,再对胶液进行保温,使用模具蘸胶→干燥→拔膜、切割和整理→成品.成品率的计算式为
成品率=成品个数/实验所制个数×100%
2) 脆碎率
取10粒空心胶囊放于表面皿中,再移入盛有硝酸镁饱和溶液的干燥器中,在25 ℃下恒温储藏24 h后再取出,立即分别逐粒放入直立在厚度为2 cm的木板上的玻璃管内,最后将圆柱形砝码(20 g)从玻璃口处自由落下,观察胶囊是否破裂.脆碎率的计算式为
脆碎率=破碎的胶囊个数/实验胶囊个数×100%
3) 外观评分
外观感官评分分为色泽均匀、形状规则、有无气泡、有无砂眼、外观光洁和无切口缺裂等五个指标,每个指标满分10 分,结果为10个人评分后的平均值.
4) 崩解时限
取6 粒胶囊,装入滑石粉,闭合,分别置于吊篮的玻璃杯中(无需加挡板),根据药典附录XA中胶囊剂项下崩解时限检查法,测定.介质为自来水,水温为(37±0.5) ℃.
5) 重量差异
同一批所制得的胶囊的重量方差.
6) 含水量
称取空心胶囊1.07 g,分开胶囊的帽和体,在105 ℃下干燥6 h,对空心胶囊进行称重,两次重量之差与空心胶囊的原重之比即为含水量[21].
2结果与分析
2.1 单因素试验结果与分析
2.1.1海藻空心胶囊配方单因素实验
1) 卡拉胶质量浓度对海藻空心胶囊的影响
在PEG400质量浓度为30 mg/mL、HPMC质量浓度为20 mg/mL、溶胶温度为80 ℃、溶胶时间为30 min、烘干温度为50 ℃以及烘干时间为1 h的条件下,考察卡拉胶质量浓度对海藻空心胶囊的影响.卡拉胶质量浓度分别为20,30,40,50,60 mg/mL,测定各处理组的各项指标,如表1所示.
从表1可知:在成品率方面,当卡拉胶质量浓度为40~50 mg/mL时,海藻空心胶囊可成型;脆碎率在卡拉胶质量浓度为40~50 mg/mL处最低,即不易发生脆碎现象;外观评分在卡拉胶质量浓度为40 mg/mL处最高;崩解时限在卡拉胶质量浓度为40 mg/mL处所需时间最短;重量差异在卡拉胶质量浓度为40~50 mg/mL处最低;含水量符合药典标准小于12.5%.综上所述,选取35,40,45 mg/mL为正交实验卡拉胶质量浓度的三水平.
2) PEG400质量浓度对海藻空心胶囊的影响
在卡拉胶质量浓度为40 mg/mL、HPMC质量浓度为20 mg/mL、溶胶温度为80 ℃、溶胶时间为30 min、烘干温度为50 ℃以及烘干时间为1 h的条件下,考察PEG400质量浓度对海藻空心胶囊的影响,测定各处理组的各项指标,如表2所示.
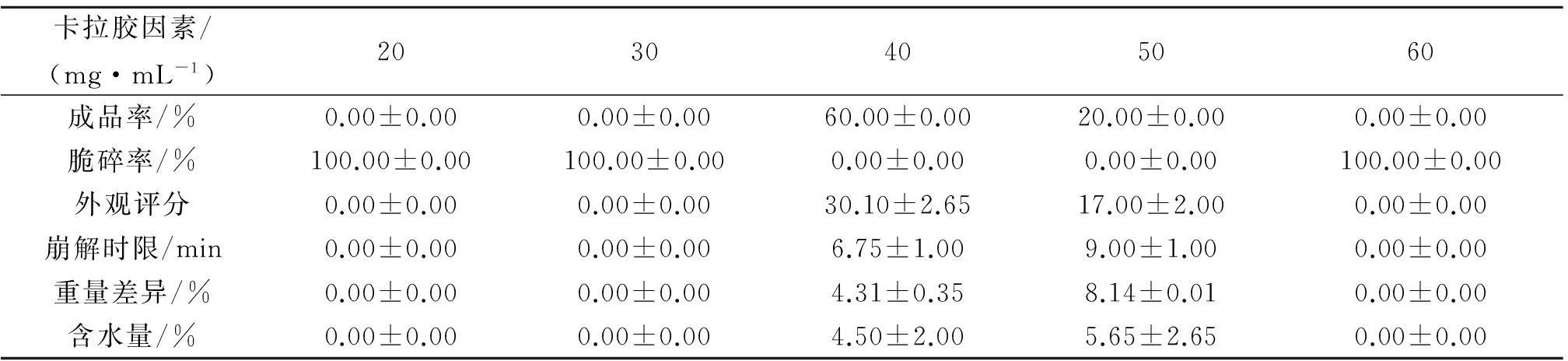
表1 卡拉胶质量浓度因素对海藻空心胶囊的影响
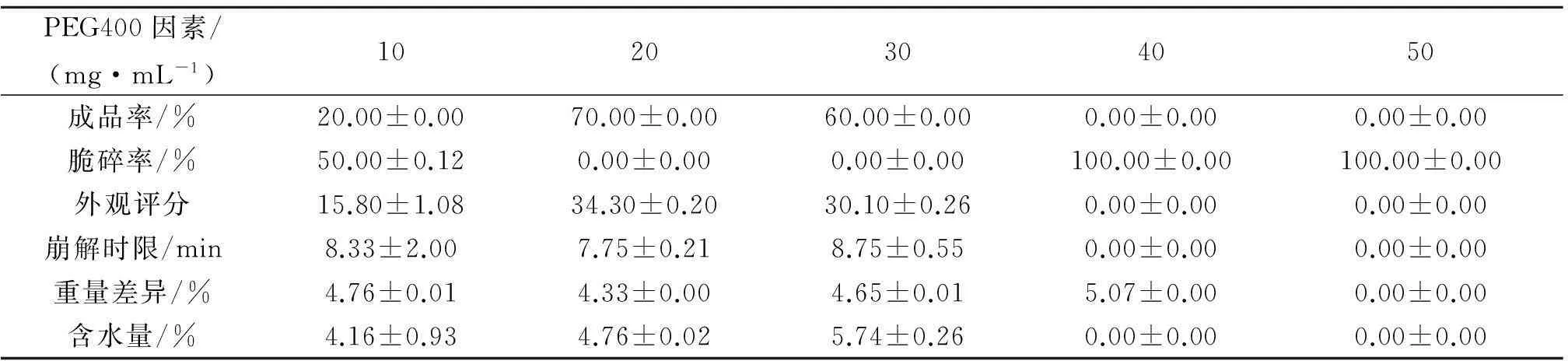
表2 PEG400质量浓度因素对海藻空心胶囊的影响
由表2可知:PEG400质量浓度为10~30 mg/mL时海藻空心胶囊可成型;脆碎率在PEG400质量浓度为20~30 mg/mL处最低;外观评分在PEG400质量浓度为20 mg/mL处最高;崩解时限在PEG400质量浓度为20 mg/mL处所需时间最短;重量差异也是在PEG400质量浓度为20 mg/mL处最低;含水量都符合药典标准.综上所述,选取15,20,25 mg/mL为正交实验PEG400质量浓度的三水平.
3) HPMC质量浓度对海藻空心胶囊的影响
在卡拉胶的质量浓度为40 mg/mL、PEG400质量浓度为20 mg/mL、溶胶温度80 ℃、溶胶时间为30 min、烘干温度为50 ℃以及烘干时间为1 h的条件下,考察HPMC质量浓度对海藻空心胶囊的影响,测定各处理组的各项指标,如表3所示.

表3 羟丙基甲基纤维素质量浓度因素对海藻空心胶囊的影响
由表3可知:在本实验HPMC质量浓度范围内,海藻空心胶囊均可成型,但是在质量浓度为20 mg/mL处,成品率最高;脆碎率在HPMC质量浓度为20~30 mg/mL处最低;外观评分在HPMC质量浓度为20 mg/mL处最高;崩解时限在HPMC质量浓度为20 mg/mL处所需时间最短;重量差异也是在HPMC质量浓度为10 mg/mL处最低,但与20 mg/mL处的数据相差不大;含水量都符合药典标准.故综上所述,选取15,20,25 mg/mL为正交实验HPMC质量浓度的三水平.
2.1.2海藻空心胶囊生产工艺单因素实验
1) 溶胶温度对海藻空心胶囊的影响
在卡拉胶的质量浓度为40 mg/mL、PEG400质量浓度为20 mg/mL、HPMC质量浓度为20 mg/mL、溶胶时间为30 min、烘干温度为50 ℃以及烘干时间为1 h的条件下,考察溶胶温度对海藻空心胶囊的影响,测定各处理组的各项指标,如表4所示.
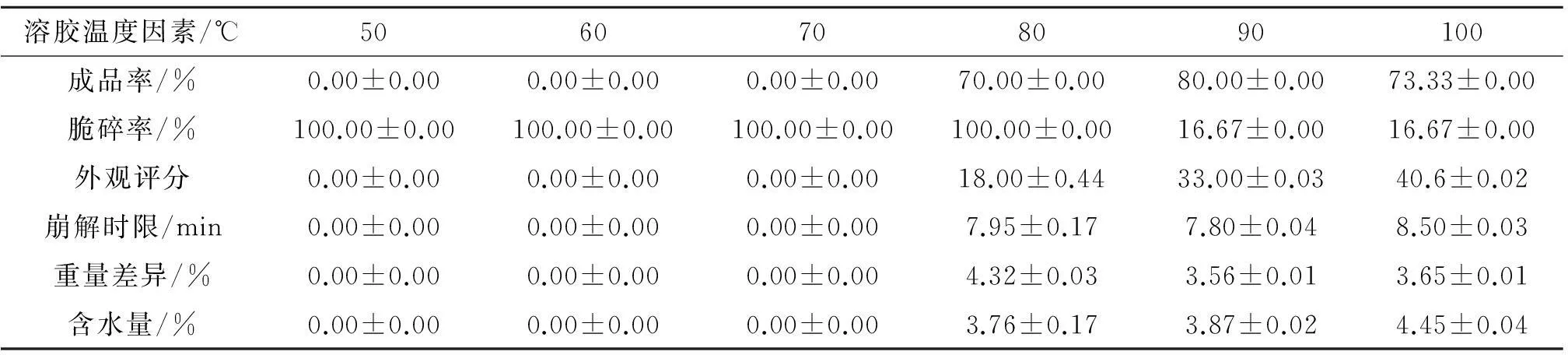
表4 溶胶温度因素对海藻空心胶囊的影响
由表4可知:溶胶温度为80~100 ℃时,海藻空心胶囊可成型;脆碎率在溶胶温度为90~100 ℃处最低;外观评分在溶胶温度为100 ℃处最高;崩解时限在溶胶温度为90 ℃处所需时间最短;重量差异是在溶胶温度为90 ℃处最低;含水量都符合药典标准.综上所述,选取85,90,95 ℃为正交实验溶胶温度的三水平.
2) 溶胶时间对海藻空心胶囊的影响
在卡拉胶的质量浓度为40 mg/mL、PEG400质量浓度为20 mg/mL、HPMC质量浓度为20 mg/mL、溶胶温度为90 ℃、烘干温度为50 ℃以及烘干时间为1 h的条件下,考察溶胶时间对海藻空心胶囊的影响,测定各处理组的各项指标,如表5所示.
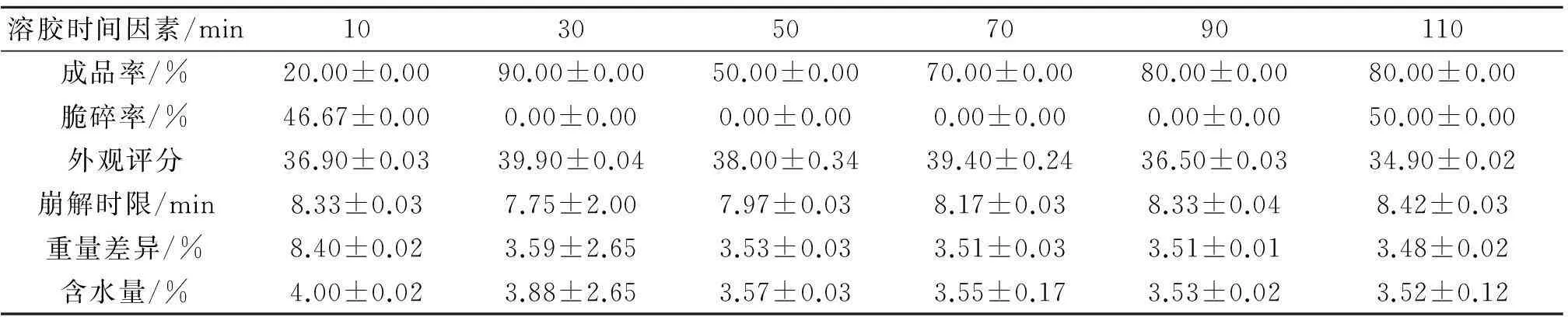
表5 溶胶时间因素对海藻空心胶囊的影响
由表5可知:在溶胶时间为30 min处的成品率最高;脆碎率在溶胶时间为30~90 min处最低;外观评分在溶胶时间为30 min处最高;崩解时限在溶胶时间为30 min处所需时间最短;重量差异是在溶胶时间30~110 min之间都差异不大;含水量都符合药典标准.综上所述,选取20,30,40 min为正交实验溶胶时间的三水平.
3) 烘干温度对海藻空心胶囊的影响
在卡拉胶的质量浓度为40 mg/mL、PEG400质量浓度为20 mg/mL、HPMC质量浓度为20 mg/mL、溶胶温度为90 ℃、溶胶时间为30 min以及烘干时间为1 h的条件下考察烘干温度对海藻空心胶囊的影响,测定各处理组的各项指标,如表6所示.
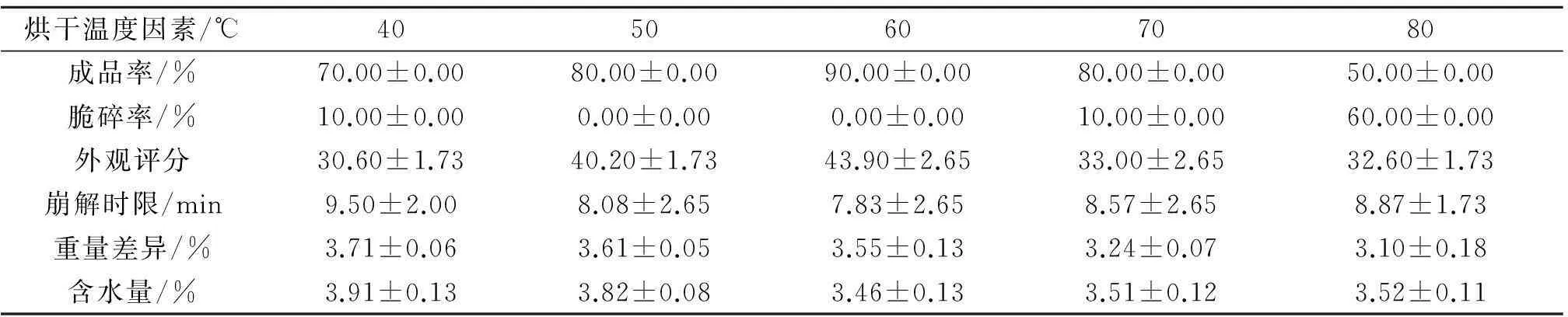
表6 烘干温度因素对海藻空心胶囊的影响
由表6可知:从成品率来看,在烘干温度为60 ℃条件下成功的概率更高;脆碎率在烘干温度为50~60 ℃处最低;外观评分在烘干温度为60 ℃处最高;崩解时限在烘干温度为60 ℃处所需时间最短;重量差异在40~90 ℃之间的数据差距都不大;含水量都符合药典标准.故综上所述,选取55,60,65 ℃为正交实验烘干温度的三水平.
4) 烘干时间对海藻空心胶囊的影响
在卡拉胶的质量浓度为40 mg/mL、PEG400质量浓度为20 mg/mL、HPMC质量浓度为20 mg/mL、溶胶温度为90 ℃以及烘干温度为60 ℃的条件下,考察烘干时间对海藻空心胶囊的影响.测定各处理组的各项指标,如表7所示.
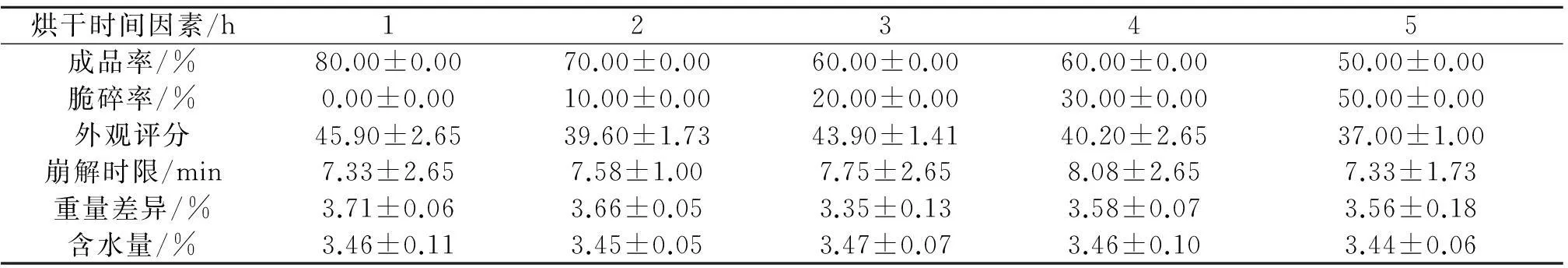
表7 烘干时间对海藻空心胶囊的影响
由表7可知:从成品率来看,在烘干时间为5 h时,成品的概率更高;脆碎率在烘干时间为1 h处最低;外观评分在烘干时间为1 h处最高;崩解时限在烘干时间为1 h和5 h处所需时间最短;重量差异在烘干时间为1~5 h内,相互之间的差异都不大;含水量都符合药典标准.综上所述,选取0.5,1,1.5 h为正交实验烘干时间的三水平.
2.2 正交试验结果及分析
根据单因素实验结果进行七因素三水平正交实验L18(37)(表8),制备各配方以及工艺条件下的海藻空心胶囊,并测量各指标,结果如表9所示.
根据表9中关于海藻空心胶囊的正交实验数据分析,得出结果见表10.
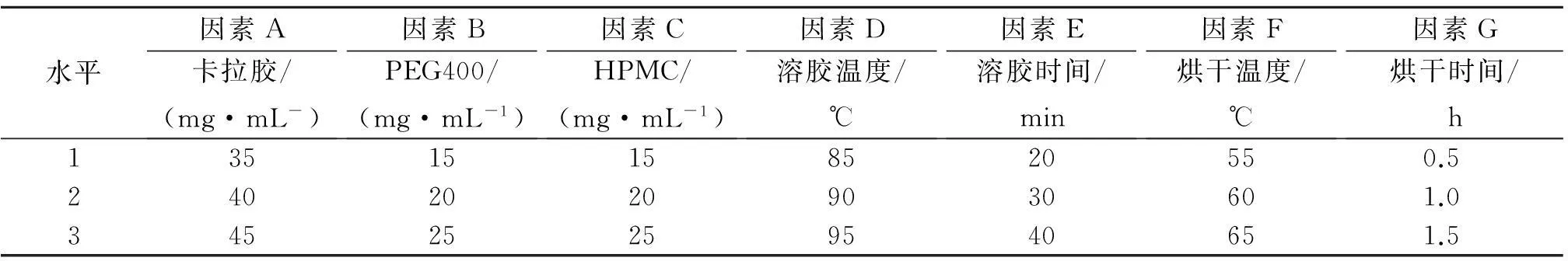
表8 正交试验因素水平编码表
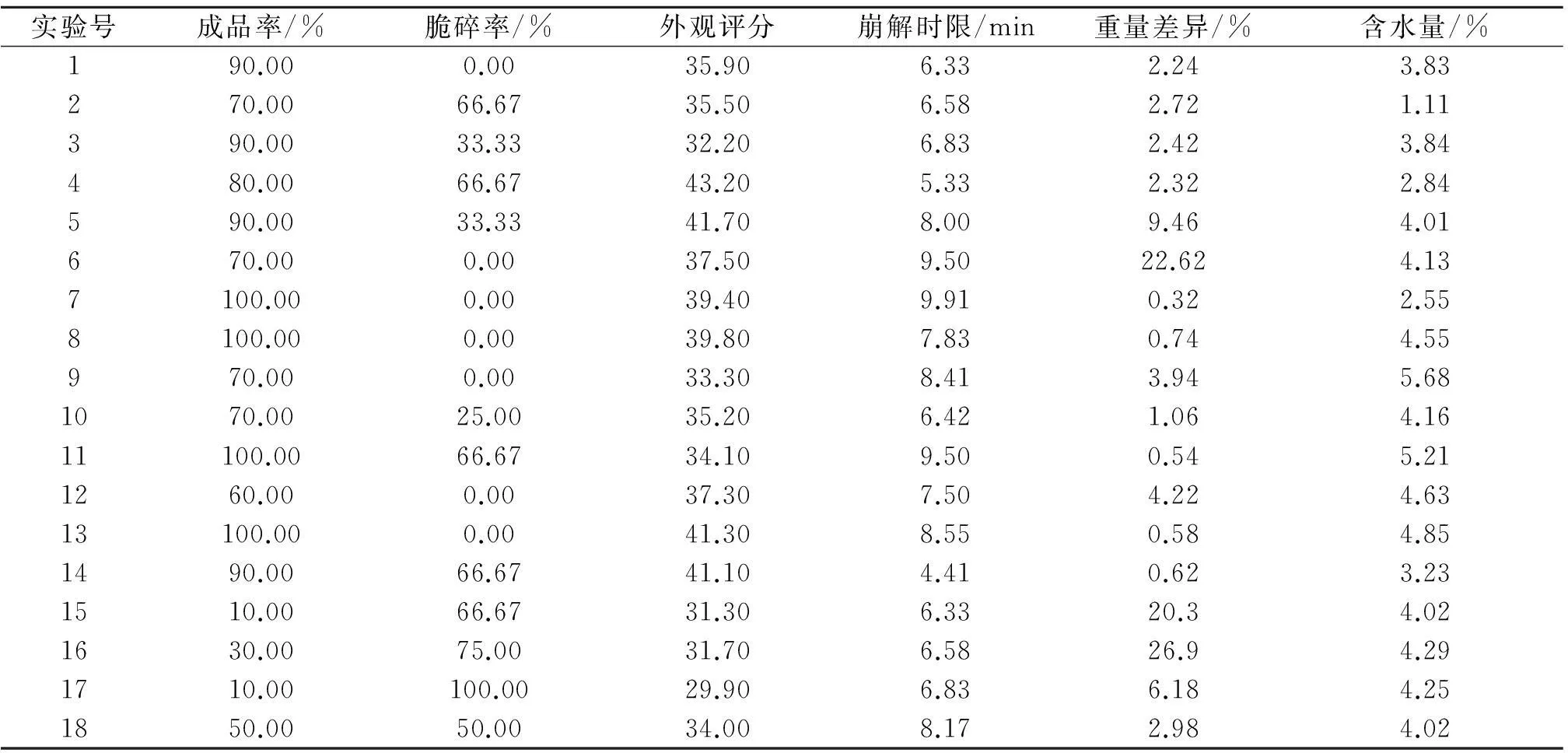
表9 L18(37)正交实验设计与结果
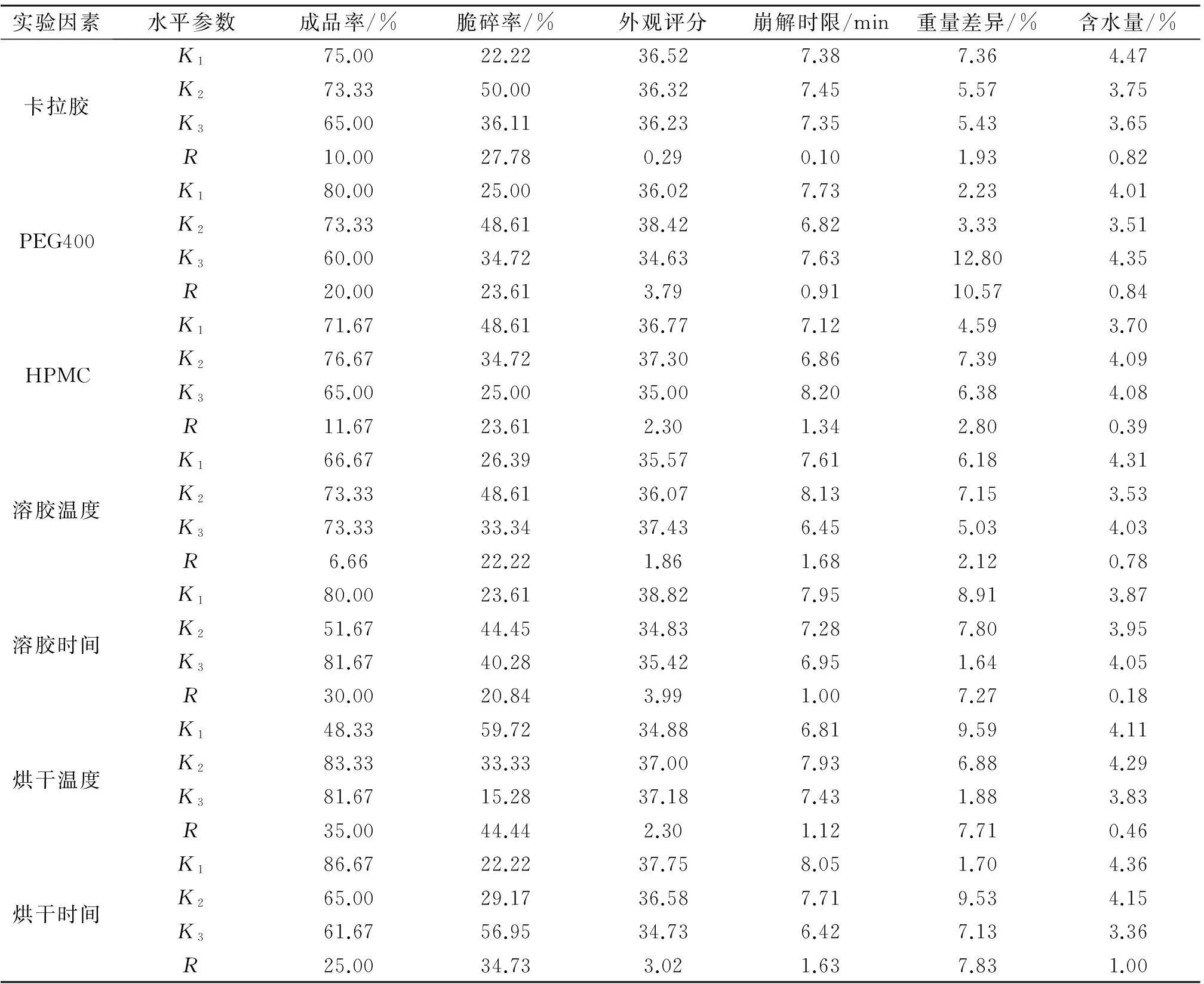
表10 L18(37)正交实验结果分析
由表10结果可知:崩解时限、重量差异及含水量均符合药典要求,因此可以不作为考察指标.从成品率角度来看,各因素对成品率的影响次序:烘干时间>烘干温度>熔胶时间>PEG400>HPMC>卡拉胶>溶胶温度.从脆碎率角度分析,各因素对脆碎率的影响大小为:烘干温度>烘干时间>卡拉胶>PEG400=HPMC>溶胶温度>熔胶时间.从外观评分来看,各因素对外观的影响大小:熔胶时间>PEG400>烘干时间>烘干温度=HPMC>溶胶温度>卡拉胶.综合成品率、脆碎度及外观评分三个考察指标可得:当卡拉胶质量浓度取K1水平时,成品率最高、脆碎率最低及外观评分最高,因此本实验应选择K1水平作为卡拉胶最佳质量浓度.PEG400质量浓度为K1水平时,成品率最高、脆碎率最低,外观评分最高的水平是K2,由于K1和K2水平外观评分差异不大,因此综合考虑选择K1水平作为PEG400最佳质量浓度.当HPMC质量浓度在K2水平时,成品率最高,脆碎率最低的水平是K3,外观评分最高的水平是K2,由于HPMC质量浓度对各指标影响次序相同,且HPMC质量浓度在K2,K3水平之间变化时,成品率波动幅度大于脆碎率,因此综合考虑选择成品率最高时的HPMC质量浓度,即本试验选择K2水平作为HPMC的最佳质量浓度.溶胶温度在K2和K3水平时,成品率最高且相同,在K1水平时,脆碎率最低,在K3水平其外观评分最高,因为溶胶温度对成品率是最次要影响因素,对脆碎率和外观评分影响次序相同,但对于脆碎率的影响幅度大于外观评分,所以选择脆碎率最低的溶解温度K1作为本试验最佳溶胶温度.当溶胶时间在K3水平时,成品率最高,溶胶时间在K1水平时,脆碎率最低、外观评分最高,因为溶胶时间是影响外观评分的最主要因素,且溶胶时间在K1和K3水平对成品率影响差异不大,因此选择K1水平作为本试验的最佳溶胶时间.烘干温度在K3水平时,脆碎率最低、外观评分最高,烘干温度在K2水平其成品率最高,由于烘干温度是影响脆碎率的最主要因素,且K2和K3水平时的烘干温度对成品率影响的差异较小,所以本试验选择K3水平作为本试验最佳烘干温度.当烘干时间取K1水平时,成品率最高、脆碎率最低及外观评分最高,因此本实验应选择K1水平作为最佳烘干时间.
由上述分析结果得出海藻空心胶囊制备工艺的最佳条件:卡拉胶的质量浓度为35 mg/mL、PEG400的质量浓度为15 mg/mL、HPMC质量浓度为20 mg/mL、溶胶温度为85 ℃、溶胶时间为20 min、烘干温度为65 ℃以及烘干时间为0.5 h.
2.3 海藻空心胶囊制备最佳工艺验证实验
在最佳工艺条件下进行海藻空心胶囊的验证实验,结果如表11所示.

表11 制备工艺验证实验
由表11可知:正交实验所得最佳工艺条件下,海藻空心胶囊的各项指标优于其他参数组合,这说明正交实验优化获得的海藻空心胶囊最佳配方和工艺条件可信,具有一定的推广应用价值与前景.
3结论
通过单因素实验及正交实验,以成品率、脆碎率、崩解时限和含水量等作为考察指标,探讨卡拉胶质量浓度、PEG400质量浓度、HPMC质量浓度、溶胶温度、溶胶时间、烘干温度和烘干时间对海藻空心胶囊制备工艺的影响.结果得出海藻空心胶囊制备的最佳工艺条件.在该工艺条件下,制作出的海藻空心胶囊的崩解时限、干燥失重等指标都满足相关规定.同时植物空心胶囊所选用的植物性囊材是新的探索,也为植物空心胶囊的实际生产应用奠定基础.
参考文献:
[1]李亚琴,周建平.药物制剂工程[M].北京:化学工业出版社,2008.
[2]郭燕峰.空心硬胶囊的发展状况.明胶科学与技术[J].2007,27(3):123-125.
[3]吴佩,张秀梅,李婷,等.海藻多糖复合胶成膜性研究[J].海洋与湖沼,2010,41(1):46.
[4]张小菊,姜发堂.羧甲基魔芋葡甘聚糖的制备及应用于空心胶囊囊材的研究[J].食品科学,2004,25(10):200-203.
[5]郑化,杜予民,周金平,等.纤维素与甲壳素共混膜的结构表征与抗凝血性能[J].高分子学报,2002(4):525-529.
[6]侯惠民,王浩,张光杰.药用辅料应用技术[M].2版.北京:中国医药科技出版社,2002.
[7]刘李梅,韩丽,杨明,等.植物空心胶囊的研究进展[J].中药与临床,2014,5(5):60-63.
[8]易喻,江威,应国清,等.羟甲基壳聚糖的制备及性能研究[J].浙江工业大学学报,2011,39(1):17-20.
[9]董玲玲,黄鑫,齐阳光,等.酶解-微波法提取黄芪多糖的工艺研究[J].浙江工业大学学报,2011,39(5):528-531.
[10]邓志峰,纪明侯.龙须菜和扁江蓠多糖的组成及其抗肿瘤效果[J].海洋与湖沼,1995,26(3):575-581.
[11]于海宁,朱惊,单伟光,等.大孔树脂法用于江蓠多糖脱色的工艺研究与优化[J].浙江工业大学学报,2014,42(4):419-421.
[12]PODCZECK F, JONES B E. Pharmaceutical capsules[M]. London: Pharmaceutical Press,2004:2-16.
[13]马欢杰.多糖类抗肿瘤作用的研究进展[J].海峡药学,2010,22(2):102-104.
[14]王安利,胡俊荣.海藻多糖生物活性研究新进展[J].海洋科学,2002,26(9):36-39.
[15]熊皓平,吉宏武,邵海艳.海藻多糖化学及生物活性的研究进展[J].天然产物研究与开发,2007,19:165-169.
[16]吴佩,李婷,李敬,等.海藻多糖空心胶囊药物溶出度研究[J].海洋科学,2010,34(20):18-19.
[17]李婷,吴佩,韩丽君,等.海藻多糖植物空心胶囊体内生物利用度与生物等效性研究[J].海洋与湖沼,2010,41(6):874-875.
[18]赵国华,陈宗道,李志孝,等.活性多糖的研究进展[J].食品与发酵工业,2001,27(7):45-48.
[19]钱俊青,唐振兴.一种制作空心胶囊的配方及其制备方法:中国,CN1623529A[P].2005-06-08.
[20]吴佩,张秀梅,李婷,等.海藻多糖复合胶成膜性研究[J].海洋与湖沼,2010,41(6):148-153.
[21]国家药典委员会.中华人民共和国药典(二部)[M].北京:化学工业出版社,2010.
(责任编辑:陈石平)
Preparation of technical algal hollow capsule
YU Haining, GUO Zhengzhao, LIU Yan, SHAN Weiguang
(College of Pharmaceutical Science, Zhejiang University of Technology, Hangzhou 310014, China)
Abstract:A new kind of algae hollow capsules which were made from natural algae carrageenan, hydroxypropyl methylcellulose and polyethylene glycol was developed. Through single factor experiments and orthogonal experiments, the yield rate friability, disintegration time and water content were used as indicators to optimize formulation and process conditions. The best preparation conditions were as follows: algae carrageenan concentration was 35 mg/mL, concentration of PEG400 was 15mg/mL, concentration of hydroxypropyl methyl cellulose was 20 mg/mL, sol temperature was 85 ℃, sol time was 20 min, drying temperature was 65 ℃ and drying time was 0.5 h. And under these conditions, the capsules had good formability, disintegration time limited≤10 min, and the drying weight losses and the ash contents both met the requirements of the national standard.
Keywords:gracilaria; carrageenan; plants hollow capsules
中图分类号:R944.5
文献标志码:A
文章编号:1006-4303(2016)01-0092-07
作者简介:于海宁(1977—),女,山东潍坊人,副教授,研究方向为天然药物,E-mail: yuhaining@zjut.edu.cn.
基金项目:浙江省自然科学基金资助项目(LQ12C02003)
收稿日期:2015-06-04
