野生药用植物红茂草生物碱化学成分的研究
2015-12-25索有瑞王廷璞
赵 强,索有瑞,王廷璞
(1.天水师范学院 生物工程与技术学院,甘肃 天水 740001;2.中国科学院 西北高原生物研究所,青海 西宁 810008)
红茂草[Dicranostigma leptodum(maxim.)Fedde,DLF]又名秃疮花、秃子花、勒马回(陕西),为罂粟科秃疮花属植物,通常为两年或多年生草本。19世纪后期,俄国植物学家C.J.Maximwicz根据1876年Potaini采自甘肃的标本,发表为Glaucum leptopodumMaxim.,并结合1909年德国植物学家F.Fedde的姓名,组合成为Dicranostigma leptopodum(Maxim.)Fedde.该植物生长于海拔400~2900(~3700)m的丘陵、草坡、路旁、田埂、墙头、屋顶等处,耐旱、耐瘠薄,有一定的抗逆性。[1]主要分布于我国青海东南部、甘肃南部至东南部、陕西秦岭北坡至西南,在山西南部、河北西南部、河南西北部、云南西北部、四川西部和西藏南部有零星分布。因其盛花期蒴果成熟后,植株茎端呈暗红色,故甘陕地区称其为红茂草。该草味苦、涩、性凉,民间全草入药,能清热解毒、消肿止痛、杀虫,治疗扁桃腺炎、咽喉痛、淋巴结核、秃疤、疥癣等症。[1-3]
从20世纪80年代开始,对红茂草药理作用的研究一直没有间断,但对其主要生物碱化学成分的分离和鉴定却报道不多。本实验从红茂草主要生物碱的提取、分离及鉴定入手,利用Al2O3柱层析用对红茂草主要生物碱进行柱色谱分离,以TLC法检测,合并流份、浓缩纯化,并利用超导核磁共振等技术鉴定其化合物的结构,以期为野生药用植物红茂草的进一步深入研究提供了实验依据。
1 材料与方法
1.1 材料
1.1.1 药材
红茂草(采自甘肃省天水市秦州区北山自然生长的红茂草,天水师范学院王廷璞研究员鉴定。自然干燥、粉碎、过筛。)
1.1.2 仪器与试剂
RE52-99型旋转蒸发仪(上海亚荣生化仪器厂);UV-9200型紫外可见光分光光度计(北京瑞利仪器分析有限公司);SGWX-4型显微熔点仪(上海精密科学仪器有限公司);Lambda 35型紫外可见光光度计(Perkin Elmer Precisely产品);Spectrum one B型傅立叶变换红外光谱仪(Perkin Elmer Precisely产品);核磁1D NMR和2D NMR:Varian INOVA-400MHz核磁共振仪,溶剂为CDCl3或DMSO-d6;质谱 ESI-MS:Bruker APEX II;341 型旋光仪;AB104-S型电子分析天平、紫外灯等。
异紫堇碱标准品(ABCR GmbH&CO.KG(Germany),批号:166401,规格:10mg),紫堇碱标准品 (ABCR GmbH&CO.KG(Germany), 批 号 :260599,规格:10mg)、原阿片碱标准品(Shanghai tautd biotech CO.LTD(China),批号:E-0411,规格:10mg),白屈菜碱标准品(Pure-one Bio Technology,CO.LTD(China),批号:060306,规格:20mg)、95%乙醇、无水乙醇、冰乙酸、氨水、层析用Al2O3(200~300目)、薄层色谱硅胶G、CMC-Na、氯仿、甲醇、氨水、三乙胺、NaOH、盐酸、三重蒸馏水等,其余试剂均为国产或进口分析纯。
1.2 方法
准确称取红茂草干草粉末500g,置于3000mL锥形瓶中,加入400mL 95%乙醇,振荡摇匀,封口浸泡2~3d.超声波振荡1h后,减压、浓缩,得浸膏18g.将浸膏纱布包裹,悬于水溶液中,加2%NaOH,调至pH在9~10,用氯仿萃取,萃取液减压浓缩,得提取部分A.水溶液加入稀盐酸,调至pH=6,用氯仿萃取,萃取液减压浓缩,得提取部分B.层析用Al2O3干法装柱,氯仿-甲醇-三乙胺(8︰1︰0.5)为洗脱剂对A部分提取物进行梯度洗脱,收集不同时间段的流份,以95%乙醇︰冰乙酸︰水︰氨水(3︰0.1︰0.5︰0.1)展开剂,在硅胶G薄板上点样,紫外灯下观察,合并Rf值相同流份,依次浓缩,得化合物Ⅰ(3.02mg)和Ⅱ(0.91mg)。同理,逐渐加大洗脱剂中氯仿的比例,得化合物Ⅲ(0.83mg)。依上法,用无水乙醇-氯仿-氨水(1︰1︰0.1)为洗脱剂,对B部分提取物进行洗脱,经处理浓缩的化合物Ⅳ(0.46mg)。
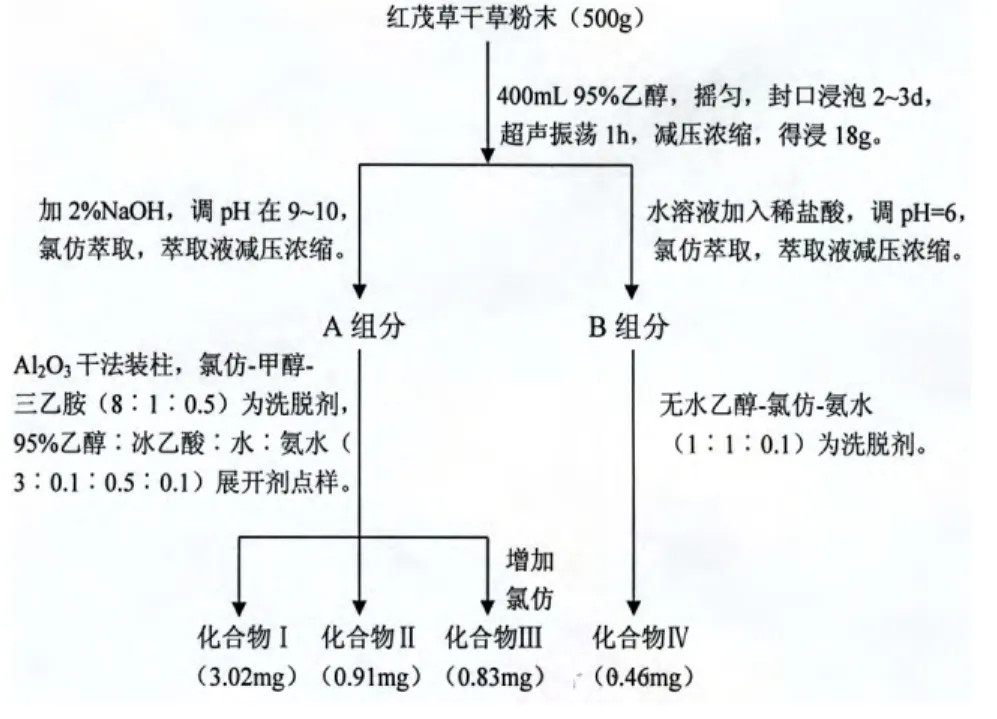
图1 红茂草生物碱分离路线
2 结果与分析
化合物Ⅰ:无色柱状结晶,mp:170~185℃;ESI-MS:m/z342[M+H]+;[ɑ]+195.4°(MeOH);UV(MeOH)304,267,220nm,IR(KBr)3689,3558,3467,3150,2926,2910,2840,1765,1384cm-1;1H-NMR(400 MHz,CDCl3) δ:8.90(1H,s),6.82(1H,d,J=8.0 Hz),6.79(1H,d,J=8.0 Hz),6.67(1H,s),3.91(3H,s),3.88(3H,s),3.67(3H,s),3.11(1H,dd,J=16.4,3.6 Hz),3.00(2H,s),2.82(1H,s),2.67(1H,dd,J=16.4,3.6 Hz),2.52(3H,s),2.49(3H,s),2.43(2H,s);13C-NMR(100 MHz,CDCl3) δ:151.2,149.4,143.9,142.0,141.7,129.9,129.2,125.8,120.1,118.9,111.0,110.8,62.8,62.0,55.8,55.4,52.7,43.9,35.9,29.3.以上数据与文献报道一致,[4-5]经鉴定该化合物为异紫堇碱(C20H23NO4)。
化合物Ⅱ:白色针状结晶,mp:135~148℃;ESI-MS:m/z370[M+H]+;[ɑ]+216°(EtOH);UV(MeOH)282,205nm;IR(KBr)3481,3413,2494,1777,1763,1696,1637,1440,1227,854cm-1;1H-NMR(400 MHz,CDCl3) δ:6.98(1H,d,J=8.0 Hz),6.95(1H,s),6.91(1H,d,J=8.2Hz),6.88(1H,d,J=8.0Hz),6.69(1H,s),6.61(1H,s),4.20(1H,d),3.85(3H,s),3.79(3H,s),3.69(1H,dd,J=16.4,3.6 Hz),3.64(3H,s),3.16(1H,s),3.15(3H,s),3.11(1H,dd,J=16.4,3.6 Hz),3.00(2H,s),2.62(2H,s),0.95(3H,dd,J=6.9 Hz);13C-NMR(100 MHz,CDCl3)δ:152.4,148.7,147.8,144.0,143.7,128.5,126.9,126.2,124.7,122.9,118.9,118.8,111.6,111.4,62.0,61.6,61.2,55.9,51.2,43.4,31.7,25.5,18.4。以上数据与文献报道一致,[6-7]经鉴定该化合物为紫堇碱(C22H27NO4)。
化合物Ⅲ:白色柱状结晶,mp:207~210℃;ESI-MS:m/z354[M+H]+;[ɑ]+284.9°(MeOH),UV(MeOH):290nm;IR(KBr)2776,1667,1658,1492,1265,1047,943,717 cm-1;1H-NMR(400 MHz,CDCl3)δ:6.94(1H,s),6.93(1H,s),6.89(1H,d,J=8.4,Hz),6.77(1H,d,=8.4 Hz),6.61(1H,s),5.92(2H,s),3.83(3H,s),3.76(3H,s),3.60(2H,s),3.46~3.32(2H,m),3.45~2.78(2H,m),1.96(3H,s),1.86(3H,s);13C-NMR(100 MHz,CDCl3)δ:192.8,151.5,148.0,147.3,146.1,135.7,132.6,129.3,128.4,127.6,117.9,110.6,110.3,109.2,108.1,101.2,60.7,57.4,55.6,50.3,46.0,41.2,32.2.以上数据与文献报道一致,[8]经鉴定该化合物为原阿片碱(C20H19NO5)。
化合物Ⅳ:淡黄色粉末,mp:133~136℃;ESI-MS:m/z354[M+H]+;[ɑ]+119°(EtOH);UV(MeOH):345,310,280,272,220nm;IR(KBr)3620,2910,1625,1585,1450,1280,1105cm-1;1H-NMR(400 MHz,CDCl3)δ:6.76(1H,d,J=7.9Hz),6.73(1H,d,J=7.9Hz),6.66(1H,s),6.64(1H,s),5.99(1H,d,J=1.5Hz),5.95(1H,d,J=1.3Hz),5.93(1H,d,J=1.5Hz),5.92(1H,d,J=1.5Hz),4.23(1H,brs),4.08(1H,d,J=15.7Hz),3.57(1H,brs),3.43(1H,d,J=15.7Hz),3.21(1H,d,J=17.5Hz),3.08(1H,dd,J=17.5,4.3Hz),2.98(1H,t,J=2.8Hz),2.27(3H,s);13C-NMR(100 MHz,CDCl3)δ:145.6,145.3,143.2,143.1,131.4,128.9,125.8,120.4,111.9,117.1,109.6,107.4,101.4,101.1,72.4,62.9,53.9,42.4,42.1,39.7.以上数据与文献报道一致,[9]经鉴定该化合物为白屈菜碱(C20H19NO5)。
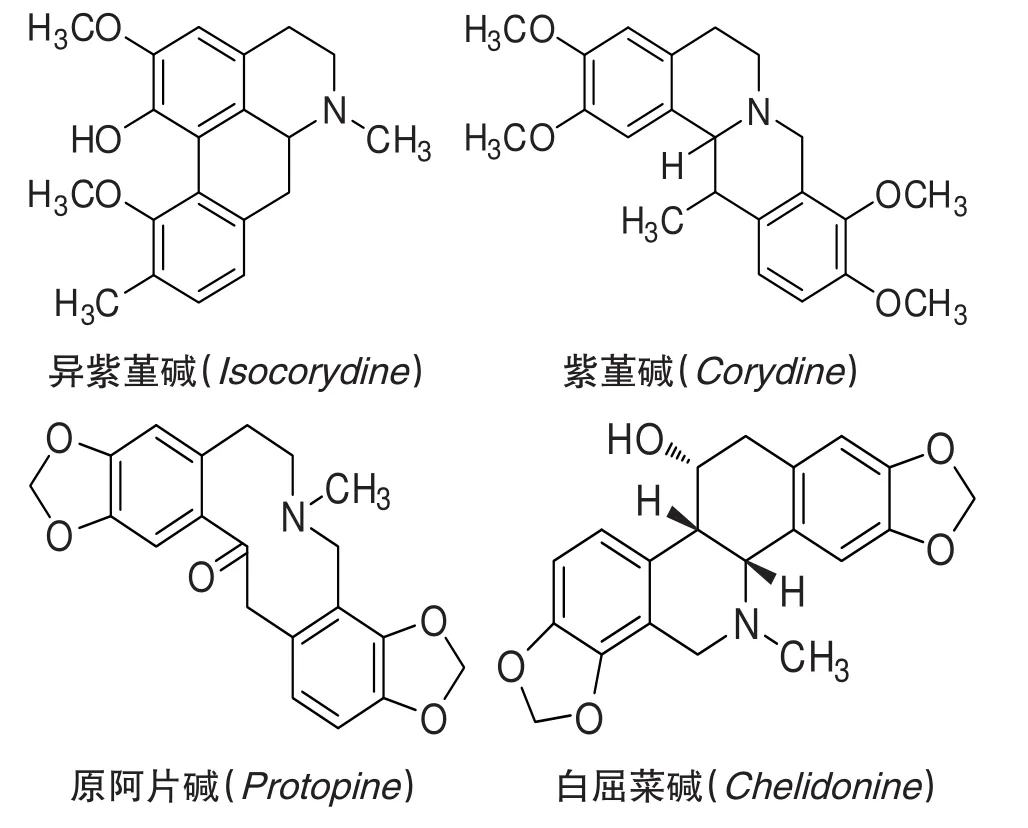
图2 化合物结构
3 结 论
我国西北地区野生药用植物红茂草化学成分研究已经开展了十多年,由于其有明显的生物活性作用,近年来又相继发现有新的药理学作用,因此对红茂草生物碱化学成分及药效物质研究又引起了新的关注。[10-14]在研究红茂草生物碱成分的过程中,采用柱色谱分离和超导核磁共振等技术,共分离鉴定得到4种主要生物碱成分,分别鉴定为异紫堇碱、紫堇碱、原阿片碱和白屈菜碱。其中异紫堇碱含量最高,白屈菜碱为首次从该属植物中分离得到。通过对野生药用植物红茂草中4种主要生物碱化学成分的研究,可以更好地开发和利用其药物资源,为其有效部位质量标准的建立和药理作用的深层次研究,奠定很好的理论基础。
[1]江苏医学院,编著.中药大辞典[Z].上海:上海人民出版社,1977:1135.
[2]赵强,王廷璞,余四九,等.红茂草生物碱正交提取工艺模式优化及清除自由基作用的研究[J].草地学报,2012,20:71-78.
[3]赵强,王廷璞,余四九,等.红茂草生物碱抑菌活性的测定[J].中国兽医科学,2008,38(10):733-736.
[4]JIANG QING-SONG,HUANG XIE-NAN,SUNAN-SHENG,et al.Relation of vasodilative action of isocorydine to cyclic nucleotides[J].Chinese Journal of Pharmacology and Toxicology,2001,15(4):251-255.
[5]YANG MING-HE,PATEL V.ASMITA,BLUNDEN GERALD,et al.Crabbine,an aporphine alkaloid from Corydalis Lutea[J].Phytochemistry,1993,33(4):943-945.
[6]LIU DA-HU,ZHANG TIAN-CAI,LIU JUN-XI,et al.Chemical constituents of alkaloids from Dicranostigma leptodum[J].Chin Tradit Herb Drugs,2011,42(8):1505.
[7]GALINIS DEBORAH L.,WIEMER DAVID F.,CazinJr.John.Cissampentin:a new bisbenzylisoquinoline alkaloid from Cissampelos fasciculate[J].Tetrahedron,1993,49(7):1337-1342.
[8]TOUSEK J,MALINAKOVA K,DOSTAL J.Theoretical and experimental NMR study of protopine hydrochloride isomers[J].Magn Reson Chem,2005,43(7):578-581.
[9]THEN M,SZENTMIHALYI K,SARKOZI A,et al.Effect of sample handling on alkaloid and mineral content of aqueous extracts of greater celandine(Chelidonium majus L.)[J].J Chromatogr A,2000,889:69-74.
[10]DANG YAN,GONG HONG-FEI,LIU JUN-XI,et al.Alkaoid from Dicranostigma leptopodum(Maxim)Fedde[J].Chinese Chemical Letters,2009,20:1218-1220.
[11]WANG FANG,LI YU-MING.New hopane triterpene from Dicranostigma leptopodum(Maxim)Fedde[J].Journal of Asian Natural Products Research,2010,12(1):94-97.
[12]赵强.甘肃省陇东南地区特色药用植物红茂草资源的研究与利用[D].甘肃农业大学,2013,(6):85-95.
[13]赵强,余四九,王廷璞,等.响应面法优化秃疮花中生物碱提取工艺及抑菌活性研究[J].草业学报,2012,21(4):206--214.
[14]王廷璞,赵强.药用植物红茂草化学成分及抗炎作用的研究进展[J].食品安全质量检测学报,2013,10(4):1323-1328.
