电解金属锰液中钠离子富集与平衡分析
2015-03-09杨远平龙小东
杨远平,龙小东
(湘西民族职业技术学院,湖南 吉首 416000)
电解金属锰液中钠离子富集与平衡分析
杨远平,龙小东
(湘西民族职业技术学院,湖南 吉首416000)
摘要:分析了在电解金属锰浸出液的MnSO4-(NH4)2SO4-H2O三元体系中,钠离子的循环富集与平衡。通过分析可知,钠离子富集到一定程度后,溶液中钠离子含量便不再增加,达到平衡状态。溶液中钠离子的最终含量与每次加入的量和渣中带走的百分比有关,最终平衡时钠离子含量为第1次合格液中的残留量除以渣中带走的百分比,结果可作为分析电解生产过程中出现黑槽、硫酸铵结晶沉积等现象的原因参考。
关键词:电解金属锰液;钠离子;循环富集;平衡
我国电解金属锰(以下简称为:电解锰)产能占世界90%以上,国内关于电解锰的研究很多,主要集中在锰矿石的浸出、二氧化锰矿的还原、电解液除重金属深度净化、无硒电解、锰渣及废水处理等电解锰生产的主要环节[1-8],而对于在电解生产过程中出现黑槽、硫酸铵结晶沉积、电解液在循环一定次数必须更新一部分才能继续生产等问题,研究较少。本文主要以硫化净化过程中带入的Na+为对象,分析其在电解锰浸出液即MnSO4-(NH4)2SO4-H2O体系中的循环富集与平衡,分析结果可作为电解锰生产过程中出现上述问题时的参考。
1钠离子来源及循环分析
1.1 钠离子来源
我国主要采用碳酸锰矿为原料生产电解锰,矿石中钠离子成分很少,在本文中假定矿石中钠离子含量为零。
在电解锰生产过程的浸出—净化—电解等几个主要环节中,在净化阶段需要采用硫化剂(以RS表示)除重金属,其反应方程式简化为:
MSO4+RS→RSO4+MS↓
M代表Cu、Cd、Ni、Co、Zn等重金属离子。电解锰生产中,很多厂家均采用福美钠(S.D.D)作硫化剂,则R为钠离子,硫化除重金属后,钠离子进入电解液中。
1.2 循环分析
钠离子在硫化净化阶段进入电解液后,在后续电解过程中,不参与电解反应,始终残留在电解液中,电解结束后,随电解阳极液等一同进入下次浸出。在浸出、氧化、中和除铁等过程中,钠离子不参与反应、不沉淀,因此含量不会减少,仍然残留在浸出液中。只有在压滤过程中,浸出液部分随滤渣带走,渣中的溶液同时带走部分钠离子。假定浸出液总的体积为x,渣中带走溶液的体积为y,则渣中带走的钠离子比例为y/x,压滤后溶液中残留钠离子的比例为(x-y)/x,残留在溶液中的钠离子进入下个循环。
2钠离子循环富集与平衡分析
2.1 以湘西某公司生产为例
2.1.1工艺过程和生产参数
湘西某公司的电解锰生产工艺见图1。
参照生产实际及有关文献计算,可知生产1 t电解锰需要合格的电解液体积约为47.63 m3[1],渣中带走电解液约为2.5 m3。为计算简化,假定压滤前合格液体积为50 m3,渣中带走2.5 m3,则压滤后合格液的体积为47.5 m3。硫化时加入钠离子量为akg,则渣中带走的比率为5%,合格液中留量为95%,即0.95akg。合格液在电解过程中,钠离子不参与反应,所以含量不会减少,残留在阳极液中进入下个生产循环。在下个循环中,生产1 t电解锰,压滤前合格液的体积仍为50 m3,硫化时加入钠离子量为akg。
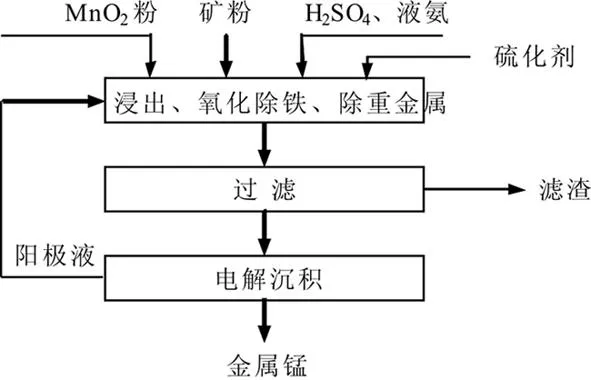
图1 湘西某公司的电解锰生产工艺
2.1.2钠离子含量计算
第1次循环,硫化时加入钠离子量为akg,合格液中留量为0.95akg。
第2次循环,硫化时加入钠离子量为akg,则压滤前电解液中钠离子含量为(0.95a+a=1.95a)kg,渣中带走5%,合格液中留量为:
(0.95a+a)×95%=0.95a+0.95×0.95a=
0.95a+0.952a
第3次循环,硫化时加入钠离子量为akg,则压滤前电解液中钠离子含量为[(0.95a+0.952a)+a]kg,合格液中残留钠离子量为:
[(0.95a+0.952a)+a]×0.95=
0.95a+0.952a+0.953a
第n次循环后,经推算可知合格钠离子含量为:
0.95a+0.952a+0.953a+…0.95na=

上式是一个等比数列,比例因子x=0.95,因为x=0.95<1,所以上式有极限,对其求极限可得:
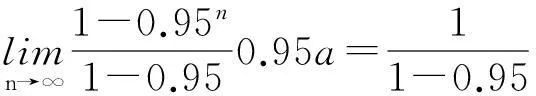
从上述分析可知,合格液中钠离子富集到一定量后便不再增加,即达到平衡状态,平衡状态钠离子含量与每次循环过程中硫化出重金属量成正比,富集程度与渣中带走的含量有关,平衡时钠离子的含量等于第1次循环时合格液中的残留量除以渣中带走的百分比。
湘西地区的电解锰生产中,除重金属硫化剂的用量大致为每生产1 t电解锰消耗1 kg福美钠,1 kg福美钠中钠离子含量为23/143=0.16 kg,生产1 t锰电解液溶液的量为47.5 m3,经多次循环到达平衡时,溶液中钠离子含量为19×0.16=3.04 kg,换算后可得每立方溶液中钠离子量为0.064 kg,即0.064 g/L,如将钠离子量换算成硫酸钠含量则为:0.064×142/46=0.2 g/L。
2.2 以广西某公司生产为例
2.2.1工艺过程及生产参数
广西某公司电解锰的生产工见图2。

图2 广西某公司电解锰的生产工艺
广西某公司电解锰的生产过程中第1次压滤渣5~6 t[9],渣中带走电解液约为1.5 m3。硫化渣量较少,硫化渣带走电解液也很少,为计算简化,假定压滤前合格液体积为49 m3,渣中带走1.5 m3,硫化渣中不带液,压滤后合格液的体积为47.5 m3。硫化加入钠离子量为bkg,则渣中带走的比率为3%,合格液中留量为97%,即0.97bkg。合格液在电解过程中,钠离子不参与反应,所以含量不会减少,残留在阳极液中进入下个生产循环。在下个循环中,生产1 t电解锰,压滤前合格液的体积仍为49 m3,硫化加入钠离子量为bkg。
2.2.2钠离子含量计算
第1次循环时,合格液中残留钠离子量为bkg。
第2次循环时,前次合格液中残留钠离子量为bkg,全部进入压滤前的49 m3液中,压滤后,滤液中残留量为0.97bkg,滤液硫化,再次加入bkg的钠离子,此时,经硫化后的合格液中残留钠离子量为:
(0.97b+b)kg
第3次循环时,前次合格液中残留钠离子量为(0.97b+b)kg,全部进入压滤前的49 m3液中,压滤后,滤液中残留量为0.97(0.97b+b)kg,滤液经硫化,再次加入bkg的钠离子,此时,经硫化后的合格液中残留钠离子量为:
0.97(0.97b+b)+b=(0.972+0.97+1)b
第n次循环时,经推导可得,硫化后的合格液中残留钠离子量为:
(0.97n-1+…+0.973+0.972+0.97+1)b=

对上式求极限得:

从上述分析可知,合格液中钠离子富集到一定量后便不再增加,即达到平衡状态,平衡状态钠离子含量的计算结论和前例一致。
广西某公司除重金属硫化剂的用量大致为每吨电解锰消耗约3 kg福美钠[9],其中钠离子含量为3×23/143=0.48 kg,那么平衡时,溶液中钠离子含量为100×0.48/3=16 kg。溶液的量为47.5 m3,换算后可得每立方溶液中钠离子量为0.34 kg,即钠离子浓度为0.34 g/L,如将钠离子量换算成硫酸钠含量则为:0.34×142/46=1.04 g/L。
3结论
1) 通过分析可知,不同公司之间,电解锰的生产工艺虽有差异,但是钠离子富集到一定程度后,溶液中钠离子含量便不再增加,达到平衡状态。
2) 溶液中钠离子的最终含量与每次加入的量和渣中带走的百分比有关,最终平衡时钠离子含量为第1次合格液中的残留量除以渣中带走的百分比。
3) 在电解锰生产过程中,经多次循环达到平衡,钠离子循环富集与平衡可作为分析电解锰生产过程中出现黑槽、硫酸铵结晶沉积的原因参考。
参考文献:
[1]谭柱中, 梅光贵, 李维健, 等. 锰冶金学[M]. 长沙: 中南大学出版社, 2004: 818.
[2]甘昌远. 电解金属锰制液Mn2+、Fe浸出行为的实验研究[J]. 中国锰业, 2012, 30(3): 21-26.
[3]蔡大为. 我国电解金属锰技术研究现状及其研究方向[J]. 中国锰业, 2009, 27(3): 12-16.
[4]杜军, 刘晓波, 刘作华, 等. 菱锰矿浸取及除杂工艺的研究进展[J]. 中国锰业, 2008, 26(2): 15-19.
[5]张文山, 石朝军. 电解金属锰有关杂质的影响及其去除方法[J]. 吉首大学学报, 2009(4): 10-13.
[6]张文山, 梅光贵, 周元敏, 等. 电解金属锰硫化除重金属的理论分析与生产实践[J]. 中国锰业, 2004,22(3): 8-10.
[7]陈南雄, 廖赞伟. 电解液成分对电解金属锰生产过程的影响[J]. 中国锰业, 2008, 26(4): 5-8.
[8]韦婷婷, 陈发明, 何朔结, 等. 电解金属锰生产中化合除杂工艺改进的研究[J]. 中国锰业, 2012, 30(3): 8-10.
[9]谢放尖, 黄丙龙, 吴长年, 等. 电解金属锰工艺清洁生产初探[J]. 四川环境, 2008, 27(3): 55-59.
A Balance Analysis of Sodium Ions Enrichment in EMM Solution
YANG Yuanping,LONG Xiaodong
(XiangxiVocationalandTechnicalCollegeforNationalities,Jishou,Hunan416000,China)
Abstract:This paper analyzed EMM MnSO4-(NH4)2SO4-H2O ternary system, including circulation and balance sodium ion concentration. In analysis, we know that when sodium ion concentration come to a certain extent , the solution does not increase the sodium ion content with an equilibrium state. Final content of sodium ions in solution with the percentage of the amount of each addition and slag away will be related to the final balance of the sodium ion content of the first qualified liquid residues divided by the percentage of each residue away, The results can be black tank, ammonium sulfate crystal deposition and other reasons as analytical reference electrolytic production process occurs.
Key words:EMM Solution; Sodium ions; Enrichment; Balance
中图分类号:TF111.3
文献标识码:A
doi:10.14101/j.cnki.issn.1002-4336.2015.04.010
作者简介:杨远平(1967-),男,湖南龙山人,副教授,研究方向:模具设计与制造教学、冶金机械与冶金工艺的教学与研究,手机:13037405963,E-mail:yang405963@sina.com.
基金项目:湖南省教育厅高校科研项目(14c1118)
收稿日期:2015-04-14
