UPLC-MS法测定大鼠血浆中荭草花的3个指标成分及其药动学研究
2015-02-26兰燕宇李勇军
黄 勇,胡 杰,陆 苑,郑 林,兰燕宇,李勇军
(贵阳医学院1.贵州省药物制剂重点实验室,2.民族药与中药开发应用教育部工程研究中心,3.药学院,贵州贵阳 550004)
UPLC-MS法测定大鼠血浆中荭草花的3个指标成分及其药动学研究
黄 勇1,3,胡 杰1,陆 苑1,3,郑 林1,3,兰燕宇2,3,李勇军2,3
(贵阳医学院1.贵州省药物制剂重点实验室,2.民族药与中药开发应用教育部工程研究中心,3.药学院,贵州贵阳 550004)
中国图书分类号:R-332;R282.71;R284.1;R969.1
摘要:目的 建立UPLC-MS法测定大鼠口服荭草花提取物后血浆中原儿茶酸、山柰素-葡萄糖、槲皮苷的分析方法,并用该方法研究原儿茶酸等3个指标成分的药物代谢动力学。方法 血浆样品选择酸化后甲醇沉淀蛋白,Waters BEH C18(2.1 mm×100 mm,1.7 μm)柱,流速:0.30 mL·min-1,流动相:0.1%甲酸乙腈-0.1%甲酸水梯度洗脱,采用电喷雾电离源(ESI),扫描方式为多反应离子监测(SIR)。结果 3种成分分别在2.74~677、0.69~186、0.82~200 μg·L-1呈良好线性关系。提取回收率、精密度、准确度和稳定性均良好达到测定要求。原儿茶酸、山柰素-葡萄糖和槲皮苷3个指标成分的Tmax(h)分别为0.46±0.1、0.79±0.33和2.63± 4.6,Cmax(μg·L-1)分别为463.8±207.81、18.53±7.82和137.38±71.09。结论 建立的UPLC-MS检测方法具有特异、快速、准确和灵敏的特点,能够同时测定生物样品中原儿茶酸等3种成分的血药浓度,并成功应用于荭草花在正常大鼠体内这3个指标成分的药动学研究。
关键词:荭草花;大鼠;UPLC-MS;原儿茶酸;山柰素-葡萄糖;槲皮苷;药代动力学
网络出版时间:2015-8-10 14:37 网络出版地址:http://www.cnki.net/kcms/detail/34.1086.R.20150810.1437.026.html
荭草花为蓼科植物荭蓼(Polygonum orientale L.)的花序,又名水荭花;荭草花具有行气活血,消积,止痛的功效,用于治疗头痛、心胃气痛、腹中痞积等。课题组在对荭草各部位药理筛选实验中发现,荭草花水煮醇沉后的正丁醇萃取部位有较强的抗心肌缺血,减少心肌梗死面积作用。化学成分研究表明,主要含有酚酸类的原儿茶酸及黄酮类的山柰素
-葡萄糖苷、槲皮苷等成分,文献报道该类化合物为主要活性成分[1]。
为此,课题组以原儿茶酸、山柰素-葡萄糖苷和槲皮苷为指标性成分,研究大鼠灌胃荭草提取物后体内的药代动力学特征,考察3个指标成份在大鼠体内的经时过程,获得其动力学参数,为进一步研究开发荭草及其制剂奠定基础[2-3]。
1 材料与方法
1.1药品与试剂 原儿茶酸对照品(批号809-200102,纯度≥0.98,中国药品生物制品鉴定所);葛根素(批号0752-9605,纯度≥0.98,中国药品生物制品鉴定所);槲皮苷对照品、山柰素-葡萄糖对照品对照品(均自制,纯度≥0.98);甲醇、乙腈和甲酸等试剂均为色谱纯。
1.2仪器 WATERS ACQUITY UPLC超高压液相三重四级杆质谱联用仪(二元梯度泵,真空脱气机,柱温箱,Masslynx 4.1质谱工作站,自动进样器);Al-legra 64R低温高速离心机(美国Beckman Coulter公司);AE240十万分之一电子天平(梅特勒-托利多仪器上海有限公司);MTN-2800D氮吹浓缩装置(天津奥特塞恩斯仪器有限公司);CQ 250A-TS超声波清洗机(上海跃进医用光学器械厂);ZH-2涡旋混合器(天津药典标准仪器厂)。
1.3实验动物 健康Wistar大鼠♀♂兼用,体质量为(230±20)g,由贵阳医学院动物中心提供[批号SCXK(黔)2002-0001]。
1.4药代动力学数据处理 采用DAS2.0数据处理软件进行药代动力学参数计算和数据拟合,选取最小AIC值拟合房室模型,AUC0-t,MRT等参数选用统计矩方法计算。并对AUC0-t,MRT进行方差分析确定其动力学模型。
1.5标准溶液的配制
1.5.1原儿茶酸等3种物质系列标准溶液的配制
精密称取原儿茶酸、槲皮苷和山柰素-葡萄糖适量,用甲醇定容至10 mL。获得原儿茶酸(1.202 g ·L-1)、槲皮苷(1.200 g·L-1)和山柰素-葡萄糖(1.216 g·L-1)的储备液。分别精密量取原儿茶酸等3种对照品储备液适量,用甲醇按梯度稀释成所需浓度,得混合系列标准溶液。置冰箱(-20℃)保存,备用。
1.5.2内标溶液的配制 精密称取葛根素(10.33 mg),用甲醇定容至25 mL。获得葛根素(0.4 132 g ·L-1)的储备液。取内标储备液适量至10 mL容量瓶中,用甲醇定容至刻度,配制成2 mg·L-1的内标溶液,置冰箱(-20℃)保存,备用。
1.6色谱条件 色谱柱Waters BEH C18(2.1 mm× 50 mm,1.7 μm)柱,保护柱:Waters Van Guard BEH C18(2.1 mm×5 mm,1.7 μm),柱温:45℃,流动相:0.1%甲酸乙腈-0.1%甲酸水梯度洗脱。进样体积为1 μL。液相梯度见Tab 1。
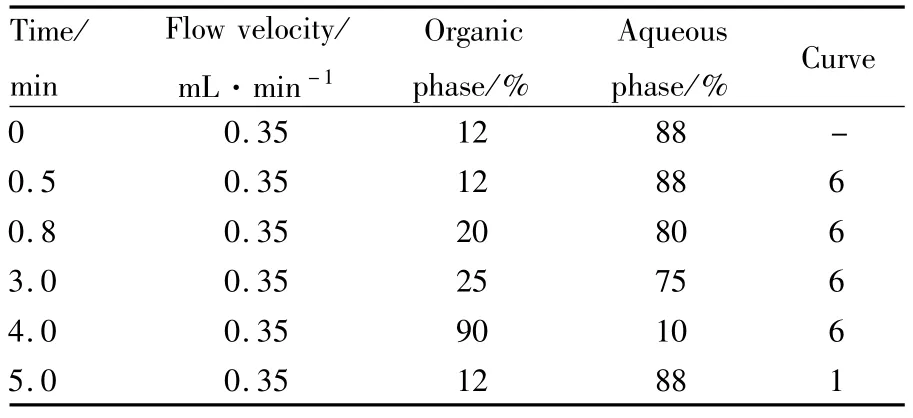
Tab 1 Four components chromatographic conditions
1.7质谱条件 采用电喷雾电离源(ESI),毛细管电离电压:3 kV,离子源温度:120℃;喷雾气与反吹气:氮气,去溶剂气流速:650 L·h-1,扫描方式为选择性离子监测(SIR),原儿茶酸等3种成分及内标用于定量分析的监测离子,见Tab 2。

Tab 2 Three components mass spectrometric conditions
1.8血浆样品处理方法 取大鼠血浆100 μL,置1.5 mL塑料离心管中,补加50 μL甲醇,依次加入2 mg·L-1内标溶液20 μL,50 μL 1%甲酸,400 μL甲醇,涡混1 min,超声5 min,离心10 min(4℃、15 000r·min-1),取上清液置离心管中,48℃下氮气吹干,残留物加500 μL甲醇复溶,超声10 min,涡混1 min,离心10 min(4℃、15 000 r·min-1),取上清液48℃下氮气吹干,残留物200 μL初始流动相溶解,取上清液进样UPLC-MS分析。
1.9实验方案与样品检测 健康Wistar大鼠6只,♀♂兼用,体质量为(230±20)g,给药剂量分别为2.5 g·kg-1,给药前12 h禁食,自由饮水。口服灌胃荭草花提取物溶液。于给药后5、10、15、30、60 min,2 h、3 h、5 h、7 h、9 h、12 h、24 h、36 h经尾静脉取血约0.4 mL置涂有肝素的塑料离心管中,4 500 r ·min-1离心8 min,分离血浆于-20℃冰箱中保存,直至分析。
2 结果
2.1UPLC-MS分析方法的确证
2.1.1专属性 在其选定的色谱条件和质谱条件下原儿茶酸、山柰素-葡萄糖苷、槲皮苷3种物质及内标葛根素监测离子反应分别为m/z 153.0、m/z 449.3、m/z 449.2、m/z 417.2。空白血浆、空白血浆外加原儿茶酸等3种物质和内标以及大鼠给药后血浆样品色谱图,原儿茶酸等3种物质及内标的保留时间分别为(1.25、2.70、2.78和1.73 min),各成分间分离良好,未见血浆中杂质干扰。
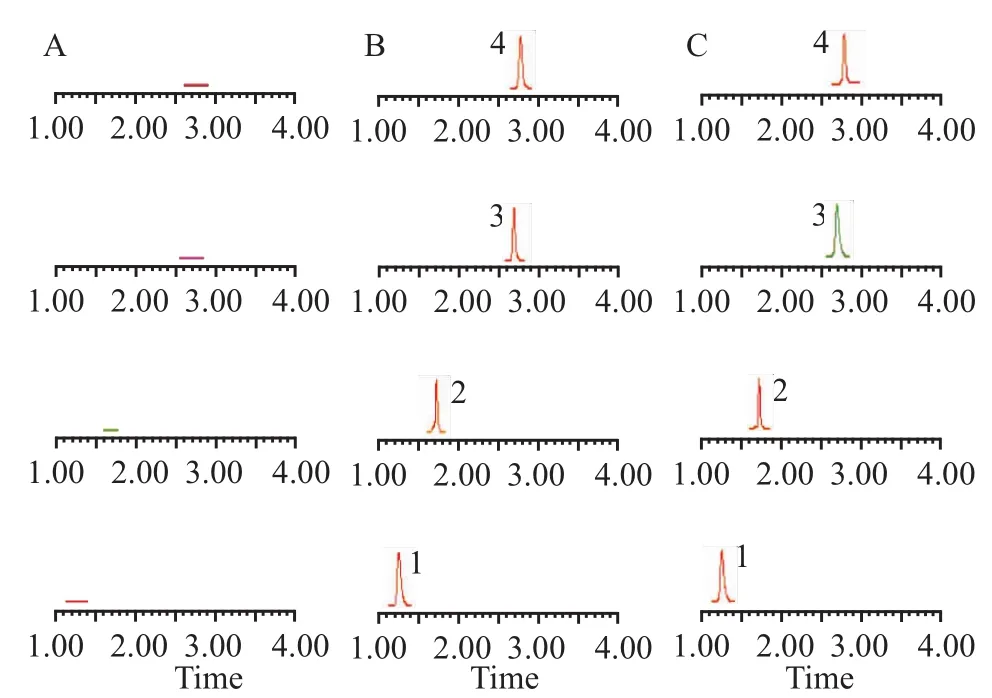
Fig 1 Typical UPLC-MS chromatograms of rat blank plasma(A);blank plasma spiked with three components and IS(B);the rat plasma sample collected at 30 min after i.g of 2.5 g·kg-1of the flower of Poly-gonumorientale L.extract to rat(C);1.protocatechuie acid;2.puerarin (IS);3.kaempferol-3-O-β-D-glucoside;4.quercitrin
2.1.2线性范围和灵敏度 取大鼠空白血浆100 μL,依次加入混合标准溶液50 μL,配制成相当于大鼠血浆药物浓度为见Tab 3,按“1.8血浆样品处理方法”项下操作,建立标准曲线。以待测物的峰面积与内标峰面积之比(A/Ai)为纵坐标Y,各物质浓度(C)为横坐标X进行直线回归,权重系数为1/X,求的直线方程,即为标准曲线。大鼠血浆中原儿茶酸等3种成分在其线性范围内线性关系良好,各成分标准曲线相关系数(r)均大于0.99。典型大鼠标准曲线和线性范围见Tab 4。
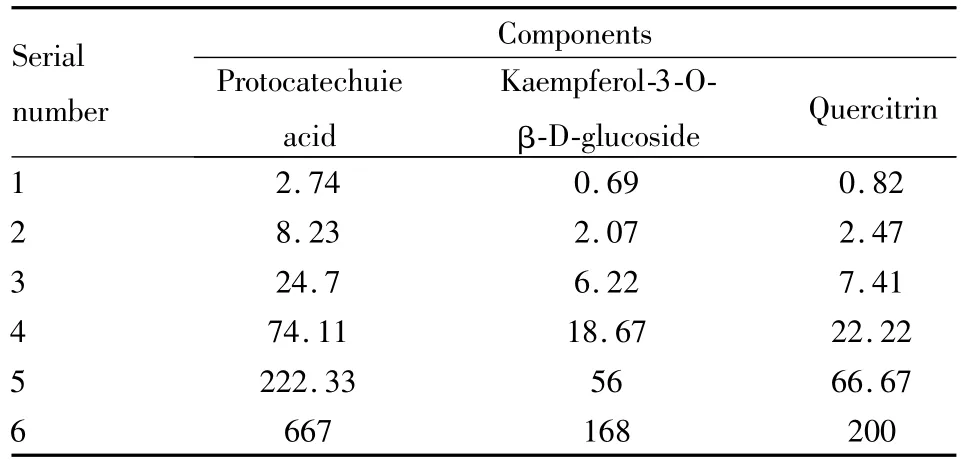
Tab 3 Concentrations of the four standard calibration samples(μg·L-1)

Tab 4 Mean values of regression equation of the analytes in rat plasma
2.1.3准确度和精密度按 “2.1.2标准曲线”项下分别配制3种成分大鼠血浆高、中、低3个浓度的质量控制样品(QC),按“1.8血浆样品处理方法”项下平行操作,每个浓度进行6样本分析,日内连续进样,并与标准曲线同时进行。每个系列浓度做6份,计算日内精密度;3种浓度连续测定5 d,计算日间精密度。结果表明原儿茶酸等3种成分日内和日间精密度RSD(%)均小于20%,准确度范围为88.28%~109.51%,提示该方法准确、可靠、重现性好。
2.1.4提取回收率 取大鼠空白血浆100 μL,按“2.1.2标准曲线”项下分别配制3种成分的大鼠血浆低、中、高3个浓度的质量控制样品(QC),每个浓度进行6样本分析,以200 μL初始流动相溶解,记录其峰面积。另取空白血浆,按“1.8血浆样品处理方法”项下操作。离心后获得上清液,加入与上述相应浓度的标准溶液(每个浓度进行6样本分析),于48℃氮气吹干,以200 μL初始流动相溶解,获得相应峰面积值。以每一浓度的两种处理方法的峰面积比值计算提取回收率,对原儿茶酸等3种成分线性范围内高、中、低3个浓度的血浆样品提取回收率进行了考察。结果表明原儿茶酸等3种成分的回收率分别为:104.55%~107.45%、92.45%~100.82%、93.36%~97.39%,提示该方法可行。
2.1.5稳定性考察 按“2.1.2标准曲线”项下分别配制原儿茶酸等3种成分的大鼠血浆低、中、高3个浓度的质量控制样品(QC),样品处理后至自动进样器中,在6 h分别进样,以每一浓度3样本分析。结果表明原儿茶酸等3种成分的处理后血浆样品在自动进样器中6 h均稳定。同法配制低、中、高3个浓度血浆样品(QC),分别在室温(约20℃)下放置6 h,4℃下冷藏8 h,冻融3次,经处理后进样测定浓度,以每一浓度3样本分析。结果表明,3种成分血浆样品在室温下放置6 h,4℃下冷藏8 h和经3次冻融循环均很稳定。
2.2大鼠给药后血浆浓度及药物动力学参数 大鼠口服荭草花提取物后,原儿茶酸等3种物质的浓度测定结果见Tab 5,平均血药浓度-时间曲线(Fig 2)。采用DAS2.0软件计算药动学参数并对药物在大鼠体内的动力学过程进行房室模型拟合并计算其相关药动学参数见Tab 6。
Tab 5 Mean plasma concentrations(μg·L-1)of three components after i.g of 2.5 g·kg-1of the flower of Polygonumorientale L.extract to rat(±s,n=6)
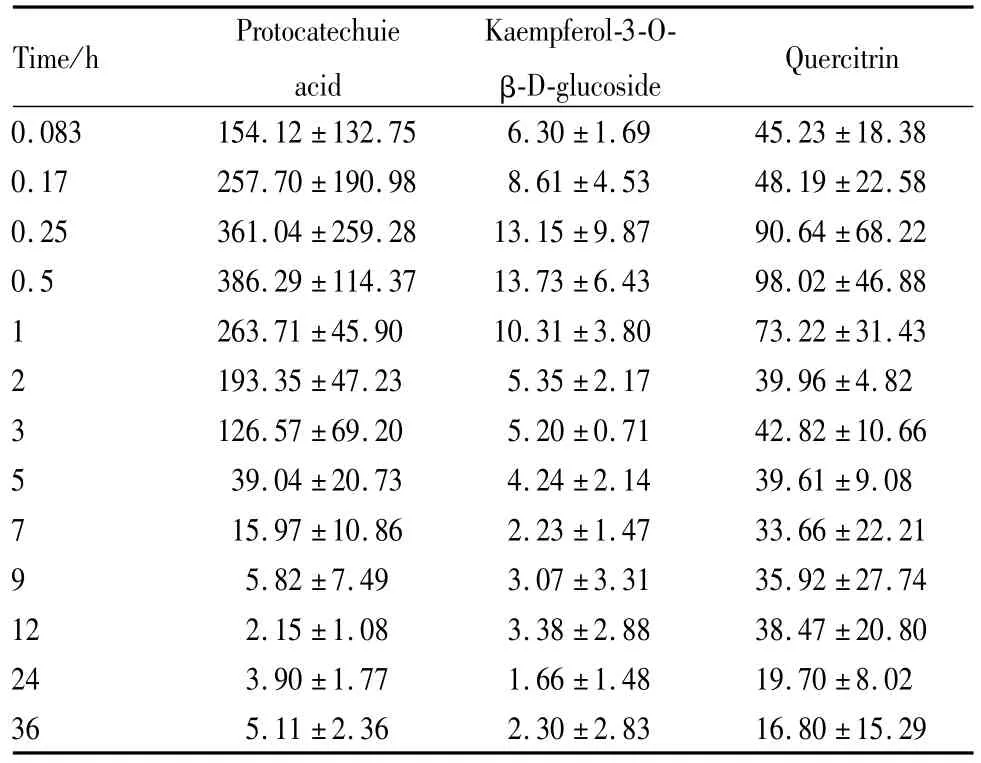
Tab 5 Mean plasma concentrations(μg·L-1)of three components after i.g of 2.5 g·kg-1of the flower of Polygonumorientale L.extract to rat(±s,n=6)
Time/h Protocatechuie acid Kaempferol-3-O-β-D-glucoside Quercitrin 0.083 154.12±132.75 6.30±1.69 45.23±18.38 0.17 257.70±190.98 8.61±4.53 48.19±22.58 0.25 361.04±259.28 13.15±9.87 90.64±68.22 0.5 386.29±114.37 13.73±6.43 98.02±46.88 1 263.71±45.90 10.31±3.80 73.22±31.43 2 193.35±47.23 5.35±2.17 39.96±4.82 3 126.57±69.20 5.20±0.71 42.82±10.66 5 39.04±20.73 4.24±2.14 39.61±9.08 7 15.97±10.86 2.23±1.47 33.66±22.21 9 5.82±7.49 3.07±3.31 35.92±27.74 12 2.15±1.08 3.38±2.88 38.47±20.80 24 3.90±1.77 1.66±1.48 19.70±8.02 36 5.11±2.36 2.30±2.83 16.80±15.29
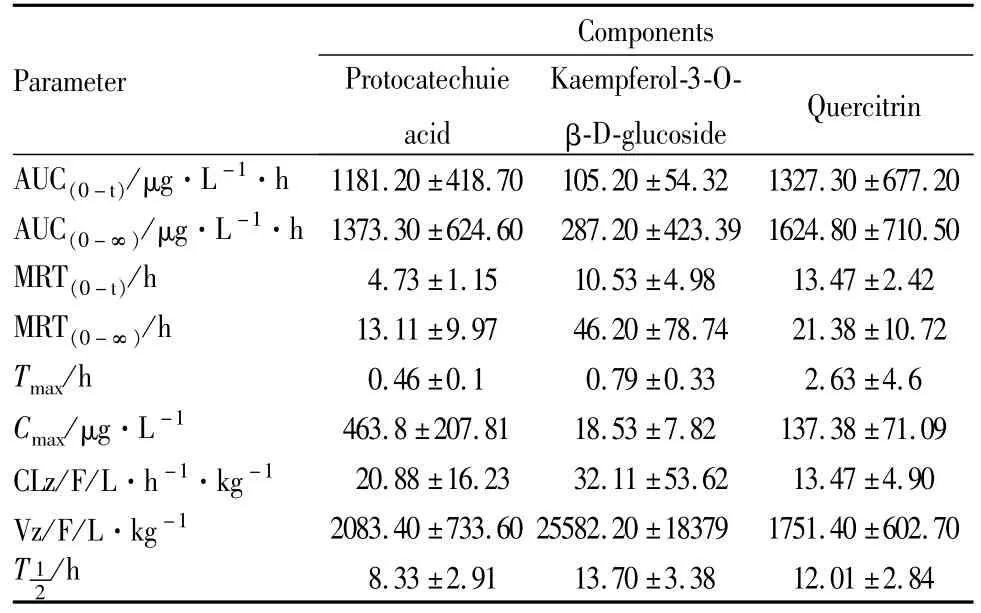
Tab 6 Pharmacokinetic parameters of three components afteri.g of 2.5 g·kg-1of the flower of Polygonumorientale L.extract to rat(n=6)
3 讨论
生物样品检测方法的建立和验证是整个药代动力学研究的基础,由于进行药代动力学研究的生物样品存在浓度较低,基质环境复杂等难题,因此,如何建立快速有效、灵敏可靠的生物样品分析方法将是本课题拟解决的关键问题之一,以实现高通量生物样品分析过程,满足药代动力学研究大样本量的要求[4]。
实验中对流动相进行了考察,发现使用乙腈比甲醇各物质的峰形较好。待测成分基本大多是黄酮类的成分,在实验中有机相和水相均加入了0.1%的甲酸,甲酸的加入可以有利于它们以游离状态存在。同时实验最开始用的是Waters C18(2.1 mm× 50 mm)的色谱柱,分离效果不理想,山奈素-葡萄糖苷与槲皮苷的分离难度较大,后用2.1 mm×100 mm的色谱柱进行替换,两者能得到较好的分离。实验中发现采用负离子检测模式线性不理想,可能是管道中存留的磷酸的影响,最后3种黄酮类成分选择正离子检测模式,酚酸类的原儿茶酸选择负离子检测模式,结果良好。
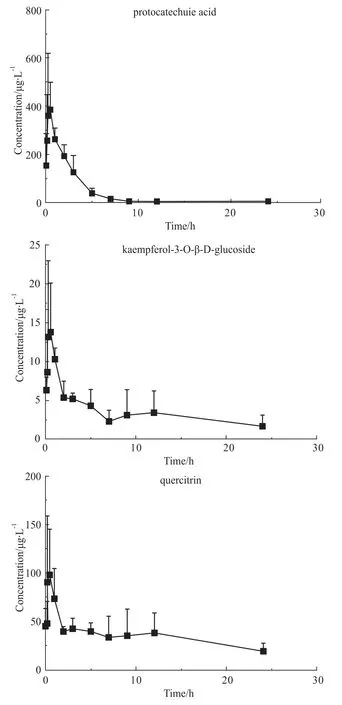
Fig 2 Concentration-time profiles of three components after i.g of 2.5 g·kg-1of the flower of Polygonumorientale L.extract to rat(n =6)
被测成分原儿茶酸、山奈素-葡萄糖苷和槲皮苷均为极性较大的弱酸性化合物,在酸性条件下处于非解离状态,有利于被测成分的提取。因此我们对在血浆样品处理中是否加酸及加酸的种类进行了考察,实验结果表明,加酸后明显有利于被测成分的提取;同时不同的酸(甲酸、盐酸、磷酸)对其提取效
率也不同,其中甲酸的效果最好,因此我们在样品处理时加入了50 μL 1%甲酸[5-7]。
(致谢:本实验在贵州省药物制剂重点实验室和民族药与中药开发应用教育部工程研究中心联合完成。真诚感谢贵州省药物制剂重点实验室和民族药与中药开发应用教育部工程研究中心为本实验开展提供相关实验耗材与仪器设备。真诚感谢实验室各位同事、老师在实验中给予我的指导与帮助。)
参考文献:
[1] 陈秀杰,刘 磊,朱文良,等.木犀草素在大鼠体内的药动学研究[J].药物分析杂志,2009,9:1462-5.
[1] Chen X J,Liu L,Zhu W L,et al.Study on pharmacokinetics of luteolin in rats[J].J Pharm Anal,2009,9:1462-5.
[2] 刘 跃,黄 勇,董永喜,等.野黄芩素及其葡萄糖醛酸结合物在大鼠体内的药动学研究[J].中国药理学通报,2014,30 (5):711-5.
[2] Liu Y,Huang Y,Dong Y X,et al.Pharmacokinetic studies of scutellarein and glucuronidescutellarin in rats[J].Chin Pharma-col Bull,2014,30(5):711-5.
[3] 曾 苏.药物代谢学[M].杭州:浙江大学出版社,2008: 234.
[3] Zeng S.Drug metabolism[M].Hangzhou:Zhejiang University Press,2008:234.
[4] 甘 萍,霍仕霞,白 鹏,等.类叶升麻苷在大鼠体内的药代动力学及组织分布研究[J].中国药理学通报,2014,30(3):417-20.
[4] Gan P,Huo R X,Bai P,et al.Pharmacokinetics and tissue dis-tribution study on acetoside in rats[J].Chin Pharmacol Bull,2014,30(3):417-20.
[5] 张宇瑶,佟苗苗,初正云,等.荭草花HPLC特征指纹图谱研究[J].中药材,2013,12:1937-9.
[5] Zhang Y Y,Tong M M,Chu Z Y,et al.Study on characteristic HPLC fingerprint of polygonumorientaleinflorescence[J].Chin Med Mat,2013,12:1937-9.
[6] Qiu F,Zhao X P,Lu X,et al.HPLC-ESI-MS/MS validation and pharmacokinetics of kalopanaxsaponin A in rats[J].RSC Ad-vances,2015,10:7260-6.
[7] 童成亮,刘晓东.HPLC法测定犬血浆中牡荆素及药代动力学研究[J].中国药理学通报,2006,22(9):1149-50.
◇复方药物药理学◇
[7] Tong C L,Liu X D.Determination of Vitexin in dog plasma by HPLC and study of its pharmacokinetics[J].Chin Pharmacol Bull,2006,22(9):1149-50.
Pharmacokinetics of three index components in flower of Polygonumorientale L.in rat plasma by UPLC-MS
HUANG Yong1,3,HU Jie1,LU Yuan1,3,ZHENG Lin1,3,LAN Yan-yu2,3,LI Yong-jun2,3
(1.Guizhou Provincial Key Laboratory of Pharmaceutics,School of Pharmacy,Guiyang Medical University,Guiyang 550004,China;2.Engineering Research Center for the Development and Application of Ethnic Medicine and TCM(Ministry of Education),Guiyang Medical University,Guiyang 550004,Guizhou,China;3.School of Pharmacy,
Guiyang Medical University,Guiyang 550004,China)
Abstract:Aims To establish a UPLC-MS method for quantifying protocatechuie acid,kaempferol-3-O-β-D-glucoside and quercitrin and to investigate the pharma-cokinetics of three indix components in flower of Poly-gonumorientale L.in rat plasma.Methods The anal-ysis was achieved by BEH C18column(2.1 mm×100 mm,1.7 μm)with a mobile phase composed of 0.1% formic acid using step gradient elution.A TQD tandem mass spectrometry equipped with electrospray ionization source was used as detector and operated by selected ion recording(SIR)mode.Results In the selected linear range,calibration curves of the three markers components showed good linearity.Extraction recovery rate,precision,accuracy and stability reached the de-termination request.The parameters of Tmax(h)in three index components were 0.46±0.1,0.79±0.33 and 2.63±4.6,respectively;Cmax(μg·L-1)in three index components were 463.8±207.81,18.53±7.82 and 137.38±71.09,respectively.Conclusion The fully validated UPLC-MS method has been successfully applied to the pharmacokinetic study of the three index components in flower of Polygonumorientale L.in rat plasma.
Key words:flower of Polygonumorientale L.;rat;UP-LC-MS;protocatechuie acid;kaempferol-3-O-β-D-glu-coside;quercitrin;pharmacokinetics
作者简介:黄 勇(1976-),男,教授,研究方向:中药活性成分及新药开发,Tel:0851-6908899,E-mail:hujie51619@sina.cn;李勇军(1973-),男,教授,研究方向:中药药效物质基础及新药开发,通讯作者,Tel:0851-6908899,E-mail:759843 553@qq.com
基金项目:国家自然科学基金资助项目(No 81360664);贵州省中药现代化科技产业研究开发专项项目(黔科合重G字[2013]4001);贵州省高等学校创新能力提升计划(黔教合协同创新字[2013]04)
收稿日期:2015-04-29,修回日期:2015-06-20
文献标志码:A
文章编号:1001-1978(2015)09-1314-05
doi:10.3969/j.issn.1001-1978.2015.09.026
