球磨时间对Cu/SiO2规整结构催化剂草酸酯加氢性能与涂层黏结性影响
2015-02-03赵玉军王胜平马新宾
王 博,赵 硕,赵玉军,王胜平,马新宾
(天津大学化工学院,绿色合成与转化教育部重点实验室,天津300072)
乙二醇(EG)是一种重要的有机化工原料,广泛应用于聚酯纤维、聚酯树脂、防冻剂、润滑剂和增塑剂等领域[1]。目前,工业上合成乙二醇采用石油路线,即乙烯氧化生成环氧乙烷,再经水合反应生成乙二醇。该合成需水高、能耗大、乙二醇选择性相对较低[2-3],而且对石油资源依赖严重,因此开发替代石油路线的绿色高效的工艺路线受到广泛的关注。以煤为原料,经气化生成合成气,再通过氧化偶联反应生成草酸酯(DMO),最后进行加氢反应得到乙二醇是一条绿色高效并且原子经济性高的合成乙二醇的煤化工路线[4-5],并且符合我国的能源结构,具有良好的应用前景。
草酸酯加氢制乙二醇反应的催化剂分为均相催化剂体系[6-9]和非均相催化剂体系[10-24],由于均相催化剂体系大都为贵金属有机化合物,制备复杂、反应压力高、反应物与催化剂分离困难以及成本高昂,限制了其在工业上的应用,因此非均相催化剂的研究引起国内外学者的兴趣。尤其是铜基催化剂,由于铜对草酸酯的羰基加氢有活性,对C—C键加氢显惰性[25-27],因此其表现出良好的草酸酯加氢的反应性能。载体的酸碱性会影响产物分布,强酸性位会引起乙二醇脱水生成乙醇,强碱性位会促进Guerbet反应,使乙二醇与甲醇或乙醇发生分子间脱水,生成 1,2-丙二醇或 1,2-丁二醇[28]。前期研究发现,以弱碱性的硅溶胶为载体制备的催化剂活性组分具有较高的分散度,从而表现出较高的催化活性[29]。
相对于传统的固定床反应器,规整结构催化剂是一种新型的结构化催化反应器,具有压力降低、传热和传质速率高、比表面积大、易于放大等特点[30-33],广泛应用于汽车尾气净化、挥发性有机化合物的催化氧化、氮氧化物处理等领域[34-37]。前期研究表明,规整结构催化剂应用于草酸酯加氢体系可以有效地消除内扩散限制,并且可以提高催化剂的稳定性[17]。但是,规整结构催化剂的应用存在一个关键的难点,即提高涂层的黏结性,若涂层黏结性弱,涂层容易脱落,则催化剂活性组分发生流失,导致催化剂的活性和稳定性大大降低。添加黏结剂是提高规整结构催化剂涂层黏结性的一种有效方法[38],另外,降低球磨胶的颗粒粒度也可以获得牢固的催化剂涂层。
通过蒸氨法获得Cu/SiO2催化剂原粉,再经球磨获得球磨胶,最后涂覆到堇青石载体上获得规整结构催化剂。球磨过程是催化剂制备过程中的一个重要环节,会影响到球磨胶的颗粒粒度,进而影响涂层的黏结性及催化剂的活性。因此,本研究通过改变球磨时间获得不同粒度分布的球磨胶,再涂覆制备催化剂,对其结构性质进行表征研究,考察球磨时间对Cu/SiO2规整结构催化剂草酸酯加氢性能与涂层黏结性的影响。
1 实验部分
1.1 Cu/SiO 2催化剂原粉制备
一定量的 Cu(NO3)2·3H2O与 25%(质量分数,下同)的氨水加入到去离子水中形成铜氨溶液,搅拌10 min,室温下将一定量的硅溶胶以一定速率缓慢滴入铜氨溶液中,高速搅拌6 h,然后将水浴温度升高到80℃进行蒸氨,使Cu2+沉积到SiO2载体上,直至溶液 pH值降到7为止,过滤并水洗,之后在120℃下干燥4 h,最后置于马弗炉中升温至400℃(3℃/min)焙烧4 h,得到20%Cu上载量的催化剂原粉。
1.2 规整结构催化剂制备
将制备好的原粉溶于盛有一定量水(水粉质量比为3∶2)的球磨罐中,在球磨机上进行一定时间的球磨获得球磨胶。将堇青石(直径15 mm,长25 mm,400目,方形孔道)浸于球磨胶中,保持1 min,将堇青石从球磨胶中取出后用压缩空气将孔道中多余的球磨胶移除,之后进行干燥称量,重复以上涂覆过程,直到达到25%(涂层质量占催化剂总质量的比例)的涂覆量为止,最后置于马弗炉中升温至400℃(3℃/min)焙烧2 h得到规整结构催化剂。
1.3 催化剂表征
球磨胶的粒度分布采用激光粒度仪Mastersizer 2000进行分析。催化剂的比表面积及孔分布采用美国Micromeritics公司的 TriStar 3000型物理吸附仪进行测定,测试前样品在90℃吹扫1 h,然后在300℃预处理4 h。催化剂的大孔孔径分布采用美国Micromeritics公司的AutoPore IV 9500型压汞仪进行测定。催化剂活性组分铜的表面分散度采用美国Micromeritics公司的 AtuochemⅡ2920全自动程序升温化学吸附仪进行分析。催化剂的体相性质采用日本理学公司Rigaku C/Max-2500型X射线衍射仪进行分析,Cu-Kα特征衍射辐射,石墨单色滤光片,工作电压 40 kV,电流 200 mA,扫描范围10°~90°。催化剂涂层的形貌采用荷兰 Philips公司的XL30ESEM环境扫描电子显微镜进行分析。
1.4 活性评价
采用先权仪器设备有限公司生产的微型反应实验装置进行催化剂的评价实验,其中管式反应器长度为350 mm,内径为15 mm,热电偶分别置于催化剂床层的上中下3处,反应器压力由背压阀控制。取2块规整结构催化剂装入管式反应器中,反应前在350℃氢气氛围下还原4 h。液相反应物(质量分数为20%的DMO溶于甲醇溶液中)由高压计量泵(Lab Alliance Series II pump)注入预热器中汽化,氢气流量由高压质量流量计控制,两者混合后进入反应器反应,保持 n(氢) /n(酯)为80,压力为2.5 MPa,温度为200℃。反应后的混合气经冷凝得到液相产物,采用Agilent 6820气相色谱氢火焰检测器对其进行检测分析,毛细管色谱柱为美国惠普公司的HP-INNOWAX型(30 m×0.32 mm×0.50μm)。
2 结果与讨论
2.1 球磨胶的性质
图1为经过不同球磨时间获得的球磨胶的粒度分布,表1为不同球磨时间的球磨胶的性质。

图1 不同球磨时间的球磨胶的粒度分布Fig.1 Particle size d istribution of slurry with differen t milling time measured by LPSA
由图1可以看出,球磨胶的粒度分布比较集中,并且随着球磨时间的延长,球磨胶的粒度先显著减小,后趋于稳定。这是由于颗粒在球磨罐中与玛瑙球长时间的相互碰撞、摩擦、剪切,使得大颗粒逐渐破碎成粒度均匀分布的超细粉末,球磨时间越长,粉末的粒度越小,最后趋于平衡。由表1可以看出,球磨时间从2 h提高到24 h后,球磨胶的平均粒径从7.1μm降低到2.8μm,d90也从17.3μm下降到6.4μm。文献中报道,球磨胶的粒度通常要低于5μm,与堇青石表面的孔道尺寸相当,利于涂层在载体表面的锚定,提高涂层的黏结性[36]。因此,球磨8 h以上即可得到粒度分布理想的球磨胶。

表1 不同球磨时间的球磨胶的性质Tab le 1 Characteristics of slur ry of different milling time
由表1可以看出,随着球磨时间的延长,球磨胶的黏度逐渐升高,由 35 mPa·s增加到68 mPa·s。这是由于颗粒的粒度小,接触面积大,相互作用强,导致球磨胶的黏度增加。而适当提高球磨胶黏度可减少涂覆次数,提高涂覆效率。
由于球磨胶的粒度随着球磨时间的延长趋于稳定,在之后的催化剂研究中,选择球磨胶粒度有一定区分度的催化剂进行研究,因此选择了球磨时间分别为2、4、12和24 h的催化剂。
2.2 催化剂涂层的物化性能
表2为Cu/SiO2规整结构催化剂的物化性能,图2为催化剂的孔径分布图。

表2 不同球磨时间的Cu/SiO2规整结构催化剂的物化性能Table 2 Physicochemical properties of Cu/SiO 2 monolithic catalysts with differentmilling time
由表2可知,当球磨时间由2 h提高到12 h,催化剂的孔道结构变化不大,但是当球磨时间为24 h时,催化剂的平均孔径和孔容明显降低,说明过长时间的球磨会影响催化剂的孔道结构。
由表2还可以发现,随着球磨时间的变化,Cu/SiO2规整结构催化剂中Cu的分散度及Cu0的表面积没有明显变化,说明球磨过程并没有改变催化剂中活性组分Cu的分散度。

图2 a)N2物理吸附法和b)压汞法测得的不同球磨时间的Cu/SiO 2规整结构催化剂的孔径分布图Fig.2 Pore size distribution of Cu/SiO 2 monolithic catalysts with differen tmilling time determined by a) N2 physical adsorption and b) MIP method

图3 a)焙烧后和b)还原后的不同球磨时间的Cu/SiO 2规整结构催化剂的XRD谱图Fig.3 XRD patterns of the calcinated a)and reduced b)Cu/SiO 2 monolithic catalysts with differen tmilling time
由图2a)可知,Cu/SiO2规整结构催化剂的孔道呈双孔分布,在3 nm左右处集中分布大量的孔道,15 nm处有少量的孔道分布,但是球磨24 h的催化剂在15 nm处的峰消失,说明大孔减少。由图2b)可知,随着球磨时间的延长,催化剂中的大孔向小孔方向偏移,这是由于长时间的球磨使球磨胶的粒度更小,形成的二次孔减小。因此,球磨24 h的催化剂的大孔转变成小孔,被3 nm的峰覆盖。而其他的催化剂的大孔孔径随着球磨时间的延长向小孔方向移动的幅度比较小,并未被3 nm的峰覆盖。
2.3 催化剂的相结构和表面形貌
图3为Cu/SiO2规整结构催化剂焙烧后和还原后的XRD谱图。
图3a)中,2θ=22°处为无定形 SiO2的特征衍射峰,2θ=35.6°处为 CuO的特征衍射峰(JCPDS05-0661)。4种催化剂中 CuO的衍射峰都比较弱,说明催化剂上铜的分散度比较好,球磨时间并不影响催化剂中铜的分散,这与表2中Cu的分散度数据吻合。图3b)中,2θ=36.8°处为 Cu2O的特征衍射峰,2θ=43.5°处为 Cu0的特征衍射峰(JCPDS04-0836)。4种催化剂Cu0的衍射峰峰形相当,都比较弱,但是Cu2O的特征峰随着球磨时间的延长逐渐减弱,说明催化剂还原后既有Cu0,也有 Cu2O,并且Cu2O的分散度随着球磨时间的延长而升高。
图4为Cu/SiO2规整结构催化剂涂层的SEM图。

图4 不同球磨时间的Cu/SiO 2规整结构催化剂涂层的SEM图Fig.4 SEMimages of the layers of Cu/SiO 2 monolithic catalysts with d ifferentmilling time
由图4可以看出,焙烧后催化剂的涂层出现不同程度的龟裂。球磨2 h的催化剂涂层的龟裂现象最严重,裂痕尺寸最大,并且涂层还有一定程度的向上翘起,随着球磨时间的延长,涂层的龟裂程度有所缓解,裂痕的尺寸也越来越小。这是由于随着球磨时间的延长,球磨胶的粒度越来越小,颗粒之间的接触面积增加,相互作用增强,因此涂层的黏结性明显提高,焙烧后涂层的龟裂程度有所缓解。所以,适当延长球磨时间,获得粒度小的球磨胶进行涂覆,可以得到黏结性高的规整结构催化剂涂层。
2.4 催化剂涂层的黏结性及催化活性
图5为反应条件为 T=200℃,p=2.5 MPa,n(H2)/n(DMO) =80,LHSV=4.0 h-1时的不同球磨时间的Cu/SiO2规整结构催化剂的DMO加氢反应性能及涂层稳定性示意图。
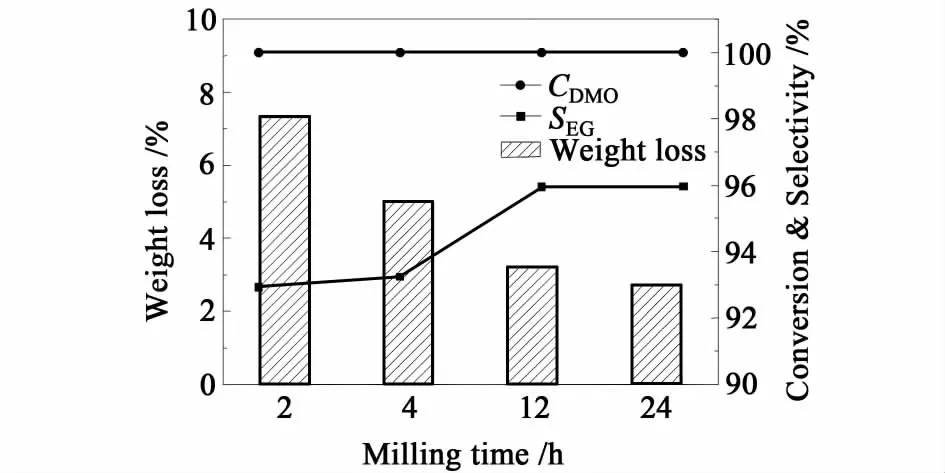
图5 不同球磨时间的Cu/SiO 2规整结构催化剂的DMO加氢反应性能及涂层稳定性Fig.5 The performance of the catalytic hyd rogenation of DMO over Cu/SiO 2 monolithic catalysts with different milling time and the washcoat stability
由图5可知,随着球磨时间的延长,Cu/SiO2规整结构催化剂涂层的脱落率明显降低,当球磨时间从2 h提高到24 h,涂层的脱落率由7.3%下降到2.7%(质量),这与催化剂涂层的表面形貌有关,催化剂涂层龟裂越严重,涂层的黏结性越差,超声时涂层的脱落率越高。另外,与催化剂的孔道结构也有关系,球磨时间延长,有利于涂层强度的提高。
图5还显示了不同球磨时间的Cu/SiO2规整结构催化剂的 DMO加氢反应性能。4种催化剂的DMO转化率均为100%,EG的选择性随着球磨时间的增加先升高,后来基本不变,球磨12 h和24 h的催化剂的活性相当,EG选择性为96%左右。结合以上的表征数据分析,催化剂的物化性能及催化剂的相结构变化不大。但是,球磨胶的粒度与催化剂的活性有相关性。随着球磨时间的增加,球磨胶的粒度先显著降低,后来趋于稳定,这导致催化剂涂层的脱落率显著降低,活性组分流失减小,因此,催化剂的活性有一定的提高。
3 结论
将蒸氨法制备的Cu/SiO2催化剂原粉球磨不同的时间获得一系列球磨胶,再涂覆到堇青石载体上获得系列的规整结构催化剂,并对球磨胶及催化剂进行表征。研究发现,延长球磨时间,催化剂中活性组分Cu的分散度及相结构变化不大,但是球磨时间过长,催化剂的孔道结构发生变化,二次孔减小,催化剂涂层的强度会提高。另外,随着球磨时间的延长,球磨胶的粒度减小,涂覆后涂层的龟裂程度显著缓解,涂层的脱落率明显降低,活性组分流失减少,催化剂的活性和涂层的黏结性得以提高。因此,12 h的球磨时间可获得粒度分布适宜的球磨胶,制备出活性高、涂层黏结性强的Cu/SiO2规整结构催化剂。
[1]Xu G,Li Y,Li Z,et al.Kinetics of the hydrogenation of diethyl oxalate to ethylene glycol[J].Industrial&Engineering Chemistry Research, 1995, 34(7): 2 371-2 378
[2]MaihomT,Namuangruk S,Nanok T,et al.Theoretical study on structures and reaction mechanisms of ethylene oxide hydration over H-ZSM-5:Ethylene glycol formation[J].The Journal of Physical Chemistry C, 2008,112(33): 12 914-12 920
[3]Altiokka MR,Akyalcin S.Kinetics of the hydration of ethylene oxide in the presence of heterogeneous catalyst[J].Industrial&Engineering Chemistry Research,2009, 48(24): 10 840-10 844
[4]Li X,Chen Y,Chen J.Progress in the synthesis of ethylene glycol through coal chemical industry route[J].Coal Chemical Industry, 2007, 35(3): 15-18
[5]Zhou Z,Li Z,Pan P,et al.Progress in technologies of coal-based ethylene glycol synthesis[J].Chemical Industry and Engineering Progress, 2010, 29(11): 2 003-2 009
[6]Matteoli U,Blanchi M,Menchi G,et al.Homogeneous catalytic hydrogenation of dicarboxylic acid esters[J].Journal of Molecular Catalysis, 1984, 22(3): 353-362
[7]Teunissen H T,Elsevier C J.Rutheniumcatalysed hydrogenation of dimethyl oxalate to ethylene glycol[J].Chemical Communications, 1997, (7): 667-668
[8]Van Engelen MC,Teunissen H T,De Vries JG,et al.Suitable ligands for homogeneous ruthenium-catalyzed hydrogenolysis of esters[J].Journal of Molecular Catalysis A: Chemical, 2003, 206(1/2): 185-192
[9]Boardman B,Hanton MJ, Van Rensburg H, et al.A tripodal sulfur ligand for the selective ruthenium-catalysed hydrogenation of dimethyl oxalate[J].Chemical Communications, 2006, (21): 2 289-2 291
[10]Chen L,Guo P,Qiao M,et al.Cu/SiO2catalysts prepared by the ammonia-evaporation method: Texture,structure,and catalytic performance in hydrogenation of dimethyl oxalate to ethylene glycol[J].Journal of Catalysis, 2008, 257(1): 172-180
[11]Yin A,Guo X,DaiW,et al.The nature of active copper species in Cu-HMS catalyst for hydrogenation of dimethyl oxalate to ethylene glycol:Newinsights on the synergetic effect between Cu0and Cu+[J].The Journal of Physical Chemistry C, 2009, 113(25): 11 003-11 013
[12]Yin A,Guo X,Fan K,et al.Ion-Exchange temperature effect on Cu/HMS catalysts for the hydrogenation of dimethyl oxalate to ethylene glycol[J].ChemCat Chem,2010, 2(2): 206-213
[13]Zhu Y,Wang S,Zhu L,et al.The influence of copper particle dispersion in Cu/SiO2catalysts on the hydrogenationsynthesis of ethylene glycol[J].Catalysis Letters,2010, 135(3-4): 275-281
[14]He Z,Lin H,He P,et al.Effect of boric oxide doping on the stability and activity of a Cu-SiO2catalyst for vapor-phase hydrogenation of dimethyl oxalate to ethylene glycol[J].Journal of Catalysis, 2011, 277 (1):54-63
[15]Wang S,Li X,Yin Q,et al.Highly active and selective Cu/SiO2catalysts prepared by the urea hydrolysis method in dimethyl oxalate hydrogenation[J].Catalysis Communications, 2011, 12(13): 1 246-1 250
[16]Yin A,Wen C,Guo X,et al.Influence of Ni species on the structural evolution of Cu/SiO2catalyst for the chemoselective hydrogenation of dimethyl oxalate[J].Journal of Catalysis, 2011, 280(1): 77-88
[17]Yue H,Zhao Y,Zhao L,et al.Hydrogenation of dimethyl oxalate to ethylene glycol on a Cu/SiO2/cordierite monolithic catalyst:Enhanced internalmass transfer and stability[J].AIChE Journal, 2012, 58(9): 2 798-2 809
[18]Lin J,Zhao X,Cui Y,et al.Effect of feedstock solvent on the stability of Cu/SiO2catalyst for vapor-phase hydrogenation of dimethyl oxalate to ethylene glycol[J].Chemical Communications, 2012, (48): 1 177-1 179
[19]Ma X,Chi H,Yue H,et al.Hydrogenation of dimethyl oxalate to ethylene glycol over mesoporous Cu-MCM-41 catalysts[J].AIChE Journal,2003, 59(7): 2 530-2 539
[20]Wang Y, Duan X, Zheng J, et al.Remarkable enhancement of Cu catalyst activity in hydrogenation of dimethyl oxalate to ethylene glycol using gold[J].Catalysis Science and Technology, 2012, 2(8): 1 637-1 639
[21]Wen C,Cui Y,Yin A,et al.Remarkable improvement of catalytic performance for a newcobalt-decorated Cu/HMS catalyst in the hydrogenation of dimethyloxalate[J].ChemCat Chem,2012,(5):138-141
[22]Zhao L,Zhao Y,Wang S,et al.Hydrogenation of dimethyl oxalate using extruded Cu/SiO2catalysts:Mechanical strength and catalytic performance[J].Industrial&Engineering Chemistry Research, 2012, 51 (43):13 935-13 943
[23]迟涵文,赵玉军,王胜平,等.Cu-MCM-41催化剂的制备及在草酸酯加氢制乙二醇催化性能[J].化学工业与工程,2013,30(3):1-6 Chi Hanwen, Zhao Yujun, Wang Shengping, et al.Preparation of Cu-MCM-41 catalyst and catalytic performance for hydrogenation of dimethyl oxalate to ethylene glycol[J].Chemcial Industry and Engineering,2013, 30(3): 1-6(in Chinese)
[24]王汝贤,徐艳,吕静,等.乙二醇精制过程的模拟分析[J].化学工业与工程,2012,29(4):63-67 Wang Ruxian, Xu Yan, Lv Jing, et al.Simulation analysis of ethylene glycol purification process[J].2012, 29(4): 63-67(in Chinese)
[25]Brands D S,Poels E K, Bliek A.Ester hydrogenolysis over promoted Cu/SiO2catalysts[J].Applied Catalysis A: General, 1999, 184(2): 279-289
[26]Toshiaki S,Mitsunori N,Akitsugu O,et al.Dehydrogenation of methanol to methyl formate over Cu-SiO2catatysts prepared by ion exchange method[J].Journal of Catalysis, 1986(102): 460-463
[27]Kobayashi H,Takezawa N,Minochi C.Methanol-Reforming reaction over copper-containing catalysts—The effects of anions and copper loading in the preparation of the catalysts by kneadingmethod[J].Journal of Catalysis, 1981, 69(2): 487-494
[28]Carlini C,Di Girolamo M,Macinai A,et al.Selective synthesis of isobutanol by means of the Guerbet reaction:Part 2.Reaction of methanol/ethanol and methanol/ethanol/n-propanolmixtures over copper based/Me-ONa catalytic systems[J].Journal of Molecular Catalysis A: Chemical, 2003, 200(1/2): 137-146
[29]Li Z.Study on catalytic hydrogenation of dimethyl oxalate to ethylene glycol[J].Chemical Reaction Engineering and Technology, 2004(20): 121-128
[30]Liu D,Zhang J,Li D,et al.Hydrogenation of 2-ethylanthraquinone under Taylor flowin single square channel monolith reactors[J].AIChE Journal, 2009, 55(3):726-736
[31]Ramanathan K,Gopinath A.Light-Off location and front diffusion in a catalyticmonolith reactor[J].AIChE Journal, 2008, 54(7): 1 860-1 873
[32]Joshi S Y, Harold MP, Balakotaiah V.Low-Dimensionalmodels for real time simulations of catalytic monoliths[J].AIChE Journal, 2009, 55(7): 1 771-1 783
[33]Avila P,Montes M,Mir E E.Monolithic reactors for environmental applications:A reviewon preparation technologies[J].Chemical Engineering Journal, 2005,109(1/3): 11-36
[34]Kapteijn F,Nijhuis T A,Heiszwolf J J,et al.Newnontraditionalmultiphase catalytic reactors based on monolithic structures[J].Catalysis Today, 2001, 66(2/4):133-144
[35]Ramanathan K,Balakotaiah V,West D H.Ignition criterion for general kinetics in a catalytic monolith[J].AIChE Journal, 2006, 52(4): 1 623-1 629
[36]Centi G,Perathoner S.Novel catalyst design for multiphase reactions[J].Catalysis Today, 2003, 79/80(1): 3-13
[37]Williams J L.Monolith structures, materials, properties and uses[J].Catalysis Today, 2001, 69(1/4): 3-9
[38]Nijhuis T A,Beers A EW,Vergunst T,et al.Preparation of monolithic catalysts[J].Catalysis Reviews,2001, 43(4):345-380
