分子印迹聚合物在高效液相色谱柱中的应用
2014-05-10唐萍萍
唐萍萍,李 华
(广西民族大学化学化工学院,广西 南宁 530006)
分子印迹聚合物在高效液相色谱柱中的应用
唐萍萍,李 华
(广西民族大学化学化工学院,广西 南宁 530006)
综述了分子印迹聚合物的制备原理、制备方法,介绍了分子印迹聚合物作为高效液相色谱固定相在分子印迹整体色谱柱、分子印迹填充色谱柱中的应用现状及 存在的问题。
分子印迹聚合物;高相液相;分子印迹整体柱;分子印迹填充柱
分子印迹聚合物(Molecularly imprinted polymers, MIPs)是以某种物质为模板分子,模板分子与单体上的某些功能基团通过共价键或非共价键的作用形成复合物,加入交联剂,发生聚合后,将 模板分子从聚合物中去除,形成在功能基排列和空间结构上都与模板相匹配的空穴的高聚物[1]。20世纪40年代诺贝尔获得者Pauling[2]提出抗体的形成学说,1972年Wulff G研究小组首次合成分子印迹聚合物,直至Mosbach等人发表关于以茶碱为模板聚合物的报道,MIPs才得到广泛的研究和应用。随着分子印迹技术逐渐成熟,分子印迹聚合物已经被广泛研究和开发。MIPs由于高选择性和稳定的物理性能成为当前高选择材料之一,在色谱分离[3-5]、传感器[6-7]、膜分离[8]、模拟酶催化[9]和药物控制释放[10]等领域得到应用。MIPs作为高效液相色谱柱的固定相, 将分子印迹的高选择性和高效液相的高灵敏度、分析 范围宽、分析速率快的优点相结合,并已经应用于拆分手性物质[11]、药物的检测[12]、植物成分的提取分离、蛋白质的分离与检测[13]等方面。本文就分子印迹聚合物制备及其在HPLC色谱柱上的应用现状进行介绍。
1 分子印迹聚合物的制备
1.1 分子印迹聚合物的制备原理
分子印迹聚合物制备主要有3个步骤:1)模板分子与具有适当功能基的功能单体形成复合物;2)加入交联剂与功能单体互相交联聚合形成聚合物,在三维空间上将功能单体的功能基固定下来;3)通过一定的化学手段将模板分子去除,即可得到具有“记忆”三维孔穴的聚合物,此聚合物能与模板分子再次结合,并对模板分子具有特异性识别,如“锁-钥匙”的关系。根据模板分子与功能单体之间相互作用性质不同,分子印迹可分为预组装法、自组装法及牺牲空间法,其制备MIPs原理示意图见图1,其优缺点见表1。
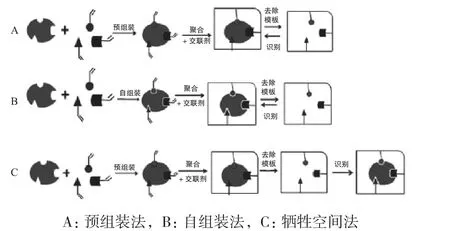
图1 MIPs制备原理示意图
1.2 分子印迹聚合物的制备方法
分子印迹聚合物得到了广泛的研究和应用,根据不同应用领域的要求,对分子印迹聚合物的制备方法进行了不断的改进。迄今为止,制备分子印迹聚合物主要有以下几种。
1)本体聚合法。本体聚合法属于包埋法,是传统的制备MIPs的方法。它是将模板分子、功能单体、交联剂、引发剂等溶解于惰性溶剂中,将其转入玻璃瓶进行交联聚合,得到块状的聚合物。此方法制备条件容易控制,操作简单,实验干扰因素较少;但是聚合物通常为块状,要经过粉碎、研磨、过筛等繁琐的后处理。研磨过程中,聚合物会存在一些不规则的颗粒,同时也会破坏结合位点,且制备时印迹位的包埋,模板分子较难除去,导致分子印迹聚合物的饱和吸附量小,利用率低。由于本体聚合存在这些明显的问题,所以该方法已经逐渐被其他方法代替。

表1 预组装法、自组装法及牺牲空间法的对比
2)原位聚合法(In Site Polymerization),是指在空的色谱柱或毛细管柱内直接合成MIPs作为固定相的方法,此方法主要用于合成MIP-HPLC整体柱。其优点为操作简单、产率高、实用性强,减少本体聚合后处理的繁琐过程。但是该方法制备的MIPHPLC柱有柱压高、选择性差、色谱峰拖尾严重等问题,限制了其在现实分离中的应用,但可以通过改变致孔剂的比例,采用梯度洗脱等方法避免上述的一些问题。
3)悬浮聚合法,是将溶有模板分子、功能单体、交联剂、引发剂等的有机相加入到水相中,形成油相小液滴悬浮在水相中聚合,是最常用、简便制备聚合物球形的方法之一,悬浮聚合物球形颗粒粒径一般为0.01~5mm。悬浮聚合法制备MIPs通常用水作为分散相,水极性较大,会影响模板与功能单体之间氢键的形成,因此Mayes, A. G.等[18],Ansell, T. J.[19]采用全氟烃作为分散相制备MIPs,并用此聚合物作为高效液相色谱柱固定相,发现色谱柱柱压低,传质速度慢,全氟烃分散效果较好,但是价格昂贵。陆续有研究者用液体石蜡、硅油等物质作为分散相合成分子印迹聚合物,但是都存在一些问题[20-21]。目前,最常用的分散相为水,虽然影响氢键形成,但是环保、成本低、分散性好,也能更好地适应工业生产。该方法制备的MIPs在高效液相色谱、固相萃取等方面得到应用。
4)沉淀聚合,也称为非均相溶液聚合法,将反应物(模板分子、功能单体、交联剂等)溶解于分散剂中,反应始于均相体系,随着聚合反应的进行,反应物进行聚合,聚合达到一定程度时,聚合物以沉淀的形式从溶液中析出。沉淀聚合法制备MIPs可能是块状、凝胶状、球形颗粒等,沉淀聚合物颗粒可小至纳米[22]。此方法操作简单、产率高,若想得到均一的粒径,溶剂黏性选择是关键。由于沉淀聚合法制备的分子印迹聚合物粒径均一,颗粒小,所以在HPLC色谱柱和毛细管柱等领域得到应用。
5)表面印迹法,是在载体表面进行分子印迹聚合,使结合位点能均匀地分布在载体表面,能更好地去除或结合模板分子。此方法不仅能获得比表面积大、粒径均一的聚合物,而且可以通过载体的性能来适应生产要求,同时,它克服了传统聚合方法制备的MIPs传质慢、结合位点包埋等问题。Yoshida M等人[23]、Tsukagoshi K人等[24]采用表面印迹法合成组氨酸分子印迹聚合物,并用其对组氨酸及衍生物进行识别。陈志萍等[25]采用表面印迹法,以硅胶微粒作为载体,合成胆红素分子印迹聚合物,其MIPs具有优良的选择识别性能,解析率达到99.39%。但是,在二维网络中形成印迹点导致结构稳定性较差,结合容量减少,可重复使用次数降低[26]。
在设计分子印迹聚合物体系时,除了适合的聚合方法外,还要做好模板分子、功能单体、交联剂、溶剂 ( 致孔剂 ) 、引发剂等的选择及确定最佳配比
2 分子印迹聚合物在高效液相色谱柱上的应用
分子印迹聚合物具有选择性高、化学稳定性好、耐酸碱性强、使用寿命长等特点。MIPs已被应用于高效液相色谱色谱柱中,作为其固定相。根据HPLC色谱柱固定相填料方式不同,分子印迹色谱柱分为分子印迹色谱整体柱和分子印迹色谱填充柱。
2.1 分子印迹整体色谱柱
整体柱,又称为整体固定相连续床或连续棒,因其制备简单、内部结构均匀、渗透率高、传质速度快和易改性等特点已被广泛应用。分子印迹整体柱是将分子印迹技术与整体柱结合,采用原位聚合法,在空的色谱柱内直接进行聚合,得到分子印迹整体柱。
Mastui等1993年首次制备了苯丙氨酸分子印迹整体柱。虽然存在着许多不足,但是将分子印迹技术和整体柱结合的尝试引起了人们的广泛关注。 近年来,分子印迹整体柱被广泛应用于手性拆分、植物提取物的分离分析、药物提取检测、蛋白质分离等。
在手性物质拆分方面,Yin Junfa等[27]采用原位聚合法,制备了那格列奈分子印迹整体柱,其能成功地拆分那格列奈及其对映体,实验表明手性识别决定于立体结构、分子印迹官能团排列及MIPs上孔穴,手性拆分是一个热焓可控过程。Elijan等[28]采用原位聚合物,制备了S-(-)-氨氯地平分子印迹整体柱,通过梯度洗脱,将S-(-)-氨氯地平分子及对映体分离。
在植物提取物的分离分析方面,San Han-wen等[29]采用原位聚合法制备了茶碱分子印迹整体柱,通过梯度洗脱方法,改善了色谱峰拖尾现象,成功测定了不同茶叶中咖啡因和茶碱的含量,分子印迹整体柱可用于植物提取物的 分离分析。尹艳凤等[30]制备了大黄素分子印迹整体柱,优化其色谱条件,印迹因子达到1.9,并成功从中药大黄片分离得到大黄素。
在药物分离检测方面,Li Xiao Xia等[31]制备了恩诺沙星分子印迹整体柱,其能将恩诺沙星与左氧氟沙星、环丙氟沙星、加替沙星、诺氟沙星完全分离,该印迹色谱柱可用于恩诺沙星药物的分离检测。
在蛋白质的分离方面,Lin Zan等[32]制备了3种不同基质的牛血清蛋白和溶霉素分子印迹整体柱,在整体柱制备过程引入溶胶-凝胶法对硅胶骨架进行了优化,减缓了整体柱的衰老速度,延长整体柱的使用寿命。在蛋白质的识别过程中发现,分子印迹整体柱在低交联度下对蛋白质识别分离效果更好。Jia Man等[33]通过原位聚合法直接制备了溶酶酵素的分子印迹整体柱,其印迹因子达到5.04且能将溶酶酵素从鸡蛋白中分离出来。
分子印迹整体柱由于其优越的性能在诸多方面得到应用,但是色谱峰较宽[34-36]、柱效低[37]等问题仍未解决,分离机制也需要进一步研究。
2.2 分子印迹填充色谱柱
分子印迹填充色谱柱是指采用干法或湿法填柱法将制备好的分子印迹颗粒填充于色谱柱内获得分子印迹填充色谱柱。目前制备分子印迹填充色谱柱固定相的方法主要有悬浮聚合、沉淀聚合及种子溶胀聚合。这些方法可以直接制备聚合物微球,不需粉碎、研磨过程,可直接作为高效液相固定相。分子印迹填充色谱柱已经应用于药物的检测分离、手性物质的拆分等方面。
在药物的检测分离方面,Zhang Yan等[38]采用悬浮聚合法,制备了20~50μm氯霉素分子印迹微球,并将其作为高效液相色谱固定相,制备分子印迹填充色谱柱,通过梯度洗脱的方式,不仅能将氯霉素相似结构分离,也能将其与红霉素和四环素分离,可用于检测分离氯霉素。Deng Qi Liang等[39]用氢化奎宁作为伪模板,采用表面印迹法制备了氢化奎宁分子印迹聚合物,并以此为HPLC固定相,能将奎宁与奎尼丁完全分离,说明印迹微球具有手性固定相的三维孔穴,表现出大量的协同作用。
在手性物质的拆分方面,Wei Shuting等[40]采用沉淀法合成100nm~3μm的 17β-雌二醇分子印迹聚合物微球,并制备了17β-雌二醇分子印迹填充柱,用于分离17β-雌二醇和17α-雌二醇,与C18相比,分子印迹填充色谱柱分离效果更好。于思明等[41]制备N-BOC-L-色氨酸分子印迹聚合物作为高效液相色谱柱固定相,对N-BOC-L-色氨酸分子进行拆分,成功将N-BOC-L-氨基酸分子和N-BOC-D-氨基酸分子对映体进行分离。
目前,分子印迹填充色谱柱虽然在药物的提取和分离、拆分对映体等方面得到应用,但是由于空隙率低,所以还未在蛋白质等大分子中应用。相对于整体柱,分子印迹填充色谱柱文献报道较少,因为分子印迹填充柱的固定相要求较为严苛,一是固定相膨胀度必须小,若是膨胀度大,流动相进入,固定相膨胀,堵塞色谱柱,柱压上升,高效液相无法运行;二是固定相耐压性要好,填充色谱柱相对整体柱,空隙率低,柱压高,固定相耐压性差,可能造成固定相崩塌,造成色谱柱无法使用。
3 结语
分子印迹聚合物由于其特异识别、高选择性及稳定的物理性能在高效液相色谱得到了研究和应用。MIPs作为高效液相色谱固定相,制备的分子印迹色谱柱具有优良的特异选择性,但是其真正应用仍存在许多问题:1)柱效低,峰型宽且拖尾,不能准确地定量分析;2)聚合体系选择有限,缺乏理论指导;3)对分子印迹色谱柱的作用机理和热动力学研究较少;4)没有统一评价标准。因此,还需要科技人员进行大量的研究。
[1] Won Jo Cheong, Song Hee Yang, Faiz Ali. Molecular imprinted polymers for separation science:A review of reviews[J]. J. Sep. Sci., 2013(36): 609-628.
[2] Pauling L.The serological properties of simple substances.Ⅶ .a quantitative theory of the inh ibition by haptens of the precipitation if heterogeneous antisera with antigens, and comparison with experimental results for polyhaptenic simple substances and for azoproteins[J]. J. Am. Chem. Soc., 1940,62(3): 2643-2657.
[3] Jiang Jiabing , Zhou Qi , Kang Chengcheng , et al. Preparation and Characterization of a Pseudo-Template Imprinted Polymer with a Chirality-Matching Monomer for the Separation of Cinchona Alkaloids by High-Performance Liquid Chromatography[J]. Journal of Applied Polymer Science., 2013,27(2): 3425-3431.
[4] Francisco Barahona, Esther Turiel, Peter A. G. Cormack et al. Synthesis of core-shell molecularly imprinted polymer microspheres by precipitation polymerization for the inline molecularly imprinted solid-phase extraction of thiabendazole from citrus fruits and orange juice samples[J]. J. Sep. Sci., 2011(34): 217-224.
[5] Shabi Abbas Zaidi, Won Jo Cheong. Preparation of an open-tubular capillary column with a monolithic layer of S-ketoprofen imprinted and 4-styrenesulfonic acid incorporated polymer and its enhanced chiral separation performance in capillary electrochromatography [J]. Journal of Chromatography A, 2009.16(12): 2947-2952.
[6] Ge Shenguang , Zhao Peini , Yan Mei, et al. Multi-branch chemiluminescence-molecular imprinting sensor for sequential determination of carbofuran and omethoate in foodstuff [J].Analytical Methods, 2012(4): 3150-3156.
[7] 申晴,崔莉凤,赵硕,等.微囊藻毒素分子印迹传感器的制备与应用[J].分析化学研究简报,2012,40(3):442-446.
[8] 马秀玲,陈日耀,等.柚皮苷分子印迹膜的水相制备与识别[J].高分子学报,2010(4): 416-422.
[9] T.A. Sergeyeva, O.A. Slinchenko, L.A. Gorbach, et al. Catalytic molecularly imprinted polymer membranes: Development of the biomimetic sensor for phenols detection [J]. Analytica Chimica Acta, 2010(659): 274-279.
[10] 郝兰芳,陈妍,黄艳萍,等.S-萘普生印迹聚合物药物释放性能的研究[J].天津医科大学学报.2009,15(3): 345-347.
[11] Ou Junjie , Kong Liang, Pan Chensong, et al. Determination of dltetra hydropalmatine in Corydalis yanhusuobyltetrahydropalmatine imprinted monolithic column coupling with reversed-phase high performance liquid chromatography [J]. J. Chromatogr. A, 2006(1117): 163-169.
[12] 权英,薛兴杰,陈梦玲,等.沙拉沙星分子印迹聚合物的制备及其性能研究[J].食品科学,2012,33 (12):28-31.
[13] Liu Jinxiang , Deng Qiliang , Yang Kaiguang, et al. Macroporous molecularly imprinted monolithic polymer columns for protein recognition by liquid chromatography [J]. J. Sep. Sci., 2010(33): 2757-2761.
[14] Wulff G, Grobe Einsler R, Vesper W, et al. Enzymeanalogue built polymer [J]. Macromol Chem, 1977(178): 2817-2825.
[15] R.Arshady, K.Mosbach, Macromol. Chem, 1981(182): 687.
[16] G.Vlatakis, L.I.Andersson, R.Muller, K. Mosbach. Nature,1993(361): 645.
[17] Whitcombe M.J., Rodriguez M.E., Villar P, et al. A new method for the introduction of recognition site functionality into polymers prepared by molecular imprinting-synthesis and characterization for polymeric receptors fir cholesterol [J].J.Am.Chem. Soc., 1995, 117(27): 7105-7111.
[18] Mayes, A.G., Mosbach, K. Molecularly imprinted polymer beads: Suspension polymerization using a liquid perfluorocarbon as the dispersing phase [J].Anal. Chem., 1996(6 8): 3769-3774.
[19] Ansell, T.J., Mosbach, K. Molecularly imprinted polymers by suspension polymerization in perfluorocarbon liquids, with emphasis on the influence of the porogenic solvent [J]. J.Chromatography.A, 1997(787): 55-66.
[20] Henrik K, Maria K. Novel method for the synthesis of molecularly imprinted polymer bead libraries [J].Micromole Rapid Common, 2004(25): 315.
[21] Wang XB, Zheng ZH, Ding XB, et al. Synthesis of molecularly imprinted polymer particles by suspension polymerization in silicone oil[J]. Chinese Chem Lett., 2006, 17(9): 1243.
[22] Keiichi Yoshimatsu, Kristina Reimhult, Anatol Krozer, et al. Uniform molecularly imprinted microspheres and nanoparticles prepared by precipitation polymerization:The control of particle size suitable for different analytical applications [J]..Analytica Chimica Acta., 2007(84): 112-121.
[23] Yoshida M, Uezu Kazuya, Goto Masahiro, et al. Metal ion imprinted microsphere prepared by surface molecular imprinting technique using water-in-oil-in-water emulsions [J].Journal of Applied Polymer Science, 1999, 73(7): 1223-1230.
[24] Tsukagoshi K, Yu Kai Yu, Ozaki Yoshihisa, et al. Surface Imprinting:Preparation of Metal Ion-Imprinted presinspbyp Used of Complication at the Aqueous-Organic Interface [J]. ACS symposium Series, 1998, 703(1): 251-263.
[25] 陈志萍,高保娇,杨晓峰,等.表面印迹法制备胆红素分子印迹材料及其识别性能[J].过程工程学报,2009(2):387-392.
[26] G.Vlatakis, L.I.Andersson, R.Muller, K. Mosbach. Nature, 1993(361): 645.
[27] Yin Junfa, Yang Gengliang, Chen Yi. Rapid and efficient chiral separation of nateglinide and its l-enantiomer on monolithic molecularly imprinted polymers[J].Journal of Chromatography A, 2005 (1090): 68-75.
[28] Elijan Amut, Qiang Fu&Qi, Fang&Rong Liu, et al. In situ polymerization preparation of chiral molecular imprinting polymers monolithic column for amlodipine and its recognition properties study [J],J Polym Res., 2010(17): 401-409.
[29] Sun Han-wen, Qiao Feng-xia, Liu Guang-yu. Characteristic of theophylline imprinted monolithic column and its application for determination of xanthine derivatives caffeine and theophylline in green tea[J]. Journal of Chromatography A, 2006(1134): 194-200.
[30] 尹艳凤,李倦生,姚运先,等.大黄素分子印迹整体柱的合成及性能表征[J].分析测试学报,2008,27(7):758-761.
[31] Li Xiao Xia, Liu Xin, Bai Li Hong, et al. Preparation of imprinted monolithic column under molecular crowding conditions [J]. Chinese Chemical Letters, 2011(22): 989-992.
[32] Lin Zan, Yang Fan, He Xiwen, et al. Preparation and evaluation of a macroporous molecularly imprinted hybrid silica monolithic column for recognition of proteins by high performance liquid chromatography [J]. Journal of Chromatography A, 2009, 16(12): 8612-8622.
[33] Jia Man, Qin Lei, He Xi-Wen, et al. Preparation and application of lysozyme imprinted monolithic column with dopamine as the functional monomer [J]. J. Mater. Chem., 2012(22): 707-713.
[34] Huang Xiaodong, Zou Hanfa, Chen Xiaoming, et al. Molecularly imprinted monolithic stationary phases for liquid chromatographic separation of enantiomers and diastereomers [J]. J. Chromatogr. A., 2003(984): 273-282.
[35] 杨清清,李娟,狄斌,等.黄芩素分子印迹整体柱的制备研究[J].药物分析杂志,2011,30(1):1-5.
[36] 张静,贺浪冲,傅强.士的宁分子印迹整体柱的制备[J].分析化学研究简报,2005,33(1):113-116.
[37] 班璐.活性/可控自由基聚合的分子印迹整体柱的制备及性能评价[D].天津:天津医科大学,2013.
[38] Zhang Yan, Lei Jiandu. Synthesis and Evaluation of Molecularly Imprinted Polymeric Microspheres for Chloramphenicol by Aqueous Suspension Polymerization as a High Performance Liquid Chromatography Stationary Phase[J]. Bull. Korean Chem. Soc., 2013, 34(6): 1839-1844.
[39] Deng Qi Liang, Li Yan Li, Zhang Li Hua. Molecularly imprinted macroporous monolithic materials for protein recognition [J].Chinese Chemical Letters, 2011 (22): 1351-1354.
[40] Wei Shuting, Alexandra Molinelli, Boris Mizaikoff. Molecularly imprinted micro and nanospheres for the selective recognition of 17-estradiol[J]. Biosensors and Bioelectronics, 2006 (21): 1943-1951.
[41] 于思明,苏立强,何丹凤.N-BOC-L-色氨酸分子印迹聚合物的手性拆分[J].化工时代,2011,25(10):18-20.
Molecularly Imprinted Polymer for High Performance Liquid Chromatographic Column
TANG Ping-ping, LI Hua
(School of Chemistry and Chemical Engineering, Guangxi University for Nationalities, Nanning 530008, China)
The preparation and recognition mechanism of molecularly imprinted polymer was introduced. The application and existing problems at present of MIP as HPLC stationary phase in molecularly imprinted monolithic column and packed column were also discu ssed.
molecularly imprinted poly mer; high performance liquid; molecularly imprinted monolithic column; molecularly imprinted packed column
O 657.7+2
A
1671-9905(2014)06-0059-05
2014-04-10
